合作猪IFN-ε基因克隆及生物信息学分析
杨姣姣,谢开会,王 伟,闫尊强 ,杨巧丽,马艳萍,滚双宝,
(1.甘肃农业大学 动物科学技术学院,兰州 730070; 2.甘肃农业大学 图书馆,兰州 730070; 3.甘肃省现代养猪工程技术研究中心,兰州 730070)
干扰素(Interferon,IFN)是由瑞士研究人员Jean-Lindenmann和英国病毒生物学家Alick Isaacs在1957年利用鸡胚绒毛尿囊膜研究流感病毒干扰现象时,发现的一种具有多种生物活性的糖蛋白[1]。依据结构和来源的不同,IFN可分为Ⅰ、Ⅱ和Ⅲ型[2],不同类型的干扰素具有相似的功能,如抗病毒、调控细胞分裂与增殖及介导机体免疫反应等[3]。IFN-ε是Ⅰ型干扰素重要成员之一,与IFN-α、IFN-β、IFN-ω、IFN-κ、IFN-δ、IFN-ν等具有相同的基因座位点、受体类型及相似的蛋白结构[4-6]。与其他Ⅰ型干扰素不同,IFN-ε表达于多种细胞,如冠状动脉平滑肌细胞、微血管内皮细胞和支气管上皮细胞[7];此外,IFN-ε也具有抵抗病毒的活性[8],在胎生哺乳动物早期胎盘发育过程中有重要保护作用[9-11],研究还发现IFN-ε能保护女性生殖系统免受病毒和细菌的感染[9]。Fischer等[12]发现,IFN-ε在马子宫内膜组成性表达,是子宫内膜固有免疫系统的一部分,能防止病毒感染子宫。Demers等[13]发现,IFN-ε可能是抵抗粘膜病原体入侵的第一道防线。研究报道,IFN-ε已被证明可以预防人上皮细胞和T细胞感染艾滋病毒(HIV)[14]。Yang等[15]发现,重组犬IFN-ε与犬恶性肿瘤细胞A72共孵育时,有50%的肿瘤细胞生长受到抑制。目前,干扰素制剂作为一种新型生物制剂,在疾病预防和控制方面发挥着重要功能。合作猪是世界上少有的珍稀高原型猪种,甘肃合作为中心产区,地理隔离及独特的高原气候,使合作猪保存了独特的遗传结构和遗传性状[16]。作为小型原始地方品种,合作猪具有体型矮小、适应性和抗病性强等特点,是开展相关疾病研究的理想实验动物模型,具有广阔的应用前景[17]。近年来,人们对IFN-ε研究日益增加,Hardy等[4]发现,小鼠IFN-ε长度为664bp,编码192个氨基酸;人IFN-ε长度为642bp,编码208个氨基酸。王庭柱等[18]发现,牛IFN-ε编码193个氨基酸,牛IFN-ε蛋白具有典型的Ⅰ型干扰分子特征。犬IFN-ε基因编码208个氨基酸,其编码蛋白N端前21个氨基酸残基为信号肽[15]。有关猪IFN-ε的研究也有报道,如研究人员利用大白和长白二元杂交猪胃组织,成功克隆得到其IFN-ε基因序列[19]。然而迄今为止,鲜有合作猪IFN-ε基因克隆及生物信息学分析的报道。因此,本试验对合作猪IFN-ε进行克隆及生物信息学分析,以期为进一步研究合作猪IFN-ε生物学功能提供参考。
1 材料与方法
1.1 材 料
1.1.1 样品 取健康合作猪(甘肃省甘南藏族自治州合作市)耳组织,液氮速冻后于-80 ℃保存,备用。
1.1.2 主要试剂 Trizol购自Invitrogen(美国)。pMD19-T Vector(6013)、反转录试剂盒(6210A)均购自宝生物工程 (大连) 有限公司。 2×TaqMaster Mix(KT211-01),DH5α感受态细胞(CB101-02),胶回收试剂盒(DP209-02),一次性培养皿均购自天根生化科技(北京)有限公司。琼脂粉,氨苄青霉素,酵母提取物,胰蛋白胨购自北京索莱宝科技有限公司。
1.2 方 法
1.2.1 合作猪IFN-ε基因引物设计与合成 下载GenBank中猪IFN-ε基因序列(登录号为NM_001105310.1),利用Premier 5.0软件设计引物,预期扩增长度为586 bp,包含582 bp的编码区,引物序列IFN-ε-F:5′- CACCATGATCAACAAGTCTTTC-3′和IFN-ε-R:5′-TCAAGGTTCCATTCCTTGTTT-3′,引物由苏州金唯智生物科技有限公司合成。
1.2.2 合作猪RNA提取与cDNA合成 用Trizol提取合作猪耳组织总RNA。用微量紫外可见分光光度计(NanoDrop 2000)测定RNA浓度和纯度,用反转录试剂盒对总RNA进行反转录,反转录体系10 μL:RNA 0.8 μL,Oligo dt Primer 1 μL,dNTP Mixture 1 μL,RNase-Free Water 7.2 μL。将10 μL反转录体系于65 ℃的水浴作用5 min,取出置于0 ℃的冰上,再加入如下体系:5× Prime Script Ⅱ Buffer 4 μL,RNase Inhibitor 0.5 μL,Prime Script Ⅱ RTase 1 μL,RNase-Free H2O 4.5 μL。将上述总体系20 μL的溶液置于48 ℃金属浴中,反应 1 h,95 ℃灭活5 min即可得到cDNA,-20 ℃保存,待用。
1.2.3 合作猪IFN-ε基因PCR扩增 反应体系(总体积为20 μL):上、下游引物各0.5 μL,2×TaqMaster Mix 10 μL,cDNA模板2 μL,RNase-Free H2O 7 μL。反应程序:95 ℃预变性5 min;95 ℃变性30 s,53 ℃退火30 s,72 ℃延伸1 min,共30个循环;最后72 ℃延伸10 min,4 ℃保存。PCR产物用1.0%的琼脂糖凝胶电泳检测正确后,按照天根DP209-02凝胶回收试剂盒的操作说明书,对目的片段进行回收纯化。
1.2.4 合作猪IFN-ε基因克隆与测序 将PCR扩增产物回收纯化后,通过TA克隆方法将该序列在16 ℃连接至pMD19-T载体,转化到大肠杆菌DH5α感受态细胞,涂板于LB固体培养基中,37 ℃恒温培养箱中培养12 h,进行蓝白斑筛选,用PCR法进行菌落鉴定,选取阳性菌液送苏州金唯智生物科技有限公司进行测序。
1.2.5 合作猪IFN-ε基因序列生物信息学分析 利用DNAMAN和Mega 5.0进行同源性比对和系统进化树构建;通过在线软件Protaram(https://web.expasy.org/protparam/)分析蛋白质基本理化性质;通过在线软件TMHMM(http://www.cbs.dtu.dk/services/TMHMM/)预测蛋白质跨膜结构;通过在线软件SignalP 4.1(http://www.cbs.dtu.dk/services/SignalP/)预测蛋白信号肽;通过在线软件ExPASy服务器中Protscale(https://web.expasy.org/protscale/)分析蛋白质的亲疏水性;通过POSORT Ⅱ Prediction在线网站(https://psort.hgc.jp/form2.html)预测蛋白质的亚细胞定位;通过NCBI网站的CDD在线工具预测基因编码蛋白保守结构域;通过在线软件Prabi服务器的SOPMA程序(https://npsa-prabi.ibcp.fr/)预测蛋白质二级结构;通过在线软件SWISS-MODEL(https://npsa-prabi.ibcp.fr/cgi-bin/npsa_automat.pl)预测蛋白质三级结构。
2 结果与分析
2.1 合作猪IFN-ε基因克隆
以合作猪耳组织cDNA为模板,PCR扩增IFN-ε基因CDS区域,产物经10 g/L琼脂糖凝胶电泳检测,发现1条长约586 bp的条带(图1),与预期片段大小一致,说明成功获得合作猪IFN-ε基因CDS区域。

M.2000 DNA marker;1.IFN-ε基因PCR扩增产物 PCR product ofIFN-εgene;2.阴性对照 Negative control
图1 合作猪IFN-ε基因PCR扩增产物
Fig.1 PCR amplification product ofIFN-εgene in Hezuo pig
2.2 合作猪IFN-ε基因序列测序及分析
测序结果显示,合作猪IFN-ε基因CDS区长582 bp,编码193个氨基酸(图2)。同源性比对结果发现,合作猪IFN-ε基因编码序列与杜洛克猪(Duroc,NM_001105310.1)、小鼠(Musmusculus,NM_177348.2)、人(Homosapiens,NM_176891.4)、黑猩猩(Pantroglodytes,XM_528573.4)、犬(Canislupusfamiliaris,XM_022425479.1)、瘤牛(Bosindicus,XM_019965656.1)、蒙古野马(Equusprzewalski,XM_008531931.1)、山羊(Caprahircus,XM_013965868.2)和绵羊(Ovisaries,XM_012127127.2)的序列同源性分别为98.4%、 56.8%、77.7%、78.2%、76.5%、87.0%、85.5%、 85.0%和86.0%(表1)。采用MEGA5.0中的N-J方法构建物种系统进化树,发现合作猪与杜洛克猪的亲缘关系最近,与瘤牛、蒙古野马、绵羊、山羊亲缘关系较近,与小鼠亲缘关系最远(图3)。

图2 合作猪IFN-ε基因CDS区和编码氨基酸序列Fig.2 Nucleotide sequence and amino sequence of IFN-ε gene CDS region in Hezuo pig
2.3 合作猪与杜洛克猪IFN-ε基因CDS序列和氨基酸序列比对
合作猪与猪参考基因组IFN-ε基因(登录号:NM_001105310.1)CDS序列比对结果表明,合作猪IFN-ε基因CDS序列存在3个碱基突变,均为错义突变,86 bp处C突变为T导致第29位丝氨酸突变为苯丙氨酸,199 bp处A突变为G导致第67位甲硫氨酸突变为缬氨酸,406 bp处T突变为G导致第136位半胱氨酸突变为甘氨酸(图4)。
2.4 合作猪IFN-ε蛋白理化性质分析
ProtParam在线服务器分析结果显示,合作猪IFN-ε蛋白由193个氨基酸残基组成(表2),分子式为C1027H1630N278O290S10,分子质量为 22.83 ku,理论等电点为8.43,说明该蛋白为碱性蛋白。肽链N端为蛋氨酸(Met),在体外的理论半衰期为30 h,不稳定系数为47.17,属于不稳定蛋白。脂肪系数为99.48,平均亲水系数为 -0.240,属于亲水蛋白。
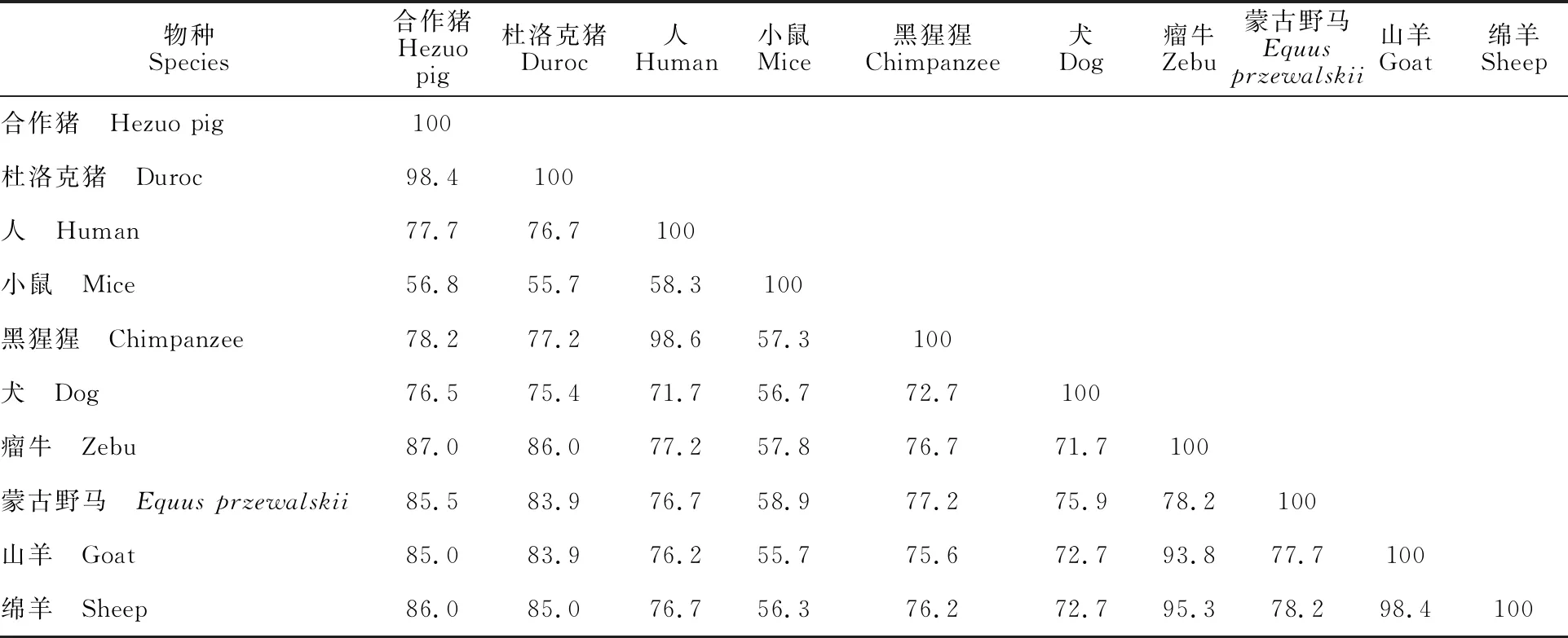
表1 IFN-ε基因CDS同源性比较Table 1 Comparison of CDS homology of IFN-ε gene %
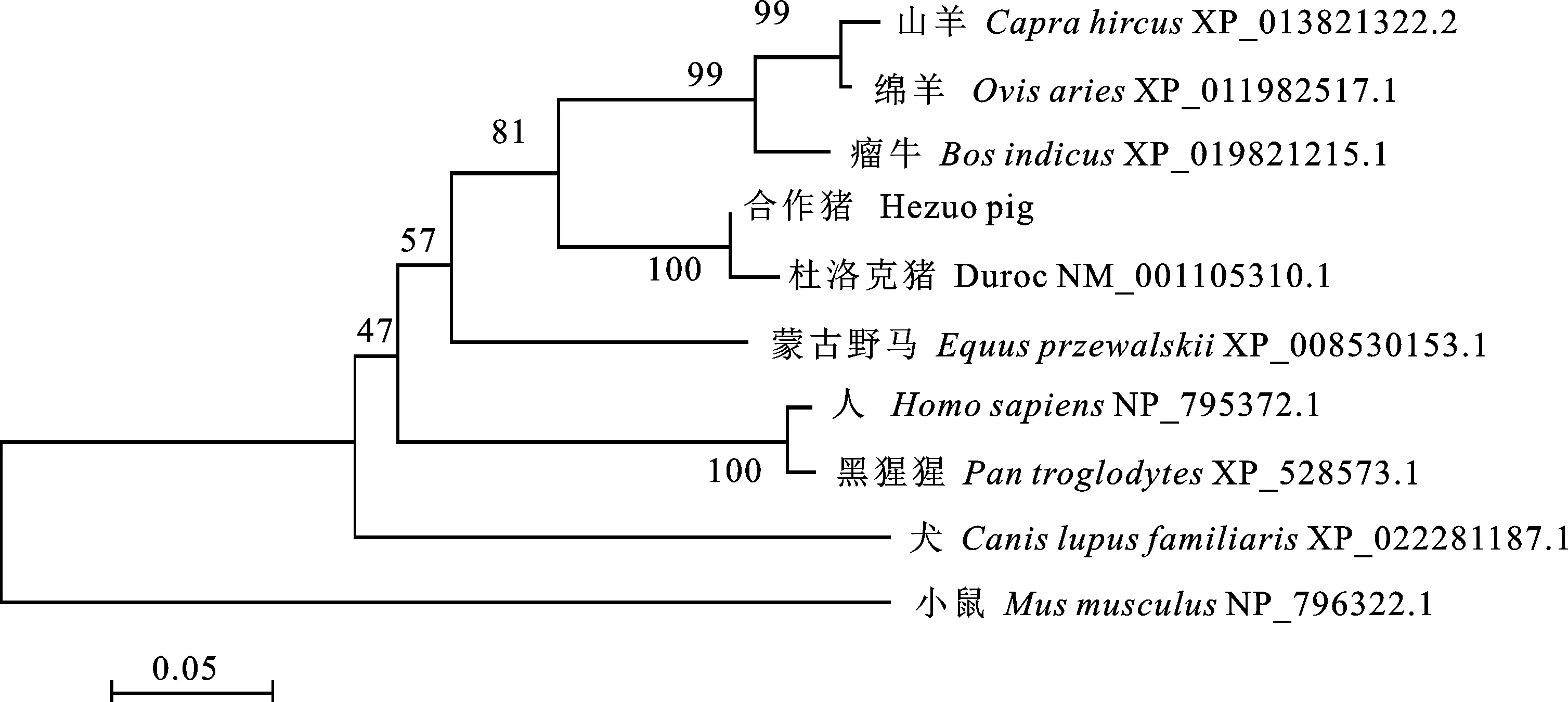
图3 IFN-ε基因系统进化树Fig.3 Phylogenetic tree of IFN-ε gene

图4 合作猪与杜洛克猪IFN-ε基因编码氨基酸序列比对结果Fig.4 Sequence comparison result of IFN-ε gene amino acid between Hezuo pig and Duroc
表2 合作猪IFN-ε蛋白氨基酸组成
Table 2 Composition of amino acids inIFN-εprotein of Hezuo pig

氨基酸Amino acids数量Number频率/%Frequency氨基酸Amino acids数量Number频率/%FrequencyAla(A)73.6Lys(K)115.7Arg(R)115.7Met(M)73.6Asn(N)84.1Phe(F)126.2Asp(D)42.1Pro(P)42.1Cys(C)31.6Ser(S)168.3Gln(Q)2110.9Thr(T)63.1Glu(E)168.3Trp(W)21Gly(G)52.6Tyr(Y)52.6His(H)52.6Val(V)105.2Ile(I)94.7Pyl(O)00Leu(L)3116.1Sec(U)00
2.5 合作猪IFN-ε蛋白疏水性分析
运用ExPASy服务器中ProtScale程序对合作猪IFN-ε蛋白做疏水性分析发现,其中第10位甲硫氨酸(Met)疏水性最强(分值为2.678),第72位酪氨酸(Tyr)疏水性最弱(分值为-3.056),在负值区域有较多氨基酸(图5),这与Protaram预测结果一致。
2.6 合作猪IFN-ε蛋白二级结构和三级结构预测分析
合作猪IFN-ε蛋白二级结构预测表明,此蛋白中α-螺旋占61.66%,无规则卷曲占30.05%,β-转角占3.11%,延伸链占5.18%(图6)。通过SWISS-MODEL平台对合作猪IFN-ε蛋白建模预测三级结构发现,IFN-ε蛋白以α-螺旋和无规卷曲为主(图7)。
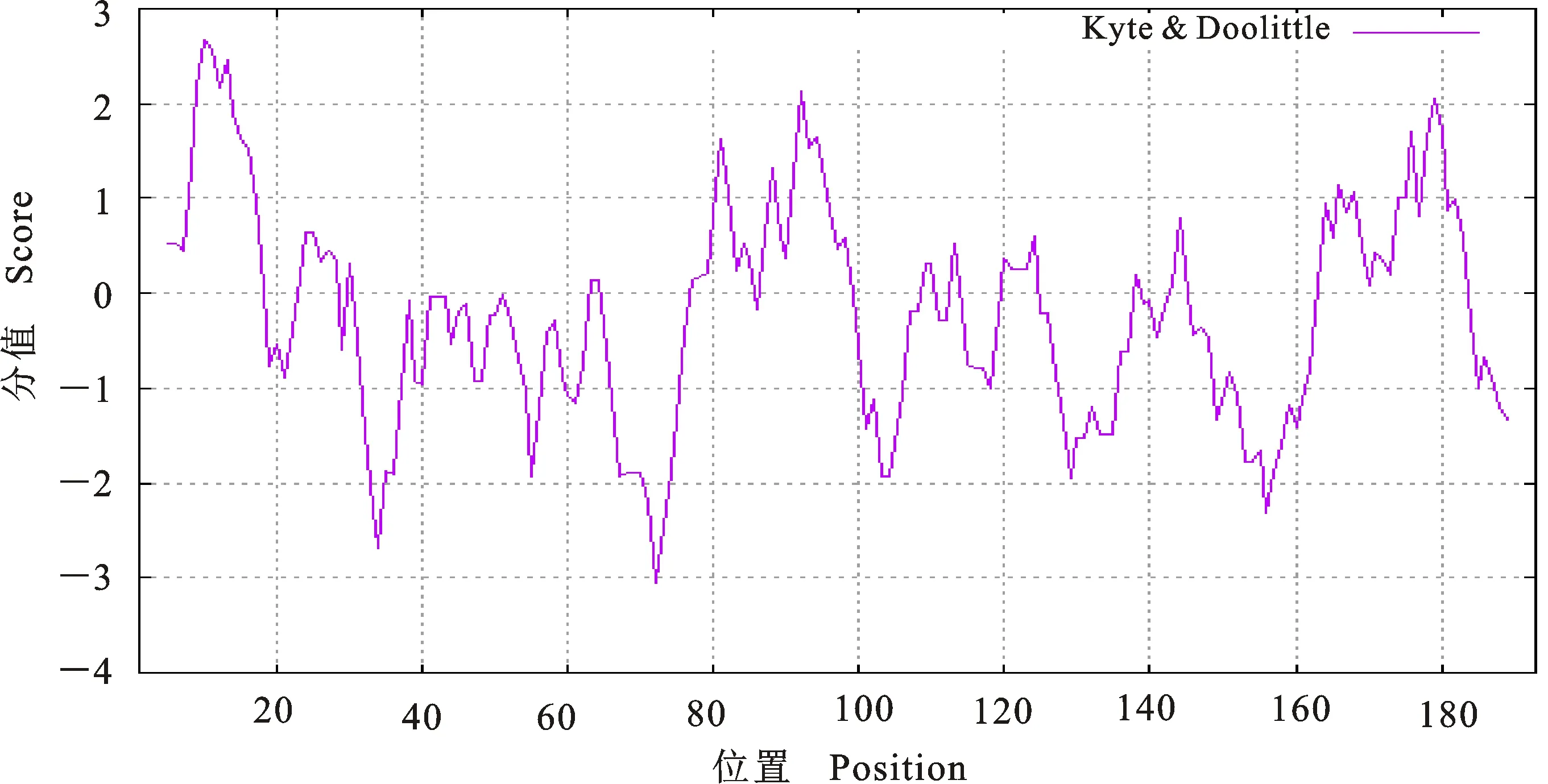
图5 合作猪IFN-ε蛋白的疏水性预测结果Fig.5 Prediction of hydrophobicity of IFN-ε protein in Hezuo pig

h.α-螺旋 Stands for alpha-helix;e.延伸链 Epresents extended chain;c.无规则卷曲 Stands for irregular curling;t.β-转角 Trefers to beta-angle of rotation
图6 合作猪IFN-ε蛋白二级结构预测
Fig.6 Secondary structure of IFN-ε protein in Hezuo pig
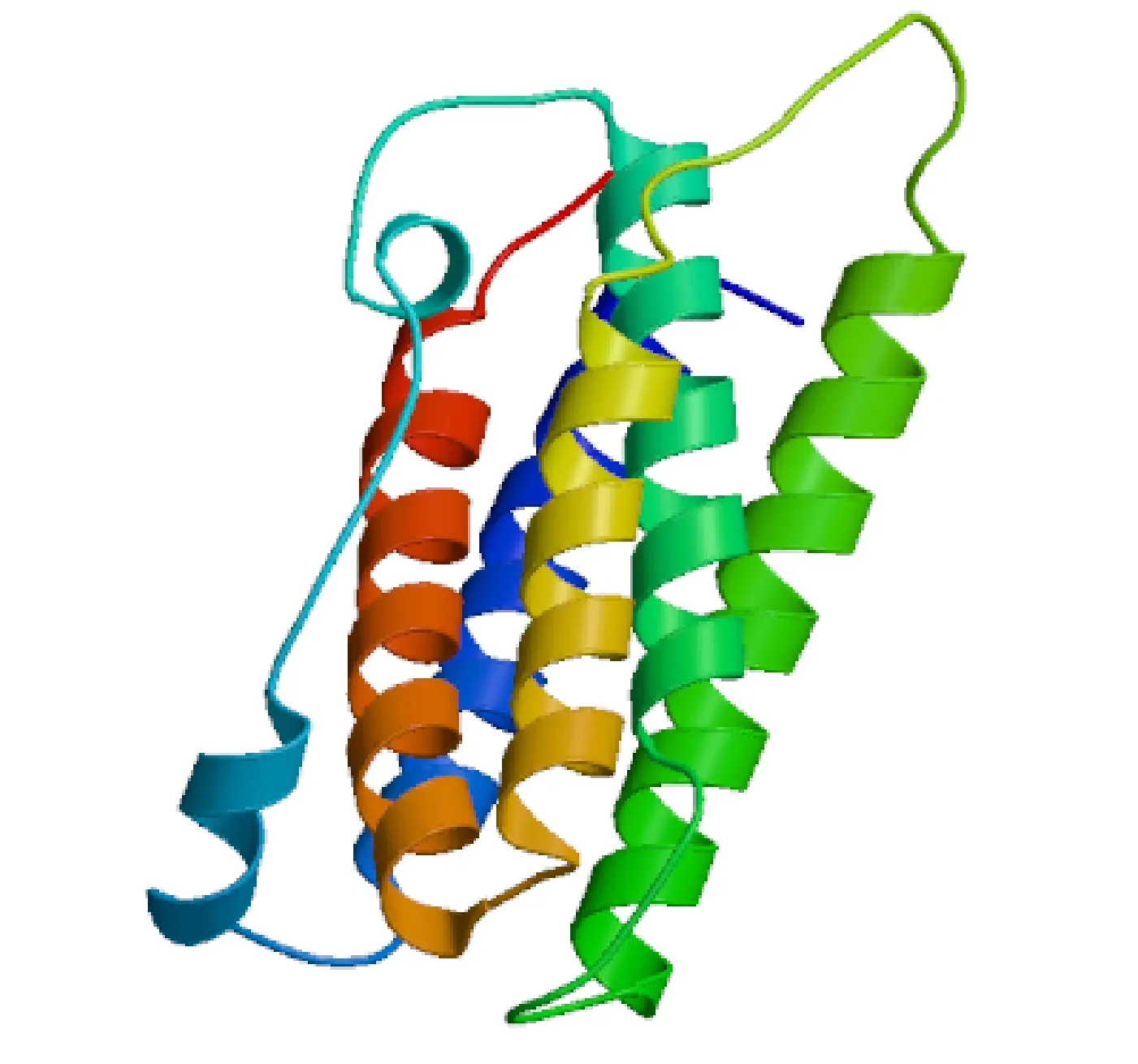
图7 合作猪IFN-ε蛋白三级结构预测Fig.7 Tertiary structureof IFN-ε protein in Hezuo pig
2.7 合作猪IFN-ε蛋白跨膜结构预测及信号肽分析
运用TMHMM对合作猪IFN-ε蛋白跨膜结构进行分析,预测结果表明IFN-ε蛋白不存在跨膜结构(图8)。使用SignalP 4.1软件预测蛋白信号肽发现,合作猪IFN-ε蛋白具有信号肽,综合考虑S值、C值、Y值的得分发现,其信号肽位于第1至第21位氨基酸残基之间(图9),说明该蛋白为分泌型蛋白。
2.8 合作猪IFN-ε蛋白的亚细胞定位分析
运用PSORT中k-NN计算程序预测合作猪IFN-ε蛋白亚细胞分布可能情况为:细胞质(cytoplasmic)11.1%、细胞核(nuclear)11.1%、线粒体(mitochondrial)11.1%、质膜(plasma membrane)22.2%、细胞外(extracellular,including cell wall)33.3%、液泡(vacuolar)11.1%,说明IFN-ε蛋白主要分布于细胞外。

图8 合作猪IFN-ε蛋白跨膜结构Fig.8 Transmembrane structure of IFN-ε protein in Hezuo pig

图9 合作猪IFN-ε蛋白信号肽预测Fig.9 Predicted result of IFN-ε protein signal peptide in Hezuo pig
2.9 合作猪IFN-ε蛋白的保守结构域预测
运用NCBI的CDD在线工具来预测合作猪IFN-ε蛋白保守结构域。结果显示,合作猪IFN-ε蛋白只含有1个超家族保守结构域,即IFab超家族,位于29~186位氨基酸残基(图10)。
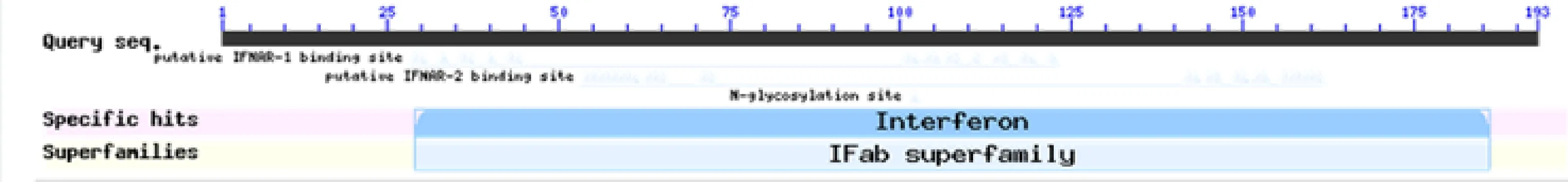
图10 合作猪IFN-ε蛋白保守结构域预测Fig.10 Conserved domain prediction of IFN-ε protein in Hezuo pig
3 讨 论
干扰素目前被确认为机体防御广谱的病毒性疾病的第一道防线[20-22],而Ⅰ型干扰素是先天性免疫和适应性免疫的核心[23]。Ⅰ型干扰素 IFN-α己经被广泛应用于临床治疗,但神经抑郁是其普遍的副作用[24];人IFN-ε具有部分IFN-α的功能,还具有维护脑神经正常等功能,有望成为IFN-α不良反应严重患者的替代药品[25];此外,IFN-ε在胎生哺乳动物早期胎盘发育过程中有重要作用[9-11]。近年来,人、鼠、犬、牛等物种IFN-ε相继被成功克隆[4,15,18]。本试验克隆获得合作猪IFN-ε基因的完整编码序列,全长582 bp,编码193个氨基酸,与台玉磊等人研究结果一致[19]。核苷酸序列对比结果发现,合作猪IFN-ε基因编码序列与杜洛克猪IFN-ε基因编码序列同源性高达98.4%,与羊、牛等哺乳动物同源性达到80%以上,而与小鼠的同源性仅为56.8%,这说明在近缘物种间IFN-ε具有较高的保守性;系统进化树结果也表明,合作猪与杜洛克猪的遗传距离最近,与小鼠遗传距离最远,进一步说明干扰素具有相对种属特异性。研究报道,大白长白二元杂交猪IFN-ε基因与小鼠IFN-ε基因同源性较差,符合物种间的亲缘关系[19],与本研究结果类似。基因编码区碱基突变,可能引起基因编码蛋白序列、结构和功能发生变化[25]。李莉莉等[26]发现,IFN-ε 155位半胱氨酸突变成丝氨酸后,重组人干扰素突变样品回收率明显高于未突变样品,但氨基酸突变后对重组人干扰素抗病毒活性没有明显影响。与杜洛克猪相比,合作猪IFN-ε基因CDS序列存在3个碱基突变,从而引起3个氨基酸突变,说明合作猪与杜洛克猪IFN-ε基因可能存在某些生物功能上的差异,这些差异是否影响猪的抗病性强弱还需今后进行深入研究分析。
合作猪IFN-ε蛋白不存在跨膜结构,说明其不是跨膜蛋白,但存在信号肽序列,表明该蛋白是分泌型蛋白,能在细胞外起作用,这与亚细胞定位预测结果一致。研究报道,人[7],犬[15],牛[18],大白长白二元杂交猪[19]IFN-ε蛋白均存在信号肽序列,且它们的蛋白编码序列N端前21个氨基酸为信号肽,与本研究结果一致。研究发现,一般情况下,新生蛋白通常在位于其N端的信号肽的指引下到达细胞特定区域,并由其介导进行跨膜转运[27],干扰素产生后必须与细胞膜上的特异性受体结合才能发挥其功能[28],合作猪IFN-ε蛋白信号肽的存在,对保证其发挥正常功能有重要意义。蛋白质半衰期与其稳定性之间存在密切联系,一般来说,半衰期长则蛋白质稳定性高[29]。有研究报道,蛋白质N端氨基酸序列与蛋白质稳定性具有很强的相关性,有近80%的短寿命蛋白含有信号肽[30]。本研究结果显示,IFN-ε蛋白具有较长的半衰期,却属于不稳定蛋白,这可能与合作猪IFN-ε蛋白存在信号肽有关。相对于IFN-ε蛋白中间氨基酸序列来说,其两端的氨基酸序列保守性较差,进一步分析发现,其中间氨基酸序列有一个保守结构域IFab。IFab结构域属于较大螺旋细胞因子超家族,包括生长激素、白细胞介素、若干集落刺激因子和若干其他调节分子,通过与细胞表面受体相互作用调节细胞活性,激活各种信号通路,能够参与抗病毒和抗增殖反应[31]。IFN通过与细胞表面受体IFNAR1和IFNAR2结合发挥其生物活性。IFN-IFNAR相互作用激活JAK1和TYK2激酶以及转录因子STAT1和STAT2[32-33]。Janus激酶/信号转导与转录激活子(The Janus kinase/signal transducer and activator of transcriptions ,JAK/STAT)信号通路和其他激酶和转录因子最终诱导IFN基因表达,保护机体免受病毒、细菌甚至真菌的感染[9,34-36]。Yang等[15]研究表明,犬IFN-ε能激活JAK/STAT信号通路,诱导干扰素诱导基因(ISGs)表达,发挥抗病毒作用[37]。本试验结果为进一步研究该基因的结构和功能提供了理论依据。
4 结 论
本试验克隆得到合作猪IFN-ε基因CDS序列,全长582bp。生物信息学分析表明,合作猪IFN-ε编码193个氨基酸,CDS序列存在3个突变,均为错义突变,其与瘤牛、蒙古野马、绵羊、山羊等物种同源性较高。IFN-ε蛋白为碱性、亲水、不稳定型蛋白,二、三级结构预测显示,该蛋白主要以α-螺旋和无规卷曲为主。

