茶树己糖激酶基因CsHXK1的克隆与表达分析
陈江飞,杨建坤,黄慧宇,余有本,王伟东
(西北农林科技大学 园艺学院,陕西杨凌 712100)
茶树[Camelliasinensis(L.)O.Kuntze]作为一种叶用经济作物,在中国乃至世界范围具有广泛的栽培种植。然而,茶树在其生长发育过程中经常面临着各种环境胁迫的影响,如冬季和早春的低温胁迫、夏季的高温和干旱胁迫,以及土壤盐渍化引起的高盐胁迫等。因此,明确茶树胁迫响应机制,筛选和鉴定抗性基因对培育抗性茶树优良品种具有重要意义。
众所周知,己糖(六碳糖,如葡萄糖和果糖)是植物中大多数代谢途径和有机物质合成的原始底物,其在参与糖酵解、呼吸作用、物质合成和分解代谢前需进行磷酸化,而己糖激酶(Hexokinase,HXK)是催化己糖磷酸化的关键酶之一[1]。目前,越来越多的研究证实HKX不仅具有催化己糖磷酸化的作用,其还参与植物糖感受和糖信号转导过程[2]。例如,拟南芥AtHXK1和AtHXK2反义转基因植株对外源葡萄糖的敏感性显著降低,而过表达转基因植株对外源葡萄糖高度敏感[3];进一步的研究表明,拟南芥AtHXK1通过感知葡萄糖水平,从而参与细胞增殖、根和花序生长、叶片膨胀和衰老以及叶片蒸腾等植物生长发育过程[4-6]。另外,植物HXK可以把叶绿体生成的糖信号传导到细胞核中,调节光合作用有关基因的表达,进而调控植物的光合作用,同时己糖激酶在质体-细胞核的信号传导中也有着至关重要的用途[7]。此外,许多研究证实HXK参与了植物对各种生物和非生物胁迫的响应过程。例如,NbHXK1、 AtHXK1和AtHXK2参与了甲基紫精和病原体感染诱导的氧化应激[8];低温、渗透和盐胁迫能够显著诱导拟南芥AtHXK2的表达,而抑制情况AtHXK3的表达[9-10];过表达的水稻OsHXK5或OsHXK6能够显著抑制植株生长,其可能依赖于对光合基因RBCS的抑制作用[11];类似地,AtHXK1在保卫细胞中的过表达促进了气孔的关闭,进而降低了糖处理下植株的蒸腾作用[6];HXK1通过氧化磷酸化调控水稻OsCIPK15基因的表达参与缺氧信号途径[12]。然而,茶树中有关NXK的研究相对滞后,其参与茶树胁迫响应的功能机制尚不清楚。
本试验从茶树中克隆获得了CsHXK1基因cDNA序列,利用生物信息学技术分析了该基因及其编码蛋白的结构特征,并利用实时荧光定量 PCR(qRT-PCR)分析了CsHXK1在高温、干旱、低温及盐胁迫下的表达模式,以期为探讨该基因逆境胁迫下的生物学功能奠定基础,为茶树抗逆分子遗传育种提供理论依据。
1 材料与方法
1.1 植物材料及处理
以长势一致的‘龙井长叶’品种茶树穴盘扦插苗为试验材料,于人工气候箱中进行预培养。2周后,分别对茶苗进行高温(40 ℃)、低温(4 ℃)、盐胁迫(200 mmol/L NaCl)和干旱胁迫(20% PEG 6000)处理,其他条件保持不变。每个处理设置3次重复,并于处理后0、2、6、12、24和48 h分别取0.1 g嫩叶;此外,取未处理茶苗的根、嫩茎、嫩叶以及花器官用于组织表达分析,所有样品用液氮速冻并置于-80 ℃保存,备用。
1.2 茶树总RNA提取和cDNA合成
茶树叶片材料的总RNA采用CTAB法进行提取,用NanoDrop 2000c(Thermo Scientific,美国)对RNA的浓度和质量进行检测,再经质量分数为1%变性琼脂糖凝胶电泳检测RNA的完整性。利用反转录试剂盒(ABM,加拿大)合成cDNA用于基因的克隆及荧光定量PCR反应。
1.3 茶树 CsHXK1基因的克隆
根据茶树基因组[13]中CsHXK1基因序列设计特异性全长引物(F:GAATCGATCTCTGAGCCTGTGATGG,R:CTGAATACTTGGCCTTTGACCAT),以‘龙井长叶’品种茶树cDNA为模板进行PCR扩增,PCR反应程序为:94 ℃ 预变性5 min;94 ℃ 30 s,60 ℃ 30 s,72 ℃ 2 min,32 个循环;72 ℃ 延伸10 min。PCR产物经质量分数为1.25%琼脂糖凝胶电泳检测并回收目的条带,回收产物连接至pMD19-T 载体(TaKaRa,大连)进行测序。
1.4 生物信息学分析
利用ProtParam tool在线软件(https://web.expasy.org/protparam/)预测蛋白理化性质;ProtScale(http://web.expasy.org/cgi-bin/protscale/protscale.pl)进行亲/疏水性分析;Netphos 3.0 Serve(http://www.cbs.dtu.dk/services/NetPhos)预测蛋白质磷酸化位点;用软件DNAMAN8 进行多序列比对,用MEGA 6.0构建系统进化树;用在线软件WoLF PSORT(https://wolfpsort.hgc.jp/)预测蛋白亚细胞定位,采用SignaIP(http://www.cbs.dtu.dk/services/SignalP/)在线软件进行信号肽预测。
1.5 实时荧光定量PCR(qRT-PCR)分析
根据基因序列设计定量引物(F:CAGAATATGATCAAGCATTGGAT,R:TATGAGGGGTCCTTAAAATAAATGG),以茶树CsPTB基因为内参基因(F:TGACCAAGCACACTCCACACTATCG,R:TGCCCCCTTATCATCATCCACAA),参照SYBR○RPremix ExTaqⅡ(TaKaRa,大连)试剂盒说明进行qRT-PCR分析,反应程序为:95 ℃ 3 min;95 ℃ 30 s,60 ℃ 1 min 30 s,循环 40次;60 ℃ 30 s,71 个循环,每次上升0.5 ℃。每个样品设3次技术重复,数据采用2-ΔΔCT算法分析[14]。
1.6 数据处理
利用Excel 2010和SPSS 22软件对试验数据进行处理和统计分析。
2 结果与分析
2.1 茶树 CsHXK1基因的克隆
以茶树‘龙井长叶’叶片的cDNA为模板,通过RT-PCR扩增获得特异性单一条带(图1),测序结果显示该条带序列全长1 534 bp,包含一个1 488 bp的开放阅读框,编码495个氨基酸,与茶树基因组中序列一致为茶树CsHXK1基因cDNA序列。此外,基因结构分析结果显示茶树CsHXK1基因由9个外显子和8个内含子组成(图2)。
M. DL2000; 1-2:PCR产物 PCR amplification product
图1 茶树CsHXK1基因cDNA全长序列RT-PCR扩增
Fig.1 RT-PCR amplification of the full-length cDNAofCsHXK1gene in tea plant
2.2 茶树CsHXK1蛋白多序列比对与进化分析
多序列比对结果显示,茶树CsHXK1蛋白与其他物种的HXK1蛋白具有较高的相似性,且均包含2个磷酸化作用位点:phosphate 1和phosphate 2、一个底物结合位点sugar binding和一个ATP结合位点(图3)。进化分析显示,茶树CsHXK1蛋白与拟南芥AtHXK1、苹果MdHXK1和甘蓝BoHXK1的进化关系较近,而与单子叶植物水稻的亲缘关系较远(图4)。
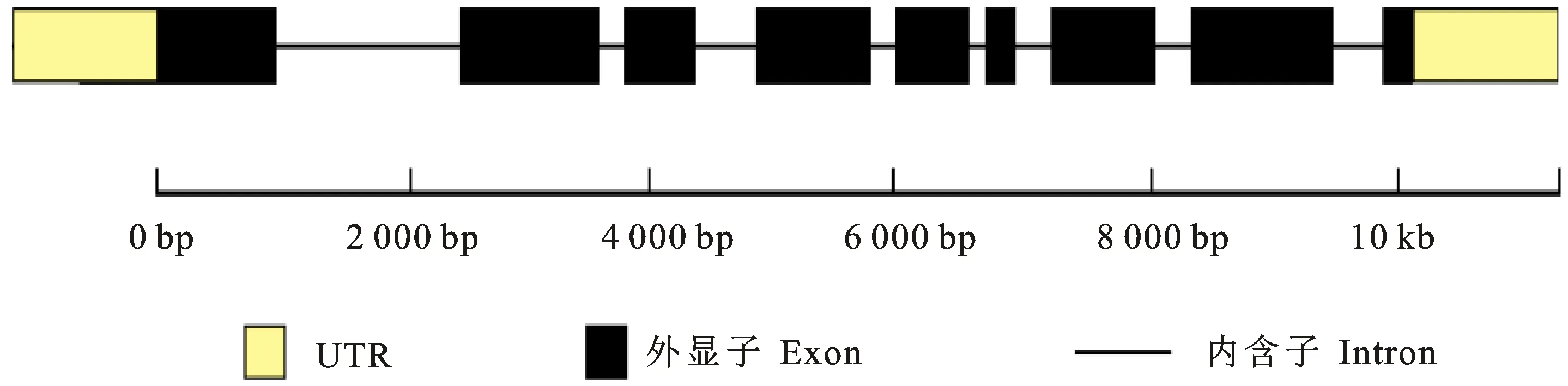
图2 茶树 CsHXK1基因的结构分析Fig.2 Structural analysis of CsHXK1 gene in tea plant
2.3 茶树CsHXK1蛋白生物信息学分析
2.3.1 茶树CsHXK1蛋白理化性质分析 蛋白理化性质预测显示,茶树CsHXK1蛋白分子式为C2379H3816N652O709S23,其蛋白分子质量为53.63 ku,理论等电点为5.96,含有负电荷残基(Asp+Glu)62个,正电荷残基(Arg+Lys)54个。疏水性分析结果显示CsHXK1蛋白的亲水区域大于疏水区域,且GRAVY指数为-0.002,表明其属于亲水性蛋白(图5)。

实线框为磷酸化位点 The solid line frame is the phosphorylation site;虚线框为ATP结合位点 The dotted line frame is the ATP binding site;下划线为底物结合位点 The underline is the substrate binding site
图3 茶树与其他植物HXK1蛋白的多序列比对
Fig.3 Multiple sequence alignment of HXK1 from tea plant and other plants
2.3.2 茶树CsHXK1蛋白磷酸化分析 磷酸化位点预测分析显示,CsHXK1蛋白包含多个磷酸化位点,其中以丝氨酸位点居多,推测其可能受到磷酸化的调控作用(图6)。亚细胞定位预测结果显示CsHXK1蛋白主要定位与叶绿体和细胞核中;此外,SignalP软件预测显示在CsHXK蛋白的第54~55位氨基酸处存在信号肽。
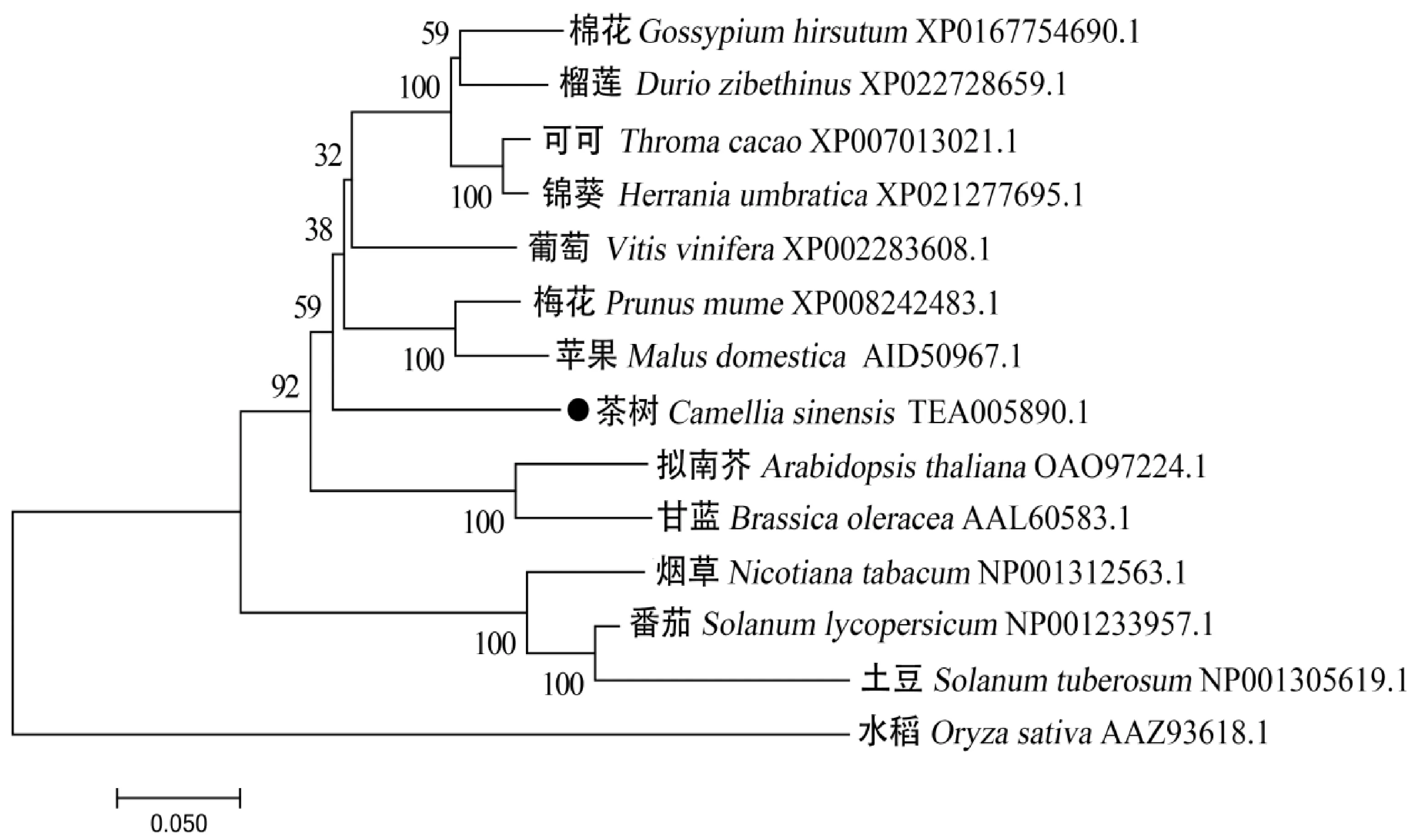
图4 不同物种的HXK1蛋白进化分析Fig.4 Phylogenetic analysis of HXK1 protein sequences from different species
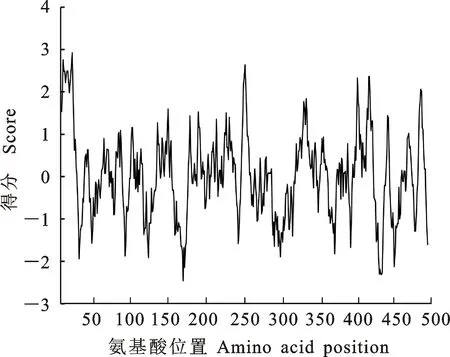
图5 茶树CsHXK1蛋白疏水性分析Fig.5 Hydrophobicity analysis of CsHXK1 protein
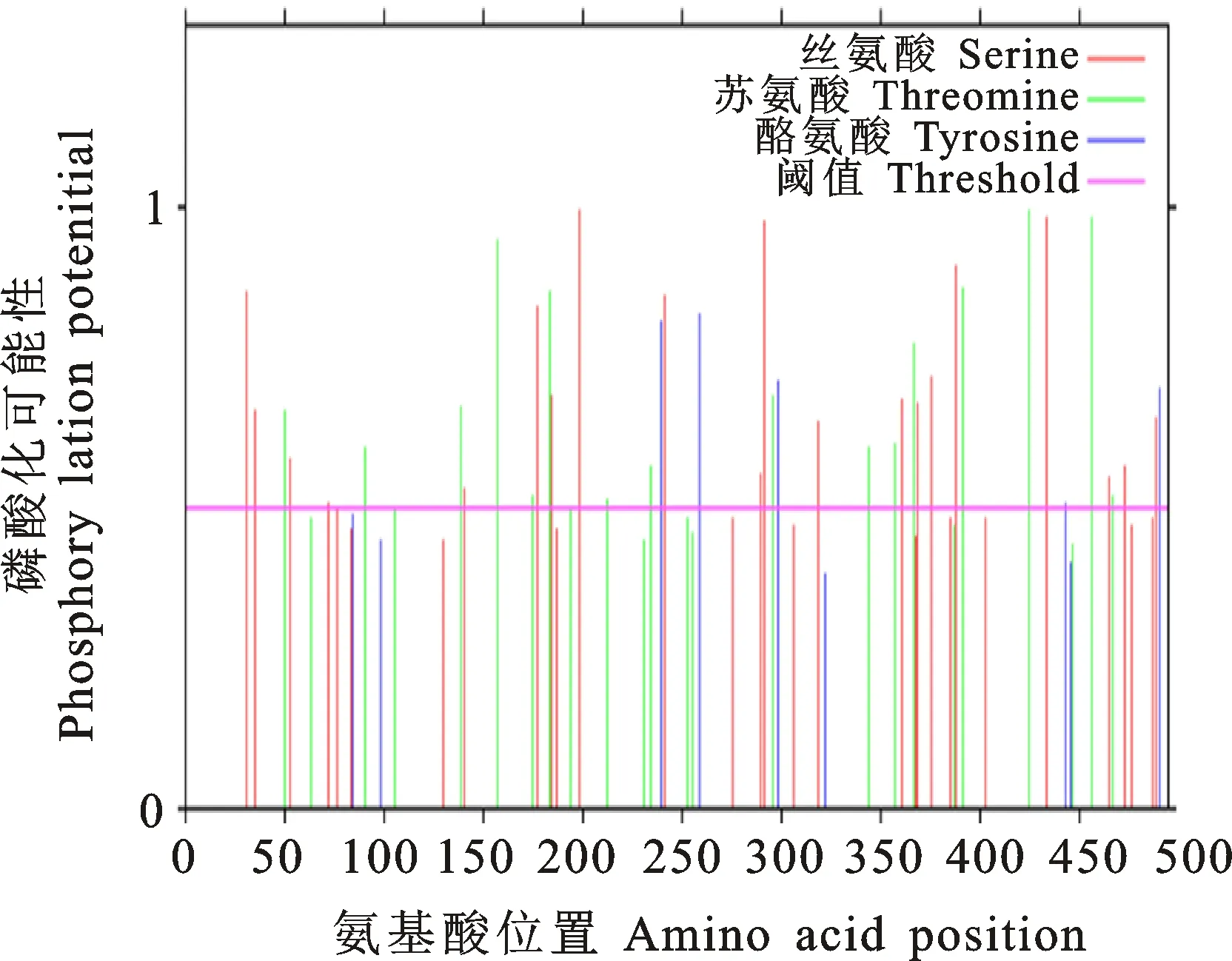
图6 茶树CsHXK1蛋白磷酸化位点分析Fig.6 Analysis of phosphorylation site of CsHXK1 protein
2.4 茶树 CsHXK1基因启动子顺式作用元件 分析
利用PLACE软件对CsHXK1基因上游启动子区域的顺式作用元件进行预测,结果发现CsHXK1基因启动子区域含有与逆境胁迫响应相关的元件,如脱落酸响应元件ABRE、机械损伤响应元件Wun-motif、脱水响应元件ACGTATERD1和低温响应元件MYBCORE等,还包含多个与激素信号转导和糖信号转运等相关的顺式作用元件,如TGACG-motif和MYCCONSENSUSAT等 (表1)。
2.5 茶树 CsHXK1在不同组织中的表达分析
如图7所示,CsHXK1基因在各个组织中都能被检测,且呈现出一定的组织表达特异性,其在茶树的花器官中表达量最高,其次是叶片,根和茎中最低。
2.6 非生物胁迫下茶树 CsHXK1基因表达模式分析
qRT-PCR结果显示,在不同胁迫处理下茶树CsHXK1基因均被诱导表达,但其表达趋势存在明显差异(图8)。其中,CsHXK1的表达水平在高温处理的前12 h快速升高,且在第12 h达到峰值,约为对照的10倍左右,之后其表达量急速回落到对照水平;而20% PEG 6000模拟干旱处理下,CsHXK1基因表达水平逐步上升,在第 48 h达到对照的6~7倍,但在12 h时有轻微的降低;在低温处理下,CsHXK1在第2 h受诱导上调表达,并在第12 h达到表达峰值,后期逐渐回落;CsHXK1在盐处理下一直维持较高的表达水平。
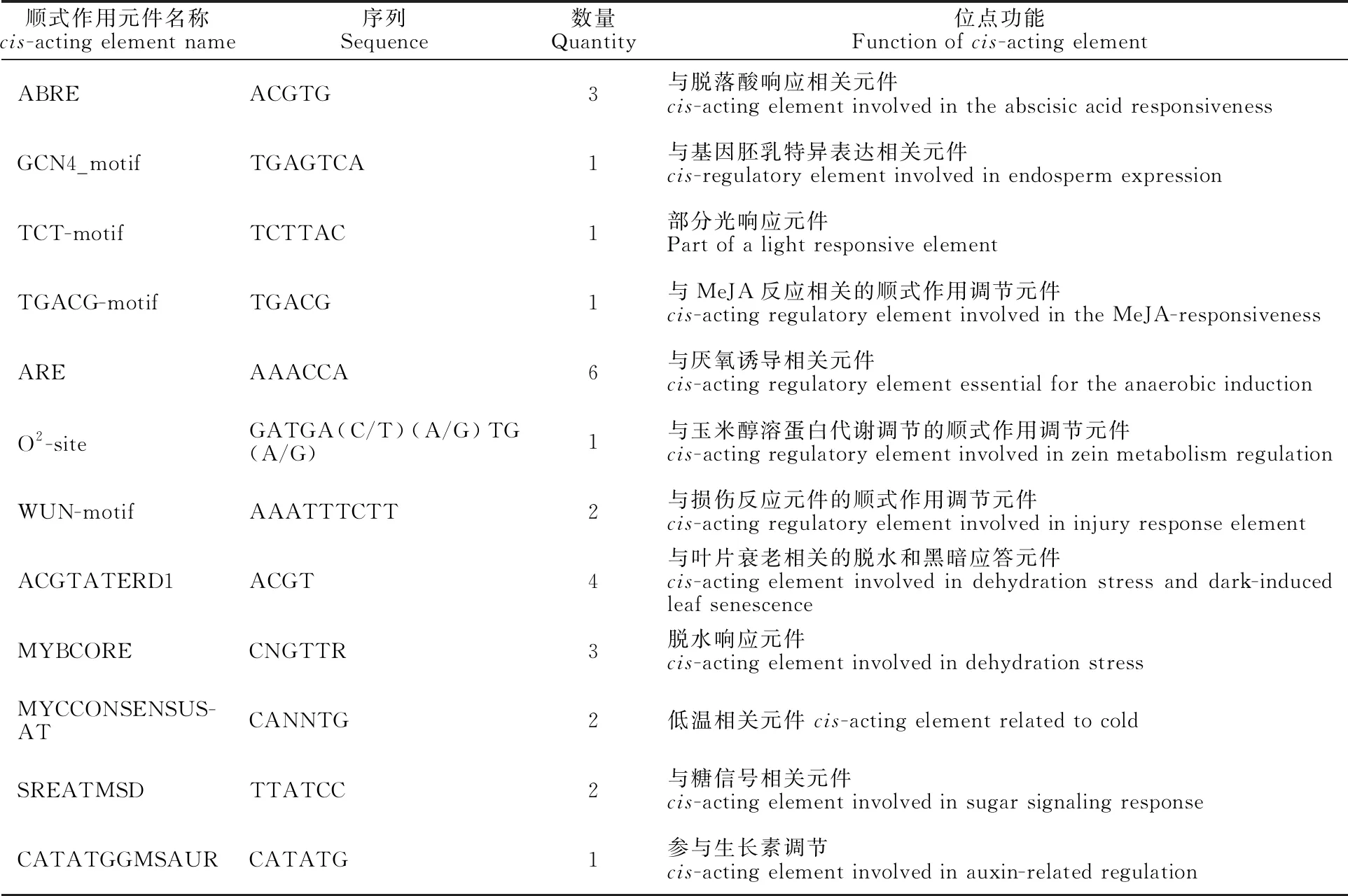
表1 茶树 CsHXK1基因启动子区域重要顺式作用元件分析Table 1 Analysis of important cis-acting regulatory elements in the upstream regulatory sequence of CsHXK1
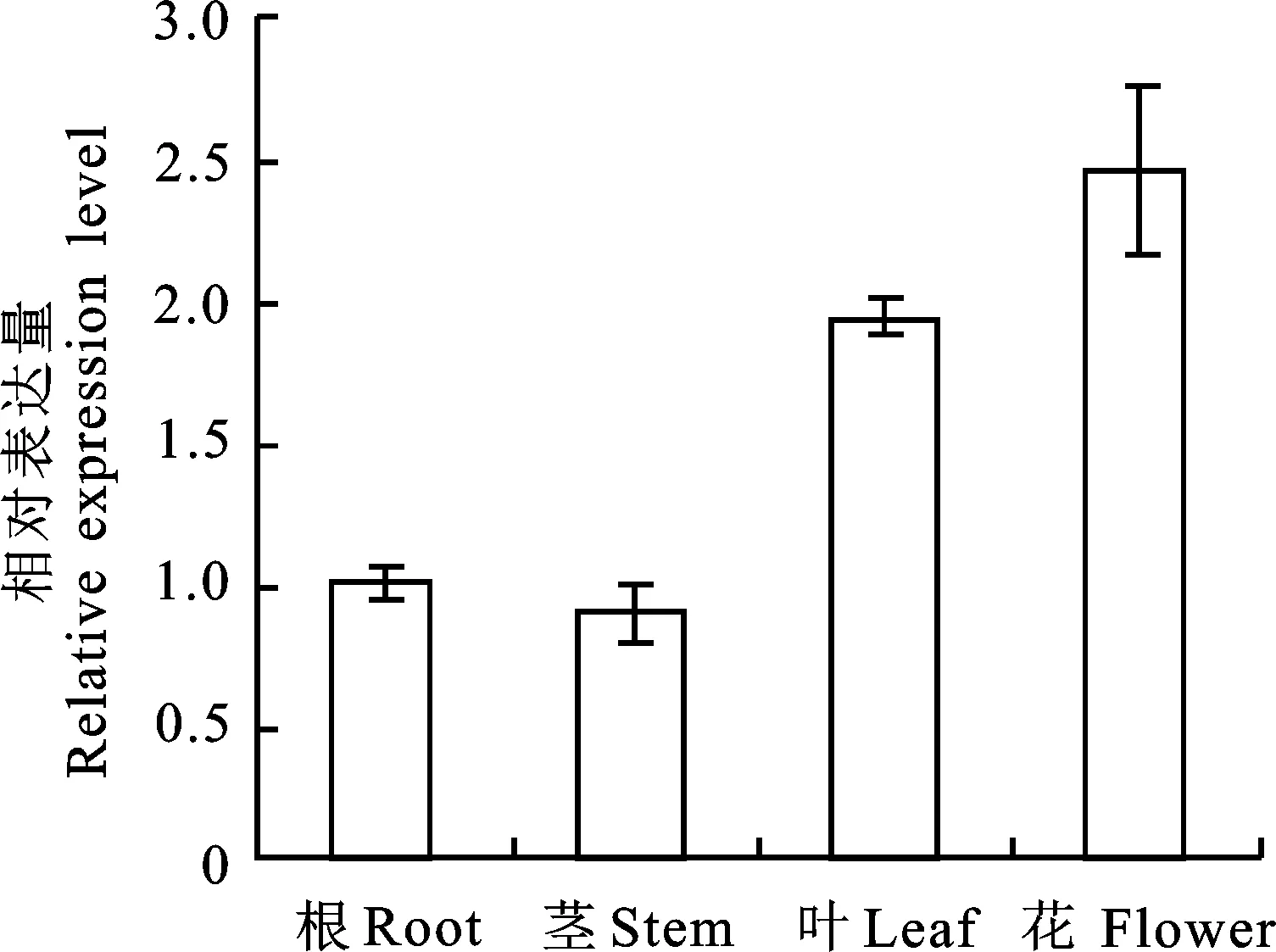
图7 茶树 CsHXK1基因在不同 组织中的表达分析Fig.7 Analysis of expression of CsHXK1 gene in different tissues
3 讨 论
HXK蛋白不仅能够催化己糖磷酸化,为植物的生命活动提供能量保证,而且在糖信号转导以及逆境响应方面也具有重要的生物学功能。目前,有关于HXK蛋白的研究已经成为广泛关注的热点[15-16]。
目前,拟南芥中鉴定有6个HXK成员,其中AtHXK1.2、AtHXK1.3、AtHXL1和AtHXL2基因包含9个外显子和8个内含子[2];Cho等[17]发现除了水稻OsHXK1之外,绝大多数的OsHXK含有相同数量的外显子和内含子。同时, Guo等[18]证实基因的内含子数目与长度对基因的表达具有重要影响。本研究中笔者也发现茶树CsHXK1基因由9个外显子和8个内含子组成,这与小立碗藓[19]和苹果[20]HXK的研究结果一致,表明单、双子叶植物的HXK1基因的结构均高度保守,推测其发挥着类似的生物学功能。另外,信号肽预测显示茶树CsHXK1蛋白在N端具有信号肽,这暗示CsHXK1可能是分泌性蛋白,其在信号肽的作用下,运输到指点地点后对其目标底物进行磷酸化作用[20]。前人的研究指出,植物HXK蛋白在细胞中的定位具有明显的不同,如拟南芥AtHXL2和AtHXL3定位于线粒体膜上[2],烟草HXK蛋白则定位于叶绿体[21],还有一些单子叶植物如水稻玉米的HXK蛋白定位于细胞质内[21],且不同的亚细胞定位也导致其功能上的差异[22]。笔者预测发现茶树CsHXK1蛋白主要定位于叶绿体和细胞核中,结合Cho等[11]研究认为细胞核内的HXK蛋白能够与VHA-B1和RPT5B结合成复合体,并作用于葡萄糖信号调节基因的启动子,以此调控目的基因的表达;而定位于叶绿体中的HXK在功能上主要是对叶绿体中的己糖进行磷酸化[19,23],推测茶树CsHXK1蛋白可能在叶绿体和细胞核中也具有相类似的功能,然而这需要进一步试验验证。
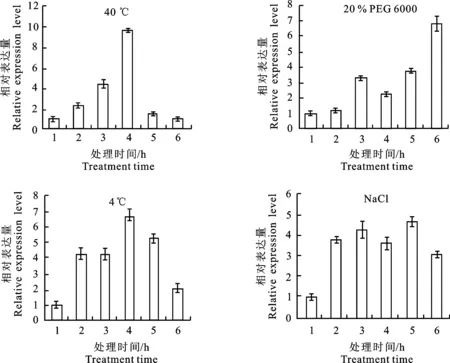
图8 茶树 CsHXK1基因的表达模式分析Fig.8 Analysis of expression pattern of CsHXK1 gene in tea plant
许多研究表明,HXK基因在植物不同组织间的表达水平有较大差异,对植物的生长发育起到不同的调控作用[2,17]。例如,甘薯IbHXK1在成熟的块茎中表达较高,参与对淀粉的酵解过程[24];水稻多数HXK在水稻的未成熟的种子、茎、叶片、花中均有表达,而OsHXK10仅在花中被检测到[2];苹果MdHXK1则主要在花中表达,并与花瓣中花青素的积累密切相关[20]。本研究发现茶树CsHXK1也在叶片和花中有较高的表达,表明其可能在上述组织器官中发挥重要作用。此外,大量研究已证实HXK广泛参与植物非生物胁迫响应过程,例如过表达拟南芥AtHXK1和AtHXK2能够明显增强转基因植株对氧化胁迫的耐受性[8];拟南芥AtHXK2受到干旱、盐和低温的显著诱导,而高温、干旱等逆境也会提升AtHXKL3的转录水平[9];在水稻和向日葵中,一些HXK的同源基因也不同程度的受非生物胁迫的诱导[25-26]。最近,赵锦等[20]发现苹果MdHXK1除了受到盐、低温及外源ABA的显著诱导,还发现其启动子区域包含多个与逆境响应的相关元件。本研究亦发现茶树CsHXK1基因启动子区域含有多个逆境响应元件,如ABA响应元件、脱水响应元件及低温响应元件,这可能与其响应逆境胁迫具有密切的联系。同时,qRT-PCR结果也表明茶树CsHXK1受到高温、干旱、低温及盐胁迫的显著诱导,这与Li等[27]的结果高度一致,意味着CsHXK1参与到多种非生物胁迫响应过程中。本研究为进一步探究茶树CsHXK1在非生物胁迫响应过程中的功能提供了重要的前期参考。

