一株链霉菌的分离、鉴定及其特性研究
雒晓芳,陈丽华,杨成波,徐娟娟,娜吾巴尔·阿布都黑力,赵梓彤
1西北民族大学实验教学部;2西北民族大学化工学院,兰州 730030;3中国人民解放军联勤保障部队第940医院 介入治疗科,兰州 730050;4西北民族大学生命科学与工程学院,兰州 730030
多环芳烃(polycyclic aromatic hydrocarbons,PAHs)是由两个或两个以上苯环构成的稠环化合,它主要来源媒,石油,木材,烟草,有机高分子化合物等有机物不完全燃烧时产生的挥发性碳氢化合物,是环境持久性污染物中最具有代表性的一类持久性有机污染[1]。PAHs有很多种,蒽属于其中的一种,由于PAHs有难降解性、生物毒性、生物累积性和很强的致癌性[2],严重威胁着人类身体健康,因此如何除去环境中的PAHs,保证人类健康和自然环境的可持续发展成为了现代学术领域的热门问题。
近几年,通过各国环境科学领域的研究和实验表明,解决环境中多环芳烃污染物主要是通过物理[3,4]、化学[5,6]和生物[7,8]三种解决途径。由于微生物的代谢,主要依靠自身产生的酶来进行,当微生物体中脱氢酶活性较高时,微生物的分解代谢能力越强,代谢效率高越高,对污染物的降解性能越好,所以目前大多数用微生物降解的方法除去环境中的污染物[9]。Fan等[10]利用微生物菌群对混合烃进行降解发现,该菌群对去除土壤中由环十二烷、正 十六烷和芘所构成的混合烃类污染物具有明显的促进作用,各类污染物的降解速率均呈现先高后低的趋势,与微生物多样性、数量以及活性变化趋势相似。Ma等[11]采用高浓度的PAHs作为环境选择压力,获得了高效多环芳烃(PAHs)降解菌群,结果表明,菲菌和芘菌对高环多烃PAHs具有较强降解能力。Luo等[12]等通过采用苏云金芽孢杆菌(Bacillusthuringiensis)在不同温度、pH、PAHs质量下对蒽、芘、芴的降解性能,实验结果表明,温度与pH交互项对蒽、芘的降解影响较显著,温度与PAHs质量交互对芴的降解影响较显著。
近年来,蒽、芘、芴通常被用来研究PAHs微生物降解机制的模式化合物。本文主要是在自然界中筛选能够对蒽进行降解的微生物[13],并对微生物进行分离鉴定,然后分析了暗黑微绿链霉菌在不同温度、pH、菌液量、盐度条件下对蒽化合物的降解性能及脱氢酶活性,通过响应面法设计和单因素实验的方法,以温度、pH、浓度为自变量,降解率为因变量分析各因素之间的交互作用,找出降解蒽的最佳脱氢酶条件,为多环芳烃污染土壤的修复技术提供资源保障和科学依据。
1 材料与方法
1.1 材料
1.1.1 菌种来源
从甘肃华庆油田油井附近地表深度为10 cm左右石油污染土壤中富集、筛选分离得到1株优势菌株,初步命名为Sa。
1.1.2 主要试剂
蒽(An)、氢氧化钠(NaOH)、盐酸(HCl)、环己烷、甲苯(以上均为分析纯),活性炭(颗粒状和粉状)、浓硫酸(H2SO4,优级纯)
1.1.3 仪器
KRQ-400P 智能型人工气候箱(上海 齐欣科学仪器有限公司);TU-1901 双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);S.SW-CJ-2F 净化工作台(上海跃进医疗器械厂)
1.2 鉴定方法
1.2.1 菌株鉴定
1.2.1.1 形态观察与生理生化鉴定
在30 ℃下,将分离筛选而得的菌悬液涂布在营养琼脂平板上培养,2天后观察菌株的生长情况,记录菌落特征。进行简单染色,在显微镜下观察该菌株的形态特征。参照《微生物学实验(第4版)》对菌株进行生理生化鉴定。
1.2.1.2 分子生物学鉴定
以细菌总DNA为模板进行扩增,采用细菌16S rDNA PCR通用引物:8F(′-AGAGTTTGATCCTGGCTCAG-3′)和1512R(5′-ACGGCTACCTTGTCGAC TT-3′),进行PCR扩增,反应条件为:94 ℃预变性5 min ,94 ℃变性1 min,55 ℃退火1 min,72 ℃延伸1.5 min,共30次循环;最后72 ℃延伸5 min。扩增后的产物寄到宝生物有限公司测序。将16S rDNA测序结果用BLAST软件与Genbank中已登录的16S rDNA序列进行同源性比较。用分子进化遗传学分析与序列比对软件MEGA5.1的邻近相接法(Neighbor-Joining Method)对clustalx多重比对结果进行系统进化分析,采用Boot strap方法500个重复进行可靠性检验。
1.3 菌株的培养基及培养条件
将制备的营养肉汤培养基,放在121 ℃高压灭菌15 min,备用。在无菌条件下将该菌株接种于待用的营养肉汤培养基中,37 ℃培养24 h。
1.4 单因素降解率的测定
用索氏提取法测定降解率,降解时间48 h左右,取出装置,提取瓶中吸取0.5 mL定容至50 mL,环己烷作为空白对照在紫外分光光度计290 nm处测定吸光度值,并与标准曲线作对比,计算得出残留量和降解率,记录数据、绘制折线图。
1.4.1 温度梯度设定及实验方法
将制备好的若干样品各加入5 mL菌液(选择40~50 h的菌悬浮液进行降解特性研究,以下类同。设计3个重复组),恒温培养箱分别调至24、26、28、30、32 ℃进行2 h恒温振荡培养[14]。
1.4.2 pH 梯度设定及实验方法
将制备好的菌液分为五份,用1 mol/L的盐酸和氢氧化钠分别调至pH为3、5、7、9、11[15],放入制备好的若干样品中(设计3个重复组),混匀放置28 ℃恒温培养箱振荡培养72 h。
1.4.3 菌液量梯度设定及实验方法
将制备好的样品分别加入1、3、5、7、9 mL Sa菌液(设计3个重复组),混匀放置28 ℃恒温培养箱振荡培养72 h。
1.4.4 盐度梯度设定及试验方法
将制备好的菌液分为五份,用NaCl分别调至盐度为40、80、120、160、200 mmol/L五个值。调制后分别加入制备好的若干样品中(设计3个重复组),混匀放置28 ℃恒温培养箱振荡培养72 h。
1.5 脱氢酶活性测定方法
将培养物称取1 g于15 mL离心管,加入3 mL蒸馏水洗涤,在离心机上4 000 rpm离心3 min,倒出上清液(设计3个重复组)。再次加入3 mL蒸馏水、2 mL Tris-HCL溶液、0.5 mL TTC溶液,放置37 ℃培养箱24 h后取出,立即加入2滴浓硫酸终止反应。振荡均匀并加5 mL甲苯。离心机上4 000 rpm离心3 min。甲苯作为空白对照,在紫外分光光度计486 nm处测上层红色液体的吸光度,对比标准曲线计算出脱氢酶活性[16]。
1.6 多因素降解
在单因素实验基础上,选出三个最能影响蒽降解多环芳烃的因素并进行条件优化。利用Box-Behnken 实验设计原理以温度,pH,菌液量3个因素为自变量,降解率为响应值设计三因素、三水平的响应面实验,温度分别为25、27.5、30 ℃,pH分别5.0、7.0、9.0,菌液量分别为3、5、7 g。每组实验重复3 次。根据实验结果,利用Design-Expert 8.0.6 Trial软件进行方差分析以及响应面分析,从而优化实验模型。
2 结果与讨论
2.1 菌株的鉴定
2.1.1 菌株的形态观察
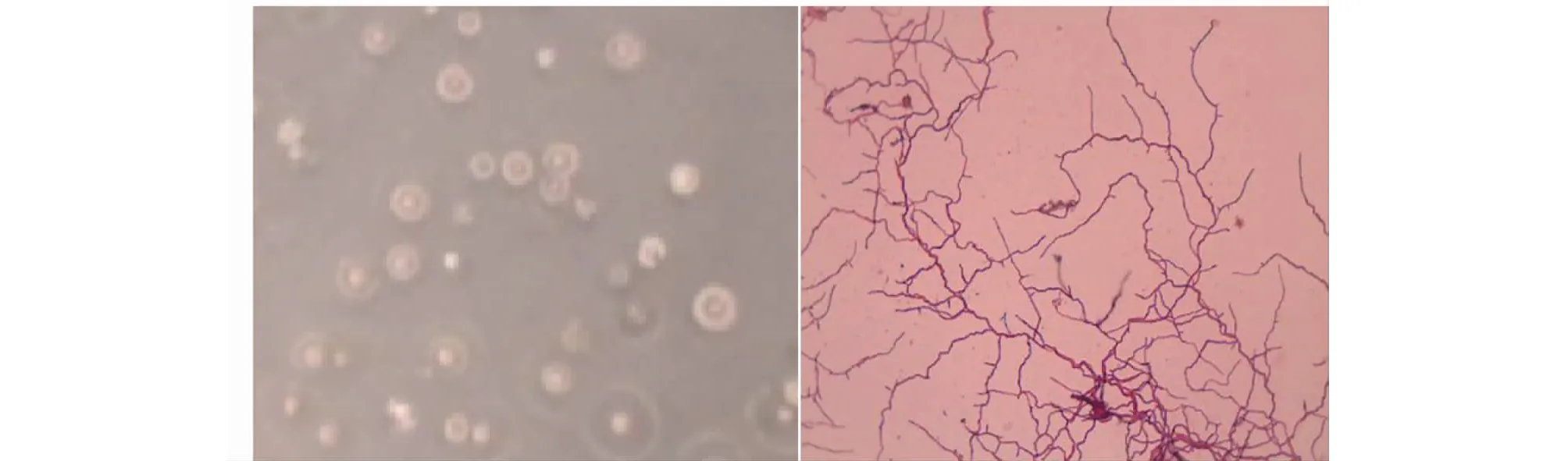
图1 菌株的菌落形态及染色(×1000)Fig.1 Colony morphology and staining of strain (×1000)注:石碳酸复红染色。Note:Red staining with carbolic acid.
该菌株培养两天后取出观察,此菌生长旺盛,菌落白色,不规则圆形,呈辐射毛绒状,表面干燥无光泽,菌落与培养基间连接紧密,不易挑取。显微镜下观察菌丝均为丝状,无运动性。根据Sa菌株的培养特征及染色后显微镜下形态观察,初步推测该菌株应为链霉菌属(Streptomyces)某菌种。
2.1.2 菌株的生理生化特征
各种微生物在代谢类型上表现出的差异反映出它们具有不同的酶系和不同的生理特征,这些特性可被用作为微生物鉴定和分类的内容。该株菌的生理化鉴定中明胶液化、淀粉水解、硝酸盐还原、葡萄糖、阿拉伯糖、木糖、鼠李糖、肌醇、甘露醇、蔗糖 、果糖,呈阳性,运动性、纤维素水解呈阴性,石蕊牛奶表现出凝固且胨化。结果表明,该株菌能利用多种糖类物质作为碳源和能源生长代谢,可分泌淀粉酶和蛋白酶,动力实验显示无运动性。
2.1.3 菌株生长曲线趋势
根据生长曲线测定方法所得此菌的生长曲线数据可知,该株菌的停滞期较长,20 h之后进入对数生长期,36 h进入稳定期,48 h后开始衰亡菌液浓度降低。
2.2 16S rDNA系统进化分析
将16S rDNA测序结果与Gen bank中已登录的16S rDNA序列进行同源性比较。结果显示,菌株Sa的16S rDNA序列与暗黑微绿链霉菌(Streptomycesatrovirens)的16S rDNA序列具有100%同源性。在此基础上利用MEGA5.1的邻近相接法构建菌株的系统发育树。综上所述,结合形态学观察、生理生化特性及16S rDNA测序结果综合分析,将菌株Sa菌株归属于暗黑微绿链霉菌(Streptomycesatrovirens)属的一种。
2.3 不同温度条件下脱氢酶活性与降解率的关系
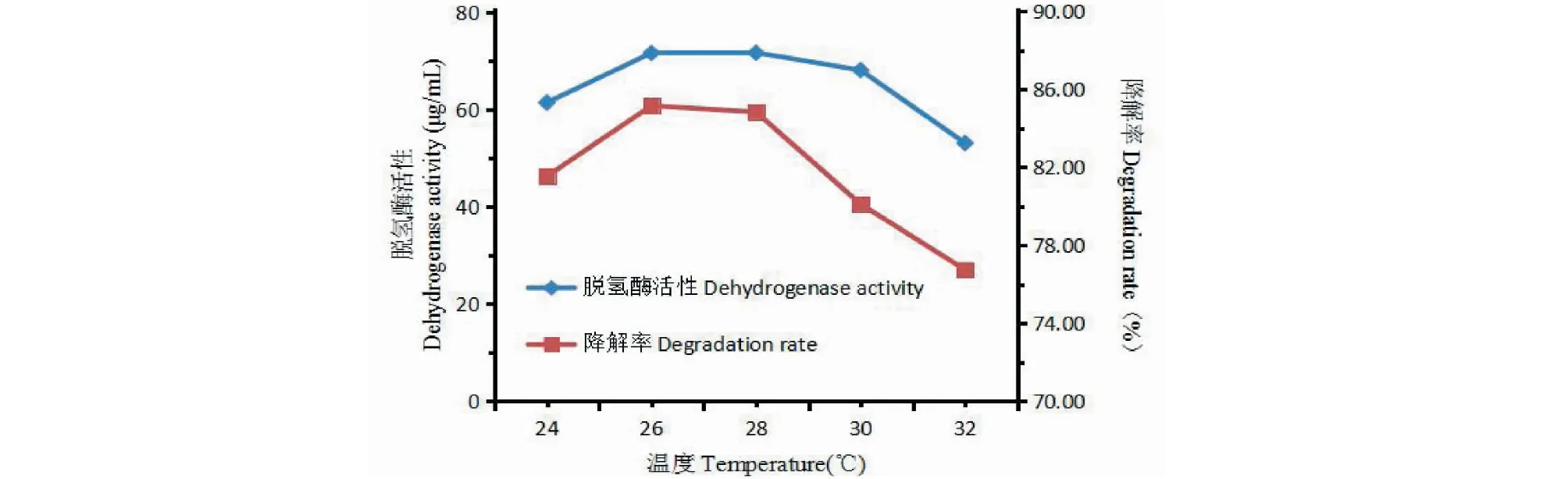
图2 不同温度下蒽的脱氢酶活性与降解率Fig.2 Dehydrogenase activity and degradation rate of anthracene at different temperatures
由图2可知,Sa在不同温度条件下对蒽降解率与脱氢酶活性呈先增大后减小趋势,蒽在样品培养温度达到28℃时脱氢酶活性最高,温度高于28 ℃时降解率与脱氢酶活性随温度升高而下降。蒽的脱氢酶活性最高达到了86.46 μg/mL,可见温度对酶活性有着较大的影响,低温或高温都会降低脱氢酶活性。因为在低温时,细胞代谢能力较低,会使降解率降低,当温度为28 ℃时,酶活性最高,代谢旺盛,降解率也会较高,当环境温度过高,酶可能失活,降解率下降[17]。因此在26~28 ℃时降解效果最好,蒽的降解率高达93.86%。
2.4 不同pH条件下蒽的脱氢酶活性与降解率关系
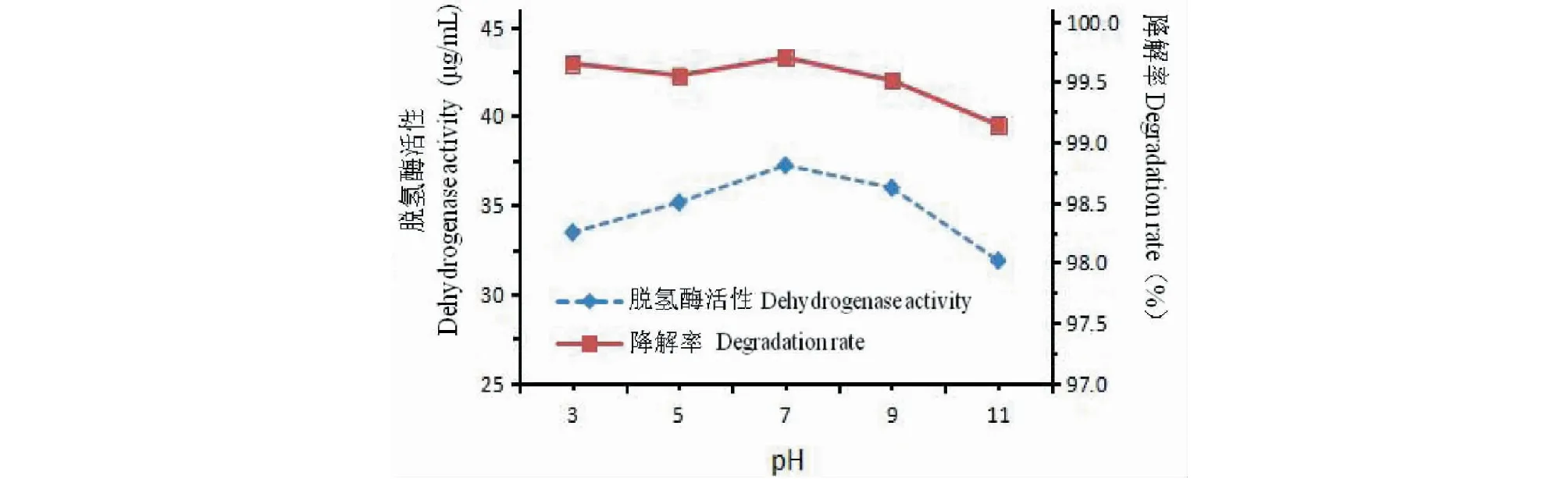
图3 不同pH条件下的蒽的脱氢酶活性与降解率Fig.3 Dehydrogenase activity and degradation rate of anthracene under different pH conditions
由于H+浓度影响微生物对营养物的吸收和生化反应,环境中pH值将会对微生物的生长具有一定的影响[18]。如图3所示,蒽的脱氢酶活性与降解率随着pH值的增大呈现出先增大后减小的趋势,在pH为7时蒽的脱氢酶活性与降解率达到了最高。由此可见pH对Sa降解蒽产生脱氢酶有较大的影响。这种现象与细胞酶的活性受pH值影响有关,pH值过高或过低均影响酶活性,从而降低细胞代谢速率。当处于最佳pH值时,利于酶发挥最佳活性,利于细胞对物质的代谢,故降解率最高。降解率表现出与脱氢酶活性同步,因此也可以判断出二者有一定相关性。
2.5 不同菌液量下蒽的脱氢酶活性与降解率关系
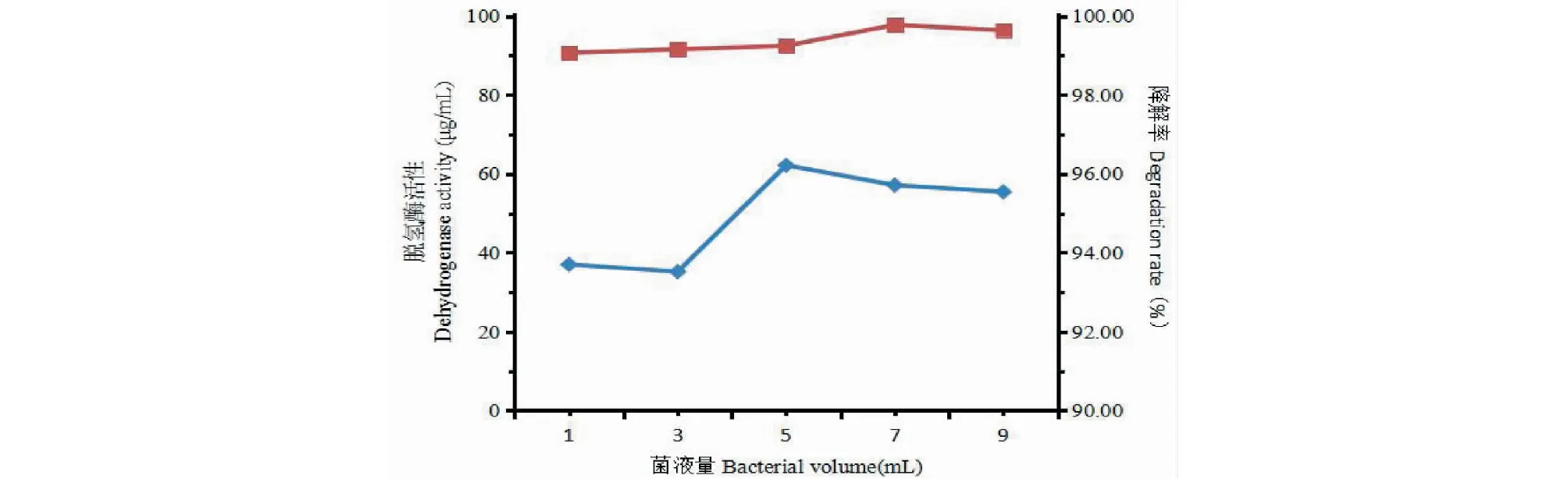
图4 不同菌液量下蒽的脱氢酶活性与降解率Fig.4 Dehydrogenase activity and degradation rate of anthracene under different bacterial liquid amounts
在环境因素固定的情况下用不同量的Sa进行降解,来测试同样活性的菌株数量在不同的情况下对降解率的影响。由图4可知,蒽的降解率随着菌液量的增加不断地增加,蒽的脱氢酶活性呈现出先增加后减小的趋势,在菌液量为5 mL时蒽的脱氢酶活性达到了62.19 μg/mL。由此得出蒽的降解率随着菌液量的增加降解率也在增加,但总体来看变化幅度不大,增长的范围小,变化不明显。蒽的脱氢酶活性随着菌液量的增加,先增加后减小,在菌液量为5 mL时活性最高。
2.6 不同盐度件下蒽的脱氢酶活性与降解率关系
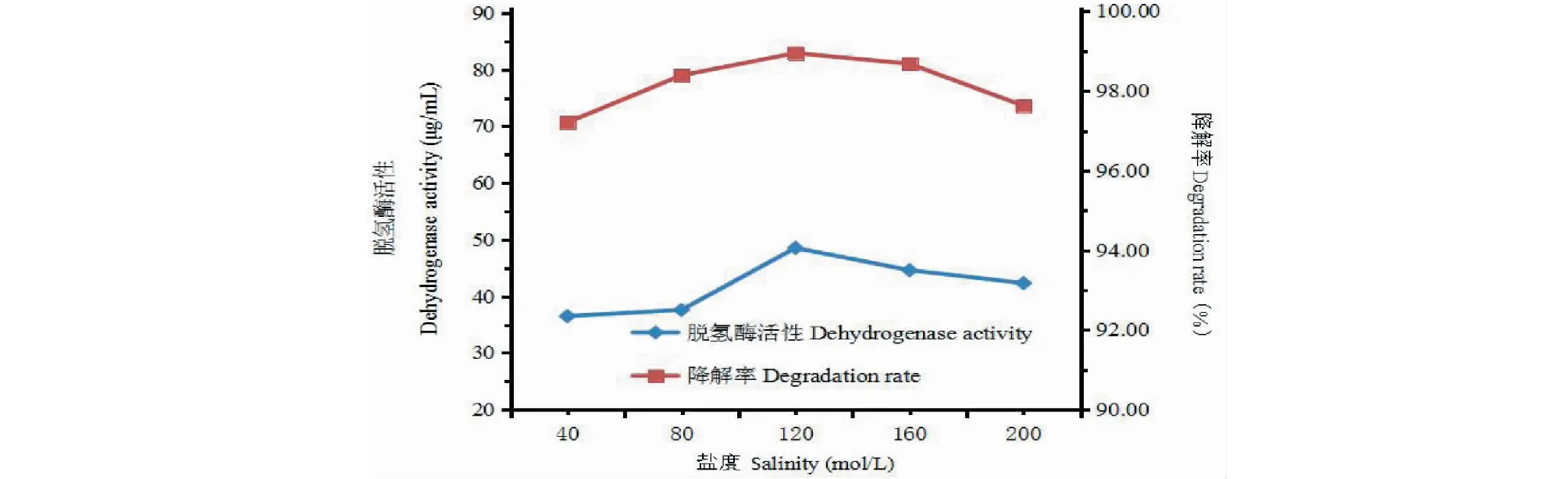
图5 不同盐度下蒽的脱氢酶活性与降解率Fig.5 Dehydrogenase activity and degradation rate of anthracene fluorene under different salinity
由图5可知蒽的脱氢酶活性和降解率随着盐度的变化呈现出先升后降的趋势,在120 mol/L时蒽的脱氢酶活性和降解率达到最大,脱氢酶活性和降解率变化范围都很小,由此可见盐度对蒽的影响不是很大。
2.7 响应面设计与分析
由单因素实验结果可知,在温度,pH,菌液量条件下,蒽的降解率比较好,而盐度因素对脱氢酶活性影响不大,由此选出最能影响脱氢酶活性的因素及条件:温度为25~30 ℃、pH为5~9、菌液量为3~7 mL,并选择脱氢酶活性为响应值,用Design-Expert8.0软件的Box-Behnken中心进行优化设计。通过表1,2中对蒽脱氢酶活性的实验结果回归分析,得到回归方程:
R=119.86-3.73A+5.34B+2.00C+3.63AB-3.95AC+12.09BC-16.78A2-28.97B2-31.70C2
一般显著性水平定为0.05,即P<0.05时,才表明交互效应显著(或说存在交互作用),0.05
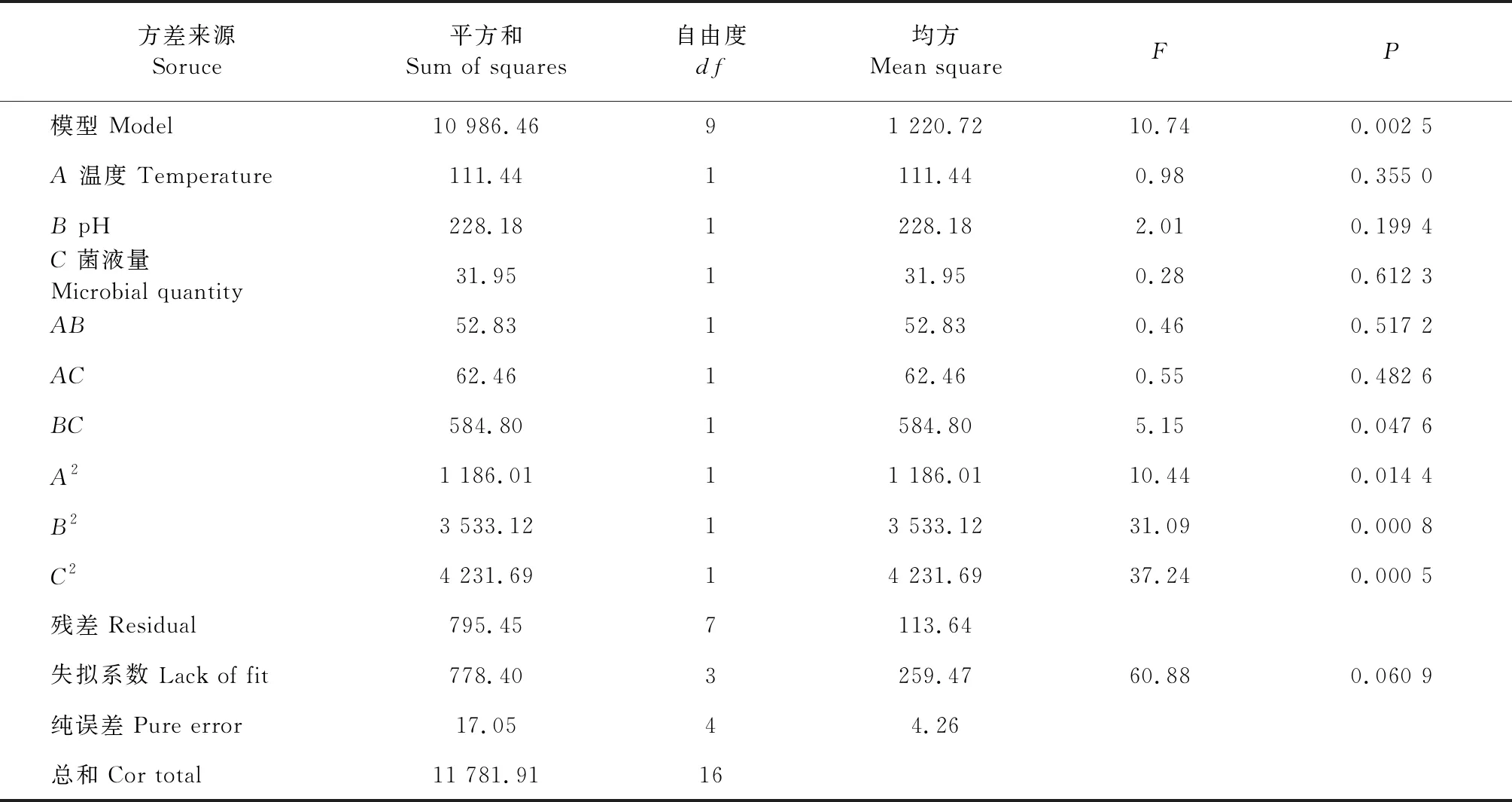
表1 蒽脱氢酶活性的回归模型方差分析Table 1 Anthracene dehydrogenase activity regression model analysis of variance
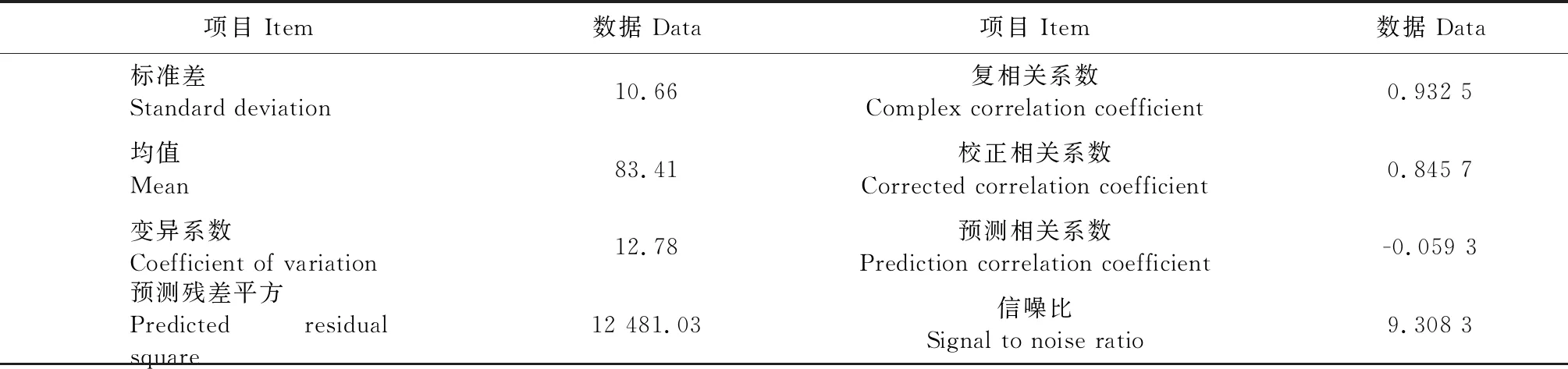
表2 蒽脱氢酶活性的响应面结果误差分析Table 2 Error analysis of response surface results of anthracene dehydrogenase activity
2.8 响应面结果与分析
由图6可知,响应面曲线走势较平缓,但等高线呈现的椭圆型明显,说明pH与温度两者交互作用对Sa降解蒽的脱氢酶活性有影响。若pH固定,温度在27~28 ℃之间脱氢酶活性达到顶峰,温度在25~27 ℃之间脱氢酶活性随温度上升而增强,在28~30 ℃时脱氢酶活性随温度下降而减弱。若温度固定,pH在7.0~8.0时脱氢酶活性达到顶峰,pH在5.0~7.0之间脱氢酶活性随pH升高而增强,pH在8.0~9.0之间脱氢酶活性随pH升高而减弱。温度在27~28 ℃,pH在7.0~8.0之时脱氢酶活性达到顶峰。
温度与菌液量以及菌液量与pH两者交互作用对Sa降解蒽的脱氢酶活性也有影响,但响应面趋势图形与图6差别不大。若菌液量固定,温度在27~28 ℃之间脱氢酶活性达到顶峰,温度在25~27 ℃之间脱氢酶活性随温度上升而增强,在28~30 ℃时脱氢酶活性随温度下降而减弱。若温度固定,菌液量在5.0 mL时脱氢酶活性达到顶峰,菌液量在3.0 ~5.0 mL之间脱氢酶活性随菌液量增加而增强,菌液量在5.0~7.0 mL之间脱氢酶活性随菌液量增加升高而减弱。温度与菌液量交互作用下菌液量在5.0 mL左右,温度在27~28 ℃之时脱氢酶活性达到顶峰。若pH固定,菌液量在5.0 mL左右时脱氢酶活性达到顶峰,菌液量在3.0~5.0 mL之间脱氢酶活性随菌液量增加而增强,菌液量在5.0~7.0 mL之间脱氢酶活性随菌液量增加升高而减弱。若菌液量固定,pH在7.0~8.0时脱氢酶活性达到顶峰,pH在5.0~7.0之间脱氢酶活性随pH上升而增强,在8.0~9.0时脱氢酶活性随pH下降而减弱。pH与菌液量交互作用下菌液量在5.0 mL左右,pH在7.0~8.0时脱氢酶活性达到顶峰。三个交互效应影响结果从大到小依次为:pH-菌液量>温度-菌液量>温度-pH。
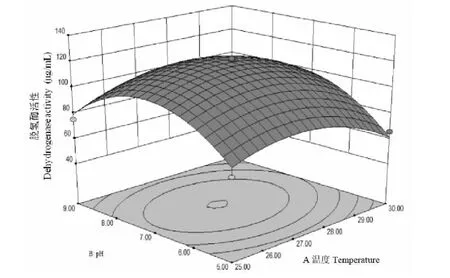
图6 温度与pH交互影响暗黑微 绿链霉菌对降蒽的响应面图Fig.6 Response surface diagram of S.anthracene reduced by interaction of temperature and pH
2.9 最优化试验检测
在最佳工艺条件下,进行优化实验检测,降解温度为27.23 ℃、降解pH为7.19、降解菌液量为5.11 mL,进行3次重复验证实验。实际测得Sa的平均脱氢酶活性为121.50 μg/mL,模型中的脱氢酶活性为120.38 μg/mL,实验值与预期值基本相符。
3 讨论
微生物代谢多环芳烃有两种方式:一是以多环芳烃为惟一碳源;二是多环芳烃与其他有机质进行共代谢。本实验使用第一种方式并以活性炭为吸附载体,研究温度、pH、菌液量、盐度对蒽的降解影响。许多微生物能以低分子量的多环芳烃(四环以内)作为唯一的碳源和能源,并将其完全矿化。然而,对于高分子量的多环芳烃,由于其化学结构的复杂性以及在水环境中的低溶解度,难以被微生物直接降解。因为研究表明,许多四环或多环且分子量较高的多环芳烃,由于其化学结构的复杂性以及在水环境中的低溶解度,难以作为惟一碳源和能源被微生物降解,而是以共代谢的方式进行[19]。
温度和pH作为环境因素,对菌株的活性及降解污染物的效果均能产生影响。当环境因素达到菌株生长的最适条件时,脱氢酶活性和降解率的效果会达到最好。而本实验单因素部分的结果也证明了,环境因素对降解率和脱氢酶活性有很大影响。多环芳烃在自然环境系统中多以混合物的形式存在,复杂的多底物混合状态势必会影响微生物的生理生态以及微生物对混合组分中单个底物的利用动力学,进而会影响降解效率。温度对微生物降解多环芳烃的影响主要表现在其对多环芳烃的理化性质、化学组成、微生物对多环芳烃的代谢以及微生物群落结构等的影响。低温下由于酶活性的降低使多环芳烃的生物降解受到抑制。此外,环境中的pH值对大多数微生物都是适合的,气候和季节的变化对pH值会产生一定的影响,不同的环境中,微生物生长的最适pH值不一定相同。
菌液量作为降解微生物自身因素对多环芳烃降解起着重要作用,从本实验的单因素及多因素结果可看出,虽然菌液量在单独作用是效果不明显,但其在多因素实验中与其他因素交互作用时对脱氢酶活性影响非常显著。当生物接种量较少时,营养物质充足,细菌相互之间不会出现抑制作用,随着生物接种量的增加,细菌之间争夺营养物质,相互之间产生竞争和抑制关系,故出现菌活性下降的现象[20]。
4 结论
通过形态特征和生理生化试验指标以及16S rDNA序列及同源性比对,初步鉴定Sa为暗黑微绿链霉菌(Streptomycesatrovirens)的一种。通过以降解过程中蒽脱氢酶活性性为响应值,考察各自变量及自变量之间的交互作用对脱氢酶活性的影响,优化降解脱氢酶活性与各自变量条件因素的响应关系,结果表明,单因素影响效果依次为:pH、温度、菌液量;交互效应影响效果依次为: pH-菌液量、温度-菌液量、温度-pH。其中pH与菌液量交互作用P值小于0.05,其交互效应对蒽的脱氢酶活性作用显著。

