火焰原子吸收法测定香菇中的铁和铜
尹 晶 吕子健
(辽宁省丹东市卫生健康服务中心 辽宁丹东 118000)
1 前言
铁(Fe)和铜(Cu)是人体必需的重要微量元素,其中Cu 是人体重要的体内催化剂,参与体内多种金属酶的组成。 人体内的Fe 是构成血红蛋白的原料,也是维持人体正常生命活动的酶的组分,与能量代谢十分密切。 在没有严重缺乏微量元素的前提下,最理想的补充微量元素或预防微量元素缺乏的方式是食补。 但由于Cu 属于重金属元素,若长期食用含Cu 过高的蔬菜,会导致Cu 在肝脏中积累,引起疾病[1],香菇作为人们日常生活中食用较多的蔬菜,准确测定香菇中的Fe 和Cu 含量有十分重要的意义。
本文利用火焰原子吸收分光光度法测定香菇中Fe 和Cu 的含量,其具有快速、准确、灵敏和干扰少等优点。
2 材料和方法
2.1 仪器和试剂
仪器:原子吸收分光光度计(热电ICE3000);马弗炉;分析天平。
试剂:盐酸(HCl)、硝酸(HNO3)、高氯酸(HClO4)(优级纯);Fe、Cu 标准溶液:1 000 mg/L,国家标准物质中心。
2.2 仪器工作条件
Cu 空心阴极灯电流:75%;吸收波长:324.8 nm;背景校正:D2;通带:0.5 nm;火焰性质:空气-乙炔火焰;燃气流量:1.1 L/min;燃烧器高度:7.0 mm。
Fe 空心阴极灯电流:75%;吸收波长:248.3 nm;背景校正:D2;通带:0.2 nm;火焰性质:空气-乙炔火焰;燃气流量:1.0 L/min;燃烧器高度:7.0 mm。
2.3 试验方法
2.3.1 样品预处理
干法灰化:称取10 份均匀捣碎的10.00 g 香菇样品置于坩埚中,在加热板上进行低温炭化后移入马弗炉,在550℃条件下灼烧至有机物完全破坏。 再用硝酸(1+3)溶解灰化后的香菇,定容至25 mL 比色管中[2]。
湿法消解:称取10 份均匀捣碎的香菇样品5.00 g,放入锥形瓶中,加入4.0 mL 浓HNO3和1.0 mL HClO4,盖上小漏斗,放置过夜,然后将锥形瓶放于加热板加热至棕色,冷却,再加入1~2 mL 浓HNO3,加热,重复以上操作。当液体冒白烟且剩余较少时,停止加热。得到无色、淡黄色或浅绿色溶液,然后移入25 mL 比色管中,加去离子水至刻度摇匀,待测[3]。
2.3.2 定容液的选择
移取2.0 mL 3.0 mg/L Fe、3.0 mg/L Cu 标准溶液3 份于25 mL 容量瓶中,分别加入5.0 mL HCl(1+4)、5.0 mL HNO3(1+5)和5.0 mL HCl+HClO4,用去离子水定容,测定吸光度。
3 结果与讨论
3.1 干法灰化与湿法消解处理样品结果比较
分别取10 份干法灰化及湿法消化前处理样品进行对照。试验结果表明,干法灰化与湿法消解结果基本一致,但干法灰化酸试剂用量少、操作简便且节约时间,适合大批量的样品预处理,结果详见表1。

表1 香菇预处理结果
试验表明HNO3为介质的吸光度值最高,且相对HClO4为介质时,HNO3对仪器的损耗以及产生的污染物最小,因此测定Fe、Cu 时应以HNO3为定容液介质,结果详见表2。
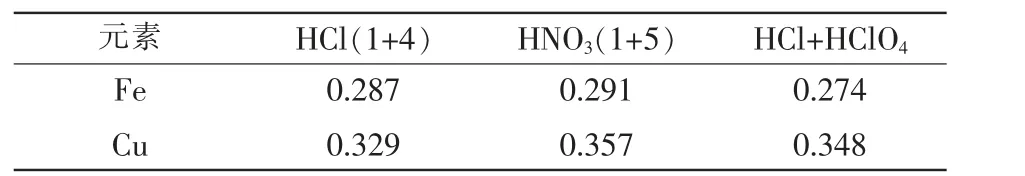
表2 不同介质中溶液的吸光度结果
3.2 加标回收率结果
另取10 份香菇样品,向其中5 份样品中加入Fe和Cu 的标准液0.500 mg/L,回收率为95.6%~96.5%,符合检验要求,结果详见表3。
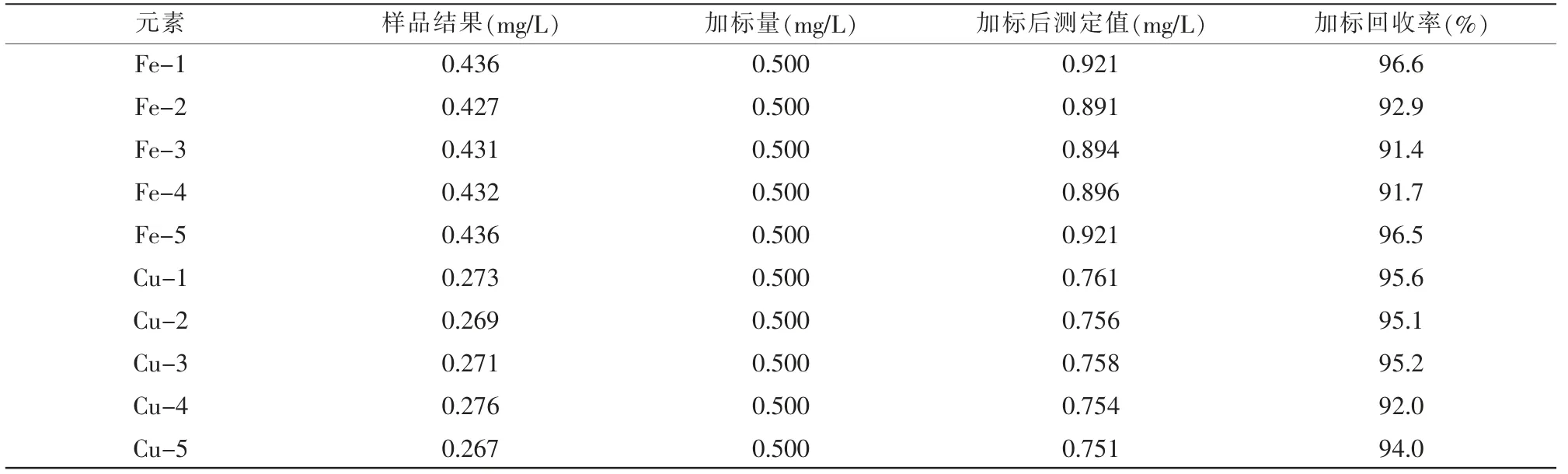
表3 加标回收率结果
3.3 精密度结果
选取1 份香菇样品进行10 次Fe 和Cu 元素的平行测定,结果详见表4。
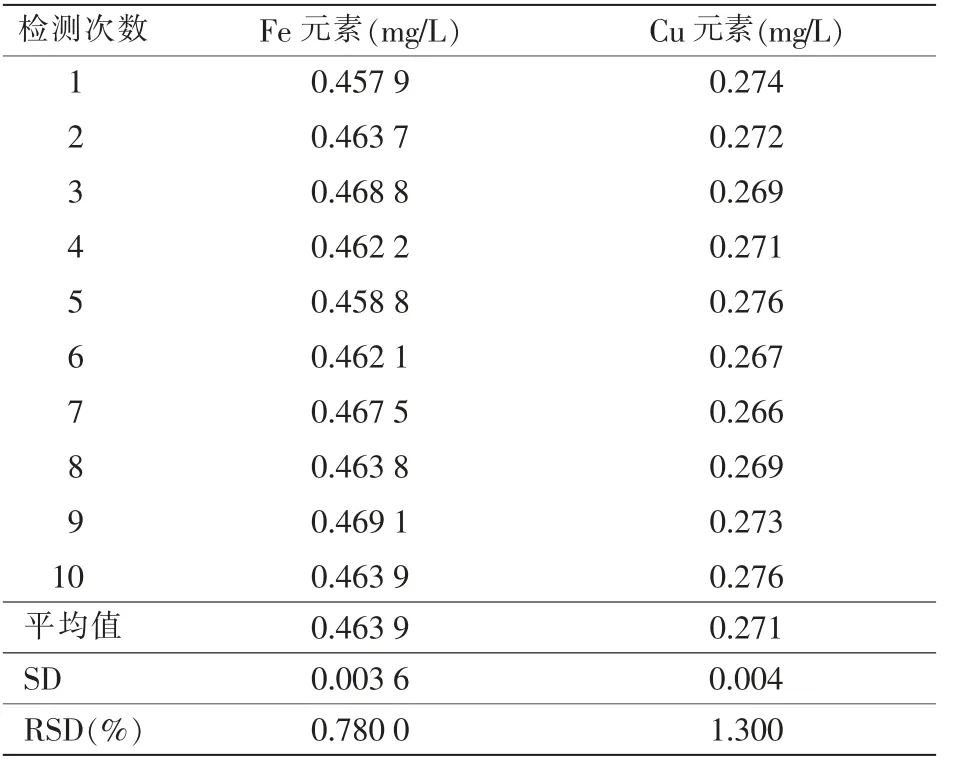
表4 方法精密度的测定结果
4 结论
本文在优化了原子吸收光谱仪测定香菇中Fe和Cu 的条件下,进行湿法消解和干法灰化的样品预处理,2 种方法均符合试验要求,干法灰化的优点是耗时短,产生污染小,适合大批量的样品处理,湿法消解可以减少元素的挥发[4]。以HNO3为介质定容,可以有效提高Fe 和Cu 的测定灵敏度,同时准确性和精密性检测试验表明,该方法精密度高,准确性好[5]。

