江苏省玉米小斑病菌的分离鉴定及致病力分析
任春梅 杨柳 缪倩 陆芳 顾雪 程兆榜


摘要:【目的】明確江苏省玉米小斑病菌的致病力水平,为玉米抗病品种选育及其田间合理布局提供指导,也为玉米小斑病的综合防治提供理论依据。【方法】采用常规组织分离法对采自江苏省东台、如东、丰县和东海4个市(县)的疑似小斑病玉米叶片进行单孢分离,显微镜下观察孢子形态;基于rDNA-ITS对分离菌株进行分子鉴定和系统进化分析;选用8个自交系玉米品种(Mo17、B73、丹340、罗31、掖478、齐319、昌7-2和掖107),采用喷雾接种法对分离菌株进行致病力测定。【结果】分别从江苏省东台、如东、丰县和东海4地各分离到1株菌株,依次标记为DT、RD、FX和DH,形态学观察发现分离菌株存在类似于玉米小斑病菌的孢子;以分离菌株的DNA为模板,PCR扩增得到550 bp左右的预期片段,测序分析发现其与玉米小斑病菌多个分离株序列的同源性达97%;结合分离菌株的形态学和分子鉴定,将分离菌株鉴定为玉米小斑病菌的江苏分离株。系统发育进化分析结果表明,东台分离株(DT)独立一枝,说明其来源较特殊。致病力分析结果显示,不同菌株间存在着明显的致病力分化,其中来自东台的菌株(DT)致病力最强;不同玉米品种在同一菌株上的抗感性差异较大,对玉米小斑病表现为抗病的有齐319和Mo17。【结论】可选用东台菌株(DT)作为江苏省玉米种质资源抗病性筛选的接种菌株,指导抗病品种的选育;可挖掘齐319和Mo17的抗病基因,为玉米小斑病抗病品种的选育提供材料。
关键词: 玉米小斑病菌;单孢分离;分子鉴定;致病力;江苏省
中图分类号: S435.131.4 文献标志码: A 文章编号:2095-1191(2020)10-2454-07
Isolation identification and pathogenicity analysis of
Bipolaris maydis in Jiangsu
REN Chun-mei1, YANG Liu1, MIAO Qian1, LU Fang1, GU Xue2, CHENG Zhao-bang1*
(1Institute of Plant Protection, Jiangsu Academy of Agricultural Sciences, Nanjing 210014, China; 2College of Plant Protection, Henan Agricultural University, Zhengzhou 450040, China)
Abstract:【Objective】The objective of this study was to clarify the pathogenicity of Bipolaris maydis in Jiangsu, provide theoretical basis forscreening disease resistant maize varieties and their layout in field, as well as for the comprehensive control of leaf spot of maize. 【Method】In this study, single spores were isolated from leaves of suspected leaf spot diseased maize in Dongtai, Rudong, Fengxian and Donghai of Jiangsu by convention tissue separation. The spore morphology was observed under microscope, and molecular identification and phylogenetic analysis were conducted based on rDNA-ITS. The pathogenicity of the isolates was determined by a spray inoculation method with eight inbred maize varie-ties(Mo17, B73, Dan340, Luo31, Ye478, Qi319, Chang7-2 and Ye107). 【Result】Eachs train was isolated from Dongtai, Rudong, Fengxian and Donghai of Jiangsu, and marked as DT, RD, FX and DH. The results showed that the spores similar to B. maydis were observed in morphology, and the expected fragment of 550 bp was amplified by PCR with isolatesDNA as template. The sequence analysis showed that the sequence homology between the Jiangsu isolates and the others was 97%, so it was identified as the B. maydis isolated from Jiangsu combined with morphology and molecular identification. Phylogenetic analysis showed that the Dongtai isolate(DT) was an independent branch, indicating that it had a special origin. The pathogenicity analysis showed that there were obvious pathogenic differentiation among different strains, among which strains from Dongtai(DT) had the strongest pathogenicity; the resistance of different maize varieties on the same pathogenic strain was quite different, and Qi319 and Mo17 were resistant tomaize leaf blight. 【Conclusion】Therefore, Dongtai strain(DT) can be selected as the screening strain for disease resistance of maize varieties in Jiangsu, to guide the breeding of resistant varieties. Resistance genes of Qi319 and Mo17 can be mined, which can provide reliable materials for breeding resistant maize varieties ofmaize leaf blight.
Key words: Bipolaris maydis; single spore isolation; molecular identification; pathogenicity; Jiangsu
Foundation item: Agriculture Major Variety Creation Program of Jiangsu(PZCZ201710)
0 引言
【研究意义】玉米小斑病属于世界性流行病害,在热带湿润和亚热带地区广泛发生,目前该病在拉丁美洲、欧洲和亚洲部分地区均有发生(Zwonitzer et al.,2010)。我国早在20世纪20年代江苏地区就发现有玉米小斑病发生,但危害程度极低,当时未引起重视(陈利锋和徐敬峰,2007)。20世纪60年代后,由于大量种植感病品种,玉米小斑病害日趋加重,湖北宜昌和河北石家庄都曾因此病大流行造成20%以上的产量损失(董金皋,2013)。20世纪70年代后,随着抗病品种的推广,玉米小斑病的发生和危害基本得到控制。但进入21世纪后,由于抗病品种大面积单一化种植和全球气候变暖,我国部分玉米产区小斑病仍时有严重发生,损失惨重。据王晓鸣(2010)报道,2003—2004年河北、河南、山东和安徽玉米主产区小斑病发生较严重,仅河南驻马店夏玉米小斑病发病面积达2.13万ha,占玉米种植总面积的50%以上,造成经济损失3000万元左右。玉米作为江苏省重要的粮食作物,其种植面积及范围正逐年上升,其中鲜食玉米在江苏已进行大面积推广(张世博等,2018),而江苏玉米生长期温暖潮湿的环境很适合小斑病菌的繁殖和传播,因而需重视对江苏省玉米小斑病的防控。不同地区玉米小斑病菌的致病力存在明显差异,对鲜食玉米的优质、安全生产造成了极大威胁(常佳迎等,2020)。因此,明确江苏省玉米小斑病菌的致病力水平,不仅为本省玉米种质资源的抗病性筛选提供最适菌株,还能为玉米品种在当地的合理布局提供参考。【前人研究进展】玉米小斑病的病原菌为玉蜀黍平脐孺孢(Bipolaris maydis),病菌传播依靠温暖潮湿的环境,最适生长温度为26~29 ℃,可在玉米的全生育期进行侵染,主要为害玉米的叶片、叶鞘、苞叶和果穗,发病严重时造成果穗腐烂,导致严重减产甚至绝收(廖蕾,2017)。玉米小斑病的主要初侵染源是田间病株残体内外越冬的病菌分生孢子(王晓梅等,2007),其分生孢子多细胞,长椭圆形或近梭形,单生或束生,榄褐色至褐色,孢痕明显(谢红辉,2010),一般的形态学鉴定方法可对病原菌进行初步判定。对自然界中真菌的分离鉴定,先对病组织表面进行消毒,然后用常规培养基进行培养分离,为了得到纯化的菌株,一般进行单孢分离(张天宇,1983)。但在自然界中真菌的种类繁多,形态学特征较复杂,有些真菌的孢子形态有相似之处,因此,单纯的形态学鉴定方法已不能满足需要,需辅以一定的分子生物学鉴定方法。真菌在内转录间隔(rDNA-ITS)区具有高度保守性,因此rDNA-ITS序列鉴定已成为病原真菌鉴定和遗传特征分析的主要手段(Cannon et al.,2012)。病原菌具有破坏寄主并诱发病害的特性,即致病性(许志刚,2001)。玉米小斑病菌是一种异宗配合真菌,在自然条件下存在2种交配型,有有性和无性两种生殖方式(Turgeon et al.,1993)。病原物在复杂多变的环境中,经过与寄主植物的相互选择,其致病性会朝着克服寄主抗性的方向变化,进而导致致病性分化。目前,国内不同地区玉米小斑病菌的致病性已有一些研究。陆宁海等(2016)鉴定河南新乡地区玉米小斑病菌的优势小种为O小种,其致病力存在明显差异;代玉立等(2018)明确了福建省各地区玉米小斑病菌存在明顯的致病力分化现象;甘林等(2018)根据小斑病菌在玉米上产生的病斑类型将福建各地区的菌群划分为15个致病型;常佳迎等(2020)测定了黄淮海地区和海南三亚玉米南繁基地玉米小斑病菌的致病性,发现强致病菌分布频率上海南三亚优于黄淮海地区。【本研究切入点】前人研究表明,玉米小斑病菌极易产生致病力分化现象,许多地区的小斑病菌存在多种致病类型。目前,有关江苏省玉米小斑病菌致病力的研究尚未见报道。【拟解决的关键问题】采用常规组织分离法对江苏省玉米小斑病菌进行单孢分离,基于rDNA-ITS对分离菌株进行分子鉴定和系统进化分析,再选用8个自交系玉米品种对分离菌株进行致病力测定,以明确江苏省玉米小斑病菌的致病力水平,为玉米抗病品种的选育及其田间合理布局提供指导,也为玉米小斑病的综合防治提供理论依据。
1 材料与方法
1. 1 试验材料
2019年7月在江苏省东台(东经120?18′36″,北纬32?50′24″)、如东(东经121?10′48″,北纬32?19′48″)、丰县(东经116?34′12″,北纬34?47′24″)和东海(东经118?45′,北纬34?32′24″)4个市(县)的夏播玉米地采集疑似玉米小斑病叶片,分别干燥保存带回实验室。供试的8个致病力测定玉米品种由江苏省种子管理站提供,分别为Mo17、B73、丹340、罗31、掖478、齐319、昌7-2和掖107。
1. 2 病原菌分离培养
1. 2. 1 组织分离 将病叶用自来水冲洗干净,取病健交接处剪成边长2~3 mm的正方形小块。剪下的病叶用无菌水冲洗10 s,2%次氯酸钠消毒2 min,75%酒精消毒30 s,再用无菌水冲洗3次,然后置于灭菌后潮湿的滤纸上,于27 ℃恒温培养箱中暗培养2~3 d。
1. 2. 2 单孢分离 参考方中达(1998)的方法,在显微镜下检查病组织分生孢子生长情况。有孢子生长的部位用无菌水洗下,静置1~2 min,取试管上半部分的孢子悬浮液30~50 μL均匀涂布在WA培养基上,暗培养至孢子萌发。待出现单个孢子时,用自制的挑孢针挑取孢子,转移到加入庆大霉素的PDA培养基上,于27 ℃恒温培养箱中培养。
1. 2. 3 菌株纯化 用接种针挑取培养基上3个圆形菌块,置于新的PDA培养基上,底部朝上放入培养箱中27 ℃暗培养5~7 d。
1. 3 病原菌鉴定
1. 3. 1 形态学鉴定 纯化后的菌株置于培养箱内27 ℃再培养7 d左右,观察并描述菌落的形态。用乳酚油为浮载剂制作少量菌丝的载玻片,在普通光学显微镜下观察孢子及分生孢子梗的形态,根据魏景超(1979)的《真菌鉴定手册》和乔秉善(2012)的《中国气传真菌彩色图谱》进行分类鉴定。
1. 3. 2 rDNA-ITS分子鉴定
1. 3. 2. 1 DNA提取 纯化后的菌落基本长满平板时,刮取菌丝体放入研钵中,加入液氮快速研磨,依照2×T5 Direct PCR Kit(Plant)试剂盒(南京擎科生物科技有限公司)操作步骤,采用加热裂解法抽提DNA,-20 ℃保存备用。
1. 3. 2. 2 PCR扩增 扩增真菌的18S通用引物ITS1和ITS4由南京擎科生物科技有限公司合成。PCR反应体系25.0 μL:12.5 μL 2×T5 Direct PCR Mix(Plant),10 μmol /L上游、下游引物各1.0 μL,DNA模板2.0 μL,8.5 μL ddH2O。扩增程序根据T5 Direct PCR Kit(Plant)试剂盒进行操作。取4.0 μL PCR产物经1%琼脂糖凝胶电泳检测后送至南京金斯瑞生物科技有限公司测序。
1. 3. 2. 3 序列比对及分析 使用NCBI的GenBank核酸数据库中的BLAST,输入测序序列,进行同源性搜索,获得同源性最高的真菌序列,鉴别病原菌属于哪种真菌。再引用GenBank中同一真菌序列,用MEGA 6.0构建系统发育进化树。
1. 4 病原菌致病性测定
1. 4. 1 玉米苗准备 将Mo17、B73、丹340、罗31、掖478、齐319、昌7-2和掖107玉米种子分别播于长540~600 mm、宽280~300 mm的穴盘中。每菌株接种每种玉米品种3穴盆。玉米苗在28 ℃左右温室中长至12片左右叶时,每个穴盆按30株的苗量进行接种。
1. 4. 2 孢子悬浮液制备 用挑菌针在长势良好的培养基上取4块菌块,分别放置在灭菌的高粱培养基中,标注菌种名称和接种时间。置于培养箱中27 ℃暗培养7 d,观察若袋内1/2的高粱粒表面长有菌丝,即用无菌水淘洗高粱粒,平铺于托盘中,盖上湿纱布保湿培养7 d,期间每2 d喷水保湿1次。待高粱粒长满菌丝后再用无菌水冲洗,用2层纱布过滤,在显微镜下观察滤液中孢子量,若每视野孢子量在20个以上,即可获得所需浓度的孢子悬浮液。
1. 4. 3 接种方法 参考Dai等(2016)的孢子懸浮液人工喷雾接种法,待玉米植株长到11~13片叶时进行接种。将产孢培养基用清水淘洗,2层纱布过滤,滤液中加入Tween-20,一般制备成1×105个孢子/mL浓度的孢子悬浮液。用喷壶将孢子悬浮液喷洒到玉米喇叭口,接种后7 d内每日喷雾清水进行保湿。
1. 4. 4 病情调查 接种10 d后,根据玉米小斑病病级划分标准调查每株玉米穗部的上、下各3叶,记载每份材料的总体病情级别。病情级别划分标准参考NY/T 1248.2—2006《玉米抗病虫性鉴定技术规范第2部分:玉米抗小班病鉴定技术规范》。将参试分离物划分为HV、SH、MV、SL和LV等5个致病类型,致病力强弱为HV>SH>MV>SL>LV。当菌株病级≥7级为强致病力(HV),病级=5级为次强致病力(SH),病级=3级为中致病力(MV),病级=1级为次弱致病力(SL),病级<1级为弱致病力(LV)。
2 结果与分析
2. 1 病原菌形态观察结果
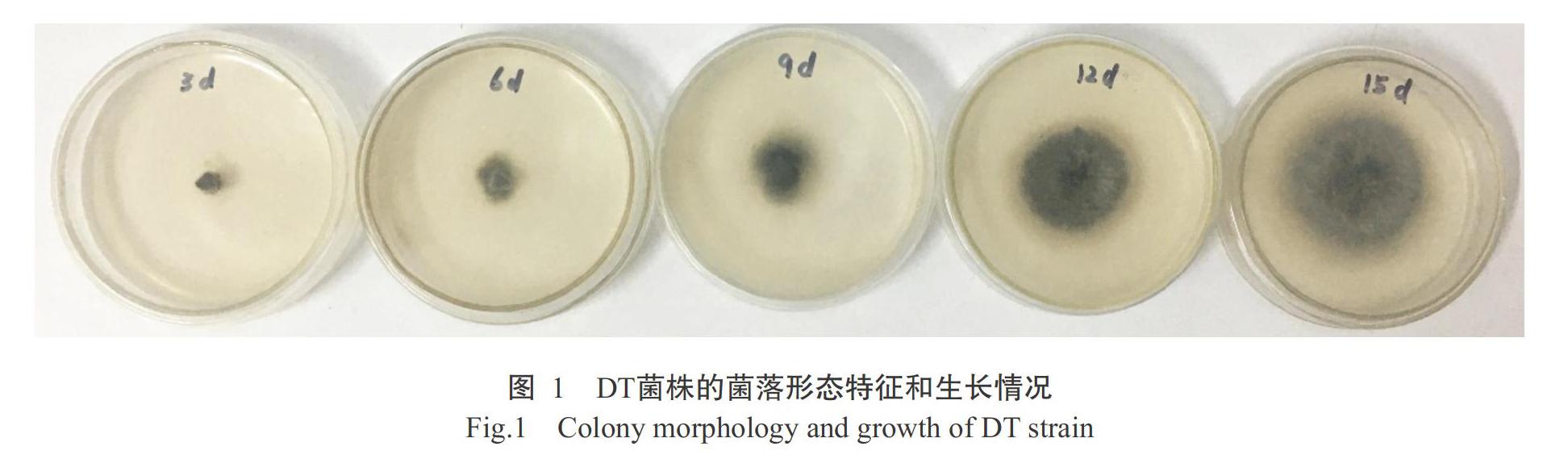
分别从江苏省东台、如东、丰县和东海4地各分离到1株菌株,依次标记为DT、RD、FX和DH,对各菌株进行再纯化,培养发现4株菌株的菌落形态一致,菌落生长速度较慢,颜色呈灰黑色,质地紧密,气生菌丝不太发达(图1)。菌株孢子梭形或长椭圆形,伸直或多向一侧弯曲,一般为多细胞,有6~8个隔膜;单个孢子大小为60.0~100.0 ?m×7.5~10.0 ?m,颜色多为褐色;分生孢子梗也为褐色,直或呈膝状曲折(图2)。综合分离菌株的形态特征初步鉴定为玉米小斑病菌。
2. 2 病原菌的分子鉴定结果
2. 2. 1 PCR扩增 以分离得到的4株菌株DNA为模板,基于通用引物IST1和IST4进行PCR扩增,产物经1%琼脂糖凝胶电泳检测,4株菌株均扩增得到长度约550 bp的预期扩增片段,阴性对照样品未扩增到条带(图3)。
2. 2. 2 序列比对及分析 回收电泳片段进行序列测定,结果表明,4株菌株的目的基因片段均含550个核苷酸,其序列全长为540 bp,将4株菌株的扩增产物序列提交至NCBI的GenBank核酸数据库进行BLAST比对,搜索同源性序列,发现其与玉米小斑病菌多个分离株rDNA-ITS核糖核酸序列的同源性达97%,说明4株菌株为玉米小斑病菌。
运用MEGA 6.0对江苏4株菌株与已发表的13株玉米小斑病菌分离株构建系统发育进化树(图4)。从系统发育进化树可看出,17株分离株可分为两大组,其中江苏东台分离株(DT)独立聚为一支,说明其来源较特殊;江苏的其他3株分离株(RD、FX和DH)与已发表的我国四川3株分离株同为一组,说明其具有更高的亲缘关系,均来自于我国;其他来自于泰国、荷兰和印度的分离物聚在一组,说明与本地分离株在进化上存在一定的地理隔离。
2. 3 致病性测定结果
2. 3. 1 自交系玉米发病时间的观察 8个自交系玉米品种在接种4株分离株后的显症时间如表1所示,接种后最快显症的是东台分离株(DT),最快显症时间为10 d;最慢显症时间为28 d,是来自于东海的分离株(DH);其余菌株的显症时间在10~28 d。不同菌株在同一自交系品种上的显症时间也不同,说明不同分离株存在着发病时间的快慢,证明其致病力存在差异。
2. 3. 2 菌株的致病力分化 4株菌株在8个自交系玉米品种上表现出不同的致病类型(表2),不同菌株间的致病力差异明显。其中,DT菌株和RD菌株的致病力较强,在罗31上表现为强致病型;而FX和DH 2株菌株在罗31上表现为次强致病型,综合比较4株菌株在8个鉴别品种上的致病类型,以DT菌株的致病力最强。同一菌株在不同品种上表现出不同的致病型,如DT菌株对B73、掖478和昌7-2均表现为次强致病型,对丹340和Mo17表现为中致病型,对掖107表现为次弱致病型,而对齐319表现为弱致病型。表明同一菌株在不同品种上的致病型呈多样性,各品种的抗体也表现出明显差异,对玉米小斑病抗性较好的品种有齐319和Mo17。
3 讨论
玉米小斑病严重影响玉米的产量和品质,其病菌分生孢子极易随气流和雨水传播,危害玉米的叶片、叶鞘、苞叶和果穗,甚者病斑遍布整个玉米植株引起枯死,轻者减产10%~20%,重者减产30%~80%,甚至绝收。近年来,江苏省玉米种植面积呈逐年上升趋势,随着种植面积的扩大、种植结构调整、玉米品种更替及频繁的引种交流,使得玉米小斑病菌的致病力发生了新变化,目前玉米小斑病仍是江苏省玉米生产上的重要叶部病害。因此,本研究通过调查和采集江苏省玉米主产区疑似小斑病病叶,分离鉴定出江苏玉米小斑病菌分离株,测定并分析其致病力,研究结果既丰富了江苏省玉米小斑病菌的菌源,为玉米抗病性鉴定提供本地菌株,又可监测江苏省玉米小斑病菌致病力分化,为江苏省玉米品种选育推广及玉米小斑病的综合防控提供理论依据。
孔令晓等(2005)研究认为,植物病原菌种内群体分化主要是病原菌与其赖以生存的寄主在一定环境条件下相互作用的结果,两者相互制约。我国地域辽阔,物产丰富,一般在同一地域会种植多个玉米品种,不同地域又会连续多年种植一个或多个相同的玉米品种,很容易在这一片地区长期使用同一细胞质类型的玉米种质,导致病原菌也出现与细胞质相对应的致病类型。早在1991年,刘克明等就发现玉米C群细胞质CⅠ亚群对玉米小斑病菌C小种严重感病,因此建议育种时要多细胞质杂交育种。李玥仁等(1993)也报道陕西省玉米小斑病O小种在不同细胞质的玉米种质上会表现出不同的致病类型,表现为强致病力的病斑长度在8 mm以上,而表现为弱致病力的病斑长度仅在3 mm以下。常佳迎等(2020)研究表明,海南三亚地区玉米小斑病菌的强致病力菌株频率高于黄淮海地区,推测其与黄淮海地区推广种植抗病品种有关。本研究选用Mo17、B73、丹340、罗31、掖478、齐319、昌7-2和掖107等8个自交系玉米品种作为鉴别寄主,这些品种均是与我国玉米主栽品种具有亲密血缘关系的自交系材料,不仅可分析玉米小斑病菌的致病性分化,还有助于评价生产上栽培品种的抗病性,从而有力地指导田间病害防治,以便更加合理地布局田间品种。本研究结果显示采自江苏省的4株分离菌株出现明显的致病力分化,其中来自江苏东台(DT)和如东(RD)的菌株致病力较强,而江苏丰县(FX)和东海(DH)的菌株致病力相对较弱,地理位置上东台和如东靠得较近,说明其致病类型与地区来源有一定关系。研究结果还显示,同一菌株或不同菌株对不同玉米品种的致病力均表现出丰富的多样性,表明玉米小斑病菌致病力分化具有普遍性和多样性。
不同玉米品种对同一菌株的表现差异也明显,表明玉米品种对小斑病的抗性不同。玉米对小斑病的抗性一般有2种:病斑数,数量遗传,可能由多基因显性控制;病斑型,质量遗传,由1个或2个隐性基因控制。虽然目前尚未发现对玉米小斑病绝对免疫的品种,但已在一些抗病材料中鉴定出与抗性相关的数量性状位点(QTL)(Zwonitzer et al.,2009;Belcher et al.,2012;施艳等,2019)。本研究中的8个玉米品种对玉米小斑病的抗性应属多基因控制的数量遗传,其中齐319和Mo17的抗性较强,可挖掘这些品种的抗性基因,为抗病品种的选育提供材料;同时,对于抗性较差的品种,应在安全生产上做好病害预防工作。江苏省在6—7月的早夏雨水较多,气温一般在25~30 ℃,特别适宜玉米小斑病的发生,因此要特别注意夏播玉米小斑病的防控。另外,鲜食玉米等感病品种大面积种植极有利于小斑病菌的生长与侵染,极可能加速田间菌源积累,引发小斑病流行。因此,监测江苏省玉米小斑病菌群体间致病力的变化动态,开展病害预测预报和玉米品种抗病性研究,针对病菌的变化合理布局玉米品种,探索抑制病菌快速流行的有效措施,对减轻病害的发生和发展仍具有重要意义。
4 结论
江苏省不同地区的玉米小斑病菌分离株具有不同强度的致病力,其中来自江苏东台的分离株(DT)致病力最强,可作为江苏省玉米种质资源抗病性筛选的接种菌株,指导抗病品种的选育。不同玉米品种在同一菌株上的抗感性差异明显,对玉米小斑病表现为抗病的有齐319和Mo17,可挖掘这2个品种的抗性基因,为抗病品种的选育和研究提供材料。
参考文献:
常佳迎,劉树森,石洁,郭宁,张海剑,马红霞,杨春凤. 2020. 海南三亚和黄淮海地区玉米小斑病菌致病性及遗传多样性分析[J]. 中国农业科学,53(6): 1154-1165. [Chang J Y,Liu S S,Shi J,Guo N,Zhang H J,Ma H X,Yang C F. 2020. Pathogenicity and genetic diversity of Bipolaria maydis in Sanya,Hainan and Huang-Huai-Hai region[J]. Scientia Agricultura Sinica,53(6): 1154-1165.]
陈利锋,徐敬峰. 2007. 农业植物病理学[M]. 北京:中国农业出版社: 185-189. [Chen L F,Xu J F. 2007. Agricultural plant pathology[M]. Beijing: China Agriculture Press: 185-189.]
代玉立,甘林,滕振勇,石妞妞,阮宏椿,杜宜新,廖蕾,陈福如,杨秀娟. 2018. 福建省玉米小斑病菌致病力的分化[J]. 西北农林科技大学学报(自然科学版),46(4): 92-97. [Dai Y L,Gan L,Teng Z Y,Shi N N,Ruan H C,Du Y X,Liao L,Chen F R,Yang X J. 2018. Pathogenicity differentiation of Cochliobolus heterostrophus in Fujian[J]. Journal of Northwest A & F University(Natural Scien-ce Edition),46(4): 92-97.]
董金皋. 2013. 农业植物病理学[M]. 第2版. 北京:中国农业出版社: 98-103. [Dong J G. 2013. Agricultural plant pathology[M] . The 2nd Edition. Beijing: China Agriculture Press: 98-103.]
方中达. 1998. 植病研究方法[M]. 北京: 中国农业出版社. [Fang Z D. 1998. Plant disease research methods[M]. Beijing: China Agriculture Press.]
甘林,代玉立,阮宏椿,石妞妞,杜宜新,陈福如,杨秀娟. 2018. 福建省玉米小斑病菌的致病型及其群体结构分析[J]. 中国农学通报,34(7): 147-151. [Gan L,Dai Y L,Ruan H C,Shi N N,Du Y X,Chen F R,Yang X J. 2018. Pathotype and its population structure of Cochliobolus heterostrophus in Fujian Province[J]. Chinese Agricultu-ral Science Bulletin,34(7): 147-151.]
孔令晓,赵聚莹,栗秋生,王连生,罗畔池. 2005. 河北省玉米小斑病菌生理小种鉴定及群体动态变化[J]. 华北农学报,20(3): 90-93. [Kong L X,Zhao J Y,Li Q S,Wang L S,Luo P C. 2005. Identification and population dyna-mics of physiological races of Bipolaris maydis in Hebei[J]. Acta Agriculturae Boreali Sinica,20(3): 90-93.]
李玥仁,商鸿生,胡必德. 1993. 陕西省玉米小斑病菌致病性分化研究[J]. 植物保护学报,20(1): 90-98. [Li Y R,Shang H S,Hu B D. 1993. Pathogenic specialization of Bipolaris maydis in Shaanxi Province[J]. Journal of Plant Protection,20(1): 90-98.]
廖蕾. 2017. 福建省玉米小斑病菌生物学特性和遗传多样性研究[D]. 福州: 福建农林大学. [Liao L. 2017. Study on biological characteristics and genetic diversity of Cochliobolus heterostrophus in Fujian Province[D]. Fuzhou: Fujian Agriculture and Forestry University.]
刘克明,苏海,崔洋,马春红,陈伟程,李大良. 1991. 玉米C群不同亚群雄性不育细胞质对玉米小斑病菌C小种侵染的反应[J]. 中国农业科学,24(4): 58-69. [Liu K M,Su H,Cui Y,Ma C H,Chen W C,Li D L. 1991. Reaction of different male-stepile cytoplasm subgroups of the C group maize to the infection of Bipolaris maydis race C[J]. Scientia Agricultura Sinica,24(4): 58-69.]
陸宁海,吴利民,郎剑锋,霍云凤,石明旺. 2016. 新乡地区玉米小斑病菌小种群体结构及致病性分析[J]. 河南科技学院学报(自然科学版),44(1): 23-27. [Lu N H,Wu L M,Lang J F,Huo Y F,Shi M W. 2016. Analysis on popu-lation structure and pathogenicity differentiation of Bipolaris maydis in Xinxiang[J]. Journal of Henan Institute of Science and Technology(Natural Science Edition),44(1): 23-27.]
乔秉善. 2012. 中国气传真菌彩色图谱[M]. 北京: 中国协和医科大学出版社:257. [Qiao B S. 2012. Color atlas of airborne fungi in China[M]. Beijing: China Union Medical University Press:257.]
施艳,燕照玲,王珂,赵清爽,席靖豪,李冠楠,刘焱昆,袁虹霞,李洪连. 2019. 河南省夏玉米品种对6种主要病害的抗性评价[J]. 河南农业科学,48(6):95-98. [Shi Y,Yan Z L,Wang K,Zhao Q S,Xi J H,Li G N,Liu Y K,Yuan H X,Li H L. 2019. Evaluation of resistant summer maize varieties against six main diseases in Henan Province[J]. Journal of Henan Agricultural Sciences,48(6):95-98.]
王晓梅,吕平香,李莉莉,见德宝,杨信东. 2007. 玉米小斑病重要流行環节的初步定量研究Ⅱ病斑产孢、孢子飞散、杀菌剂筛选[J]. 吉林农业大学学报,29(2):128-132. [Wang X M,Lü P X,Li L L,Jian D B,Yang X D. 2007. Preliminary quantitative studies on important epidemic links of Bipolaris maydis Ⅱ. Lesion sporulation,spore dispersion and fungicide screenin[J]. Journal of Jilin Agricultural University,29(2): 128-132.]
王晓鸣. 2010. 玉米病虫害田间手册:病虫害鉴别与抗性鉴定[M]. 北京:中国农业科学技术出版社: 7-10. [Wang X M. 2010. Field manual of maize diseases and insect pests: Identification and resistance identification[M]. Beijing: China Agricultural Science and Technology Press: 7-10.]
魏景超. 1979. 真菌鉴定手册[M]. 上海: 上海科学技术出版社:227. [Wei J C. 1979. Handbook of fungal identification[M]. Shanghai: Shanghai Science and Technology Press: 227.]
谢红辉. 2010. 玉米小斑病菌生物学特性研究[J]. 广西热带农业,(6): 1-4. [Xie H H. 2010. Study on the biological characteristics of Bipolaris maydis[J]. Guangxi Tropical Agriculture,(6):1-4.]
许志刚. 2001. 普通植物病理学[M]. 北京:中国农业出版社:10-11. [Xu Z G. 2001. General plant pathology[M]. Beijing: China Agriculture Press:10-11.]
张世博,施龙建,俞春涛,陈国清,刘志勇,袁建华,陆卫平,陆大雷. 2018. 江苏省玉米生产情况调研与分析[J]. 江苏农业学报,34(6):1410-1418. [Zhang S B,Shi L J,Yu C T,Chen G Q,Liu Z Y,Yuan J H,Lu W P,Lu D L. 2018. Research and analysis of maize production in Jiangsu Province[J]. Jiangsu Journal of Agricultural Scien-ces,34(6):1410-1418.]
张天宇. 1983. 介绍一项用于单孢子分离和制片以备显微摄影的显微操作技术[J]. 真菌学报,2(3): 197-200. [Zhang T Y. 1983. A technique using micromanipulator for isola-ting single spores and preparing slide for photomicrogragh[J]. Acta Mycologica Sinica,2(3): 197-200.]
Belcher A R,Zwonitzer J C,Cruz J S,Krakowsky M D,Chung C L,Nelson R,Arellano C,Balint-Kurti P J. 2012. Analysis of quantitative disease resistance to southern leaf blight and of multiple disease resistance in maize,using near-isogenic lines[J]. Theoretical and Applied Genetics,124: 433-445.
Cannon P F,Damm U,Johnston P R,Weir B S. 2012. Colletotrichum-curret status and future directions[J]. Studies in Mycology,73: 181-213.
Dai Y L,Yang X J,Gan L,Chen F R,Ruan H C,Du Y X,Shi N N,Gao Z M. 2016. First report of southern leaf blight caused by Cochliobolus heterostrophus on corn(Zea mays) in Fujian Province,China[J]. Plant Disease,100(8): 1781.
Turgeon B G,Bohlmann H C,Ciuffetti L M,Christiansen S K,Willi Sch?fer G Y,Yoder O C. 1993. Cloning and analysis of the mating type genes from Cochliobolus heterostrophus[J]. Molecular Genetics and Genomics,238:270-284.
Zwonitzer J C,Bubeck D M,Bhattramakki D,Goodman M M,Arellano C,Balint-Kurti P J. 2009. Use of selection with recurrent backcrossing and QTL mapping to identify loci contributing to southern leaf blight resistance in a highly resistant maize line[J]. Theoretical and Applied Genetics,118: 911-925.
Zwonitzer J C,Coles N D,Krakowsky M D,Arellano C,Holland J B,McMullen M D,Pratt R C,Balint-Kurti P J. 2010. Mapping resistance quantitative trait Loci for three foliar diseases in a maize recombinant inbred line population-evidence for multiple disease resistance[J]. Phytopathology,100(l): 72-79.
(责任编辑 麻小燕)

