凡纳滨对虾微粒体谷胱甘肽硫转移酶3基因克隆及其功能分析
郑佩华 汪蕾 张秀霞 李军涛 张泽龙 王冬梅 冼健安 王安利


摘要:【目的】明確凡纳滨对虾微粒体谷胱甘肽硫转移酶3(LvMGST3)在机体抗逆境胁迫与抵御病原体侵染过程中的功能作用,为有效提高对虾的抗胁迫能力和抗病力提供理论依据。【方法】采用RACE克隆LvMGST3基因cDNA序列,以EditSeq、ExPASy、SignalP 5.0、TMHMM 2.0、Clustal X和MEGA 6.0等在线软件进行生物信息学分析,再应用半定量PCR进行组织表达量分析。凡纳滨对虾分别进行氨氮胁迫(20.00 mg/L)及脂多糖(LPS,8 μg/g)刺激后,采用实时荧光定量PCR检测分析LvMGST3基因的表达响应情况。【结果】LvMGST3基因cDNA序列全长826 bp,包含85 bp的5'端非编码区(5'-UTR)、321 bp的3'端非编码区(3'-UTR)和420 bp的开放阅读框(ORF),在ploy(A)尾前端15个核苷酸处存在加尾信号AATAAA。LvMGST3基因编码139个氨基酸残基,包含MGST3亚家族共有的保守结构域FNCX1QRX2H,此序列为FNCYQRAH。LvMGST3蛋白分子量为15.53 kD,理论等电点(pI)为9.38,具有3个跨膜结构域,但不存在信号肽。LvMGST3氨基酸序列与软甲纲普通卷甲虫(Armadillidium vulgare)的MGST3氨基酸序列(RXG56258.1)相似性最高,为71.22%;基于MGST3氨基酸序列相似性构建的系统发育进化树显示,LvMGST3与节肢动物门和软体动物门的MGST3亲缘关系较近。LvMGST3基因在凡纳滨对虾肝胰腺、鳃组织和眼柄中的基础表达量较高;经氨氮胁迫后,肝胰腺中的LvMGST3基因相对表达量分别在胁迫6和24 h时极显著上调(P<0.01,下同),鳃组织中的LvMGST3基因相对表达量在胁迫12 h时显著上调(P<0.05,下同)、胁迫48 h时极显著上调;肝胰腺中的LvMGST3基因在LPS刺激前期表达受抑制,至刺激12 h时极显著上调,鳃组织中的LvMGST3基因分别在LPS刺激3和48 h时出现2个表达峰值,其相对表达量均极显著高于对照组,分别是对照组的4.39和6.45倍。【结论】LvMGST3基因具有典型的MGST3亚家族结构特征,主要在凡纳滨对虾的肝胰腺、鳃组织和眼柄中表达,且氨氮胁迫和LPS刺激可明显诱导凡纳滨对虾肝胰腺和鳃组织中LvMGST3基因的表达水平,即MGST3在对虾抗逆境胁迫及抵御病原菌感染的调控机制中发挥重要作用。
关键词: 凡纳滨对虾;谷胱甘肽硫转移酶3(MGST3);基因克隆;氨氮胁迫;脂多糖(LPS)刺激
中图分类号: S945.49 文献标志码: A 文章编号:2095-1191(2020)10-2311-10
Cloning and function analysis of microsomal glutathione transferase 3 gene(MGST3) from Litopenaeus vannamei
ZHENG Pei-hua1,2, WANG Lei1, ZHANG Xiu-xia2,3, LI Jun-tao2,3, ZHANG Ze-long2,3,WANG Dong-mei2,3, XIAN Jian-an2,3*, WANG An-li1*
(1School of Life Sciences, South China Normal University/Guangdong Provincial Key Laboratory for Healthy and Safe Aquaculture/Guangzhou Key Laboratory of Subtropical Biodiversity and Biomonitoring/Key Laboratory of Ecology and Environmental Science in Guangdong Higher Education, Guangzhou 510631, China; 2Institute of Tropical Biosciences and Biotechnology, Chinese Academy of Tropical Agricultural Sciences/Hainan Provincial Key Laboratory for Functional Components Research and Utilization of Marine Bio-resources, Haikou 571101, China; 3Hainan Institute of Tropical Agricultural Resources, Chinese Academy of Tropical Agricultural Sciences, Haikou 571101, China)
Abstract:【Objective】The purpose of this study was to clarify the function of the microsomal glutathione thitransfera-se 3(LvMGST3) in the process of resisting stress and pathogen infection, and to provide theoretical basis for effectively improving the stress resistance and disease resistance of Litopenaeus vannamei. 【Method】RACE was used to clone the cDNA sequence of LvMGST3 gene, and online softwares such as Editseq, Expasy, SignalP-5.0, TMHMM 2.0, Clustal X and MEGA 6.0 was used for bioinformation analysis, and then semi-quantitative PCR was used for tissue expression ana-lysis. Shrimp were stimulated by ammonia nitrogen stress(20.00 mg/L) and lipopolysaccharide(LPS, 8 μg/g) injection respectively, and the expression responses of LvMGST3 were analyzed by real-time fluorescence quantitative PCR. 【Result】LvMGST3 was 826 bp in length, including 85 bp 5' non-coding region(5'-UTR), 321 bp 3'-UTR and 420 bp open reading frame(ORF), and the polyadenylate signal AATAAA presented at 15 nucleotides in front of ploy(A). LvMGST3 encoded 139 amino acids, including the unique structural sequence FNCX1QRX2H of MGST3 subfamily, this sequence was FNCYQRAH. The molecular weight of LvMGST3 protein was 15.53 kD, and the theoretical isoelectric point(pI) was 9.38. It had three transmembrane domains, but there was no signal peptide. The amino acid sequence of LvMGST3 had the highest similarity to MGST3 amino acid of Malacostraca Armadillidium vulgare(RXG56258.1), which was 71.22%. Phylogenetic trees based on the similarity of MGST3 amino acid sequence showed that LvMGST3 was closely related to MGST3 of Arthropoda and Mollusca. The basal expression of LvMGST3 was high in hepatopancreas, gills and eyestalk. After ammonia-nitrogen stress, expressions of LvMGST3 in hepatopancreas were extremely significantly up-regulated at 6 h and 24 h of stress (P<0.01, the same below), and expressions of LvMGST3 in gills were significantly up-regulated at 12 h of stress(P<0.05, the same below) and extremely significantly up-regulated at 48 h of stress. Under LPS stimulation, expression of LvMGST3 in hepatopancreas was inhibited in the early stage, and then it was extremely significantly up-regulated at 12 h. There were two expression peaks of LvMGST3 in gills at LPS stimulation for 3 h and 48 h, and their relative expression levels were significantly higher than those in control group, which were 4.39 times and 6.45 times of control, respectively. 【Conclusion】LvMGST3 has typical structural characteristics of MGST3 family, and is mainly expressed in hepatopancreas, gills and eyestalk. The expression levels of LvMGST3 in the hepatopancreas and gill of L. vannamei are significantly induced by ammonia nitrogen stress and LPS stimulation, indicating that LvMGST3 plays an important role in the defense mechanism of shrimp against environmental stress and pathogenic bacteria infection.
Key words: Litopenaeus vannamei; microsomal glutathione transferase 3(MGST3); gene cloning; ammonia nitrogen stress; lipopolysaccharide(LPS)
Foundation item: Hainan Natural Science Foundation(319QN306); Guangdong Natural Science Foundation (2017A0 30313194); Basic Research Project of Chinese Academy of Tropical Agricultural Sciences(1630052019013,1630052016 011)
0 引言
【研究意義】凡纳滨对虾(Litopenaeus vannamei)又称南美白对虾,是节肢动物门(Arthropoda)甲壳纲(Crustacea)十足目(Decapoda)对虾科(Penaeidae)中的重要人工养殖物种之一。近年来,在市场需求量的刺激下,凡纳滨对虾养殖产业得到快速发展,但在高密度集约化养殖模式下,养殖水质恶化、病害频发等一系列严峻问题随之涌现,而造成虾类免疫功能受损及抗应激能力下降(麦康森等,2004;蒋葛等,2019)。因此,明确凡纳滨对虾抗逆境胁迫及抗病相关免疫调节机制是解决以上问题的重要理论依据,也是制定疾病防控策略的关键。【前人研究进展】谷胱甘肽硫转移酶(Gluthione S-transferases,GSTs)是一种由多个基因编码,在生物体各种组织和细胞间发挥多种生理功能的小分子蛋白酶(来有鹏等,2008;达爱斯等,2014)。依据GSTs在细胞中分布位置的不同,可将其分为三大类(Hayes et al.,2005):第一类是研究最广、功能性较强且具有普遍存在性的胞质GSTs(Cytosolic GSTs);第二类是主要位于哺乳动物线粒体和过氧化物酶体中的线粒体GSTs(Mitochondrial GSTs)(Sheehan et al.,2001;Morris et al.,2011);第三类是微粒体GSTs(Microsomal GSTs,MGSTs),也称为膜结合GSTs,已列入花生四烯酸和谷胱甘肽代谢膜关联蛋白(Membrane associated proteins in eicosanoid and glutathione metabolism,MAPEG)超家族(Jakobsson et al.,1999a;Konishi et al.,2005)。真核生物的MAPEG超家族主要参与催化花生四烯酸和谷胱甘肽代谢,在细胞解毒和内外源性脂类新陈代谢中发挥着极其重要的生物学作用(Jakobsson et al.,1996,1999b);而MGSTs型蛋白因具有GST特性,还介入体内抗亲电基团和氧自由基攻击等重要生理过程(羊红玉,2011)。至今,有关MGSTs基因的研究主要集中于脊椎动物,包括大鼠(Rattus norvegicus)(Fetissov et al.,2002)、食蟹猕猴(Macaca fascicularis)(Uno et al.,2013)、人类(曾宝真等,2017)及鲤(Cyprinus carpio)(Fu and Xie,2006)、暗纹东方鲀(Takifugu obscurus)(Kim et al.,2009)和松江鲈(Trachidermus fasciatus)(张秋霞,2013)等鱼类,以及甲藻(Prorocentrum minimum)、条斑紫菜(Pyropia yezoensis)、褐藻(Laminaria japonica)和牵牛花[Pharbitis nil (L.) Choisy]等植物(Nebert and Vasiliou,2004;de Franco et al.,2008;佟少明等,2017),而针对无脊椎动物的研究甚少,仅涉及珍珠牡蛎(Pinctada martensii)(Chen et al.,2011)、飞蝗(Locusta migratoria)(Zhang et al.,2014)及桡足类动物(Roncalli et al.,2015)。上述研究结果均表明,MGSTs不仅具有解毒代谢功能,还在机体抗氧化应激时发挥保护作用。【本研究切入点】抗氧化和解毒是凡纳滨对虾有效抵抗和防御不良环境的关键方式,MGSTs是抗氧化和解毒途径中的重要因子,但至今鲜见有关凡纳滨对虾MGSTs基因(LvMGSTs)的研究报道。【拟解决的关键问题】采用RACE克隆LvMGST3基因cDNA序列,进行生物信息学分析,并探讨其在氨氮胁迫和脂多糖(Lipopolysaccharide,LPS)刺激下的表达响应,明确LvMGST3在凡纳滨对虾抗逆境胁迫与抵御病原体侵染过程中的功能作用,为有效提高对虾的抗胁迫能力和抗病力提供理论依据。
1 材料与方法
1. 1 供试凡纳滨对虾
试验所用凡纳滨对虾均购自海南省海口市某养殖基地,总数量约450尾,其生长状况良好,体重8~11 g/尾。试验前1周将凡纳滨对虾置于循环水养殖系统中以适应新环境,水温24~25 ℃,盐度20‰,pH 7.8~8.0,持续曝气增氧,并进行循环过滤处理。
1. 2 凡纳滨对虾总RNA提取及cDNA合成
随机剖取3尾健康凡纳滨对虾的肝胰腺组织置于液氮中进行研磨,按TRIzol法抽提组织总RNA,利用NanoDrop 2000分光光度计(Thermo Scientific,USA)估算其纯度及浓度,再以1.0%琼脂糖凝胶电泳检测其完整性。将质量较好的总RNA按反转录试剂盒PrimeScript RT reagent Kit With gDNA Eraser (TaKaRa)说明反转录合成cDNA,-20 ℃保存备用。
1. 3 LvMGST3基因cDNA序列克隆
依据从凡纳滨对虾转录组中筛选获得的LvMGST3基因表达序列标签(EST)序列,设计中间片段的扩增引物MGST3-F1和MGST3-R1(表1)。然后进行第一轮PCR扩增,以凡纳滨对虾肝胰腺cDNA为模板,扩增程序:94 ℃预变性3 min;94 ℃ 30 s,58 ℃ 30 s,72 ℃ 1 min,进行35个循环;72 ℃延伸10 min。以1.0%琼脂糖凝胶电泳检测PCR扩增产物。PCR凝胶条带采用SanPrep柱式DNA胶回收试剂盒[生工生物工程(上海)股份有限公司]进行回收纯化,连接至pMD18-T载体,然后转化大肠杆菌(Escherichia coli)DH5α感受态细胞(TaKaRa)。阳性克隆质粒经菌落PCR鉴定后,送至深圳华大基因股份有限公司测序。
LvMGST3基因5'末端扩增根据SMART RACE cDNA Amplification Kit试剂盒(TaKaRa)说明进行操作,采用Primer Premier 6.0设计的基因下游引物MGST3-5'-R1和Universal Primer Mix(UPM)进行配对扩增,扩增程序:94 ℃ 30 s,68 ℃ 30 s,72 ℃ 3 min,进行30个循环。LvMGST3基因3'末端扩增使用3'-Full RACE Core Set with PrimeScript RTase试剂盒(Clontech,USA),根据确定的中间片段序列设计基因上游引物MGST3-3'-F1,然后与3'-RACE Outer Primer进行PCR扩增,扩增程序:94 ℃预变性3 min;94 ℃ 30 s,58 ℃ 30 s,72 ℃ 1 min,进行35个循环;72 ℃延伸10 min。5'-RACE和3'-RACE扩增产物进行胶回收纯化,并与克隆载体连接、转化感受态细胞,然后挑选阳性克隆进行测序。将LvMGST3基因5'末端和3'末端测序结果联合中间片段进行拼接,以获得LvMGST3基因cDNA序列。
1. 4 LvMGST3基因序列分析
通过EditSeq分析LvMGST3基因开放阅读框(ORF)及其推导氨基酸序列,采用NCBI网站上的BLAST(http://www.ncbi.nlm.nih.gov/blast)程序查找LvMGST3基因同源核苷酸序列及其氨基酸序列。利用ExPASy(http://au.expasy.org/tools/)预测LvMGST3蛋白理化特性,以SignalP 5.0(http://www.cbs.dtu.dk/services/SignalP/)预测其信号肽,运用TMHMM 2.0(http://www.cbs.dtu.dk/services/TMHMM/)分析LvMGST3蛋白跨膜结构域,利用ProtScale(http://web.expasy.org/protscale/)预测其氨基酸疏水区域;再通过NCBI的保守结构域(CDD)(http://www.ncbi.nlm.nih.gov/Structure/cdd/wrpsb.cgi)预测其保守结构域和特殊位点;运用Clustal X和MEGA 6.0对不同物种的MGST3蛋白序列进行多重比对及聚类分析,并以邻接法(Neighbor-joining,NJ)构建系统发育进化树(Bootstrap=1000)。
1. 5 LvMGST3基因组织分布特征分析
随机选取15尾凡纳滨对虾,平均分为3组,分别解剖采集其血细胞、眼柄、鳃组织、肝胰腺、肠道和肌肉,冻存于液氮中或直接用于提取总RNA。以凡纳滨对虾的β-Actin F/β-Actin R為引物、各组织cDNA为模板进行半定量PCR检测,扩增程序:94 ℃预变性3 min;94 ℃ 30 s,58 ℃ 30 s,72 ℃ 1 min,进行30个循环;72 ℃延伸10 min,4 ℃结束扩增。获得的扩增产物采用1.0%琼脂糖凝胶电泳进行检测。根据条带亮度调整各组织cDNA模板用量,使β-Actin引物扩增的片段亮度基本一致,最终确定各组织cDNA用量。在相同状态下,以MGST3-RT-F和MGST3-RT-R为引物扩增LvMGST3基因片段,并通过1.0%琼脂糖凝胶电泳进行检测。
1. 6 氨氮胁迫及LPS刺激后LvMGST3基因表达差异分析
选取规格一致的健康凡纳滨对虾共150尾,平均分为氨氮胁迫组和对照组,每组3个平行。根据Lin和Chen(2001)、Liu和Chen(2004)的研究结果设氨氮胁迫浓度为20.00 mg/L(实测值20.26±0.51 mg/L),试验期间每隔24 h更换1次海水,换水量为总水量的1/3,并以氯化铵(分析纯)调整氨氮浓度,使其与设置的氨氮胁迫浓度保持一致。LPS注射试验也设2个处理组(LPS剌激组和对照组),每组3个平行,每个平行25尾凡纳滨对虾。LPS溶液是将LPS(2 mg/mL,E.coli L2880)溶解于0.8%生理盐水配置而成,终浓度为2 μg/μL。根据Xian等(2016)的研究结果,LPS刺激组按8 μg/g的剂量注射LPS溶液,对照组注射等量的无菌生理盐水。于氨氮胁迫或LPS刺激后0、3、6、12、24和48 h分别取样,从各处理组中随机采集9尾凡纳滨对虾(每个平行3尾)的肝胰腺和鳃组织,经液氮速冻后保存于-80 ℃冰箱,用于实时荧光定量PCR检测。根据已验证的LvMGST3基因cDNA序列及β-Actin内参基因,分别设计引物(MGST3-RT-F和MGST3-RT-R、β-Actin F和β-Actin R)。运用Stratagene Mx3005P仪(Agilent,USA)进行实时荧光定量PCR检测,扩增程序:94 ℃预变性3 min,95 ℃ 15 s,58 ℃ 15 s,72 ℃ 20 s,进行40个循环。获得的数据采用2–ΔΔCt法进行换算,并以SPSS 19.0进行t检验,分析氨氮胁迫和LPS刺激下LvMGST3基因在凡纳滨对虾肝胰腺及鳃组织中的表达变化情况。
2 结果与分析
2. 1 LvMGST3基因cDNA序列分析结果
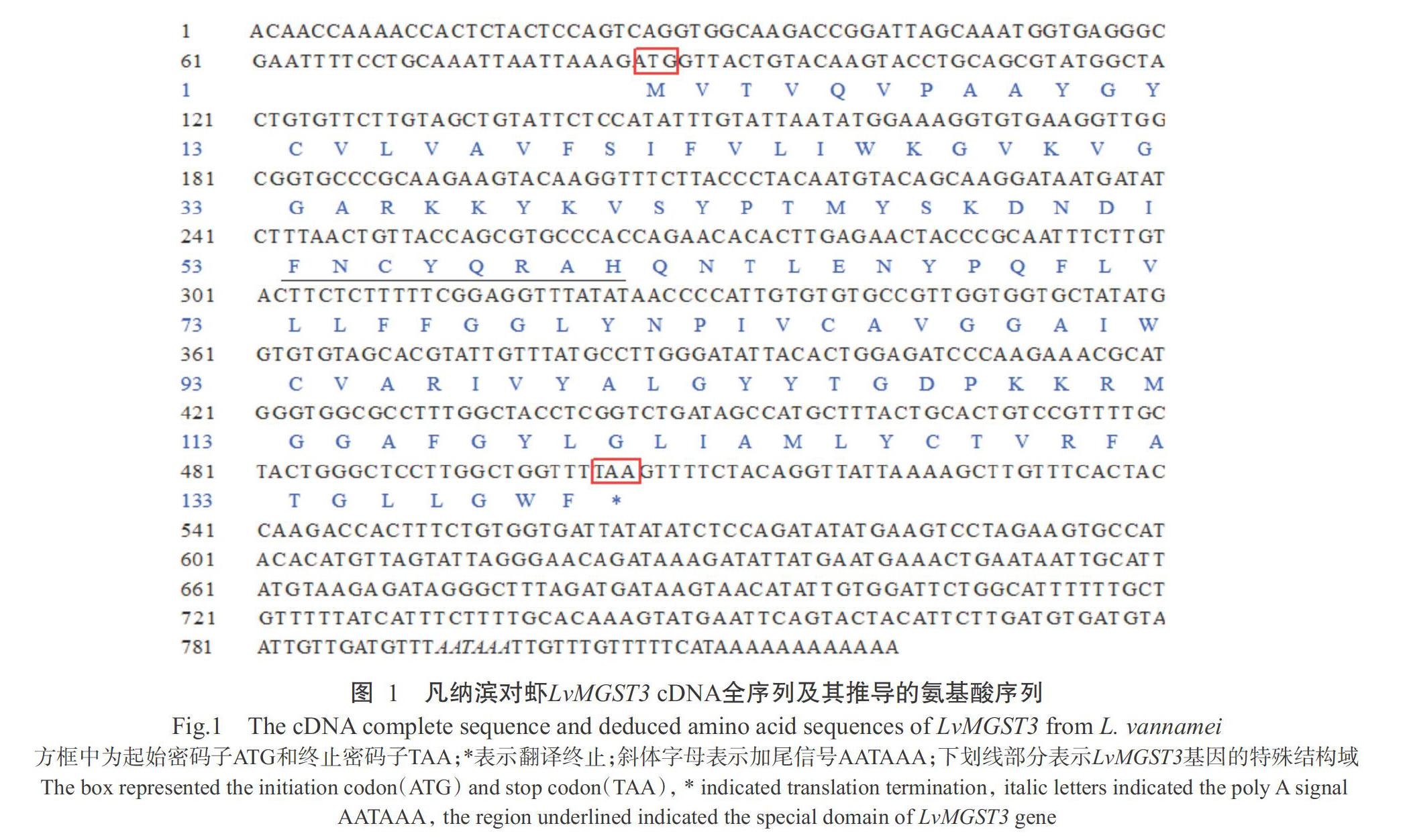
以MGST3-F1和MGST3-R1为引物进行PCR扩增,获得381 bp的LvMGST3基因中间片段;通过此片段设计5'-RACE和3'-RACE的特异性引物,分别扩增获得538和603 bp的基因片段。将所有片段进行拼接得到LvMGST3基因cDNA序列全长为826 bp,包括85 bp的5'端非编码区(5'-UTR)、321 bp的3'端非编码区(3'-UTR)和420 bp的开放阅读框(ORF),且在ploy(A)尾前端15个核苷酸处存在加尾信号AATAAA。LvMGST3基因编码139个氨基酸残基,其蛋白分子量为15.53 kD,理论等电点(pI)为9.38,富含缬氨酸残基(Val)和甘氨酸残基(Gly),均占11.51%。LvMGST3氨基酸序列中包含MGST3亚家族共有的保守结构域FNCX1QRX2H(Chen et al.,2011),此序列为FNCYQRAH(图1)。
2. 2 LvMGST3蛋白生物信息学分析结果
MGST3是一类膜结合蛋白,理论上存在1个及1个以上的跨膜结构域。TMHMM 2.0预测分析结果表明,LvMGST3蛋白具有3个跨膜结构域,分别位于第4~26位氨基酸残基、第70~92位氨基酸残基和第112~134位氨基酸残基。其中,第1~3位氨基酸残基和第93~111位氨基酸残基位于膜外侧,第27~69位氨基酸残基和第135~139位氨基酸位残基于膜内侧(图2-A)。膜蛋白的跨膜区域通常为疏水区域,由20个左右的疏水性氨基酸残基构成。经ProtScale在线预测分析得知,LvMGST3蛋白存在3个明显的高峰值(正值)区域,即疏水区域(图2-B),与TMHMM 2.0预测蛋白跨膜区的氨基酸残基位置基本吻合,说明跨膜结构域与疏水区域间能相互验证。此外,SignalP 5.0预测结果显示LvMGST3蛋白不存在信号肽。
2. 3 LvMGST3基因同源性及系统发育进化树分析结果
扩增获得的LvMGST3基因与凡纳滨对虾基因组对应核苷酸序列(GenBank登录号XM_027382177.1)的相似性达100.0%,但在5'-UTR和ploy(A)尾共有74个核苷酸碱基不同,其覆盖率为98%。LvMGST3氨基酸序列与软甲纲普通卷甲虫(Armadillidium vulgare)的MGST3氨基酸序列(RXG56258.1)相似性最高,为71.22%;与软甲纲三疣梭子蟹(Portunus trituberculatus)(MPC14949.1)的相似性次之,为68.35%;与瓣鳃纲3种牡蛎[Crassostrea gigas(MPC14949.1)、C. virginica(XP_022294415.1)和C. brasiliana(APJ38 067.1)]的相似性分別为64.57%、59.70%和59.26%;与双壳纲日本扇贝(Mizuhopecten yessoensis)(XP_021369437.1)、剑尾纲美洲鲎(Limulus polyphemu)(XP_013784372.1)、弹尾纲白符虫兆(Folsomia candida)(XP_021966114.1)、蛛形纲隆头蛛(Stegodyphus mimosarum)(KFM81199.1)的相似性分别为58.99%、58.70%、57.89%和55.80%。
多重序列比对分析结果(图3)显示,LvMGST3蛋白包含对MGST蛋白基本结构和功能具有重要意义的保守结构域FNCYQRAH,其活性位点FNCX1QRAH也高度保守,且所有氨基酸残基均位于相同的位点,疏水性氨基酸残基占主要部分(图中红色标注部分)。说明不同物种的MGST3蛋白存在数量不等的疏水区域,与ProtScale预测LvMGST3蛋白存在疏水区域的结论一致。基于MGST3氨基酸序列相似性构建的系统发育进化树(图4)显示,软体动物门双壳纲日本扇贝和瓣鳃纲3种牡蛎聚为一支,节肢动物门甲壳纲凡纳滨对虾和弹尾纲跳虫白符虫兆聚为一支,而剑尾纲美洲鲎和蛛形纲隆头蛛聚为另一分支。
2. 4 LvMGST3基因在凡纳滨对虾各组织中的表达分析结果
以β-Actin为内参基因进行半定量PCR扩增,结果(图5)显示,LvMGST3基因在凡纳滨对虾的血细胞、眼柄、鳃组织、肝胰腺、肠道及肌肉等6个组织中均有表达,但表达量在不同组织间存在一定差异。其中,在肝胰腺、鳃组织和眼柄中的表达水平较高,在血细胞和肠道中次之,而在肌肉中的表达水平相对较低。
2. 5 氨氮胁迫下LvMGST3基因的表达变化特征
由图6可看出,氨氮胁迫下凡纳滨对虾肝胰腺中的LvMGST3基因相对表达量在胁迫6 h时极显著上升(P<0.01,下同),且达最高表达水平,是对照组的1.48倍;至胁迫12 h时出现急剧下降趋势,但在胁迫24 h时又有所回升;胁迫48 h时其相对表达量降至对照组水平以下,且极显著低于对照组。凡纳滨对虾鳃组织中的LvMGST3基因相对表达量在胁迫12 h时显著高于对照组(P<0.05,下同),至胁迫48 h时其相对表达量达峰值,是对照组的3.12倍;其他胁迫时间点的LvMGST3基因相对表达量与对照组间均无显著差异(P>0.05,下同)。
2. 6 LPS刺激后LvMGST3基因的表达变化特征
由图7可看出,凡纳滨对虾肝胰腺中的LvMGST3基因相对表达量在LPS刺激3 h后极显著低于对照组,随后急剧回升,但至刺激6 h时仍显著低于对照组;LPS刺激12 h后LvMGST3基因的表达量达峰值,其相对表达量是对照组的1.57倍。在LPS刺激下,LvMGST3基因在凡纳滨对虾鳃组织中的表达模式与在肝胰腺中的恰好相反,分别在LPS刺激3和48 h时出现2个表达峰值,其相对表达量均极显著高于对照组,分别是对照组的4.39和6.45倍;在刺激12 h时LvMGST3基因相对表达量达最低值,但与对照组间无显著差异。
3 讨论
MGST3是一种具有GST活性的微粒体膜结合蛋白,作为MAPEG超家族的主要组成之一,其在生物体抗氧化胁迫及细胞解毒过程中发挥着不可或缺的生物学作用(Jakobsson et al.,1999a)。目前,关于MGST3的研究主要集中在哺乳动物(Fetissov et al.,2002;Nebert and Vasiliou,2004)、鱼类(Fu and Xie,2006;张秋霞,2013)及某些植物(de Franco et al.,2008;佟少明等,2017)上,针对节肢动物甲壳纲的研究甚少(Roncalli et al.,2015)。本研究从凡纳滨对虾肝胰腺中克隆获得LvMGST3基因cDNA全长序列,经蛋白保守结构域预测及BLAST比对分析确定LvMGST3蛋白属于MAPEG超家族,其氨基酸序列中包含FNCX1QRX2H保守结构域,与其他物种的MGST3氨基酸序列高度同源。LvMGST3基因与凡纳滨对虾基因组对应核苷酸序列(XM_027382177.1)进行比对,结果发现二者具有98%的覆盖率;综合LvMGST3蛋白跨膜結构域、疏水区域及多序列比对分析结果可知,LvMGST3与节肢动物门和软体动物门的MGST3亲缘关系较近,是存在于微粒体中的膜结合蛋白,而疏水跨膜区的存在可能更有利于其稳定停留在细胞膜中。
MGST3基因在暗纹东方鲀(Kim et al.,2009)、珍珠牡蛎(Chen et al.,2011)、松江鲈(张秋霞,2013)和飞蝗(Zhang et al.,2014)等多种物种中广泛存在,但其表达量在不同组织间具有明显差异。在哺乳动物的相关研究中发现,MGST3基因的组织分布主要集中在肝脏、大脑和心脏(Gessner et al.,2013;Uno et al.,2013;Ashbrook et al.,2014);在水生动物中除上述3种组织外,在胃、肾脏、肠道及鳃组织中也有较高的表达量(Chen et al.,2011;张秋霞,2013)。本研究首次检测MGST3基因在甲壳动物组织中的表达分布情况,结果显示,LvMGST3基因在凡纳滨对虾各组织中均有表达,存在基础的表达量,暗示其发挥着广泛性的生物学功能作用。其中,LvMGST3基因在凡纳滨对虾肝胰腺和鳃组织中的表达量较高,与Chen等(2011)在研究珍珠牡蛎时得出的结论相似,推测MGST3在凡纳滨对虾和珍珠牡蛎2种动物中具有相似的生物学功能。MGST3在多数物种间的高度保守性和组织分布特异性均表明其具有重要的生物学功能。小鼠MGST3基因在其胚胎脑组织中广泛分布,主要参与氧化应激过程中的解毒和神经保护作用(Fetissov et al.,2002);在小鼠体内外的肝脏发育过程均能检测到MGST3基因的不同表达模式,说明其不仅参与肝脏形态发育过程,还与肝脏功能的成熟完善有关(Zhu et al.,2008;Cui et al.,2010);MGST3基因表达模式还与小鼠海马体的体积相关,当其调节失控后会对一系列神经退行性疾病如帕金森病及阿尔茨海默病等造成影响(Ashbrook et al.,2014)。此外,珍珠牡蛎MGST3基因表达水平在镉诱导和细菌刺激下呈明显的时间依赖性增长趋势,且具有谷胱甘肽(GSH)依赖的过氧化物酶活性,表明MGST3在镉和细菌引起的氧化应激中发挥着重要防御作用(Chen et al.,2011);甲藻受重金属铜胁迫后,其体内的MGST3基因转录水平提高,GSH水平降低,也揭示MGST3基因在甲藻体内发挥氧化调控和抗氧化防御作用(Guo et al.,2014)。为此,本研究探讨LvMGST3基因在氨氮胁迫和LPS刺激下的表达响应,旨在揭示MGST3在对虾抗环境胁迫和病原菌感染防御过程中的功能作用。
氨氮作为水产经济动物养殖水体中普遍存在的环境胁迫因子之一,主要通过水生动物氮代谢废物排放及饲料残饵分解途径产生(徐杨等;2015;常兴涛等,2018;刘亚娟等,2018)。氨氮对水生动物尤其是甲壳动物具有明显的毒害作用(Lin and Chen,2001;Miranda-Filho et al.,2009)。氨氮胁迫不仅会影响对虾的形态发育和生理生化状态,损伤机体的器官组织结构,还降低其免疫系统功能及抗氧化能力,致使对虾对环境的耐受力和抵抗力下降,而对病原体的敏感性升高,最终引起对虾病害频发甚至大批量死亡(芦光宇等,2014;冼健安等,2014)。此外,氨氮胁迫会诱导有毒的活性氧(ROS)/活性氮(RNS)过量产生,机体为应对氧化胁迫而激活抗氧化防御相关基因的表达。本研究结果表明,经氨氮胁迫后LvMGST3基因相对表达量在凡纳滨对虾肝胰腺和鳃组织中均有不同程度的上调表达,即LvMGST3参与氨氮胁迫的防御过程,且通过氧化还原调节和抗氧化防御途径发挥作用。凡纳滨对虾肝胰腺和鳃组织中的LvMGST3基因均表现出上调的表达模式,但在鳃组织中的相对表达量整体上高于肝胰腺,在肝胰腺中的相对表达峰值是对照组的1.48倍,在鳃组织中的相对表达峰值则是对照组的3.12倍,说明鳃组织中LvMGST3基因对氨氮胁迫的表达响应更强烈。这可能是由于鳃组织作为水生动物氧气交换的重要器官,对其生命维持至关重要,且鳃组织是水生动物与水体环境直接接触的器官,氨氮和亚硝酸盐等环境胁迫因子主要经鳃组织进入虾类等水生动物体内,因此在环境胁迫过程中鳃组织更易受到胁迫损伤。
革兰氏阴性菌是造成对虾病害暴发的主要病原,其细胞壁外膜上具有特征性结构成分——LPS,宿主一般通过识别革兰氏阴性菌外膜上的LPS而引起免疫系统反应(Rodríguez-Ramos et al.,2008)。LPS自身带有细胞毒性和免疫学活性,在毒理学上被认为是促炎症和免疫调节因子,能刺激各种免疫因子表达,并诱导超氧化物自由基及其他活性氧物质释放,从而引起机体的氧化应激(Saluk-Jusczak and Wachowicz,2005)。已有研究表明,LPS刺激会导致虾类血细胞中产生大量ROS和NO,激发Ca2+介导的血细胞凋亡通路,降低虾体血细胞总数,导致其免疫力下降(Xian et al.,2017)。凡纳滨对虾受LPS刺激后,其不同组织中的谷氧还蛋白2(Grx2)和细胞色素P450(CYP370C2)呈不同程度的上调表达趋势,表明抗氧化与解毒相关基因参与了抗病原菌感染的免疫防御过程(Zheng et al.,2019)。本研究结果显示,经LPS刺激后凡纳滨对虾鳃组织中的LvMGST3基因表达在反应时间和反应强度上均较肝胰腺中的LvMGST3基因更敏感。在鳃组织中LvMGST3基因的表达水平在前期(刺激3 h)即呈显著上升趋势,且相对表达量是对照组的5.00倍以上;在肝胰腺中LvMGST3基因的表达在前期受到抑制,至刺激12 h时才呈显著上调趋势。可见,在氨氮胁迫和LPS刺激下,LvMGST3基因在凡纳滨对虾鳃组织中均呈现出更强烈的表达响应,推测LvMGST3主要在凡纳滨对虾鳃组织中发挥防御功能作用。
冼健安,錢坤,郭慧,苗玉涛,王安利,王冬梅. 2014. 氨氮对虾类毒性影响的研究进展[J]. 饲料工业,35(22):52-58. [Xian J A,Qian K,Guo H,Miao Y T,Wang A L,Wang D M. 2014. Research progress in toxic effects of ammonia-N on shrimp[J]. Feed Industry,35(22):52-58.]
徐杨,肖炜,李大宇,邹芝英,祝璟琳,韩珏,杨弘. 2015. 慢性氨氮胁迫对尼罗罗非鱼幼鱼生长及生理功能的影响[J]. 南方农业学报,46(2):327-331. [Xu Y,Xiao W,Li D Y,Zou Z Y,Zhu J L,Han J,Yang H. 2015. Effects of chronic ammonia stress on growth and physiological function of juvenile Nile tilapia(Oreochromis niloticus)[J]. Journal of Southern Agriculture,46(2):327-331.]
羊红玉. 2011. MAPEG致炎信号通路激活与马兜铃酸I肾毒性相关性[D]. 杭州:浙江大学. [Yang H Y. 2011. MAPEG activated inflammatory signaling pathway is involved in aristolochic acid I induced nephrotoxicity[D]. Hangzhou:Zhejiang University.]
曾宝真,葛春蕾,付桥粉,张志伟,宋鑫,黄文华. 2017. 稳定过表达人MGST1基因抑制肺腺癌细胞SPC-A-1的凋亡[J]. 中国肿瘤生物治疗杂志,24(6):608-614. [Zeng B Z,Ge C L,Fu Q F,Zhang Z W,Song X,Huang W H. 2017. Stable overexpression of human MGST1 gene inhibits apoptosis of lung adenocarcinoma cell line SPC-A-1[J]. Chinese Journal of Cancer Biotherapy,24(6):608-614.]
张秋霞. 2013. 松江鲈(Trachidermus fasciatus)谷胱甘肽S-转移酶基因的克隆、表达与功能分析[D]. 威海:山东大学. [Zhang Q X. 2013. Cloning,expression and functional analysis of glutathione S-transferase genes in roughskin sculpin(Trachidermus fasciatus)[D]. Weihai:Shandong University.]
Ashbrook D G,Williams R W,Lu L,Stein J L,Hibar D P,Nichols T E,Medland S E,Thompson P M,Hager R. 2014. Joint genetic analysis of hippocampal size in mouse and human identifies a novel gene linked to neurodege-nerative disease[J]. BMC Genomics,15(1):850-859.
Chen J H,Xiao S,Deng Y W,Du X D,Yu Z N. 2011. Clo-ning of a novel glutathione S-transferase 3(GST3) gene and expressionanalysis in pearl oyster,Pinctada martensii[J]. Fish & Shellfish Immunology,31(6):823-830.
Cui J Y,Choudhuri S,Knight T R,Klaassen C D. 2010. Genetic and epigenetic regulation and expression signatures of glutathione S-transferases in developing mouse liver[J]. Toxicological Sciences,116(1):32-43.
Fetissov S O,Schr?der O,Jakobsson P J,Samuelsson B,Haeggstr?m J Z,H?kfelt T. 2002. Expression of microsomal glutathione S-transferase type 3 mRNA in the rat nervous system[J]. Neuroscience,115(3):891-897.
de Franco P O,Rousvoal S,Tonon T,Boyen C. 2008. Whole genome survey of the glutathione transferase family in the brown algal model Ectocarpus siliculosus[J]. Marine Genomics,1(3-4):135-148.
Fu J,Xie P. 2006. The acute effects of microcystin LR on the transcription of nine glutathione S-transferase genes in common carp Cyprinus carpio L[J]. Aquatic Toxicology,80(3):261-266.
Gessner D K,Schlegel G,Keller J,Schwarz F J,Ringseis R,Eder K. 2013. Expression of target genes of nuclear factor E2-related factor 2 in the liver of dairy cows in the transition period and at different stages of lactation[J]. Journal of Dairy Science,96(2):1038-1043.
Guo R Y,Ebenezer V,Ki J S. 2014. PmMGST3,a novel microsomal glutathione S-transferase gene in the dinoflagellate Prorocentrum minimum,is a potential biomarker of oxidative stress[J]. Gene,546(2):378-385.
Hayes J D,Flanagan J U,Jowsey I R. 2005. Glutathione transferases[J]. Annual Review of Pharmacology and Toxi-cology,45:51-88.
Jakobsson P J,Mancini J A,Ford-Hutchinson A W. 1996. Identification and characterization of a novel human microsomal glutathione S-transferase with leukotriene C4 synthase activity and significant sequence identity to 5-lipoxygenase-activating protein and leukotriene C4 synthase[J]. The Journal of Biological Chemistry,271(36):22203-22210.
Jakobsson P J,Morgenstern R,Mancini J,Ford-Hutchinson A,Persson B. 1999a. Common structural features of MAPEG—A widespread superfamily of membrane associated proteins with highly divergent functions in eicosanoid and glutathione metabolism[J]. Protein Science,8(3):689-692.
Jakobsson P J,Thorén S,Morgenstern R,Samuelsson B. 1999b. Identification of human prostaglandin E synthase:A microsomal,glutathione-dependent,inducible enzyme,constituting a potential novel drug target[J]. Proceedings of the National Academy of Science of the United States of America,96(13):7220-7225.
Kim J H,Raisuddin S,Rhee J S,Lee Y M,Han K N,Lee J S. 2009. Molecular cloning,phylogenetic analysis and expression of a MAPEG superfamily gene from the pufferfish Takifugu obscurus[J]. Comparative Biochemistry and Physiology,149(3):358-362.
Konishi T,Kato K,Araki T,Shiraki K,Takagi M,Tamaru Y. 2005. A new class of glutathione S-transferase from the hepatopancreas of the red sea bream Pagrus major[J]. The Biochemical Joumal,388(1):299-307.
Lin Y C,Chen J C. 2001. Acute toxicity of ammonia on Litopenaeus vannamei Boone juveniles at different salinity levels[J]. Journal of Experimental Marine Biology and Ecology,259(1):109-119.
Liu C H,Chen J C. 2004. Effect of ammonia on the immune response of white shrimp Litopenaeus vannamei and its susceptibility to Vibrio alginolyticus[J]. Fish & Shellfish Immunolgy,16(3):321-334.
Miranda-Filho K C,Pinho G L L,Wasielesky Jr W,Bianchini A. 2009. Long-term ammonia toxicity to the pink-shrimp Farfantepenaeus paulensis[J]. Comparative Biochemistry & Physiology,150(3):377-382.
Morris M J,Liu D,Weaver L M,Board P G,Casarotto M G. 2011. A structural basis for cellular uptake of GST-fold proteins[J]. PLoS One,6(3):e17864.
Nebert D W,Vasiliou V. 2004. Analysis of the glutathione S-transferase(GST) gene family[J]. Human Genomics,1(6):460-464.
Rodríguez-Ramos T,Espinosa G,Hernández-López J,Gollas-Galván T,Marrero J,Borrell Y,Alonso M E,Bécquer U,Alonso M. 2008. Effects of Echerichia coli lipopolysaccharides and dissolved ammonia on immune response in southern white shrimp Litopenaeus schmitti[J]. Aquaculture,274(1):118-125.
Roncalli V,Cieslak M C,Passamaneck Y,Christie A E,Lenz P H. 2015. Glutathione S-transferase(GST) gene diversity in the crustacean Calanus finmarchicus—Contributors to cellular detoxification[J]. PLoS One,10(5):e0123322.
Saluk-Jusczak J,Wachowicz B. 2005. The proinflammatory activity of lipopolysaccharide[J]. Postepy Biochemii,51(3):280-287.
Sheehan D,Meade G,Foley V M,Dowd C A. 2001. Structure,function and evolution of glutathione transferases:Implications for classification of non-mammalian members of an ancient enzyme superfamily[J]. The Biochemi-cal Journal,360(1):1-16.
Uno Y,Murayama N,Kunori M,Yamazaki H. 2013. Characteri-zation of microsomal glutathione S-transferases MGST1,MGST2 and MGST3 in Cynomolgus macaque[J]. Drug Metabolism and Disposition,41(9):1621-1625.
Xian J A,Zhang X X,Guo H,Wang D M,Wang A L. 2016. Cellular responses of the tiger shrimp Penaeus monodon haemocytes after lipopolysaccharide injection[J]. Fish and Shellfish Immunolgy,54:385-390.
Xian J A,Zhang X X,Wang D M,Li J T,Zheng P H,Lu Y P. 2017. Various cellular responses of different shrimp haemocyte subpopulations to lipopolysaccharide stimulation[J]. Fish & Shellfish Immunology,69:195-199.
Zhang X Y,Wang J X,Zhang M,Qin G H,Li D Q,Zhu K Y,Ma E B,Zhang J Z. 2014. Molecular cloning,characteri-zation and positively selected sites of the glutathione S-transferase family from Locusta migratoria[J]. PLoS One,9(12):e114776.
Zheng P H,Wang L,Wang A L,Zhang X X,Ye J M,Wang D M,Sun J F,Li J T,Lu Y P,Xian J A. 2019. cDNA clo-ning and expression analysis of glutaredoxin(Grx) 2 in the Pacific white shrimp Litopenaeus vannamei[J]. Fish & Shellfish Immunology,86:662-671.
Zhu D Y,Du Y,Huang X,Guo M Y,Ma K F,Yu Y P,Lou Y J. 2008. MAPEG expression in mouse embryonic stem cell-derived hepatic tissue system[J]. Stem Cells and Development,17(4):775-783.
(責任编辑 兰宗宝)

