偶联尿苷二磷酸循环体系的天然产物体外糖基化修饰
刘潇斐,张良,冯旭东,李春
(北京理工大学化学与化工学院,北京100081)
天然产物作为生物体代谢过程中产生的内源性 化合物,因其种类繁多、结构多样以及具备丰富的生理药理活性而引起越来越多的关注,并且被广泛应用于食品、化妆品和医药等领域。而在实际应用过程中,很多天然产物存在着一些固有缺陷,如大部分黄酮苷元及部分黄酮苷类在水中溶解度低,而部分五环三萜类化合物如甘草次酸在临床上长期使用易引起低钾血症、高血压和醛固酮增多症等副作用,这都限制了天然产物的进一步应用。为了更好地满足人们的需求,通过对天然产物结构进行改造,得到性状优良的衍生物已经成为天然产物开发应用过程中的重点和热点。
天然产物的改性策略中通常会涉及一些重要的修饰反应,比如羟化、糖基化、甲基化、氨基化以及乙酰化等修饰,其中糖基化修饰尤为引人注目。本文主要以糖基化修饰的功能、体外糖基化的优势、糖苷化合物的合成方法入手,重点介绍了尿苷二磷酸(UDP)循环再生体系对于天然产物如萜类化合物、黄酮类化合物和其他天然产物的糖基化修饰应用,并就UDP 循环体系对于天然产物糖基化修饰的应用前景进行了讨论。
1 天然产物糖基化修饰
糖基化修饰在自然界中广泛存在,并且几乎涉及所有重要的反应过程[1]。糖基化修饰是由糖聚合物或糖与其他生物分子之间以糖苷键进行连接,包括蛋白质、脂质、核酸和天然的次级代谢物。在原核生物中,大多数糖基化修饰发生在细胞质、质膜和周质中,而在真核生物中,糖基化修饰通常发生在高尔基体和内质网中[2]。糖基化修饰通常是天然化合物生物合成的最后一步,与羟化、酰化和甲基化反应相协调[3],有助于提高天然产物结构的多样性和复杂性。在功能上,这些糖组分通常参与靶细胞的分子识别,直接或间接影响到化合物的生物学活性[4]。
1.1 糖基化修饰的功能
天然产物的糖基化修饰大大提高了天然产物结构的多样性,从而使天然产物的生物学特性有了明显提高。从化学角度来看,糖基化修饰提高了天然产物的稳定性和水溶性。花青素是自然界中广泛存在于植物中的水溶性天然色素,对其3号位的羟基进行糖基化修饰可以加固其芳香环,从而使花青素具有很高的化学稳定性[5]。糖基化不仅在修饰花色方面发挥重要作用,还通过糖基与周围水分子的外部氢键结合而增加疏水性,从而提高类黄酮的溶解度和稳定性[6]。糖基化修饰还会影响天然产物相关的膳食化合物的生物利用度,使其表现出抗氧化、抗动脉粥样硬化和抗癌活性[7]。
糖基化修饰除了能够提高天然产物的水溶性、稳定性和生物利用度,还能提高天然产物的药理学活性,通过增强靶向性并降低毒副作用。香叶醇和芳樟醇对植物本身有毒并且是化学疏水性的,因此影响它们在植物组织中的迁移和转运,通过糖基化修饰形成的单萜醇葡糖苷可以使其毒性变小、稳定性增强、并且改变香味的挥发性[8]。对人参皂甙和齐墩果酸进行糖基化修饰后提高了其抗病毒、抗炎和神经保护等多种药理学特性[9]。通过口腔给药,发现经糖基化修饰后的大豆苷比大豆苷元具有更好的生物利用度[10]。除此之外,通过糖基化修饰所得的糖苷化合物还具有信息转移、能量储存、维持细胞结构完整性、分子识别、信号传导和化学防御等多种功能[11]。
1.2 糖苷化合物的合成方法
天然产物的体外糖基化修饰在食品、医药、化妆品行业都表现出来诸多优良特性[12],所以获得糖基化修饰的天然产物成为研究的重点和热点,目前天然产物糖苷化合物的合成有体内和体外两种方式[13]。相比于依赖活细胞系统、反应不可控的体内合成方式,体外合成天然产物糖苷化合物组分明确、更易控制,近年来引起了广泛关注[14]。目前体外糖基化修饰主要存在着化学法和酶法两种方法。
1.2.1 化学法
化学法合成糖苷是基于异头中心离去基团的活化进行的,糖基供体和受体的选择性高度依赖于它们的端基异构活化和糖环携带的保护基团[15]。现在有许多巧妙的方法可用于调整糖基供体的选择性,包括激活或抑制保护基团、正交异头活化基团或选择活化试剂,使得将结构单元直接引入寡糖的合成当中。糖苷合成中的一个非常重要的问题是形成所需的α-或β-异头连接,它在很大程度上取决于连接的类型,几乎每种类型都必须利用相邻群体参与立体电子效应的组合来自行解决,目前已经进行了一些研究,在形成糖苷键之前通过束缚糖基供体和受体来形成有利的连接[16]。目前化学法合成糖苷已经取得了一些成就和进展,如刘志辉等[17]利用乙酸水解三七总皂苷制备人参皂苷Rg3并优化其工艺,Lee等[18]通过酸催化处理人参皂苷Rf,用核磁共振和质谱法鉴定其化学结构发现产生新的人参皂苷。
虽然化学法在一定程度上可以对天然产物进行糖基化修饰,然而包括经典的Koenigs-Knorr 反应在内,化学法都存在产率低、选择性差、高毒性、环境不友好、需要复杂的保护及脱保护过程等缺陷[19],导致化学法的应用受到广泛限制,在实际生产过程中存在局限。
1.2.2 酶法
酶法主要是指是利用糖合酶、水解酶和糖基转移酶对天然产物进行糖基化修饰的方法。依赖于酶的生物法操作条件比较温和,操作步骤相对简便,选择性高,而且在有些条件下,一些化学法难以或无法进行的反应可以用生物法完成。
糖合酶是一类新的糖苷酶突变体,它可以在不水解产物的情况下进行转糖基反应,从而为多糖和聚糖合成提供有价值的资源[20]。Withers等[21]通过将农杆菌属的β-糖苷酶的亲核试剂残基E358突变为非亲核残基,发现了第一个可以进行转糖基反应糖苷合成酶。Yang 等[22]报道了Humicola insolens纤维素酶Cel7B 的糖苷合酶突变体E197S的新特性,表明该Cel7B-E197S突变体能够高效地直接糖基化黄酮类化合物,从而提高它的生物学活性。
水解酶是能够将化合物的糖苷键进行水解的一类酶,张丹等[23]筛选到一株葡萄糖苷酶的高产菌株,以人参皂苷Rg3为底物水解掉一个葡萄糖后得到药理学活性更高的人参皂苷Rh2。Choi 等[24]利用一株乳酸菌产的糖苷酶水解糖苷型异黄酮得到了具有更高生物活性的异黄酮苷元。
糖基转移酶是自然界存在最广泛的转糖基酶,是一类将单个活化的单糖单元转移到特定受体的生物合成酶,它以活化的尿苷二磷酸糖为糖基供体来对天然产物进行修饰,以达到改性的目的。
甘草次酸是来源于甘草的五环三萜类化合物,其水溶性较差且应用于临床易引起毒副作用。在糖基转移酶UGT73C11的催化作用下,尿苷二磷酸葡萄糖可以将一分子葡萄糖转移至甘草次酸的三号位上形成3-O-葡萄糖基甘草次酸,提高了化合物的水溶性和生物利用度[25]。从茶树中分离出的多酚糖基转移酶CsUGT72AM1 可以在体外对黄酮醇或松柏醛进行糖基化,分别形成3-O-葡糖苷和4-O-葡糖苷,以降低茶叶中的苦味和涩味[26]。Luo 等[27]从枯草芽孢杆菌CCTCC AB 2012913 中克隆了三个UDP-糖基转移酶基因,它们可以使用人参皂苷Rh1 作为底物,以产生3-O-β-D-吡喃葡萄糖基-6-O-β-D-吡喃葡萄糖基-20(S)-原人参三醇,提高了化合物的水溶性和生物利用度。
利用糖基转移酶的酶法在催化过程中具有较高的区域选择性和立体选择性,反应条件温和、过程简单、环境友好且安全性高,因此受到广泛关注。
体外无细胞催化体系自身存在着很大的优势,因此被认为是一种新的生物制造平台[28]。首先,它可以在没有细胞膜控制的情况下,更容易地使各种物质在体外进行反应。其次,它可以在不形成副产物或细胞集团的情况下实现非常高的产物收率。例如,每葡萄糖单元的多糖和水可以产生近12个H2,其产氢量是厌氧产氢微生物的三倍[29]。第三,没有细胞膜屏障的酶系统通常具有比微生物系统更快的反应速率,比如酶促燃料电池具有比微生物燃料电池更高的输出功率[30]。第四,无细胞体外反应体系的酶混合物比微生物细胞系统更好地耐受有毒化合物[31]。最后,酶混合物能够在较为宽松的条件下进行反应,例如高温、低pH 以及有机溶剂或者离子液体存在的情况下都可以进行体外无细胞酶的催化反应[32]。
尽管体外合成生物学存在着诸多优点,但是在体外无细胞催化反应时通常需要制备纯化酶进行实验,这都提高了实验成本。随着对天然产物深入研究,人们发现在代谢途径中引入含有级联酶的酶复合物来修饰天然代谢物是具有吸引力的。因为这不仅显着降低了蛋白质纯化成本和劳动力,而且可能提高天然产物修饰的产率。
2 UDP循环体系的概述
2.1 糖基供体的合成途径
糖基转移酶通常以活化的UDP-糖为糖基供体,当它以天然产物为糖基受体时,可以将糖基供体的高能磷酸键通过能量转移至糖基受体上,在天然产物和糖基供体间形成糖苷键。
常见的UDP-糖主要有两种类型,一种为五碳糖,包括UDP-阿拉伯糖、UDP-木糖和UDP-芹菜糖等;一种为六碳糖,包括UDP-葡萄糖、UDP-半乳糖、UDP-葡萄糖醛酸、UDP-半乳糖醛酸和UDP-鼠李糖等。
UDP-葡萄糖是合成其他UDP-单糖的起始化合物。UDP-葡萄糖可以经过脱氢、脱羧、差向异构三步反应形成UDP-阿拉伯糖。具体步骤为UDP-葡萄糖在UDP-葡萄糖脱氢酶(UGDH)的作用下形成UDP-葡萄糖醛酸,UDP-葡萄糖醛酸在UDP-木糖合酶的催化下形成UDP-木糖,UDP-木糖在UDP-木糖差向异构酶(UXE)的作用下形成UDP-阿拉伯糖。与此同时,UDP-葡萄糖在UDP-葡萄糖差向异构酶(UGE)的作用下形成UDP-半乳糖,UDP-葡萄糖醛酸在UDP-葡萄糖醛酸差向异构酶(UGlcAE)的作用下形成UDP-半乳糖醛酸,UDP-葡萄糖醛酸在UDP-芹菜糖合酶(UAXS) 的作用下形成UDP-芹菜糖。此外,UDP-葡萄糖为底物还可以生成UDP-鼠李糖,具体步骤为UDP-葡萄糖在4,6-脱水酶(rmlB)和NAD+的作用下生成UDP-4-酮基-6-去氧葡萄糖,然后在3,5-异构酶(rmlC)的催化下生成UDP-4-酮基-鼠李糖,最后在4-还原酶(rmlD) 和NADPH的作用下生成UDP-鼠李糖(见图1)[33]。
2.2 偶联蔗糖合酶的UDP循环体系的概述及应用
糖基转移酶能够以高立体选择性和区域选择性对大量的天然产物进行糖基化修饰,应用前景十分广泛,但是到现在为止依然存在着一些问题。像UDP-葡萄糖之类的糖基供体价格昂贵,这限制了它们在工业过程中的应用,在体外反应时不足以用于大规模的工业化生产[34-35],因此,UDP-糖的有效原位再生是规模化生产的天然产物糖苷化合物的必要条件。
为了解决这一问题,在反应体系中引入蔗糖合酶(SuSy)。由于蔗糖成本低、易获得,因此可大规模应用于工业化生产[36]。使用蔗糖合酶将蔗糖分解为葡萄糖和果糖,以尿苷二磷酸为糖基受体,生成活化的尿苷二磷酸糖,实现了从经济廉价的蔗糖和UDP向昂贵的UDP-葡萄糖转化的生产过程(见图2)[37]。

图1 UDP-糖的生物合成途径
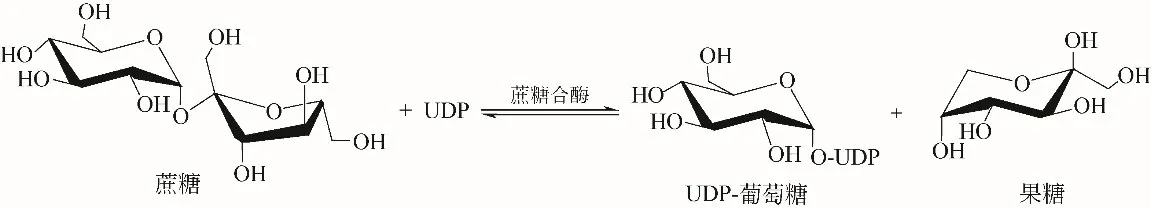
图2 蔗糖合酶的催化反应
近年来,将蔗糖合酶与糖基转移酶偶联起来,建立多酶偶联的原位UDP-葡萄糖循环体系成为趋势。该系统利用相对廉价、易获得含有高能糖苷键的蔗糖,在蔗糖合酶的催化作用下,水解生成的一分子葡萄糖被UDP 活化,生成活化的尿苷二磷酸糖供糖基转移酶使用,合成糖苷化合物后,生成的游离UDP 又可再次被循环利用,合成UDP-葡萄糖。这样周而复始,从而为糖苷化合物的合成提供了大量的糖基供体,也解除了UDP 对糖基转移酶的抑制作用,大大提高了催化效率(见图3)[38]。

图3 多酶偶联催化的原位UDP-糖循环体系
偶联蔗糖合酶和糖基转移酶构建尿苷二磷酸糖再生系统,高效合成具有高附加值的天然产物糖苷化合物,目前是国内外研究的重点和热点。
2.3 偶联海藻糖合成酶的UDP 循环体系的概述及应用
与蔗糖合酶的可逆催化类似,近年来,研究人员鉴定了来源于掘越氏热球菌(Pyrococcus horikoshii)的海藻糖合成酶。一方面它能够以UDP-葡萄糖为糖基供体将葡萄糖转移到D-葡萄糖受体上,直接形成海藻糖;另一方面,它能够水解海藻糖成两分子葡萄糖,其中一分子葡萄糖被UDP 活化形成UDP-葡萄糖(见图4)[39]。表明了海藻糖合成酶具有将海藻糖的葡糖基部分转移至UDP 的能力,从而有效地合成相应的UDP-葡萄糖。
通常,除了UDP-葡萄糖,UDP-半乳糖也是较常用的尿苷二磷酸糖,它可以作为哺乳动物在内的各种物种的糖基转移酶的糖基供体。研究人员鉴定了来源于掘越氏热球菌(Pyrococcus horikoshii)的海藻糖合成酶(TreT)和UDP-半乳糖4'-差向异构酶(pGALE),在仅添加起始原料海藻糖和UDP的情况下,TreT 可以将海藻糖水解并活化一分子葡萄糖形成UDP-葡萄糖,而pGALE 可以使UDP-葡萄糖和UDP-半乳糖相互转化[40]。这为UDP-半乳糖的再生提供了一种新的有效和实用的方法,并为糖基转移酶提供了更多样的糖基供体。
偶联海藻糖合成酶和糖基转移酶的尿苷二磷酸糖再生系统,在一定程度上丰富了UDP 循环体系的多样性,同时可以对天然产物进行糖基化修饰合成具有高附加值的糖苷化合物。但是由于海藻糖价格高于蔗糖,且pGALE 也可以在蔗糖合酶的循环体系中将UDP-葡萄糖转化为UDP-半乳糖。因此相对于偶联蔗糖合酶的UDP 循环体系来说,偶联海藻糖合成酶的UDP 循环体系目前在国内外研究中没有成为首要选择。
3 偶联UDP 再生的天然产物糖基化修饰

图4 海藻糖合成酶的催化反应
蔗糖合酶于1955 年在植物中被发现,它较高的热稳定性对于工业的发展有重要作用[41]。而在1994 年就有报道指出,通过糖基转移酶可以建立尿苷二磷酸糖的再生系统,并且已经可以对UDP-葡萄糖、UDP-半乳糖、UDP 葡糖醛酸实现再生。随着人们对于天然产物关注度的提升,研究人员逐渐将蔗糖循环体系应用于天然产物以对其进行糖基化修饰,并取得了丰硕成果。本文将针对萜类、黄酮类、及其他重要的植物天然产物的体外糖基化修饰进行综述。
3.1 萜类化合物的体外糖基化修饰及UDP再生
3.1.1 萜类化合物
萜类化合物是自然界中天然产物最多样化的家族之一。它是由异戊二烯单元(C5H8)缩合产生的衍生物,可以看成是由异戊二烯或异戊烷以各种方式连结而成的一类天然化合物,在高等植物、真菌、微生物中广泛存在。萜类化合物在工业上被广泛应用于食品行业,如用作香料或调味剂,并且还是用于工业生产维生素和其他基础化学品的重要起始材料。许多特定的萜类化合物作为抗病毒、抗疟疾和抗癌药物而被应用于临床医学[42],而法呢烯和异戊二烯分别作为生物燃料和生产优质橡胶的前体受到关注[43-44]。它在植物细胞生理学中也具有重要作用,例如通过光合作用收获光能、维持膜完整性、通过氧化还原化学转移电子,以及通过植物激素进行生长调节。根据用于构建不饱和烃类固体分子的异戊二烯C5 单元的数量来分类,可以将萜类化合物分为单萜、倍半萜、二萜类、三萜类和四萜类化合物。到目前为止,已知有超过40000种不同的萜类化合物结构[45]。
3.1.2 萜类糖苷化合物的体外合成
所有类别的萜类化合物在植物系统中都被糖基化,从而影响它们的物理化学性质和生物活性[46]。由于萜类化合物具有广泛的生理活性,大量的萜类糖苷已经被分离出来并进行结构鉴定,其中有些萜类化合物由于其高附加值的性能已被用于高额的商业化生产。由于其广泛且有前途的生理效应,已经分离出大量的萜类糖苷并在结构上被鉴定。糖基化的萜类化合物在自然界中广泛分布,并且由于多种糖苷配基和碳水化合物的组合而包含多种多样的结构。
随着人们对于天然产物关注度的提升,研究人员逐渐将蔗糖循环体系应用于天然产物以对其进行糖基化修饰,并取得了丰硕成果。人参皂甙是人参主要的有效成分,表现出不同的生物学活性,UDP-糖基转移酶(UGT)介导的糖基化是人参皂甙的最后一个生物合成步骤。Dai 等[47]将来自枯草芽孢杆菌168 的糖基转移酶Bs-YjiC 与蔗糖合酶偶联进行one-pot 反应,以原人参二醇(PPD)作为糖苷配基,用蔗糖和UDP 再生UDP-葡萄糖,将葡糖基部分转移至原人参二醇(PPD)游离的C3-OH和C12-OH以形成人参皂苷(见图5)。通过优化反应条件,最终获得3.98g/L F12(3-O-β-d-吡喃葡萄糖基-12-O-β-d-吡喃葡萄糖基-20(S)-原人参二醇)和0.20g/L Rh2。同时,该课题组使用来自枯草芽孢杆菌168 的糖基转移酶Bs-YjiC 对原人参三醇(PPT)的C3-OH、C6-OH和C12-OH进行糖基化修饰,这有助于提高PPT型人参皂苷的结构和功能多样性[48]。
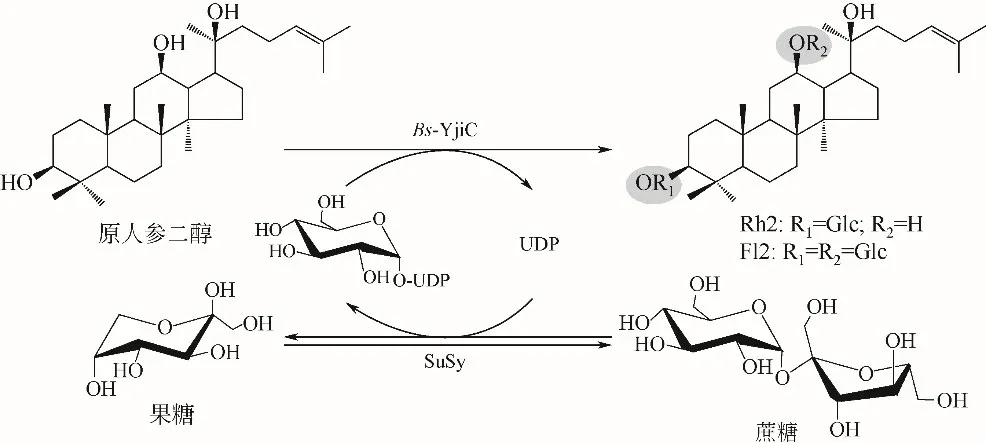
图5 偶联UDP再生的原人参二醇糖基化修饰[47]
甜菊糖和莱鲍迪甙A是甜叶菊叶中存在的主要二萜糖苷。莱鲍迪甙A具有甜味,而甜菊糖会产生残留的苦味。以甜菊糖为底物酶促合成莱鲍迪甙A可以提高甜菊糖苷产品中莱鲍迪甙A与甜菊糖甙的比例,从而提供一种理想的策略来改善甜菊糖苷产品的感官特性。Wang 等[49]通过偶联来自甜叶菊的重组UDP-葡糖基转移酶UGT76G1和来自拟南芥的蔗糖合成酶AtSUS1,证明了甜菊糖能有效转化为莱鲍迪甙A。通过AtSUS1再生UDP-葡萄糖,可以使得UDP用作UDP-葡萄糖再循环的初始材料,而不需要大量添加昂贵的UDP-葡萄糖(见图6)。研究表明,莱鲍迪甙A在30h内用2.4mmol/L甜菊糖、7.2mmol/L 蔗糖和0.006mmmol/L UDP 可以达到78%的产率。莱鲍迪甙D是来源于甜叶菊的天然零卡路里甜味剂,甜度为蔗糖的350倍,具有比莱鲍迪甙A更低的苦味和相当的甜味。Chen等[50]通过耦合番茄的重组UDP-葡糖基转移酶UGTSL2 和来自马铃薯的蔗糖合成酶StSuSy 开发了莱鲍迪甙D 合成和UDP-葡萄糖再循环的途径。经过优化从20g/L莱鲍迪甙A 获得了17.4g/L 的莱鲍迪甙D,产率达到了74.6%。
香叶醇是存在于植物中的一种单萜类化合物,具有抗菌、驱虫等功效,但是它自身的毒性不仅限制了其应用,而且对于植物组织的迁移和转运都有影响。Huang 等[38]克隆得到了三株植物来源的糖基转移酶CaUGT2、VvGT14a、VvGT15c以及真菌来源的糖基转移酶SbUGTA1,将它们与大豆来源的蔗糖合酶GmSuSy 在大肠杆菌中共表达。当VvGT15c与GmSUS 和UDP 一起反应时,香叶醇形成香叶基葡糖苷。用单酶(GT)系统和一锅二酶(GT 和SUS)系统进行对比,研究了VvGT15c 对香叶醇的葡糖基化的影响。当在单酶系统中进行香叶醇的葡糖基化时,即使在0.2mmol/L UDP-葡萄糖得添加量下,萜烯醇也未完全转化,然而,香叶醇在0.05mmol/L UDP-葡萄糖的一锅双酶系统中被完全消耗,证明了偶联蔗糖合酶和糖基转移酶的UDP循环体系的高效性。
萜类糖苷化合物的合成依赖于高效的糖基转移酶,然而目前为止,对萜烯类糖基转移酶的报道较少。这种偶联蔗糖合酶和糖基转移酶用于UDP-糖原位再生的方法,将为结构上更为复杂的萜类糖苷化合物的合成打开大门。
3.2 黄酮化合物的体外糖基化修饰UDP再生
3.2.1 黄酮类化合物
黄酮类化合物是植物产生的重要次级代谢产物,是自然界中多种药用植物的有效成分,具有抗氧化、抗炎、抗癌、抗菌和抗病毒活性[51],并且在花和果实生长、UV-B保护剂和信号分子传递中起重要作用[52]。黄酮类化合物主要是指基本母核为2-苯基色原酮类化合物,目前泛指两个具有酚羟基的芳香环(A环和B环)通过中央三碳链相互作用连接而成的一系列化合物。基于它们的化学结构,已经鉴定了上千种黄酮类化合物,其中许多是造成花、果实和叶子诱人色彩的原因[53]。自1930 年起,黄酮类化合物开始根据其分子结构分为不同的类别,如黄酮和黄酮醇、二氢黄酮和二氢黄酮醇、异黄酮和二氢异黄酮、查耳酮和二氢查耳酮类、花色素和黄烷醇类等。黄酮类化合物的药理活性因其结构而异,在自然界中,糖基化黄酮类化合物是黄酮类化合物的主要衍生物。糖基化不仅改善了黄酮类化合物的溶解性和稳定性,而且赋予这些化合物特殊的活性,改善了其选择性和药理学性质[54-55]。
3.2.2 黄酮类糖苷化合物的体外合成
绝大多数植物体内都含有黄酮类化合物,它在植物的生长、发育、开花、结果以及抗菌防病等方面起着重要的作用。但是大部分黄酮苷元及部分黄酮苷类在水中溶解度低,限制其开发和应用。由于黄酮类化合物结构复杂,使用化学合成方法对其进行结构修饰具有巨大挑战,因此利用糖基转移酶对黄酮类化合物进行糖基化修饰成为更有利的选择。

图6 偶联UDP再生的甜菊糖糖基化修饰[49]
糖基化修饰可以提高黄酮类化合物的水溶性和稳定性,但是需要添加昂贵的UDP-葡萄糖作为糖基供体,国内外科研人员利用偶联UDP 循坏再生体系解决了这一问题。根皮素的糖苷化合物具有比根皮素更广泛的药理学活性和稳定性。其糖苷键不易被水解,因此具有很高的稳定性[56-57]。此外,它还具备多种药理学活性,如抗氧化和抗血栓,以及对糖尿病治疗有积极的效果[58-59]。当提供二氢查尔酮根皮素作为受体时,来自水稻的C-糖基转移酶(OsCGT)与尿苷5'-二磷酸葡萄糖(UDPG)反应,蔗糖经蔗糖合酶水解后产生的一分子葡萄糖被UDP 活化成为糖基供体,对根皮素进行糖基化修饰形成了根皮素二氢查耳酮-β-D-葡糖苷,这是一种独特的类黄酮糖苷,具有罕见的C-糖苷结构,UDP在该过程中循环45次[60]。Son等[61]将黄酮类O-葡萄糖基转移酶(OsUGT-3) 和蔗糖合酶(AtSuSy)的基因进行融合,当提供蔗糖和UDP时,SUS-UGT 能够将槲皮素转化为槲皮素O-葡萄糖苷。此外,将蔗糖加入反应混合物中时,UDP-葡萄糖被再循环,该融合蛋白可用于酶促生产类黄酮O-葡糖苷。Gutmann 等[62]将来源于西洋梨中的O-糖基转移酶(PcOGT)与来源于大豆的蔗糖合酶SuSy 的UDP 依赖性蔗糖转化偶联,建立平行生物催化级联反应,将葡萄糖转移至根皮素2'-OH 上形成根皮苷(2'-O-β-D-根皮素葡糖苷)。为了寻找具有不同区域选择性的糖基转移酶,他们将来源于水稻的糖基转移酶OsCGT的121位异亮氨酸突变成天冬氨酸,从而在催化时得到了两种新的O-β-D-葡萄糖基化产物。SuSy不仅使得UDP-葡萄糖供体的再生率高达9倍,而且还克服对二氢查尔酮的热力学限制。通过优化反应条件得到了根皮素2'-O-或4'-O-β-D-葡糖苷高于88%的收率。
金丝桃苷具有抗炎、抗抑郁和抗真菌等许多生物学特性,且比槲皮素更易溶于水,Pei 等[63]建立了UDP-半乳糖再生系统的一锅法合成金丝桃苷。使用大肠杆菌UDP-半乳糖4-差向异构酶(GalE)可以将UDP-葡萄糖生成更为昂贵的UDP-半乳糖作为糖基供体,在来源于矮牵牛的糖基转移酶PhUGT 的作用下,以槲皮素为糖基受体,生成具有多种生物学活性的金丝桃苷。大豆蔗糖合成酶(GmSUS)与GalE 偶联,使用蔗糖作为合成UDP-半乳糖的廉价和可持续的碳源实现UDP-半乳糖的再生。这种用于从UDP和蔗糖再生UDP-半乳糖的方法可广泛用于类黄酮和其他生物活性物质的糖基化(见图7),且使得UDP-半乳糖的再生循环次数达到18.4。早期能够催化黄芩素糖基化以形成黄芩素7-O-葡糖苷的糖基转移酶F7GT,被证明对其他类黄酮也显示广泛的底物特异性[64]。Masada等[65]为了证实目前将UDP-葡萄糖再生与糖基转移酶偶联的一锅二酶系统适用于亲脂性小分子的酶促糖基化,将F7GT和AtSUS1偶联起来对芹菜素进行糖基化修饰,结果芹菜素7-O-葡糖苷的转化率达到100%,而不添加AtSUS1时,约50%的芹菜素未被葡萄糖基化,以此证明了UDP 循环体系的高效性。
黄酮类化合物结构复杂、类型多样,但是限制其最广泛应用的便是它较低的水溶性和稳定性。通过偶联蔗糖合酶和糖基转移酶的UDP 循环体系,不仅实现了黄酮类化合物的体外糖基化修饰,提高了它的药理学活性和生物利用度,而且实现了UDP-糖的有效原位再生,为黄酮类糖苷化合物的大规模的工业化生产提供了技术支持。
3.3 其他化合物的体外糖基化修饰UDP再生
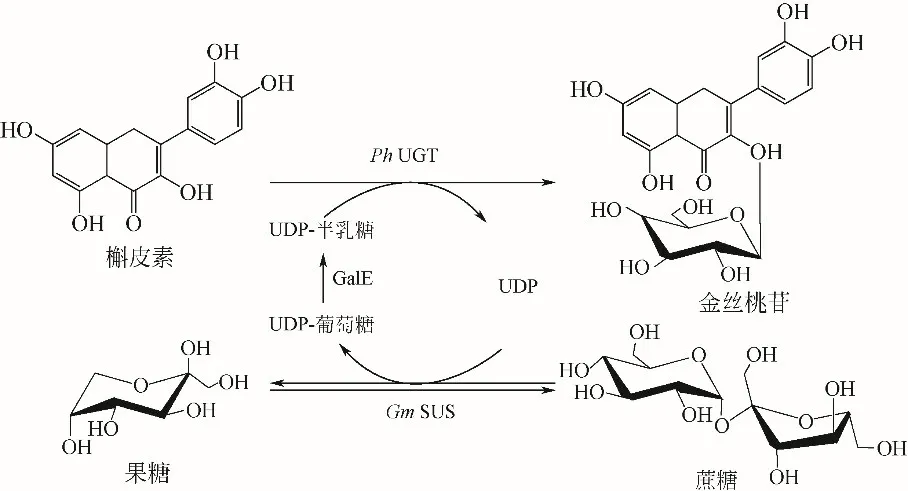
图7 偶联UDP再生的槲皮素糖基化修饰[63]
紫檀芪是白藜芦醇的天然二甲氧基化衍生物,主要存在于蓝莓和葡萄中,具有多种显著的药理学特性,如抗氧化、抗癌、抗焦虑和抗炎等。此外,紫檀芪被认为是衰老和阿尔茨海默病的有效神经调节剂。然而,由于其水溶性差和口服给药后吸收差,因此需要获得紫檀芪的糖苷化合物以提高其溶解度、稳定性和生理药理学活性。Dai 等[66]从拟南芥中克隆得到了蔗糖合酶AtSuSy,通过将来自枯草芽孢杆菌的糖基转移酶Bs-YjiC 与AtSuSy 偶联,使用一锅法反应进行紫檀芪的糖基化,得到紫檀芪的糖苷化合物紫檀芪4'-O-β-葡萄糖苷(见图8),水溶性得到显著提高。反应中摩尔转化率达到90%,且无需添加昂贵的UDPG。
脱氧雪腐镰刀菌烯-3-β-D-葡萄糖苷(D3G)是霉菌毒素脱氧雪腐镰刀菌烯醇(DON)的Ⅱ期植物代谢产物,存在于天然的镰刀菌污染的谷物中,是最重要的掩蔽的霉菌毒素。然而,D3G的毒理学意义尚不完全清楚,因此获得纯化和足量的D3G化合物以进行毒理学风险评估和用作分析标准至关重要。Michlmayr 等[67]将来源于水稻的糖基转移酶OsUGT79与来源于拟南芥的蔗糖合酶AtSUS1偶联,使得蔗糖合成酶AtSUS1 用于在葡糖基化反应期间再生UDP-葡萄糖,在糖基转移酶OsUGT79的作用下对DON 进行糖基化修饰形成D3G。通过这种方法,可以在昂贵的辅因子UDP-葡萄糖的有限浓度下获得最佳转化率,得到足够的数量和纯度的D3G用于研究。
姜黄素(二烯酰基甲烷)是一种从姜科植物姜黄等的根茎中提取得到的黄色色素,为酸性多酚类物质。目前除了被用作食品的着色剂外,还有抗炎、抗菌、抗氧化和抗肿瘤等多种活性。Kaminaga等[68]早先证明了长春花细胞悬浮培养物可以将姜黄素主动转化为一系列葡萄糖苷,使其水溶性提高2×107倍。随后,Masada 等[65]构建了一锅双酶反应系统,用于有效生产姜黄素葡萄糖苷。其中来源于长春花的糖基转移酶CaUGT2 催化UDP-葡萄糖向姜黄素的葡糖基转移,产生其单葡糖苷和二葡萄糖苷。来源于拟南芥的蔗糖合酶AtSUS1 以UDP 为受体催化UDP-葡萄糖的再生。实验表明通过添加AtSUS1 和蔗糖显著提高了反应效率,但总体葡糖基化产率在2h 内仅达到约55%的转化率。此外,该策略适用于利用UDP-葡萄糖作为糖供体的各种天然产物的糖基化。
大豆低聚糖(SBOS)因其在制药、化妆品和食品工业中的潜在应用而引起了相当大的关注,而棉子糖和水苏糖是大豆低聚糖的主要生物活性成分。这些低聚糖传统上是从植物中提取的,但这种提取过程通常会导致低产量和高生产成本。Tian等[69]提出了一种生物催化方法,使用五种酶开发了体外多酶系统,即蔗糖合成酶(SuSy)、UDP-葡萄糖4-差向异构酶(GalE)、肌醇半乳糖苷合成酶(GS)、棉子糖合成酶(RS) 和水苏糖合成酶(STS),以蔗糖为底物生产棉子糖和水苏糖,同时达到了UDP 和肌醇的回收利用。具体步骤为蔗糖和UDP 在蔗糖合酶的催化作用下可逆转化为果糖和UDP-葡萄糖,UDP-半乳糖4-差向异构酶可以容易地将UDP-葡萄糖异构化成所需的UDP-半乳糖,随后以肌醇和UDP-半乳糖为底物经过肌醇半乳糖苷合成酶催化形成肌醇半乳糖苷作为糖基供体,棉子糖合酶和水苏糖合成酶催化肌醇半乳糖转移分别产生棉子糖和水苏糖,其中UDP 转换数达到337 次,将反应体系中的肌醇再循环5次,得到128.9g/L棉子糖。
目前多种天然产物的糖基化修饰揭示了蔗糖合酶对UDP-葡萄糖再生的效率以及GT-SuSy 级联反应的整体性能是多么重要。UDP-葡萄糖的再循环是优化转化动力学的有效策略,并且对于减少昂贵的辅因子UDP-葡萄糖的添加量具有经济意义。

图8 偶联UDP再生的紫檀芪糖基化修饰[66]
4 结语
多年来,天然产物的糖基化修饰对于其自身的生理药理活性有重要影响,尤其在医药上具有重大意义,因此糖基转移酶因其在天然产物糖基化修饰中的多种作用而引起了相当大的兴趣。越来越多的糖基转移酶已被公认为植物和动物界中细胞稳态的关键组分。糖基化是影响植物激素和次级代谢物活性的主要机制,并且是植物处理环境毒素的保障。然而由于UDP-糖高昂的价格不适用于大规模的工业化生产,因此通过偶联蔗糖合酶和UDP 糖基转移酶的UDP循环体系实现UDP-糖的有效原位再生成为一种最经济并高效的方法。而UDP-糖再生循环次数的最大化更是直接影响了工厂效益,一般来说,通过降低添加的UDP 浓度可以降低UDP 导致的产物抑制,从而实现最大的循环效率。此外,建议应用低UDP 的Michaelis-Menten常数的蔗糖合酶来进行UDP-糖的原位再生,而蔗糖浓度与循环次数无关,通常不在考虑范围[70]。

