开环异落叶松树脂酚的提取及其对乳液稳定性的影响研究
程 晨,陈 鹏,王新天,于 坤,郑 畅,黄庆德,邓乾春
(中国农业科学院 油料作物研究所,油料脂质化学与营养湖北省重点实验室,农业部油料加工重点实验室,武汉 430062)
亚麻木酚素是一种以开环异落叶松树脂酚二葡萄糖苷(SDG)为单位结构、具有抗氧化活性的生物大分子,在人体肠道中的菌群作用下经过水解、去羟基化、去甲基化和氧化形成具有预防乳腺癌、结肠癌、前列腺癌等功能的肠二醇(END)和肠内酯(ENL)[1-5]。亚麻木酚素特殊功能特性主要来源于END和ENL[6],其生物利用率也主要取决于SDG通过转化形成ENL和END的比例[7-8]。研究表明,约57.2%SDG在人体肠道内能被转化形成ENL和END[9],但远低于其水解产物开环异落叶松树脂酚(SECO)在人体肠道内的转化率(72%)[7]。因此,SECO可能比SDG具有更强的对人体健康的干预调理作用。
乳液口服递送体系作为一种经典的脂质载体,可有效提高脂溶性生物活性成分的生物利用率[10],目前被广泛应用于牛奶、蛋黄酱、蛋白饮料、奶油、冰激凌等食品体系中。乳液通常为热力学不稳定体系,在储藏过程中易发生絮凝、聚集、奥氏熟化、乳析等现象,严重影响相关产品的外观及口感。此外,由于乳液的粒径较小,增大了油脂与氧气接触的表面积,降低了乳液的氧化稳定性。研究表明,SECO、SDG是良好的天然抗氧化剂,能有效防止油脂的自动氧化[11],显著提高乳液体系中油脂的氧化稳定性。在脂质体体系中,弱极性SECO在乳液界面处聚集,与磷脂分子发生相互作用,有利于提升体系物理稳定性[12],但极性SDG在储藏过程中,其糖苷基可进入脂质体膜相邻磷脂分子之间的空隙,增大界面膜的间隙,破坏体系的物理稳定性[13]。综上,考察SDG和SECO对乳液稳定性的影响具有重要意义。然而目前市售SDG、SECO主要通过化学合成法获得,具有产量低、成本高、安全性差等特点,限制了其在食品工业中的研究与应用。因此,本实验通过水解植物性来源的亚麻木酚素制备SECO,对于获取高纯度的SECO提取物、降低生产应用成本和实现产业化应用具有重要参考价值。
本实验选用含50%SDG的木酚素粗提物(50%SDG)为原料进行酸水解,以SECO含量为指标,对SECO的HCl浓度和水解时间进行优化,进一步通过有机溶剂萃取、真空冷冻干燥工艺获得SECO粗提物,探究水解前后亚麻木酚素粗提物对在高温储藏环境下的磷脂-亚麻籽油乳液稳定性影响,以期为扩大亚麻木酚素的应用领域、推进PUFAs相关产品开发提供理论依据。
1 材料与方法
1.1 实验材料
1.1.1 原料与试剂
50%SDG,购于成都仕凯生物科技公司;一级亚麻籽油,购于红井源油脂有限责任公司;大豆卵磷脂(s-75),购于LipoidTM公司。
盐酸、甲醇、异丙醇、异辛烷、丁醇、三氯化铁、醋酸钠、乙酸、无水乙醚、三氯乙酸、硫氰酸铵、氯化钡、硫酸亚铁,国药化学试剂有限公司;硫代巴比妥酸(TBA),Aladdin公司;开环异落叶松树脂酚葡萄糖苷(SDG,98%)、开环异落叶松树脂酚(SECO,95%)、过氧化氢异丙苯、1,1,3,3-四乙氧基丙烷(TEP),西格玛奥德里奇上海贸易公司;开环异落叶松树脂酚单葡萄糖苷(SMG,98%)、脱水开环异落叶松树脂酚(98%),上海源叶生物科技有限公司;CH3COOH、CH3OH,色谱纯。
1.1.2 仪器与设备
分析天平,恒温水浴摇床,电热恒温箱,台式离心机,IKA数字高速剪切机,高压微射流均质机,Waters超高效液相分析仪,DU800紫外-可见分光光度仪。
1.2 实验方法
1.2.1 亚麻木酚素的酸水解
参照臧茜茜等[14]的方法进行酸水解亚麻木酚素。取6 g 50%SDG于50 mL玻璃管中,依次加入40 mL不同浓度HCl溶液(0.2~2 mol/L),2 500 r/min 下振荡30 min后,将每个浓度样品平均分为5份(每份8 mL)于玻璃管中,置于95℃水浴摇床水解210 min,在水解期间定时取样。样液在5 000 r/min离心10 min,取上清液过0.22 μm滤膜,滤液用超高效液相色谱(UPLC)测定SDG和SECO含量。
1.2.2 SECO的萃取
取10 mL 1.2.1中水解液(最佳酸水解条件进行该实验)于50 mL离心杯中离心,取上清液,加入30 mL无水乙醚,在5 000 r/min下涡旋30 min,用分液漏斗收集上层溶液,重复提取3次,将获得的萃取液汇总并在37℃下旋蒸至10 mL,氮吹除去有机溶剂,再于-80℃下预冻30 min,置于真空冷冻干燥机中干燥,得到SECO粗提物。
取10 mg SECO粗提物于100 mL容量瓶,使用甲醇(色谱法)定容,0.22 μm滤膜过滤后,用UPLC测定SECO含量。
1.2.3 SDG和SECO含量的UPLC测定
UPLC条件:流动相A为甲醇、B为0.5%乙酸水溶液,进样量2 μL,在洗脱流速0.1 mL/min下进行非线性梯度洗脱(0~8 min 15%A,8~12 min 15%A~28%A,12~16 min 28%A,16~24 min 28%A~55%A,24~28 min 55%A~85%A,28~32 min 85%A,32~33 min 85%A~15%A,最后以15%A保持2 min),紫外检测波长280 nm。采用SDG、SECO标准曲线进行定量,相关系数为0.999。
1.2.4 磷脂-亚麻籽油乳液的制备及储藏稳定性
以20%亚麻籽油为油相,含3%大豆卵磷脂的5 mmol/L磷酸缓冲液为水相,分别加入50% SDG、SECO粗提物,使SDG/SECO在整个体系中的浓度为200 μmol/L。将油水混合物使用高速剪切机在8 000 r/min下高速剪切5 min获得粗乳液,使用高压微射流均质机在82 MPa的均质压力下循环4次,分别制备对照组、50% SDG组和SECO组磷脂-亚麻籽油乳液。将乳液放置于65℃恒温恒湿箱中避光保存7 d并定期取样,对乳液粒径、氧化产物等指标进行测定,探究在高温储藏条件下水解前后亚麻木酚素粗提物对乳液稳定性的影响
1.2.5 乳液粒径的测定
使用马尔文纳米粒径分析仪测定在不同储藏时间下磷脂-亚麻籽油乳液的粒径。
1.2.6 初级氧化产物氢过氧化物含量的测定
使用紫外分光光度计对磷脂-亚麻籽油乳液体系中氢过氧化物含量进行测定[15]。取0.3 mL乳液与1.5 mL破乳剂(异辛烷-异丙醇,体积比3∶1)混合,涡旋振荡10 s,重复3次,每次间隔20 s,将混合液在5 000 r/min下离心10 min,取200 μL上层液体于10 mL离心管中,加入2.8 mL甲醇-丁醇(体积比2∶1)混合液,接着加入30 μL Fe2+(将0.132 mol/L BaCl2(0.4 mol/L HCl配制)与0.144 mol/L FeSO41∶1混合,5 000 r/min下离心5 min)和3.14 mol/L硫氰酸铵的混合液(体积比1∶1),振荡均匀,暗反应20 min后在510 nm波长下测定吸光度。使用过氧化氢异丙苯制备标准溶液绘制标准曲线。
1.2.7 次级氧化产物丙二醛含量的测定
使用紫外分光光度计对磷脂-亚麻籽油乳液体系中丙二醛的含量进行测定[16]。在耐高温螺盖玻璃皂化管中将1 mL乳液与2 mL TBA试剂混合,振荡均匀,沸水浴15 min,冷却至室温后将反应液在5 000 r/min下离心15 min,取上清液在532 nm波长下测定吸光度。用1,1,3,3-四乙氧基丙烷配制标准溶液绘制标准曲线。以TBARS值表征丙二醛含量。
1.2.8 数据统计分析
采用Origin 9.1软件绘制图表,IBM SPSS 24.0对数据进行ANVOA显著性比较分析(p<0.05时,具有显著性差异)。所有实验均做3个平行,数据结果以“平均值±标准差”表示。
2 结果与分析
2.1 盐酸浓度和水解时间对SDG及SECO含量的影响
准确称取6 g 50% SDG于50 mL玻璃管中,在HCl浓度分别为0.2、0.5、1.0、1.5、2.0 mol/L,水解时间分别为100、120、150、180、210 min的条件下进行水解,使用UPLC对水解产物进行定量分析,通过与标准品对比分别确定SDG和SECO的出峰时间,考察HCl浓度和水解时间对SDG及SECO含量的影响,结果如图1所示。
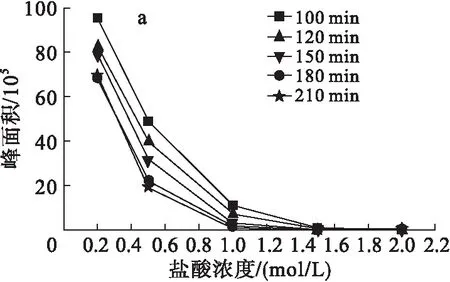
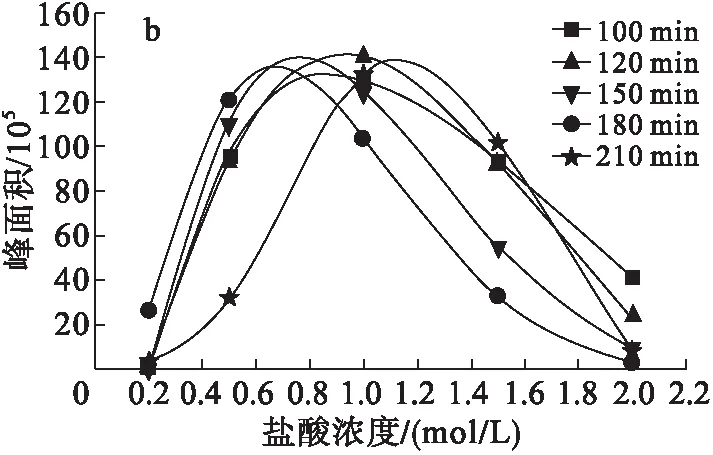
图1 不同HCl浓度和水解时间条件下SDG(a)和SECO(b)的含量
从图1可以看出,当水解时间相同时,随着HCl浓度的增加,SDG逐渐被消耗(图1a),而SECO含量呈先升高后降低的趋势(图1b)。这是由于当HCl浓度低时,不利于分子间的相互作用,导致水解速率低;随着HCl浓度增加,分子间的相互作用加快,从而提升了水解速率,因此SECO含量增加;但当HCl浓度过高时,SECO进一步发生水解,致使SECO含量降低。当HCl浓度相同时,随着水解时间的延长,SDG逐渐被消耗产生SECO,但SECO含量与水解时间无明显相关性。在水解时间为120 min时具有最大的SECO含量。综合考虑,选取水解时间为120 min、HCl浓度为1 mol/L进行下一步实验。
2.2 亚麻木酚素酸水解产物分析
在HCl浓度1 mol/L条件下,考察50% SDG水解100~210 min内的水解过程,对其UPLC图谱进行分析,结果如图2所示。
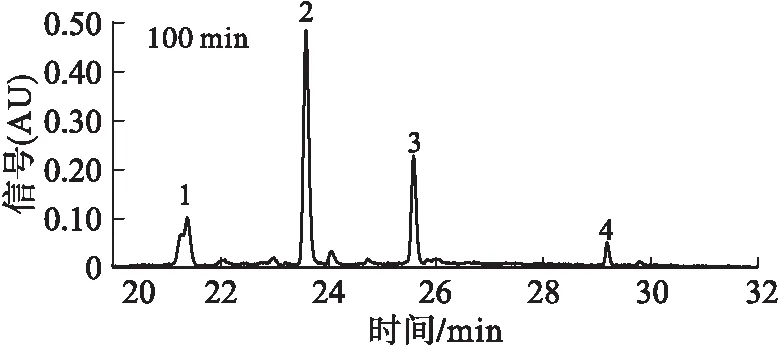
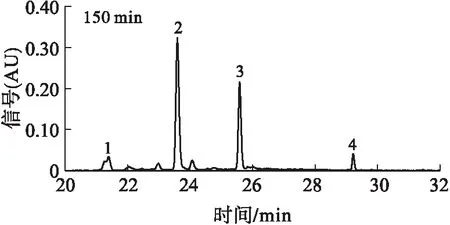
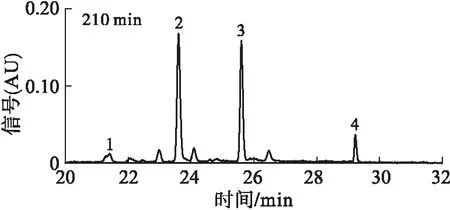
注:1.SDG;2.SMG;3.SECO;4.脱水SECO。
通过与标准品进行对比,结合参考文献,确定图2中峰1为SDG,峰2为SMG,峰3为SECO,峰4为脱水SECO[17]。可见,随着水解时间的延长,SDG的峰面积不断减小,SDG转化为SMG的同时SMG向SECO转化,且有少量的脱水SECO产生。因此,可推断,在SDG的酸水解过程中,当HCl浓度为1 mol/L时,SDG水解主要分为3个阶段,且同步进行:第一阶段,SDG分子脱去一分子糖苷生成SMG;第二阶段,SMG脱去一分子糖苷生成苷元化合物SECO;第三阶段,SECO脱去水分子形成脱水SECO。本实验结果与张文斌[18]研究结果一致,在盐酸浓度为1 mol/L时,SDG主要水解产物为SMG、SECO和脱水SECO。
2.3 粗提物中SECO的含量
采用优化后的水解参数对50%SDG进行水解,取水解后的溶液冷却至室温,使用无水乙醚萃取、真空冷冻干燥制备SECO粗提物,通过UPLC测定粗提物中SECO的含量,其图谱如图3所示。结果表明,粗提物中SECO含量为65%(以下以65%SECO表示)。
2.4 50%SDG和65%SECO对磷脂-亚麻籽油乳液稳定性的影响
按照1.2.4方法使用高压微射流法制备磷脂-亚麻籽油乳液对照组、65% SECO组和50% SDG组,测得其初始粒径分别为243、260 nm和255 nm。将乳液在65℃下避光储藏7 d,对乳液储藏过程中的粒径、初级氧化产物和次级氧化产物含量进行测定,结果如图4、图5所示。

图3 SECO粗提物的UPLC图谱

图4 65%SECO和50%SDG对磷脂-亚麻籽油乳液粒径的影响
从图4可以看出,在储藏过程中,对照组乳液和50%SDG组乳液的粒径随着储藏时间的延长而增大,且50%SDG组乳液粒径整体大于对照组。产生该现象的原因可能是随着储藏时间的延长,SDG向磷脂界面处移动,其糖苷基插入界面膜内,使磷脂分子间隙增大,加速乳滴相互碰撞,致使乳滴发生絮凝和聚集[13]。此外,65℃储藏7 d,与对照组相比,65% SECO组乳液粒径降低了77%,且在整个储藏过程中,65% SECO组乳液粒径无显著变化(p>0.05),表明SECO显著提高了磷脂包埋的亚麻籽油的物理稳定性。产生该结果的原因可能为弱极性分子SECO主要存在于乳液界面位置,与磷脂分子发生氢键结合[12],增加了乳液界面厚度,提高乳液稳定性。
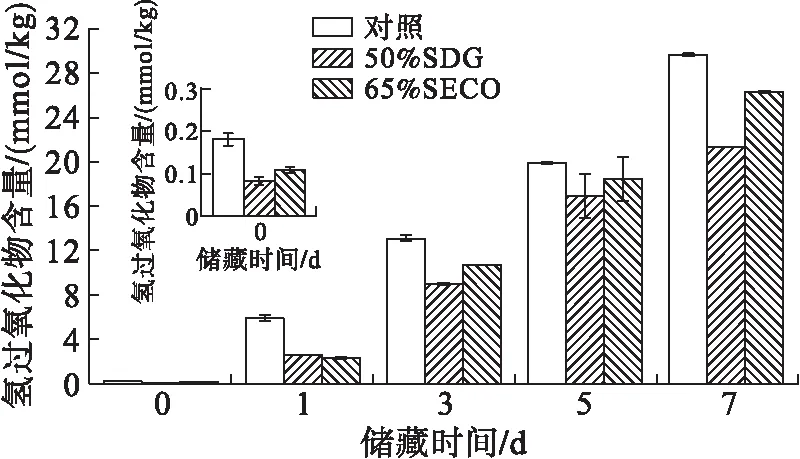
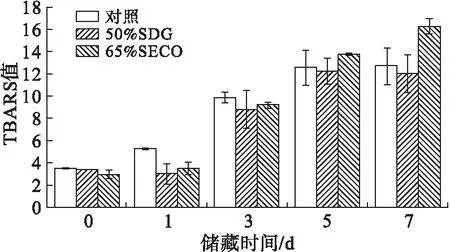
图5 65%SECO和50%SDG对磷脂-亚麻籽油乳液氢过氧化物和TBARS值的影响
从图5可以看出,对照组乳液初始氢过氧化物含量最高,为(0.181±0.014)mmol/kg,高于含65%SECO和50%SDG的乳液组。说明在乳液制备过程中,65%SECO和50%SDG均具有抑制乳化过程中亚麻籽油氧化的作用。乳液体系中氢过氧化物含量随储藏时间的延长而升高,储藏7 d的对照组乳液中氢过氧化物含量高达(29.647±0.168)mmol/kg,而65% SECO和50% SDG分别将乳液体系中氢过氧化物含量降低11%和27%。由此可得,在乳液体系中50%SDG具有最佳的抑制亚麻籽油发生初级氧化能力。原因可能为SDG具有较好的热稳定性[19],因此在65℃高温下,SDG能稳定存在并发挥抗氧化效应。此外,在65% SECO中仍残留少量的Cl-(约0.08%),由于盐离子可在液滴表面堆积,改变液滴的表面特性,增加了水相中金属离子等阳离子促氧化成分与油脂的接触,从而加速了油脂氧化[20-21]。
在乳液储藏前期(0~3 d),50% SDG和65% SECO均具有抑制亚麻籽油氧化产生氢过氧化物的作用。储藏1 d,与对照组乳液相比,分别将乳液氢过氧化物含量降低55%和60%。原因可能是由于亚麻木酚素类多酚化合物在氧化初期能延缓乳液中油脂氧化,降低氢过氧化物等初级氧化产物的含量,但对氢过氧化物进一步裂解产生醛、醇、酮等次级氧化产物含量的过程无直接影响[16],因此50% SDG组和65% SECO 组乳液的TBARS值的变化无显著性差异(储藏1 d,与对照组相比,50% SDG组和65% SECO组乳液TBARS值分别降低了42%和40%)。但储藏7 d,65% SECO组乳液中TBARS值比对照组提高了28%,加速了次级氧化的进程,原因为65% SECO中除SECO以外的盐离子、亚麻蛋白等其他物质在高温下长期储藏可能会产生促进氢过氧化物裂解的物质,加速了次级氧化产物的积累,但目前具体机理尚不明确,仍需进一步探究。
3 结 论
(1)本实验对水解亚麻木酚素(含50%SDG)提取SECO的条件进行了优化,确定最佳水解条件为HCl浓度1 mol/L、水解时间120 min,此时SECO含量最高。进一步通过无水乙醚萃取,真空冷冻干燥制备了SECO含量为65%的SECO粗提物。通过对水解产物UPLC图谱分析发现,当盐酸浓度为1 mol/L时,SDG首先脱去一分子糖苷生成SMG,SMG进一步水解失去一分子糖苷生成SECO,SECO在酸的作用下失去一分子水,形成脱水SECO,且以上水解过程同时进行。
(2)磷脂-亚麻籽油乳液的储藏稳定性实验表明,50%SDG和水解产物65%SECO均具有抑制乳化过程中亚麻籽油氧化的作用。65℃储藏7 d,与对照组相比,65%SECO组乳液粒径降低了77%,因此65% SECO抑制了乳液在高温储藏过程中的聚集、絮凝现象的发生,显著提高了乳液的物理稳定性;储藏1 d,50%SDG和65%SECO分别可将乳液体系中氢过氧化物含量降低55%和60%,TBARS值降低42%和40%。但储藏7 d,65%SECO组TBARS值比对照组提高了28%,加速了次级氧化的进程,其具体原理还需进一步探究。

