滤过泡相关性真菌性眼内炎1例
杨晓伟,朱蓉嵘
(南通大学附属医院眼科,江苏 南通 226001)
感染性眼内炎是一种非常严重的眼科急症,炎性反应迅速波及眼内组织和液体,包括房水、玻璃体、视网膜、葡萄膜、甚至角巩膜和眼眶组织,发展为眼球周围炎[1]。感染性眼内炎是青光眼术滤过术实施后最严重的并发症之一。由于滤过泡的存在而发生的眼部感染,称为滤过泡相关性眼部感染,包括滤过泡炎和滤过泡相关性眼内炎。真菌性眼内炎是由浅部、深部病原真菌或条件致病真菌引起的眼内感染,具有发病隐匿、潜伏期长、病程长及易复发等特点,其眼部组织严重损害,甚至丧失视力、眼球萎缩[2]。本文回顾分析1例临床病例资料,现报告如下。
1 临床资料
患者,男,74岁,因“右眼红痛2周”于2018年10月22日至南通大学附属医院门诊就诊。患者2周前出现右眼红,稍有疼痛,未重视,1周前症状加重,在当地医院就诊,诊断:右眼葡萄膜炎,予以全身及局部糖皮质激素抗炎治疗。治疗1周后,眼部症状加重。遂至南通大学附属医院进一步诊治。患者15年前因双眼急性闭角型青光眼在南通大学附属医院行双眼小梁切除+周边虹膜切除术。否认眼部外伤病史。眼科检查:右眼视力:光感/1 m,右眼结膜混合充血,上方球结膜水肿,颞上方原滤过泡处破溃,角膜透明,前房周深1/3角膜厚度(corneal thickness,CT),下方积脓2 mm(图1A),瞳孔药物性散大,晶状体表面见白色絮状混浊,晶状体混浊,玻璃体腔混浊,眼底窥不见,眼压:12.0 mmHg(1 mmHg=0.133 kPa)。右眼B超见右眼玻璃体混浊(图1B)。左眼视力:0.06,左眼球结膜无充血,颞上方滤过泡较薄,扁平,角膜透明,前房周深1/2 CT,颞上方虹膜周切口通畅,瞳孔圆,直径约3 mm,晶状体混浊,玻璃絮状混浊,眼底见视盘色淡,边界清,杯盘比约0.8,视网膜动静脉直径比值1:2,视网膜平伏,黄斑中心凹反光未见,眼压:17.0 mmHg。辅助检查:血常规、肝肾功能以及心电图未见明显异常。入院诊断:右眼感染性眼内炎,双眼并发性白内障,双眼闭角型青光眼,双眼小梁切除+周边虹膜切除术后。初步考虑患者右眼细菌感染,遂急诊行右眼白内障超声乳化吸出+玻璃体切除+滤过泡修补术。术中冲洗滤过泡下脓性分泌物,抽取前房水和玻璃体液行病原学检查;术中见玻璃体炎性混浊,眼底见杯盘比约0.8,视网膜动静脉直径比值1:2,血管走形可,视网膜平伏,未见脉络膜视网膜浸润病灶。术中涂片结果示:房水标本中见大量的炎性细胞,以中性粒细胞为主,未见真菌、细菌等病原体;玻璃体标本见少量炎症细胞,以中性粒细胞为主,未见真菌、细菌等病原体。前房水、玻璃体液培养5 d未见真菌、细菌生长。术后全身使用甲泼尼龙琥珀酸钠抗炎治疗、头孢曲松钠抗感染治疗,局部使用妥布霉素地塞米松滴眼液、氧氟沙星眼膏滴眼等治疗。术后第1天,右眼结膜水肿、充血,缝线在位,角膜水肿,角膜后表面见灰白粗颗粒状沉着物,晶状体缺如,后囊膜在位,玻璃体腔轻度混浊,眼底模糊,隐见视网膜红色反光。术后第2天见角膜上方灰白混浊,角膜基质层水肿,后弹力层褶皱,后表面见灰白色粗颗粒状角膜后沉着物增多。术后第3天,角膜上方灰白混浊加重(图2A),玻璃体腔混浊,眼底窥不见。考虑患者眼部病情加重,遂行右眼前房灌洗+玻璃体腔灌洗+硅油注入术。术后第1天,角膜上方灰白混浊,较前无明显改变。予以球结膜下注射头孢他啶,并予以万古霉素滴眼,局部抗感染治疗。术后第2天,角膜上方灰白混浊向下方蔓延,角膜基质层混浊,下方角膜后表面见大量灰白色颗粒状沉着物。患者眼部感染加重,予以口服盐酸米洛环素胶囊,球结膜注射庆大霉素等治疗。术后第5天,患者诉右眼疼痛,右眼视力眼前光感,右眼全角膜灰白混浊,上方角膜部分溶解变薄,隐见下方角膜后灰白沉着物(图2B)。患者病情加重,行右眼前房灌洗,并前房注射万古霉素治疗。结膜囊分泌物涂片提示见中性粒细胞,未见真菌、细菌等病原体。经验性使用亚胺培南静脉滴注治疗,并予以头孢他啶滴眼局部抗感染治疗。2018年11月3日,患者眼部疼痛加剧,无光感,患者右眼角膜混浊(图3),眼内结构窥不见,遂行右眼内容物剜除术。术中见:角膜后表面黄白色脓苔,原滤过手术巩膜隧道深部呈灰白色脓疡改变。术中角膜溃疡面涂片:大量炎症细胞,以中性粒细胞为主;中等量的真菌菌丝。术后病理(图4)示:右眼真菌性角膜炎,感染性眼内炎;右眼滤过泡符合真菌感染。11月5日报告提示:角膜组织及巩膜组织真菌培养为丝状真菌,镰刀霉菌。确定患者右眼为镰刀霉菌感染。追问病史:患者有手癣病史(图5),未正规治疗,自诉曾因眼部瘙痒而揉眼。
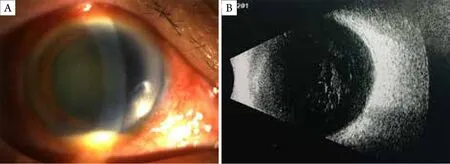
图1 入院时患者右眼前节及B超图像Figure 1 Right anterior segment of the eye and B-mode ultrasonography were taken upon admission
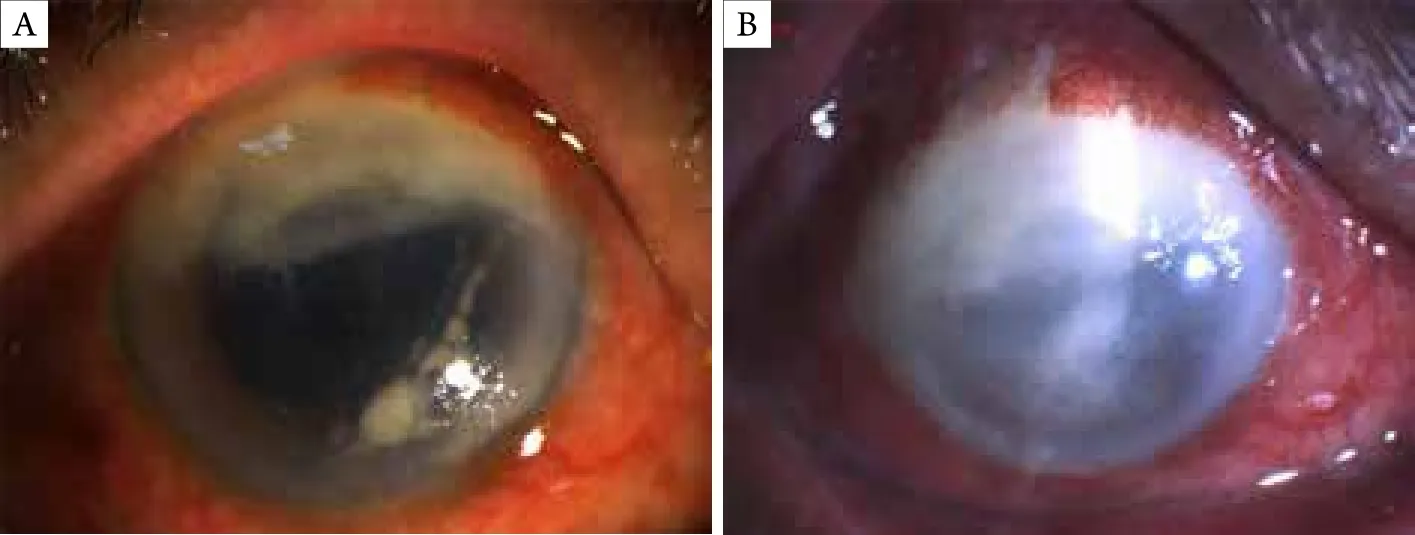
图2 在积极手术及抗感染治疗情况下,角膜混浊却逐渐加重Figure 2 Although surgery and anti-infective treatment have been carried out, corneal opacity has been gradually aggravated

图3 右眼前节照片:右眼角膜混浊,右眼球内结构窥不见Figure 3 Anterior segment photograph of right eye: loss of transparency in the right cornea, and the intraocular structure of the right eye is invisible
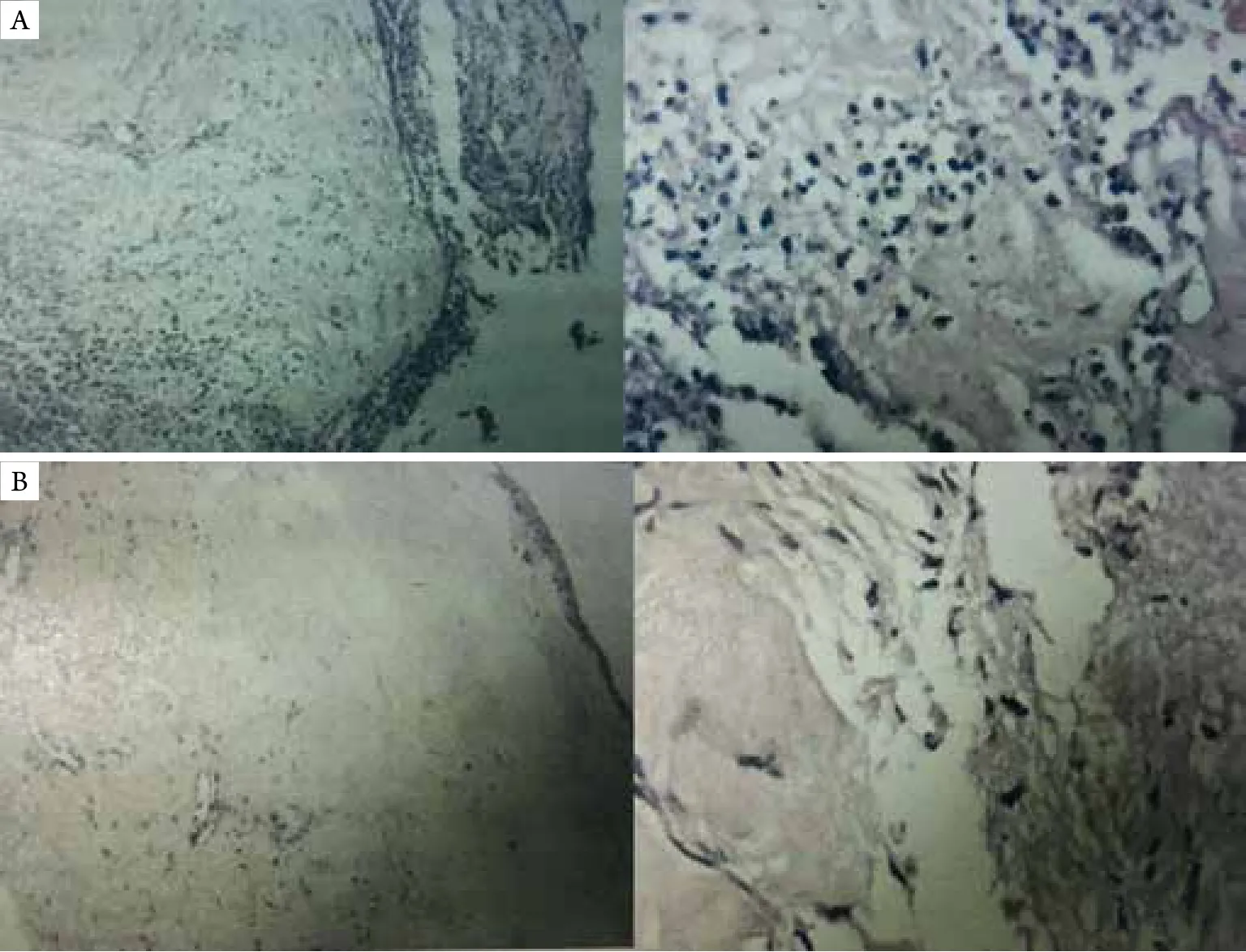
图4 术后角膜及滤过泡病理报告图像Figure 4 Pathological examination of cornea and follicles

图5 患者左手照片Figure 5 Photograph of the patient's left hand
2 讨论
感染性眼内炎是青光眼术后最严重的并发症之一。因滤过泡的存在而发生的眼部感染,称为滤过泡相关性眼部感染,分为滤过泡炎和滤过泡相关性眼内炎。后者根据发病时间分为急性眼内炎与慢性眼内炎或者迟发性眼内炎。前者发生于术后6周以内,后者则是术后6周以后,后者较为常见[3]。据报道,小梁切除术后迟发性眼内炎的发病时间为1个月~60年(平均3.1年)[4]。本例患者已行小梁切除术15年。青光眼滤过手术后滤过泡的囊壁是避免眼内组织受到病菌侵袭的重要屏障。如果囊壁较薄,特别是在受到轻微外伤的情况下,就有可能导致囊壁受到损伤发生渗漏,而渗漏的通道也就成为病原菌侵袭入眼的通道。本例患者年龄大,眼部卫生意识欠缺,经常揉眼睛;检查见滤过泡破裂,考虑揉眼后导致菲薄的滤过泡破裂。因此对于薄壁滤泡患者应嘱其避免眼部受伤、揉眼,注意眼部卫生。定期复诊,如果出现滤泡渗漏,一定要及时进行修补。
真菌性眼内炎为临床较为少见的感染性眼病。据报道青光眼术后滤过泡相关性眼内感染较内眼术后感染率高,0.4%~6.9%[5-6],其中主要为细菌,真菌所占比重较小。一项回顾性研究[7]报道:真菌在其观察的滤过术后眼内炎病原学中的构成比是2.57%。真菌性眼内炎致病菌种类主要为丝状真菌和酵母菌。常见丝状真菌有曲霉菌、镰刀菌、青霉菌等;酵母菌有白色念珠菌、隐球菌等。曲霉菌是报道的最常见的真菌,占白内障术后真菌性眼内炎病例的56%~74%[8],占创伤后真菌性眼内炎病例的4%~14%[9]。本例术后病理及培养的结果是镰刀霉菌。
在发病早期,真菌性眼内炎与其他无菌性眼内炎的症状难以鉴别。患者在出现眼红、眼痛后在当地医院先予以全身及局部激素抗炎数天,症状无改善后又予以全身抗感染治疗2 d,未行病原学检查。至南通大学附属医院虽然急诊行玻璃体切除并对玻璃体液进行培养,但是结果是未见明确病原菌。这可能是抗炎治疗和抗生素治疗的同时对房水、玻璃体标本进行病原菌培养阳性率较低的原因。对于青光眼滤过术后迟发性眼内炎主要采取玻璃体腔注药及玻璃体切除治疗。患者入住南通大学附属医院时考虑细菌性感染性眼内炎,急诊行右眼白内障超声乳化吸出+玻璃体切除+滤过泡修补术,术中玻璃体腔使用万古霉素灌洗,术中见玻璃体炎性混浊,视网膜未见明显浸润病灶,术后予以抗生素治疗。在缺乏明确病原菌检出及培养结果的情况下,我们联合使用多种抗生素,忽略了真菌感染的可能性。真菌性眼内炎早期临床常表现为虹膜睫状体炎或脉络膜视网膜炎,常因误诊为葡萄膜炎而延误治疗,导致真菌在眼内的扩散,使病情加重。因此,对于诊断为葡萄膜炎的患者,经激素正规治疗病情反而加重,出现前房积脓、玻璃体混浊时应考虑真菌感染的可能性。本例患者最初前部炎症反应明显、前房积脓,术中玻璃体炎性混浊,前部玻璃体较为明显,视网膜未见明显异常,考虑细菌感染,而术后角膜混浊,出现疑似内皮斑,足量抗生素治疗后无效,病情进展较快,此时才考虑到真菌感染可能性。
然而,医师仅凭眼内炎的临床表现是无法确定病原菌,需要实验室检查才能确诊。传统方法获得眼内液标本后,进行涂片染色显微镜下检查、微生物培养来获取准确的病原学信息。由于染色后显微镜下观察的阳性率低,以及培养的时间长,导致患者经常错过临床治疗的时机。眼内液聚合酶链式反应是早期快速诊断真菌性眼内炎的方法,而随后发展的多重聚合酶链式反应、DNA微阵列技术等为真菌早期、精准的诊断提供策略[2]。血浆(1-3)-β-D葡聚糖(G试验)是一种早期诊断深部真菌感染的快速、简便的方法,联合传统真菌培养可提高诊断的敏感度、特异度及诊断价值[10]。有研究[11]认为:泪液中(1-3)-β-D-葡聚糖水平的检测可用于真菌性角膜炎的早期诊断及病情变化监测。虽然目前国内用G实验来诊断真菌性眼内炎的报道较少,但是检测眼内液(1-3)-β-D-葡聚糖水平为真菌性眼内炎早期诊断提供检测策略。在本例报告中,我们只是采用传统方法,虽然急诊行玻璃体切除以及涂片,前房水及玻璃体液培养,但是未找到确凿的真菌感染的病原学证据。目前病原菌培养是诊断真菌眼内炎的“金标准”,但因真菌的培养用时较长,临床上不应过分依赖培养结果再采取治疗措施。因此在怀疑真菌性眼内炎时,不仅要及时行玻璃体切除术, 同时要采取上述真菌的检测方法,尽早明确诊断,及时行抗真菌药物治疗。
真菌性眼内炎可分为外源性与内源性两种。外源性眼内炎是由于手术后或外伤后的并发症,或由于玻璃体内注射的问题而发生的,而内源性眼内炎则由于病原体在眼内的血源性传播而发生,主要在于免疫功能受损的个体中。外源性真菌眼内炎早期表现主要局限于前房、虹膜睫状体及前部玻璃体病变,常见前房积脓和虹膜睫状体炎。内源性真菌性眼内炎常以视力减退为首发症状,黄斑和视网膜后极部最先见散在分布的黄白色渗出物,在视网膜下及玻璃体后界膜下形成半圆形的脓性液平面[2]。该患者15年前行双眼小梁手术,右眼滤过泡破裂;第1次术中见视网膜面无明显病灶。追问病史后发现患者有手足癣。有报道[12]显示:1名肝炎伴足癣眼内炎患者经培养后确诊为内源性真菌性眼内炎。内源性眼内炎患者中大约一半能找到全身系统性疾病,其中肝炎最常见。本例患者有手足癣病史,全身无系统性疾病,且滤过泡破裂,考虑右眼外源性眼内炎。
该患者是何时感染真菌的呢?笔者认为有两种可能性:第一,患者最初可能存在真菌感染,由于长期、联合应用多种抗生素,导致正常菌群平衡失调,直接或间接的损伤正常菌群的定植抵抗能力,削弱防御感染的生物屏障作用,有利于真菌生长,繁殖;第二,滤过泡修补术后、玻璃体术后出现真菌感染。患者系老年患者,结膜组织菲薄,滤过泡修补时发现已有部分结膜组织缺失。在滤过泡修补后和玻璃体切除术后,可能出现与内眼交通的腔隙。由于患者未注意手、眼卫生,而导致眼部继发真菌感染。因未及时找到患者眼部真菌感染依据,未使用抗真菌治疗,最终患者丧失视力。
综上,真菌性眼内炎临床表现不典型,对于初诊为葡萄膜炎或细菌性眼内炎的患者,长期规范性激素或抗生素治疗无效者应怀疑真菌性眼内炎的可能,应积极使用多种真菌检测方法,明确诊断并及时治疗,以免病情加重。需详细询问检查全身情况,特别是全身有真菌性疾病的情况下,需提高警惕。

