铬渣污染土壤PM10和PM2.5组分中六价铬的生物可给性及健康风险评估
李宁,夏天翔,刘增俊,张丹,姜昱聪
1.首都师范大学资源环境与旅游学院,北京 100048 2.北京市环境保护科学研究院,污染场地风险模拟与修复北京市重点实验室,北京 100037
铬作为一种典型的工业原料,其污染主要来源于工业生产。在长期的生产和应用中,铬的开采、冶炼以及铬盐的生产等产生的废水、废气和废渣对土壤环境产生了严重的污染。三价铬和六价铬是土壤中铬的主要存在形式,三价铬毒性小,不易迁移,对环境的危害作用小;而六价铬毒性较强,易在土壤中迁移,对环境有持久的危害性,且容易被人体吸收产生致癌效应,故评估土壤中六价铬的健康风险尤为重要。
土壤中的六价铬主要通过口部摄入、皮肤接触和呼吸途径进入人体。美国卫生和公众服务部、国际癌症研究机构已经研究证实了六价铬是人体致癌物质,呼吸吸入和口部摄入六价铬均会引起癌症。此外,由《污染场地风险评估技术导则》(HJ25.3—2014)[1](以下简称“HJ25.3—2014”)可知,六价铬的呼吸吸入致癌斜率因子(SFi=329)远大于经口摄入致癌斜率因子(SFo=0.5),二者相差658倍,而对于其他重金属如砷,其呼吸吸入致癌斜率因子(SFi=14.5)仅为经口摄入致癌斜率因子(SFo=1.5)的9.7倍,二者差异较小。这表明不同于其他重金属,相比于经口摄入而言,呼吸吸入可能是六价铬产生人体健康风险的重要途径。因此,评估六价铬经呼吸途径产生的健康风险是非常必要的。近年来,可吸入颗粒物PM10和PM2.5在人体内的生物可给性研究越来越多。Wiseman和Zereini[2]的研究表明,PM10、PM2.5及PM1中V、Pb、Cu、As和Sb在模拟肺液中的溶解度均达到80%;Silva等[3]对巴西里约热内卢城市PM10中重金属的可给性进行研究,得出其可给性范围为1.1%~93%;Hernándezpellón等[4]利用可给性结果对PM10中Cd的健康风险进行评估,得出其由呼吸途径产生的致癌风险高达1×10-6~1×10-4。这些研究结果均表明,呼吸途径会对人体产生很大的健康风险,故研究可吸入颗粒物中重金属在肺阶段的生物可给性并对其进行健康风险评估具有重要意义。然而,目前在进行人体健康风险评价时一般以土壤中污染物的总量为基准,但很多研究表明,重金属进入人体胃、肠及肺液后并不会被完全吸收,从而导致以污染物总量为基准的健康风险评估较为保守,容易造成场地的过度修复。因此,测定重金属在人体内的生物可给性(溶解于胃肠及肺液中的重金属含量与摄入土壤中重金属总量的比值),体外模拟人体消化和呼吸过程来测试能够溶解于胃、肠及肺液中的重金属含量,并以此为基准来对人体健康风险进行评价,能够降低风险评估的不确定性,部分克服现有方法过于保守的问题,对场地风险水平的管控具有重要的现实意义。
目前,重金属在消化系统中的可给性研究已经较为成熟并形成了统一的可给性测试方法(UBM);然而,重金属在肺阶段的可给性研究尚少,其在方法上未形成统一的标准,Guney等[5]研究了不同模拟液和不同提取时间下土壤PM20组分中重金属的生物可给性,表明相比肺模拟液(Gamble’s solution, GS)而言,利用人工溶酶体液(artificial lysosomal fluid, ALF)得到的可给性较高,且在提取时间为2周时达到最大;Julien等[6]还研究了固液比对可给性结果的影响,并表明GS较水溶液产生的可给性更高,且在提取时间为24 h、固液比在1/500~1/50 000范围内时可给性最大;此外,Kastury等[7]对不同搅拌方式对可给性结果的影响也进行了研究,结果表明,使用翻转振荡器(45 r·min-1)作为搅拌混合方式时,得到的可给性更高,并推荐使用模拟液为ALF溶液、固液比为1/5 000、提取时间为24 h,作为PM2.5呼吸途径可给性测试的标准参数。此外,大量研究也表明,土壤粒径的大小对重金属在人体内的行为和生物可给性也有着很大影响。研究表明,人体吸入土壤颗粒后,粒径>10 μm的颗粒主要附着在上呼吸道中,然后通过纤毛从肺部运出,而粒径<10 μm的颗粒会进入人体的支气管区域,尤其是粒径<4 μm的部分,一般会到达肺泡及深肺中,难以清除[8],故土壤细颗粒中的重金属会通过呼吸系统对人体健康产生很大影响。Sheppard等[9]的研究也表明,相比于粒径更大的颗粒,粒径<250 μm的土壤颗粒最容易粘附到儿童手上并被摄取,建议在摄入暴露中使用粒径<250 μm的土壤颗粒进行研究。
虽然重金属在人体内的可给性已经受到越来越多的关注,然而大多数研究主要集中在Cd、Pb、As和Zn等重金属上,对六价铬的研究鲜有报道,而且目前的研究大都集中于胃肠阶段,对重金属在肺阶段的可给性研究尚少。综上,本研究采集了西宁市某铬渣污染场地的8个土壤样品,并将其分为<250 μm、<10 μm及<2.5 μm这3种不同的粒径,旨在(1)分析不同土壤粒径中六价铬、总铬的浓度分布差异和特征;(2)依据土壤粒径大小对人体健康行为的影响,选取合适的粒径,通过UBM和呼吸吸入生物可给性测试方法(IBM)分别测定六价铬在消化和呼吸系统中的生物可给性;(3)以生物可给性浓度作为暴露浓度,对原有的健康风险评估方法进行优化,提高风险评估的可靠性;并通过对比摄入和呼吸途径产生的健康风险评估结果,评价六价铬对人体健康产生危害的主要途径。
1 材料与方法(Materials and methods)
1.1 供试土壤
由于表层土壤是人体口部摄入和呼吸途径的主要暴露部分,故为了使供试土壤样品具有较好的代表性,样品主要采集于西宁市某铬渣污染场地的表层土壤。将采集后的土壤样品置于实验室内风干、研磨,一部分样品过60目尼龙筛,获得粒径<250 μm的土壤样品;另一部分样品利用实验室内的颗粒物再悬浮检测系统,选用美国URG公司的PM2.5和PM10标准旋风式采样器,设置采样流量为16.7 L·min-1,空气动力学直径切割粒径分别为10 μm和2.5 μm,获得PM10和PM2.5的滤膜样品。
<250 μm的土壤颗粒是在手-口接触过程中最容易被摄入的部分,主要用于胃肠阶段生物可给性的测定及土壤理化参数的测定;而空气动力学直径<10 μm和<2.5 μm的土壤颗粒被人体吸入后会沉积到支气管、肺泡和深肺中,主要用于肺阶段生物可给性的测定。
供试土壤样品检测指标主要包括土壤的粒径组成、pH、有机质(OM)、六价铬及总铬含量,其中,粒径组成采用马尔文粒度分析仪测定;土壤pH采用电位法测定[10];OM采用重铬酸钾外加热法测定[10];PM250中的六价铬和总铬分别采用二苯碳酰二肼分光光度法及火焰原子吸收分光光度法测定[10];PM10和PM2.5中的六价铬和总铬采用国标GBZ/T160.7—2004中空气有毒物质的测定方法测定[11]。其中,粒径分析仪测定结果为各粒径的体积百分比,然而,由管孝艳等[12]的研究结果可知,当样品粘粒含量小于8%左右时,其均匀性最好,故可以假设不同粒径组分中其密度是相同的,从而测得的体积百分比即为各粒径的质量百分比。土壤基本理化参数检测结果如表1所示。
1.2 试剂与仪器
实验所用试剂均为分析纯,生物试剂购自Sigma奥利奇上海(贸易)有限公司,其余试剂购自中国国药有限公司。所用仪器及型号分别为:激光粒度分析仪(Mastersizer 2000,上海普迪生物技术有限公司,中国)、pH酸度计(FE28,梅特勒-托利多仪器(上海)有限公司,中国)、电热恒温油锅(DU-20,上海一恒科技有限公司,中国)、振荡翻转器(TCLP-12B,常州市金坛博科试验设备研究所,中国)、离心机(LD5-2A,北京京立离心机有限公司,中国)、原子吸收分光光度计(AA3510-4,上海精密仪器仪表有限公司,中国)。
1.3 实验方法
1.3.1 胃肠阶段生物可给性测试方法
胃肠阶段生物可给性测试主要采用国外最新研究的UBM方法,它是英国地质调查局联合7个国家于2005年制定的一种测试重金属在人体内可给性的国际标准方法,主要模拟了土壤中重金属在口腔、胃及肠3个阶段的释放过程。由于重金属在口腔中停留时间短,且唾液的pH值(6.5±0.5)接近中性,重金属释放量很少,故在研究中一般将土壤重金属在口腔中的释放过程忽略[13]。具体步骤如下[14]:
(1) 胃提取阶段 ①提取前一天提前配制好新鲜的胃、肠和胆汁液,配制方法参考Wragg等[15]所使用的方法,并在(37±2) ℃下提前预热2 h;②称取5 g土壤样品放入聚乙烯瓶中,加入112.5 mL胃液,摇匀,测定pH是否在1.1±0.2范围内,若不在,用10.0 mol·L-1NaOH或37% HCl进行调节;③将聚乙烯瓶放入翻转仪中翻转1 h,温度设置为(37±2) ℃,模拟胃肠的蠕动;④1 h后取出测定其pH是否在1.1±0.2范围内,否则重新实验;⑤取100 mL提取液在4 000 r·min-1下离心10 min,并用针式过滤器(孔径0.45 μm)对离心后的上清液进行过滤,然后滴加1~2滴1%的硝酸保护,并储存在4 ℃以下用于胃阶段六价铬可给性浓度的测定。
(2) 肠提取阶段 在④的基础上加入225 mL肠液和75 mL胆汁液,摇匀,调节pH至6.3±0.5范围内;将聚乙烯瓶放入翻转仪中翻转4 h取出,测定其pH是否在6.3±0.5范围内,否则重新实验;取100 mL提取液在4 000 r·min-1下离心10 min,并用针式过滤器(孔径0.45 μm)对离心后的上清液进行过滤,然后滴加1~2滴1%的硝酸保护,并储存在4 ℃以下用于肠阶段六价铬可给性浓度的测定。
1.3.2 肺阶段生物可给性测试方法
肺阶段生物可给性测试主要参考Broadway等[14]在对格拉斯哥铬污染土壤生物可给性测试中所用的方法,所用溶液为GS。GS是目前被广泛认可的一种体外测试方法,它代表了深肺的细胞外环境[5],而且利用这种方法得到的生物可给性被证明和体内实验有很好的一致性[16]。具体步骤为:①提前一天配制好新鲜的肺液,配制方法参考Wragg和Klinck[17]所用的方法,并在(37±2) ℃下提前预热2 h;②将制备好的滤膜用不锈钢剪刀剪碎,放在30 mL的聚乙烯瓶中,加入20 mL肺液;③把聚乙烯瓶放在翻转仪中翻转24 h,温度保持在(37±2) ℃,取出;④取20 mL提取液在4 000 r·min-1下离心10 min,然后滴加1~2滴1%的硝酸保护,并储存在4 ℃以下用于肺阶段六价铬可给性浓度的测定。
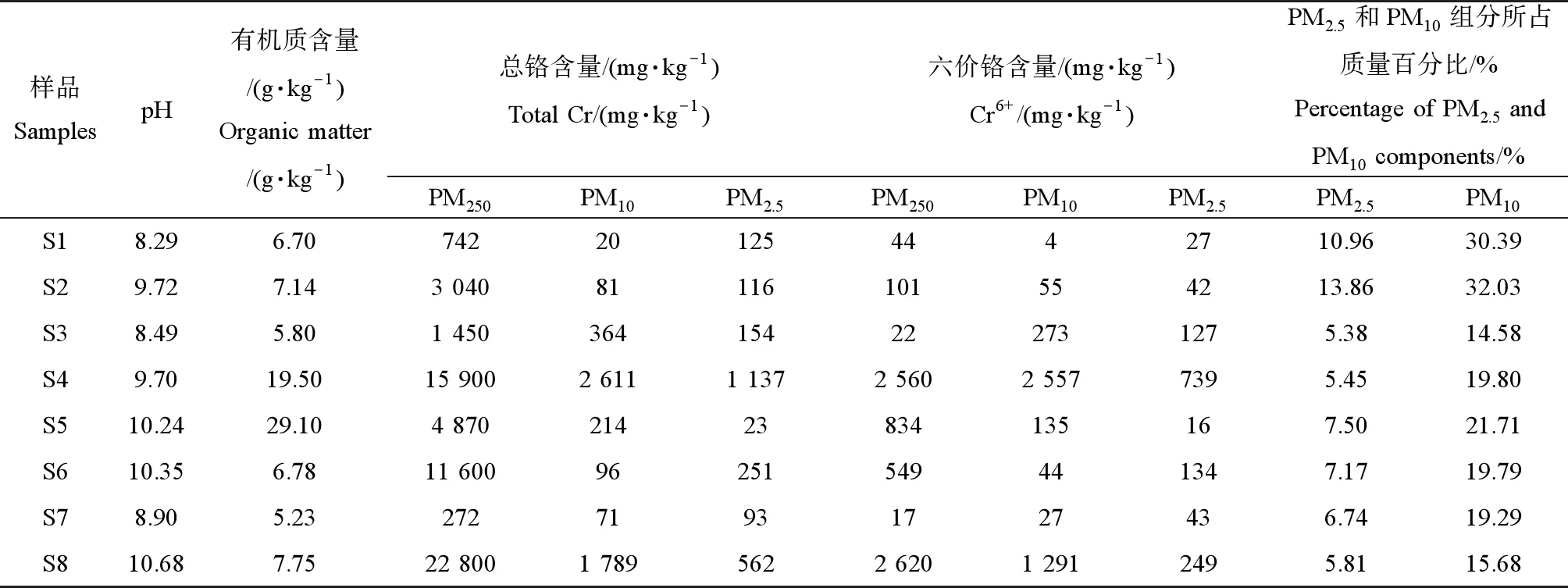
表1 土壤理化参数Table 1 Physical and chemical parameters in soils
1.3.3 生物可给性计算
六价铬在胃、肠和肺阶段的可给性浓度和可给性计算公式如下[13]:
(1)
(2)
(3)
(4)
(5)
(6)
式中:Cgb为土壤中Cr6+在模拟胃阶段的人体可给性浓度(mg·kg-1);Cgib为土壤中Cr6+在模拟肠阶段的人体可给性浓度(mg·kg-1);Clb为土壤中Cr6+在模拟肺阶段的人体可给性浓度(mg·kg-1);Cs为供试土壤中Cr6+的总浓度(mg·kg-1);C(Cr6+)g为模拟胃液中Cr6+的浓度(mg·L-1);vg为测试过程中模拟胃液的体积(L);m为可给性测试过程中土壤的质量(mg);C(Cr6+)gi为模拟肠液中Cr6+的浓度(mg·L-1);vgi为测试过程中模拟肠液的体积(L);C(Cr6+)l为模拟肺液中Cr6+的浓度(mg·L-1);vl为测试过程中模拟肺液的体积(L);Biog为胃阶段Cr6+的人体可给性,无量纲;Biogi为肠阶段Cr6+的人体可给性,无量纲;Biol为肺阶段Cr6+的人体可给性,无量纲。
2 结果与讨论(Results and discussions)
2.1 不同土壤粒径中六价铬和总铬的浓度分布特征
为了表明不同粒径中六价铬和总铬的浓度分布规律,利用累积因子(accumulation factors, AF)AF来对重金属的富集程度进行描述。其计算公式如下[18]:
(7)
式中:Xfraction和Xbulk分别代表不同粒径组分中重金属的浓度及原土中重金属的浓度。
由表1可知,六价铬和总铬在PM10和PM2.5组分中的含量大多明显低于PM250组分(除样品S3、S7外)。且经计算得到,PM10组分中六价铬和总铬的AF分别为0.080~12.297和0.008~0.261,PM2.5组分中六价铬和总铬的AF分别为0.019~5.721和0.005~0.342(图1),较低的OM含量可能是导致样品S3和S7六价铬AF较大的主要原因。相似的结果在已有的研究中也被发现,李恋卿等[19]通过分馏系数指示重金属在土壤颗粒中的分布差异,发现铬在土壤中主要赋存于较粗的团聚体颗粒中;Ajmone-Marsan等[20]调查了5个欧洲城市中重金属的分布,发现在TOR(Torino)和GLA(Glasgow)这2个城市中铬在细颗粒及粗颗粒中的比例分别<20%和<45%,在AVE(Aveiro)、SEV(Sevilla)和LJU(Ljubljana)这3个城市中所占的比例分别为41%~59%和53%~66%,即均呈现出向粗颗粒聚集的趋势;Gong等[21]的研究也表明,相比于细颗粒,铬在粗颗粒中的浓度更高,这表明由于各种复杂的因素,如重金属可能会嵌入到粗颗粒的微团聚体中而被粗颗粒优先吸附等,导致重金属不仅仅倾向于在细颗粒中聚集,也有可能在粗颗粒中聚集。此外,由图1可知,PM10和PM2.5组分中六价铬的AF均大于总铬,表明相比于总铬而言,六价铬在细颗粒中的累积程度更高。
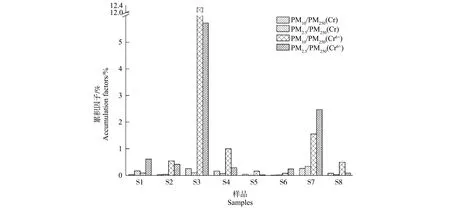
图1 总铬和六价铬在PM2.5和PM10组分中的累积因子Fig. 1 Accumulation factors of total Cr and Cr6+ in PM2.5 and PM10 fractions
在样品S3、S7中,六价铬的AF均大于1,这可能与其较低的OM含量有关。由图2中OM与六价铬的拟合结果可知,随着OM的增加,六价铬整体表现为先增加后减小的趋势,这可能是由于土壤OM中的胶体带有大量负电荷,随着含量的增加,其对六价铬的吸附能力越来越强,六价铬浓度越来越高;但当OM含量过高时,较高的OM含量又促进了部分六价铬的还原作用,导致六价铬含量又逐渐降低。对于样品S3和S7,其OM含量较低,分别为5.80 g·kg-1和5.23 g·kg-1),对六价铬的吸附能力较弱,故此时PM250组分中六价铬的含量较低,从而使得AF相对较高。

图2 PM250组分中有机质与六价铬含量的拟合关系Fig. 2 The relationship between organic matter and Cr6+ in PM250 component
然而,不同粒径中六价铬与总铬的比例关系表现出了不同的规律性。由图3可知,在粒径<250 μm、<10 μm及<2.5 μm的土壤颗粒中,六价铬占总铬的比例分别为2%~17%、21%~98%及22%~82%,表明相对于粗颗粒而言,细颗粒中的铬更多地以六价铬的形式存在。而六价铬作为铬中毒性最强的一种形态富集在细颗粒中,极易受到自然或人为因素的作用进入到大气中,具有较强的转移能力;此外,转移到大气中的细颗粒极易通过呼吸道侵入人体并沉积在肺泡中,有很强的致癌作用。因此,细颗粒中的六价铬存在很大的环境和健康风险,由呼吸吸入的六价铬应该作为六价铬健康风险评估的一个重要方面。
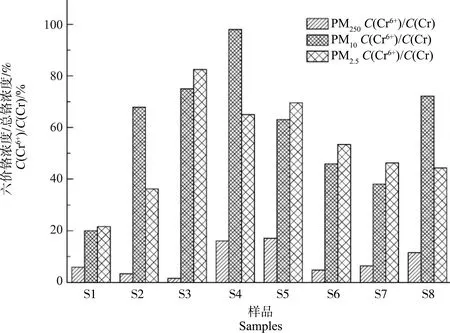
图3 不同粒径中六价铬占总铬的比例Fig. 3 Percentage of Cr6+ to total Cr in different particle size fractions
2.2 供试土壤中六价铬的生物可给性
2.2.1 六价铬经口摄入的生物可给性
供试土壤样品在胃肠阶段的可给性浓度和可给性如表2所示。由表2可知,六价铬在胃肠阶段的可给性浓度均小于供试土壤样品中六价铬的总浓度,这表明进入人体消化系统中的六价铬,即使是在酸性很强的胃环境中也不可能完全溶解,并进入到人体的血液循环中对人体健康产生威胁,因此,测试重金属的生物可给性,并以此为基础对人体健康风险进行评价是非常必要的。供试土壤中的六价铬在不同阶段的生物可给性差异较大,其中,胃阶段为0.0301%~0.9483%,平均值为0.4821%;肠阶段为0.0018%~0.3934%,平均值0.1578%,约为胃阶段的0.33倍。由此可见,六价铬在胃肠阶段的生物可给性均极低,这主要是由于在UBM提取过程中,由于胃液的强酸性环境及土壤中的有机质含量共同构成了良好的氧化还原条件,导致六价铬在进入小肠之前被大量的还原为三价铬[22],而且,由于三价铬氧化为六价铬的动力学非常缓慢,土壤中很少存在三价铬向六价铬的转化[23],从而导致了六价铬在胃中的生物可给性整体表现极低。然而,Yu等[24]在对铬矿物残渣的研究中发现,六价铬在胃肠阶段具有较高的生物可给性,分别为53.8%和42.9%,这主要是由于铬矿物残渣中有机组分含量较低所致,当向其中加入牛奶、面团等有机组分较高的物质时,较低的pH环境和较高的有机质组分促使了六价铬的大量还原,生物可给性降低了1个数量级,可给性结果与本研究结果相似。另外,Yu等[24]的研究也表明,由于pH的升高,铬在形成的原位铁氧化物上大量吸附,并与铁形成共沉淀,导致其在肠阶段的可给性比胃阶段更低。

表2 胃肠阶段可给性浓度和可给性测试结果Table 2 Bioaccessible concentrations and bioaccessibility in stomach and intestine
虽然在低pH及高有机质含量的情况下,六价铬的还原作用导致其在胃肠阶段的生物可给性极低,然而,在某些重污染场地,如果六价铬的含量远远超过了胃阶段的还原能力,则高浓度的六价铬仍可穿过胃粘膜导致胃肠系统的大量吸收,从而存在潜在的健康危害[25]。由于六价铬在吸收过程中存在着形态的转变,故对As、Pb和Cd等重金属得出的生物可给性结论并不能完全适用于六价铬,对六价铬的健康影响还应该进行更深入的研究。
2.2.2 六价铬经呼吸吸入的生物可给性
供试土壤样品在肺阶段的可给性浓度和可给性如表3和表4所示。由表可知,PM10和PM2.5组分中的六价铬在肺阶段的生物可给性分别为2.52%~41.50%和2.40%~88.12%,平均值分别为14.47%和48.86%。总体表现为由PM2.5的可给性显著高于PM10,平均约为PM10的3.38倍。这主要是因为粒径较小的颗粒的比表面积较大,与体液接触较为充分,六价铬的吸收量也更高,从而导致了PM2.5较高的生物可给性。故相比于粒径较大的颗粒而言,粒径较小的颗粒更容易溶解并被有效地吸收。而且相关研究也表明,颗粒越细,越容易沉积到深肺中难以清除,因此,细颗粒中六价铬的吸入可能对人体的呼吸道疾病产生严重的影响。目前,肺阶段生物可给性研究较少,尚未形成统一的测试方法,本研究所用方法主要参考Broadway等[14]在对铬与六价铬的研究中所用的方法,该研究所用土壤样品为PM10颗粒,得到的可给性约为7.8%和14.4%,与本实验结果较为一致,故利用该方法来测定六价铬的可给性较为可行。
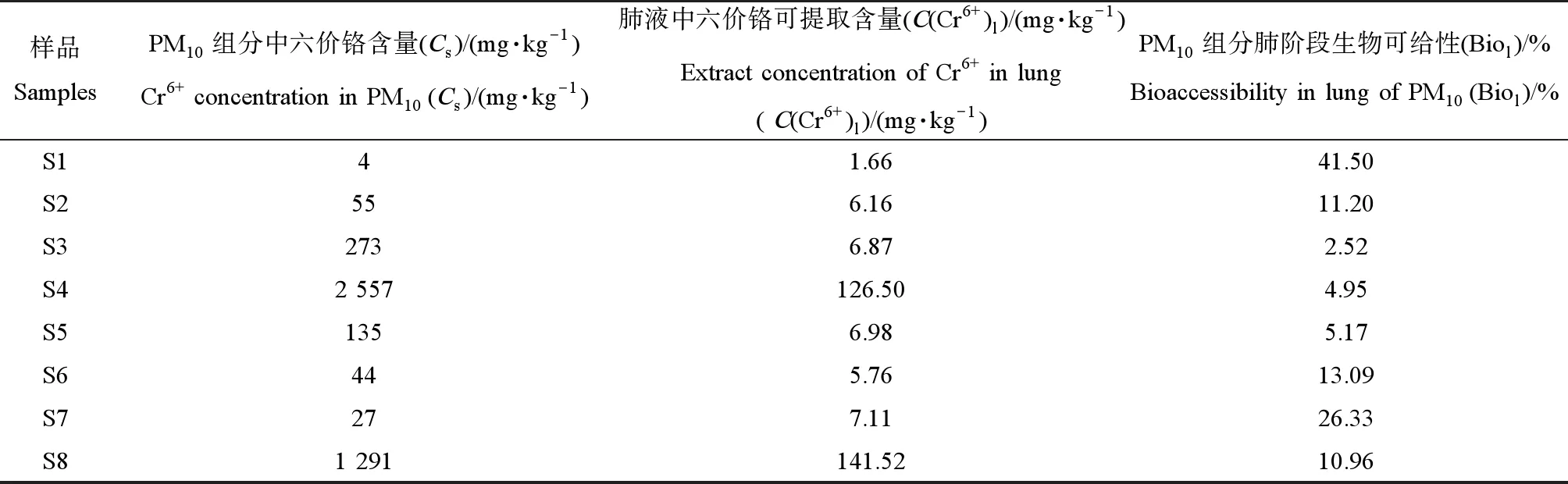
表3 PM10组分肺阶段可给性浓度和可给性测试结果Table 3 Bioaccessible concentrations and bioaccessibility of PM10 component in lung

表4 PM2.5组分肺阶段可给性浓度和可给性测试结果Table 4 Bioaccessible concentrations and bioaccessibility of PM2.5 component in lung
总体来看,六价铬在各提取阶段的可给性浓度与供试土壤样品中总的六价铬浓度并无相关性,如样品S4在PM2.5中具有最高的六价铬浓度,然而它在肺中的生物可给性最低,仅为2.40%,故具有较高总元素浓度的样品并不一定具有很高的生物可给性,这主要是由于不同土壤样品中六价铬存在的形态比例不同,从而直接影响了重金属在人体中的转化及毒性。另外,颗粒比表面积、有机质含量等参数也会对重金属的溶解度产生影响。因此,只有当土壤中重金属含量较高,且同时具有很高的生物可给性时,才会对人体健康造成很大的危害。
2.3 六价铬生物可给性对人体健康风险评估的影响
分别以土壤中六价铬的人体可给性浓度及总六价铬浓度作为暴露浓度,按照“HJ25.3—2014”[1],计算经口摄入土壤和吸入土壤颗粒物这2种暴露途径下六价铬的致癌风险,并对其差异进行分析。
(1)经口摄入土壤中单一污染物的致癌风险,采用下式计算:
CRois=OISERca×Csur×SFo
(8)
式中:CRois表示经口摄入土壤而导致暴露于单一污染物的致癌风险,无量纲;Csur为土壤中污染物的浓度,mg·kg-1;SFo为经口摄入致癌斜率因子,(mg·kg-1·d-1)-1,取值0.5;OISERca表示经口摄入土壤暴露量,kg·(kg·d)-1,其计算公式见“HJ 25.3—2014”附录A中的公式(A.1)。
(2)吸入土壤颗粒物中单一污染物的致癌风险,采用下式计算:
CRpis=PISERca×Csur×SFi
(9)
式中:CRpis表示吸入土壤颗粒物而导致暴露于单一污染物的致癌风险,无量纲;Csur为土壤中污染物的浓度,mg·kg-1;SFi为呼吸吸入致癌斜率因子,(mg·kg-1·d-1)-1,其计算公式见“HJ 25.3—2014”附录B中的公式(B.1);PISERca表示吸入土壤颗粒物的土壤暴露量,kg·(kg·d)-1,其计算公式见“HJ 25.3—2014”附录A中的公式(A.7)。
在考虑六价铬生物可给性的条件下,对不同样品的健康风险进行计算,计算结果如表5所示。由表5可知,在考虑生物可给性因素前后,六价铬产生的人体总致癌风险分别为47.44×10-6~10 255.08×10-6和5.52×10-6~476.85×10-6,平均值分别为2 430.04×10-6和125.83×10-6,二者差异显著。而且,在考虑生物可给性条件下,呼吸途径产生的健康风险极高,是经口摄入的5.04~176.38倍(胃)、10.92~10 198.00倍(肠),最高相差2个数量级。可见,相比于经口摄入,六价铬对人体的健康危害主要是通过呼吸途径产生的。且如果仅以土壤中总的六价铬浓度作为暴露浓度来进行风险评价,将使结果过于保守。而以人体胃肠及肺液中的可给性浓度作为暴露浓度来计算,能够使健康风险评价的结果更为客观。尤其是对六价铬经口摄入的暴露风险评估来讲影响最为显著,在未考虑可给性浓度的条件下,8个采样点风险值均远远高于致癌水平10-6,而在考虑可给性浓度的条件下进行筛选,仅S4、S5、S6和S8这4个点的风险值略高于可接受风险致癌水平10-6,这主要是六价铬在胃液中的强还原作用导致的。与本研究结果相似,许多研究都把六价铬的还原这一现象作为证据来表明六价铬经口摄入的暴露途径并不会对人体健康产生风险[26],但是在污染严重的铬污染场地,六价铬对人体产生的健康风险仍然不能被忽视。
Broadway等[14]在对铬污染土壤可给性的研究中发现,居住用地条件下铬的土壤环境质量指导值(Soil Guideline Values, SGV)为200 mg·kg-1,而在考虑可给性因素下得到的SGV范围为850~31 600 mg·kg-1,风险水平显著降低。因此,生物可给性作为一个调控场地风险的重要指标,提高了潜在暴露风险评估的精确度,为后期污染场地的风险管理提供了更为科学的依据。
综上,(1)不同粒径中六价铬和总铬的浓度分布存在差异,故依据颗粒大小对人体健康行为的影响作用,选取合适的粒径组分进行人体不同系统的健康风险评估是非常必要的。(2)基于生理的体外模拟实验有效地模拟了PM250、PM10和PM2.5中六价铬在胃肠及肺阶段的生物可给性,结果表明,在消化系统中,PM250在胃阶段产生的可给性较肠阶段更高;在呼吸系统中,PM2.5产生的可给性较PM10更高。(3)人体健康风险评估结果表明,以可给性浓度作为暴露浓度计算得到的健康风险远低于以污染物总浓度作为暴露浓度得到的健康风险,且由呼吸途径产生的健康风险远高于消化系统。相对于经口摄入途径而言,呼吸吸入是六价铬产生致癌风险的主要暴露途径。因此,土壤PM10和PM2.5组分作为呼吸途径的主要颗粒物来源,对人体健康风险评估结果有着显著的影响。评估PM10和PM2.5中六价铬在人体内的生物可给性,并利用该指标对人体健康风险进行评价,对场地的风险管控具有重要意义。

表5 考虑Cr6+人体可给性前后土壤的健康风险值(数量级:10-6)Table 5 The health risk value before and after considering bioaccessibility of Cr6+(Magnitude: 10-6)
注:根据“HJ 25.3—2014”,此处呼吸途径致癌风险是基于PM10组分计算的;总致癌风险为口部摄入和呼吸吸入途径致癌风险之和,皮肤接触途径致癌风险由于缺乏皮肤吸收因子(ABSd)参数,无法计算。
Note: According to “HJ 25.3—2014”, the risk of cancer caused by respiratory pathways is calculated based on PM10. The carcinogenic risk is the sum of the risk of oral intake and respiratory inhalation pathway carcinogenesis. Carcinogenic risk of skin contact cannot be calculated due to lack of dermal absorption factor (ABSd) parameters.
致谢:感谢北京市环境保护科学研究院黄玉虎研究员在细颗粒样品制备中给予的帮助。

