木质素基重捕剂处理含砷酸性废水研究
耿 静
(呼伦贝尔职业技术学院,内蒙古呼伦贝尔021000)
随着科学技术的进步,中国的工业有了长足的发展,但是随之出现的水体重金属污染问题愈发严峻。矿业冶炼、电镀、农药、医药、涂料等工业废水中含有大量金属离子,其在微量情况下即表现出较大的生物毒性,难以自然降解,可通过食物链传递富集,其引发的生态危害极大,国家对重金属废水的排放有严格的控制标准。废水中的重金属离子根据去除原理不同[1],分为化学法(沉淀、还原、电化学等)、物理法(吸附、分离、离子交换等)、生物法(生物絮凝、吸收、富集等),其中化学沉淀法应用最为广泛,即向重金属废水中加入碱性药剂[NaOH或Ca(OH)2]使废水中的重金属以氢氧化物沉淀的形式从废水中析出[2-3]。
含重金属离子的酸性工业废水常规处理工艺:向废水中加入足量石灰,中和废水中的酸并沉淀出大部分重金属离子,剩余重金属离子经重捕剂螯合絮凝处理后达到排放标准,过程中会产生大量含重金属的沉淀泥,固废处理成本较高,废酸难以回用。笔者以碱木质素为基体制备二硫代氨基甲酸型(DTC)重金属捕集剂[4],可在酸性条件下螯合重金属经絮凝生成沉淀,处理后酸性水可回用;对重捕剂加入量、反应时间、溶液pH、絮凝剂投加量等因素进行分析,得到最佳螯合工艺,为碱木质素型重捕剂的工业化应用提供可靠的数据参考。
1 实验部分
1.1 原料、试剂与仪器
原料:酸性废水取自石家庄某制药厂药物提纯工段。废水pH为1~2,硫酸质量分数为2.5%~5.0%,主要成分见表1。处理要求:废水酸度不变,处理后ρ(总砷)<0.5mg/L、ρ[Cd(Ⅱ)]<0.1mg/L、ρ[Cu(Ⅱ)]<5.0mg/L,处理后的酸性水(H2SO4)进入系统循环使用。

表1 酸性废水成分分析 mg/L
试剂:碱木质素(工业品);NaOH、己二胺、CS2、HNO3均为分析纯;乙醇(工业级,纯度为99.5%);聚丙烯酰胺(阴离子型 PAM);As、Cd、Cr、Cu、Hg、Pb 混合标准物质(100 mg/L);实验所用去离子水均为超纯水(实验室自制)。
仪器:HK-2000 型 ICP-AES 光谱仪(ICP)。
1.2 DTC型重捕剂合成与表征
1.2.1 Lig-DTC合成
将8.5 g碱木质素溶于适量水中,用0.5 mol/L NaOH溶液调节水相pH至10~12,充分搅拌使木质素溶于水中,过滤除杂,收集滤液[5]。碱性滤液移入500 mL三口烧瓶中,开启磁力搅拌及冷凝循环水,升温至85℃。用两组恒压滴液漏斗分别滴入己二胺(HMDA)12.2 mL、质量分数为37%的甲醛(HCHO)水溶液10.5 mL,滴加完毕后升温至95℃,反应持续4.0 h。停止加热,将反应液冷却至室温,用恒压滴液漏斗逐滴加入CS29 mL,反应1.5 h。反应结束后抽滤,滤饼用去离子水洗涤至中性,乙醇洗涤2~3次,25℃真空干燥12 h,得到浅黄色固体粉末,即为木质素基二硫代氨基甲酸盐(Lig-DTC)。加入的HCHO、CS2、HMDA 物质的量比为 1.4∶1.5∶1,产率为 72.4%。
1.2.2 Lig-DTC红外光谱分析
待测样品与KBr干燥后混合、研磨、压片,待测样与KBr质量比为1∶50,采用IR-960型红外光谱仪(FT-IR)分析待测样品官能团构型。
1.2.3 Lig-DTC扫描电镜分析
碱木质素和Lig-DTC经红外烘箱干燥、磨粉、制样、表面喷金处理,通过Phenom Pro扫描电镜(SEM)观测样品表面的微观形貌。
1.3 Lig-DTC重捕剂去除废水重金属实验
1.3.1 Lig-DTC合成与吸附重金属原理
重金属螯合作用的官能团在酸性条件下易分解,无法有效去除重金属离子,因此大部分重捕剂需在碱性或接近中性条件下使用。废酸若循环利用,去除重金属离子工艺不能采用调碱+重捕剂,而木质素型重捕剂可在酸性条件下螯合重金属离子。
Lig-DTC合成可分解为Mannich反应及CS2加成反应。Mannich反应:1)甲醛在α-H位与HMDA(伯胺)发生加成反应;2)HMDA端位胺甲基化中间体取代碱木质素C5位的α-H,生成木质素胺(Mannich碱)。CS2加成反应:在碱性条件下,CS2与木质素引入的支链端位胺发生加成反应,生成木质素基二硫代氨基甲酸钠己二胺盐。反应历程:
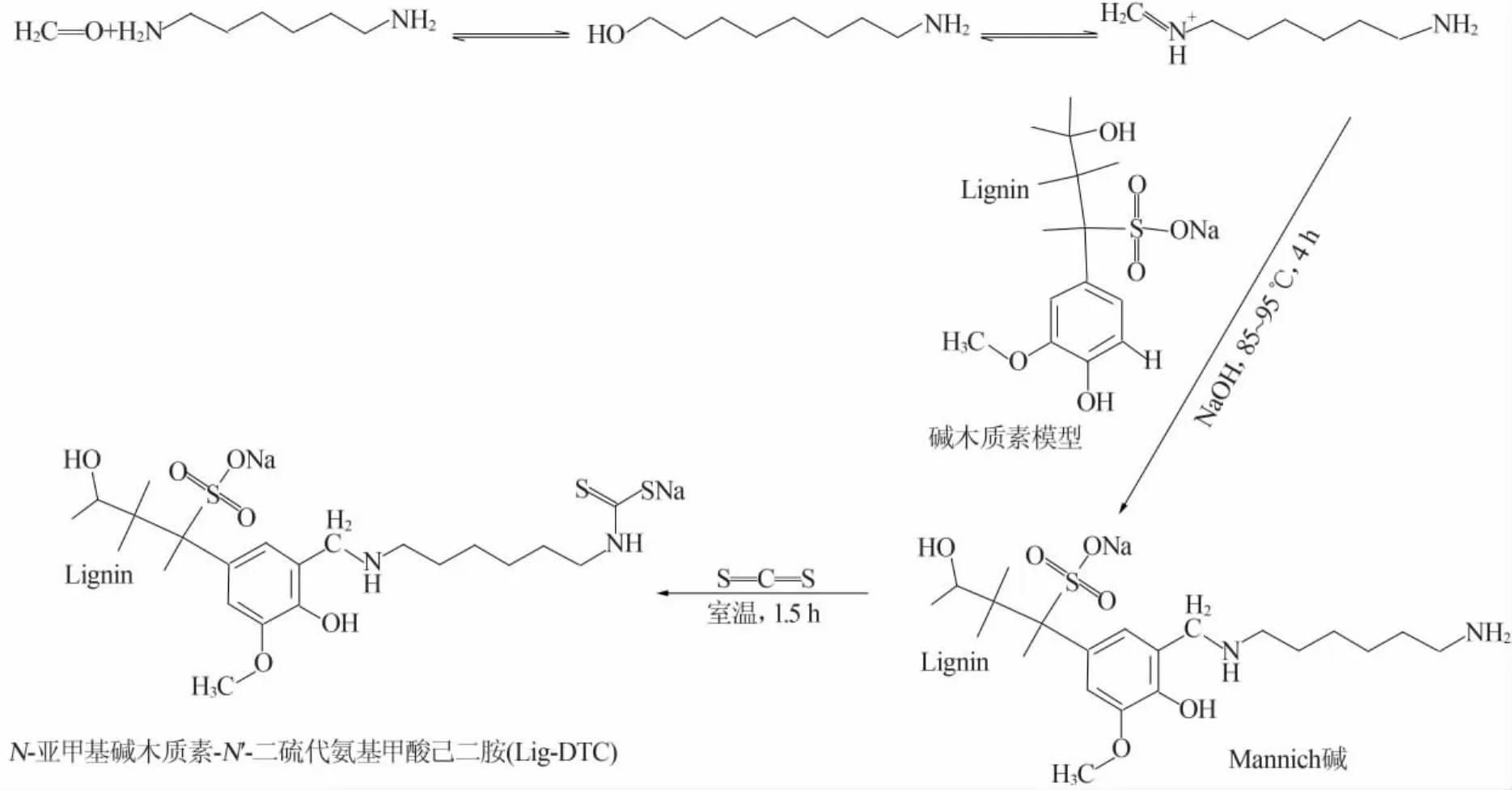
Lig-DTC含有N、S等配位原子,根据配位场理论,具有3组孤对电子的S能够占据重金属离子的空轨道,形成不溶于水的立体交联构型螯合物。DTC型重捕剂螯合重金属离子过程:
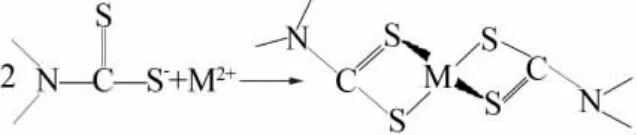
二硫代氨基甲酸基团在酸性条件下易分解生成CS2和胺盐,降低重金属离子的螯合效果。而以木质素为基体,其电子云流动性较大,质子不易靠近N原子,官能团碱性降低,在酸性条件下不易分解,具有一定的稳定性。
1.3.2 正交实验
在前期因素-水平筛选探索实验基础上,对重捕剂加入量、反应时间、废水pH、PAM加入量(质量分数为0.1%)等因素进行正交实验。正交表选择L9(34),正交实验因素和水平见表 2。

表2 正交实验因素及水平
1.3.3 实验方法
取100mL含重金属废水置于250mL锥形瓶中,采用 H2SO4溶液(0.5 mol/L)或 NaOH 溶液(0.5 mol/L)调节废水pH,根据表 2条件加入Lig-DTC,室温下搅拌反应一定时间,加入PAM高速搅拌30 s后静置30 min。反应液经中速滤纸过滤,收集滤液过0.45 μm水性滤膜,采用ICP测定重金属离子质量浓度 ρ1(M)(单位为 mg/L),滤渣经干燥称其质量。
1.4 金属离子测定
1.4.1 ICP工作条件
ICP工作条件:蠕动泵转速为90 r/min,反射功率为5 W,入射功率为1 150 W,氩气冷却气流量为15 L/min,氩气载气流量为0.5 L/min。分析线波长[6]:As,193.70 nm;Hg,253.65 nm;Cr,267.72 nm;Cu,327.39 nm;Cd,214.44 nm;Pb,220.35 nm。
1.4.2 混合标准溶液配制
用 移 液 枪 从 As、Cd、Cr、Cu、Hg、Pb 混 合 标 准物 质 中 分 别 移 取 0、100、500、1 000、1 500 μL,用1.0 mol/L的HNO3定容至100 mL,通过ICP测定标准物质在不同质量浓度下的吸光度A,绘制标准工作曲线。
2 结果与讨论
2.1 Lig-DTC合成与表征
2.1.1 Lig-DTC制备原料加入量确定
研究发现,化学合成的DTC型重捕剂具有一定的生态毒性,且难以自然降解。而以天然高分子(纤维素、淀粉、壳聚糖等)为基体引入二硫代氨基基团合成的新型DTC类重捕剂,其原料来源广泛、制备成本较低、易于自然降解。木质素也属于天然高分子,未经改性的木质素对重金属吸附量较低[7]。以麦草氧碱制浆黑液中提取的碱木质素为基体制备木质素型DTC重捕剂,即可以利用制浆副产物,还能有效处理重金属污染问题,符合绿色化学的可持续发展理念。
木质素提取方式不同,其分子量也有明显差异。木材中的天然木质素相对分子质量在10 000以上,而从麦草氧碱制浆黑液中提取的碱木质素相对分子质量为700~1 500。制备Lig-DTC原料中HMDA造价较高,将HMDA化学计量定为1;甲醛、CS2沸点较低,易挥发,实际添加量与理论用量有一定差异,但从环保角度考虑二者不宜添加过量。固定碱木质素和HDMA用量,调整甲醛及CS2用量,Lig-DTC产率见表3。由表3看出,Lig-DTC产率随甲醛、CS2用量增加而增长。甲醛与CS2在理论用量时产率最低(45.3%),n(甲醛)∶n(CS2)∶n(HDMA)=1.4∶1.5∶1时产率达到71.3%,之后用量增加产率涨幅较小。故在碱木质素用量为8.5 g、HDMA用量为12.2 mL时,甲醛、CS2、HDMA最佳物质的量比为1.4∶1.5∶1。
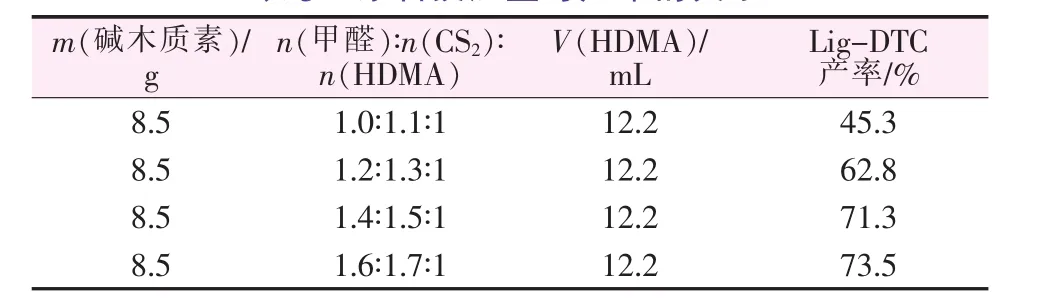
表3 原料投加量与产率的关系
2.1.2 Lig-DTC红外光谱表征
图1为碱木质素、Lig-DTC红外光谱图。从图1看出,1 060~3 420 cm-1处出现的特征吸收峰主要是碱木质素苯环、—OH、—COCH3等官能团的红外特征吸收峰;3420~3445cm-1处为氢键缔合O—H伸缩振动峰;2 920~2 930 cm-1处为 CH3、CH2、CH 的C—H伸缩振动峰;1 630~1 650 cm-1处为侧链α、β碳原子间共轭双键结合的吸收(木素)峰;1150~1170cm-1处为C—O—C不对称“桥伸展振动”(碳水化合物)峰;1 060~1 070 cm-1处为C=O伸展振动(碳水化合物)峰。880~1 375 cm-1处出现的特征吸收峰主要是二硫代氨基甲酸官能团的红外吸收峰;1 325~1 375 cm-1处为 N—CS2伸缩振动吸收峰;1 100~1 120 cm-1处为C=S伸缩振动吸收峰;1 050~1 070 cm-1处为C—N伸缩振动吸收峰;880~900 cm-1处为C—S伸缩振动吸收峰。由此可知二硫代氨基基团已经成功接枝在碱木质素上。
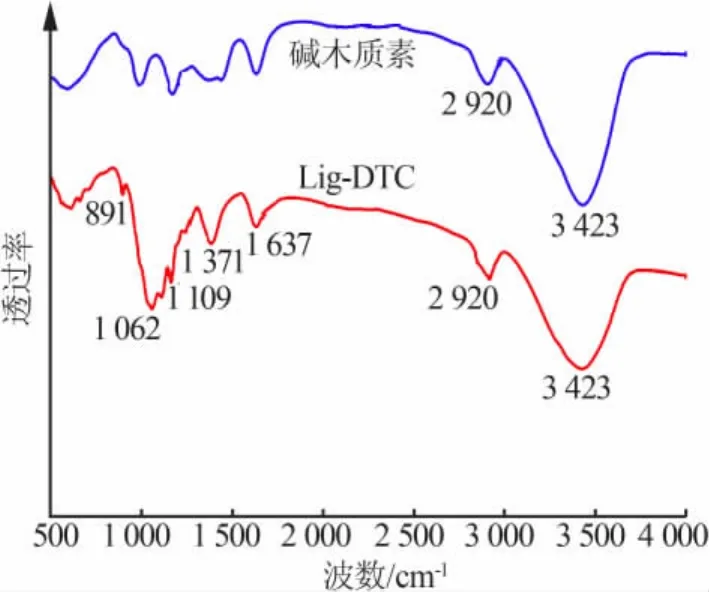
图1 碱木质素、Lig-DTC红外光谱图
2.1.3 Lig-DTC的SEM表征
碱木质素与Lig-DTC扫描电镜照片见图2。高分子木质素微观形貌是网状结构,改性后碱木质素表面较为有序平整,其分散程度也优于未改性的,这种分散均匀的网状结构利于螯合重金属离子。
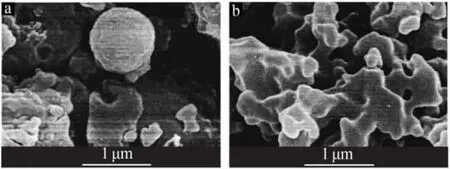
图2 碱木质素(a)与 Lig-DTC(b)的 SEM 照片
2.2 Lig-DTC处理重金属废水研究
2.2.1 正交实验
以废水中剩余重金属离子质量浓度为评价指标,对重捕剂加入量、反应时间、废水pH、PAM加入量(质量分数为0.1%)等因素进行评价,经极差分析得到最佳工艺配方组合,相关数据见表4。
针对多评价指标筛选最佳实验组合,可采用综合平衡法进行分析,相关数据见表5。Lig-DTC添加量(A)对各指标的影响:从As、Cd剩余质量浓度分析A极差最大,以A3水平效果最佳;从Cu剩余质量浓度的极差可知,Lig-DTC添加量以A2水平效果最佳,但重捕剂添加量不是Cu剩余质量浓度的最显著影响因素,综合分析Lig-DTC添加量优选50 mg。反应时间(B)对各指标的影响:反应时间对3组评价指标的极差均不是最大值,属于次要因素;以As指标来看B2(10min)水平为最优,从 Cu、Cd 指标来看B3(15 min)最佳;针对次要因素,反应时间可选择15 min。废水pH(C)对各指标的影响:对于Cu,废水pH是对指标影响最大的因素,C2(pH=2)水平最好;对于Cd,该因素属于第三位的次要影响因素,因此废水pH可选择pH=2。PAM加入量(D)对各指标的影响:PAM加入量与反应时间对各指标的影响趋势类似,极差均非最大值,综合考虑PAM加入量选择1.1 mL。综上所述,经正交实验得到的最佳组合:Lig-DTC加入量50 mg,反应时间为15 min,废水pH=2,PAM加入量1.1 mL。
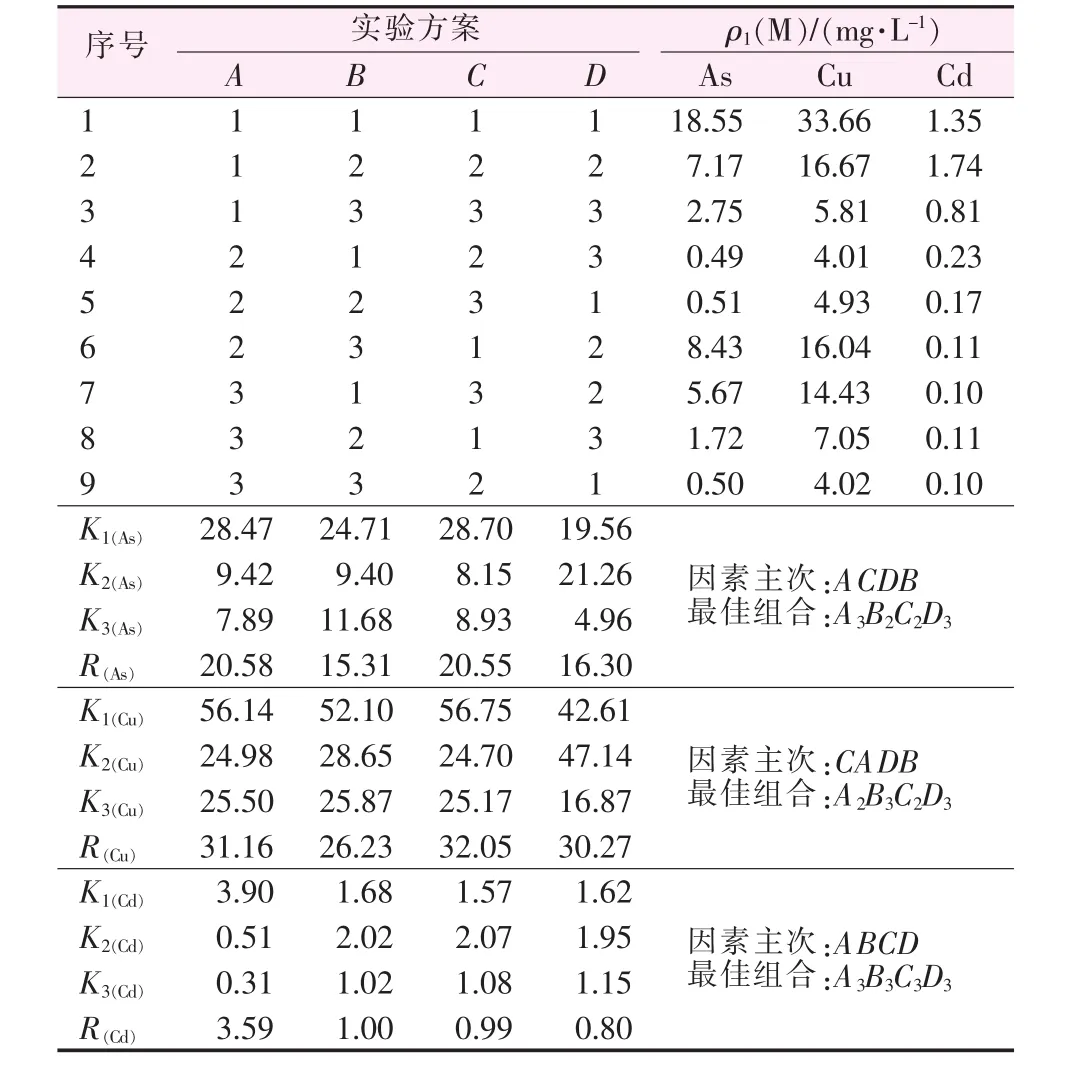
表4 正交实验方案及结果
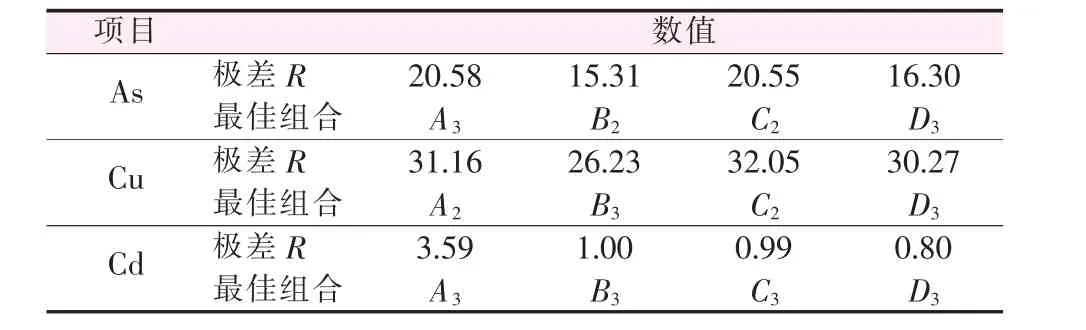
表5 综合平衡法对指标的分析
2.2.2 Lig-DTC加入量对废水重金属去除的影响
重捕剂加入量对重金属离子的去除有较大的影响。其他条件不变,改变重捕剂加入量,考察其对酸性废水中As、Cu、Cd的去除情况,结果见图3。由图3看出,随着Lig-DTC用量增加,废水中重金属离子质量浓度逐步降低,当重捕剂用量达到45 mg时,酸性废液中 Cu(Ⅱ)质量浓度为 4.81 mg/L(<5.0 mg/L);当重捕剂用量为50mg时,总砷质量浓度降至0.50 mg/L、Cu(Ⅱ)质量浓度为 4.4 mg/L,但是 Cd(Ⅱ)质量浓度降至0.22 mg/L,未达到规定的处理要求;当重捕剂用量增至60 mg时,总砷质量浓度降至0.48 mg/L、Cu(Ⅱ)质量浓度为 4.0 mg/L、Cd(Ⅱ)质量浓度降至0.09mg/L,重金属离子质量浓度达到处理要求。为保证重金属离子去除达到要求,Lig-DTC用量需调整为60 mg。
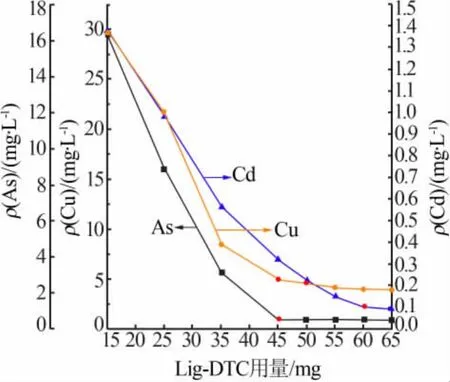
图3 Lig-DTC用量对废水重金属去除的影响
2.2.3 pH对废水重金属去除的影响
废水pH对重金属离子的去除也有较大的影响。酸性重金属废水源自制药厂的提纯工段,pH会在一定范围内波动。对Lig-DTC重捕剂在不同pH(0.3、1.0、1.5、2.0、6.0、10)条件下对重金属离子的螯合进行评价。废水pH通过0.1mol/LH2SO4或1mol/L NaOH溶液调节,重捕剂用量分别为10、30、60 mg,其他条件不变,实验结果见图4。
ρ1(Cd):当 pH=0.3 时,Lig-DTC 对 Cd 几乎没有去除效果;pH=2时,需向100 mL废水中加入60 mg Lig-DTC才能满足处理要求;当pH=10时,仅加入10 mg Lig-DTC即可使Cd(Ⅱ)质量浓度降低至0.089 mg/L(<0.1 mg/L,达标)。
ρ1(Cu):废水 pH<1.0 时,加大重捕剂投入量,Cu(Ⅱ)质量浓度变化不大;pH=2.0时,加入30mgLig-DTC,Cu(Ⅱ)质量浓度降至 4.724 mg/L(<5.0 mg/L);pH=6.0时,加入10 mg重捕剂可达到处理要求。
ρ1(As):当 Lig-DTC 用量为 10 mg 时,pH 逐渐上升至10,总砷质量浓度并没有随pH增加而达到处理要求;pH=10时,重捕剂用量为30 mg,As剩余质量浓度为 0.21 mg/L(<0.5 mg/L);pH=2 时,重捕剂用量需增至60 mg才能满足处理标准。
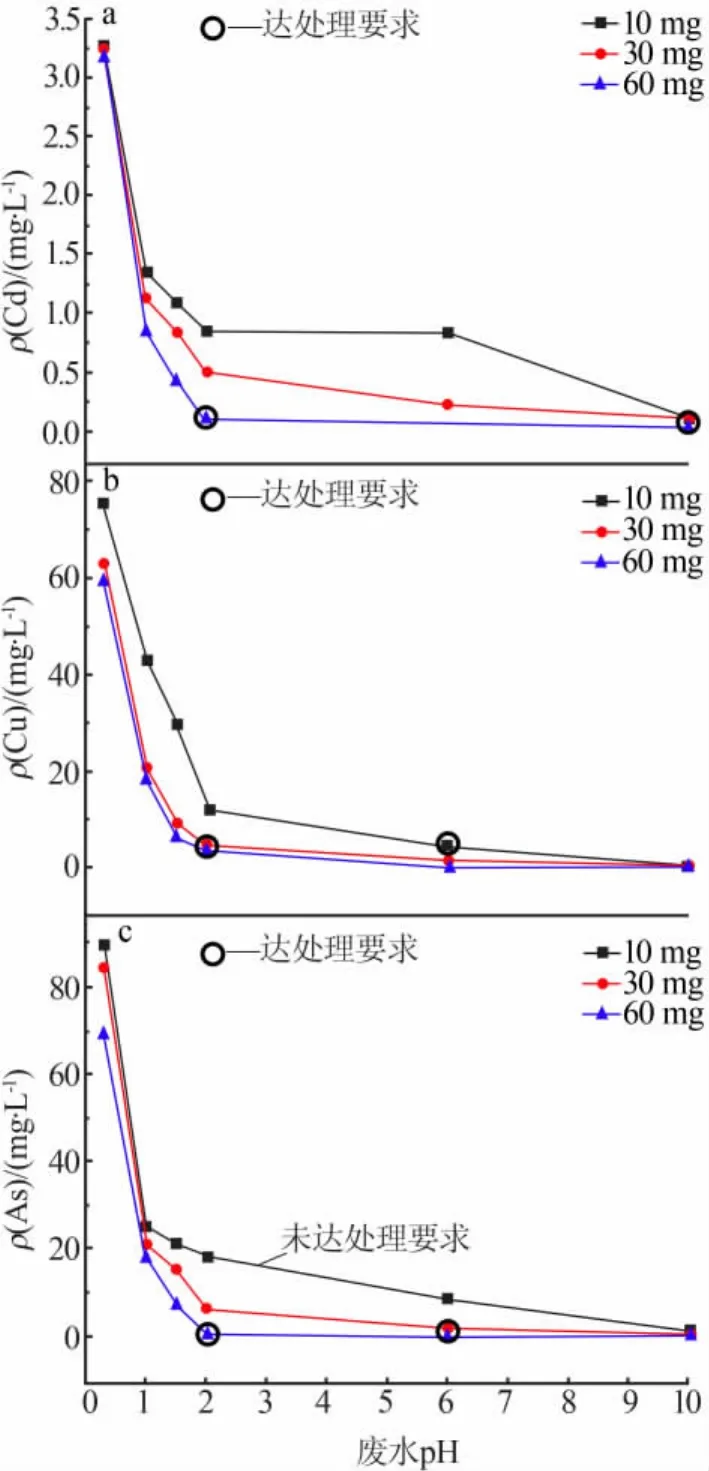
图4 不同pH条件下重捕剂对重金属离子的去除情况
pH<1.0时,部分Lig-DTC的二硫代官能团被分解,重捕剂对重金属离子的螯合程度降低,废水中剩余重金属浓度偏高,去除效果不理想;pH≥2时,Lig-DTC对As、Cu、Cd的螯合效果提升,加入较少的重捕剂即可满足相关排放标准。
2.3 Lig-DTC与EDTC、TDDP使用效果比较
取适量450mg/L含Cu(Ⅱ)模拟废水(由CuSO4·5H2O配制)置于锥形瓶中,用0.1 mol/L H2SO4或1 mol/L NaOH溶液调节pH,与Cu物质的量比为1∶1的量加入捕集剂EDTC[N,N-双(二硫代羧基)乙二胺]、TDDP[N,N,N,N-4(二硫代羧基)二并哌嗪]、Lig-DTC,经搅拌、絮凝沉淀,通过ICP测定水中Cu质量浓度,结果见图5。EDTC、TDDP在酸性条件下对Cu(Ⅱ)的去除效果不理想,Lig-DTC在较宽pH范围内去除效果较为明显。这是由于木质素基体可促进二硫代氨基甲酸基团在酸性条件下的稳定性。
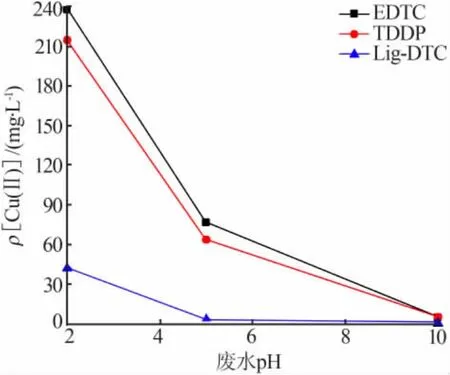
图5 3种重捕剂效果比较
2.4 Lig-DTC处理后废水分析
取100mL废水,pH≈2(未调节废水pH),在Lig-DTC用量为60 mg、反应时间为15 min、PAM加入量为1.1 mL条件下絮凝,然后静置30 min,过滤,对滤液中的主要成分进行分析,结果见表6。As、Cu、Cd达到处理要求,酸性废水(H2SO4)可循环回用。重捕剂螯合重金属离子产生的沉淀量约为石灰法的1/20,可显著降低固废处理成本。
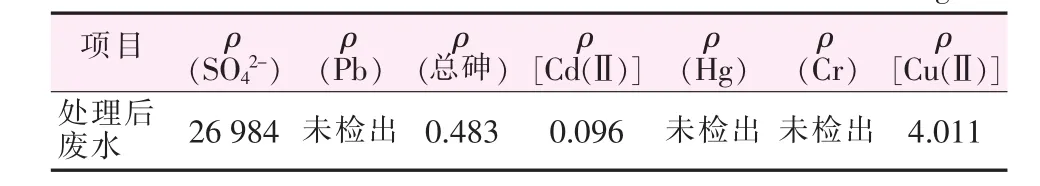
表6 处理后的废水成分分析 mg/L
3 结论与展望
以碱木质素为基体通过Mannich反应、CS2加成反应合成新型重捕剂N-亚甲基碱木质素-N′-二硫代氨基甲酸己二胺钠盐(Lig-DTC),通过正交实验和单因素实验,以废水重金属离子剩余质量浓度为评价标准,对重捕剂加入量、反应时间、溶液pH、絮凝剂投加量进行测定。在不调节废水酸性前提下,以100 mL废水计,在Lig-DTC用量为60 mg、反应时间为 15 min、PAM(质量分数为0.1%)加入量为1.1 mL、静置时间为30 min条件下絮凝,废水中As、Cu、Cd达到处理要求,酸性废水可循环回用。木质素是具有三维结构的高分子化合物,其结构存在丰富的活性基团(芳香基、酚羟基、醇羟基、碳基共扼双键等),木质素改性反应机制及Lig-DTC螯合重金属离子的机理还有待进一步研究。

