两种淋巴细胞比预测经皮肾镜碎石取石术后全身炎症反应的作用
王羿翔 李明山 刘屹立 王平
1 中国医科大学附属第四医院泌尿外科110032 沈阳
经皮肾镜碎石取石术(percutaneous nephrolithotomy,PCNL)作为一种微创手术,具有创伤小、预后好、取石率高等优势,一直被视为是直径>2 cm 肾结石的一线治疗方法[1]。全身炎症反应综合征(systemic inflammatory response syndrome,SIRS)是一种常见的PCNL 术后并发症,发生率可达9.8%~37.0%,部分患者可进一步发展成尿脓毒血症,严重者可导致感染性休克甚至多器官功能障碍综合征(multiple organ dysfunction syndrome,MODS),死亡率高达25%~50%[2]。很多文献探究了影响PCNL 术后发生SIRS 的因素,但中性粒细胞-淋巴细胞比率(neutrophil-lymphocyte ratio,NLR)与血小板-淋巴细胞比率(platelet-lymphocyte ratio,PLR)对其的影响却鲜有研究。NLR 与PLR 是在炎症期间升高的生物标志物,目前有许多研究指出其在肿瘤疾病中起着重要的作用[3-5]。我们对术前NLR 和PLR 值以及其他临床数据进行统计分析,探究影响PCNL术后发生SIRS 的危险因素,以便尽早采取干预措施。
1 资料与方法
1.1 临床资料
收集2015 年8 月-2018 年8 月在中国医科大学附属第四医院泌尿外科因肾结石行常规PCNL治疗的患者资料。纳入标准:患者首次行单侧标准PCNL 手术,具有完整的临床资料及血常规检查结果,基于排除标准筛选。排除标准:①年龄<18 岁的患者;②术前评估至少有一项SIRS 标准的患者;③患有肿瘤疾病的患者或有放置的肾造瘘管或尿道支架史的患者;④同一时段经历过同侧或对侧输尿管镜介入治疗的患者;⑤行双侧标准PCNL 的患者。研究共纳入147 例患者,其中男82 例,女65 例,年龄(53.8±12.4)岁。根据患者术后是否发生SIRS,将患者分为非SIRS 组和SIRS 组,非SIRS 组106 例,SIRS 组41 例。根据2001 年国际脓毒症定义会议标准[6],当满足以下两个或多个标准时,患者即被诊断为SIRS:体温<36℃或>38℃,心率>90 次/min,呼吸频次>20 次/min,PaCO2<4.256 kPa(32 mmHg),外 周血白细胞计数>12×109/L 或<4×109/L,未成熟粒细胞>0.1。
1.2 评估项目
对入组患者的年龄、性别、体质量指数(body mass index, BMI)、是否为糖尿病、结石负荷、术前NLR 和PLR、血红蛋白减少量和有无残余结石等临床因素进行评估。术前所有患者接受体格检查、血细胞计数、血生化和尿液分析检查,对所有患者进行CT 扫描评估并计算结石负荷,术后密切监测生命体征,进行血细胞计数分析,并预防性使用抗生素治疗(头孢地嗪,2.0 g/100 mL,2 次/d)直至移除肾造瘘管。
1.3 统计学方法
采用SPSS 22.0 对数据进行统计分析,服从正态分布的计量资料以表示,非正态分布以中位数和四分位间距表示,计数资料以例数和百分比表示。使用独立样本t 检验或Mann-Whitney U 检验比较数值变量组间差异,使用卡方检验比较分类变量组间差异。对纳入的临床数据进行单因素和多因素Logistic 回归分析。构建受试者工作特征(ROC)曲线,并确定术前PLR 的临界值。P<0.05 被认为差异有统计学意义。
2 结果
本研究共纳入147 例患者,年龄18~81 岁,平均(53.8±12.4)岁。 BMI 为(24.1±4.6)kg/m2(18.0~38.9 kg/m2)。结石负荷中位数为663.0 mm2。术前NLR 为0.54~6.50,平均(2.4±1.0),术前PLR 为54.7~192.0,平均(117.2±26.3)。其中共有41 例(27.9%)患者在PCNL 术后发生了SIRS。详见表1。
单因素分析显示术前NLR 和PLR(P=0.012,P<0.001),血红蛋白减少量(P=0.035)和有无结石残余(P=0.026)之间存在显著的组间差异(表1)。多变量分析显示只有术前PLR 是影响SIRS 术后发展的独立因素(95%CI:1.021~1.058,OR=1.039,P=0.001)(表2)。其他变量如术前NLR 结果显示均不显著。根据ROC 曲线,选择PLR 的最佳界值(cut-off 值)130.8(敏感度与特异度之和最大值),其具有63.4%的敏感性,85.0%的特异性,61.9%的阳性预测值和85.7%的阴性预测值(表2)。ROC 曲线下面积为87.3%(图1)。
3 讨论
PCNL 术后并发症的发生率为4.0% ~50.8%[2],其中尿脓毒血症是PCNL 术后一种严重的并发症,有着较高的发病率与死亡率[7]。一些研究指出尿脓毒血症是其围术期死亡的最常见病因。SIRS 是由缺血,炎症,创伤,感染等原因引起,包括由感染因素导致的脓毒症、非感染因素导致的炎症反应综合征两部分[6]。目前已有研究者就PCNL 术后SIRS 的发生和进展情况展开调查,但对其预测PCNL 术后发生SIRS 的风险因素尚未达成共识。有学者的相关研究结果显示,手术时间长短、结石大小、肾盂肾盏是否扩张、进入通道数量和是否进行输血治疗是导致PCNL 术后发生SIRS 的危险因素,并且还指出具备这些因素的患者发生SIRS 的风险较一般人群增加20 倍[8]。Erdil 等[9]的研究结果则表明术前尿液、术中肾盂尿及结石细菌培养阳性会导致PCNL 术后SIRS 的发生,而其他任何因素对其均没有影响。
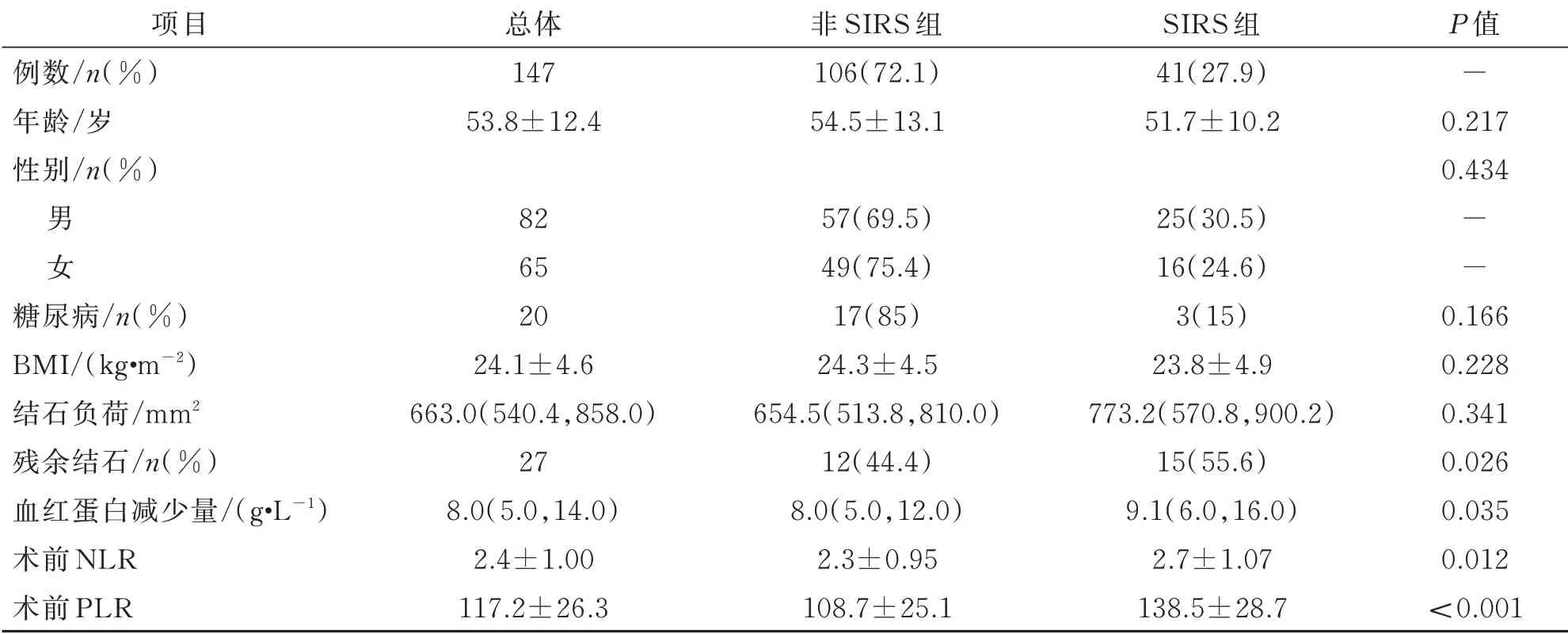
表1 患者的一般临床资料

表2 PCNL 术后发生SIRS 的多因素回归分析
结石是细菌附着的载体,在碎石过程中,结石内部包裹住的细菌被释放,如果术后仍有结石被残留在体内,细菌则会有更多的时间和机会流入血液内,释放内毒素,当细菌和毒素积累到一定程度后,就会引起尿脓毒血症。另一方面在手术过程中,难免会有激光或者碎石摩擦损伤尿路黏膜,破坏表面的粘多糖保护层,更加方便细菌的侵袭入血。
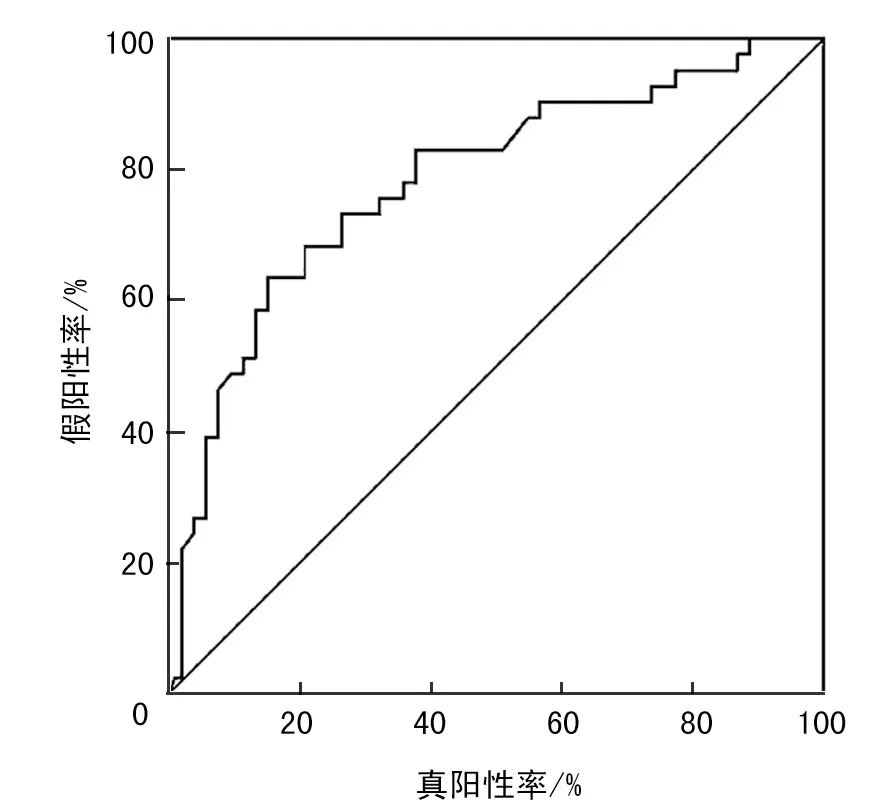
图1 PLR 值的ROC 曲线
血红蛋白的下降往往提示术中出血量较大,组织损伤较为严重。一方面可能与操作通道的数量相关,由于结石位置、大小等原因,为了方便术中操作常会选择多孔通道进行,因此肾脏创面较大,细菌与其接触面积增加,患者术后有着更高的感染风险[10-11]。另一方面,术后血红蛋白下降可能也有患者肾实质厚度相关,肾实质越厚,术中操作对其组织损伤相对越重,导致术中出血量越多,Tepeler 等[10]也认为肾实质较厚的患者由PCNL 引起的损伤更为严重,术后SIRS 的发生率更高。PCNL 术后患者的血红蛋白下降在两组之间之所以存在统计学差异,很可能是由于多通道或肾皮质较厚引起的创伤增加,从而增强机体对创伤的全身性炎症反应,使PCNL 术后发生SIRS的风险更高。
除了以上因素之外,我们的研究结果显示NLR 和PLR 是预测PCNL 术后发生SIRS 的新型非侵入性生物标志物。NLR、PLR 是常规血液学检测指标,其升高常常表示机体处于炎症反应期,也是SIRS 患者中少数与其相关的血液学标志物。此外也有诸多学者报道NLR 和PLR 与胃肠道和泌尿生殖系统肿瘤密切相关[3-5],Proctor等[12]对27 000 名患者进行的大规模研究,证实了其在预测各种癌症结局中的重要作用。中性粒细胞在全身和局部炎症反应中起积极作用,同时中性粒细胞的上调可以反映侵袭性,当其受到造血细胞因子的刺激可产生精氨酸酶、一氧化氮、活性氧和抑制细胞毒性淋巴细胞。血小板可以促进血管生成、细胞外基质降解、生长因子和粘附分子的释放,这些可作为炎症扩散及肿瘤增殖转移的基础。血小板的覆盖有助于细胞团克服血液中的压力,包括免疫系统和物理因素的攻击。同时各种促炎细胞因子,如白细胞介素-1,白细胞介素-3 和白细胞介素-6,可促进巨核细胞增殖,导致血小板数量增多[13-14]。由于NLR 和PLR都是反映全身炎症水平的生物标志物,因此通常NLR 水平较高的患者也具有较高的PLR 水平,反之亦然。
在我们此次研究中,NLR 和PLR 在两组患者中都差异有统计学意义,并且多变量分析的结果认为PLR 可以作为PCNL 术后发生SIRS 的独立预测因素。当PLR 取cut-off 值130.8 时,拥有63.4%的敏感性,85.0%的特异性。目前研究表明术前预防性使用抗生素可以减少术后感染的可能,但对于SIRS 并不能完全预防,所以对于预测SIRS,或者在感染早期能及时发现并加以阻断,有很重要的临床意义。PLR 这种易获取、安全和低成本的生物标志物更便于在临床中应用。但此次研究仍存在一些局限性:本研究为回顾性研究,样本量不够大,可能会出现偏倚。此外,术中尿液和结石培养分析等多种因素由于数据收集不完全而无法纳入此次研究进行评估。
综上所述,对于医生和患者来讲,预测术后SIRS 的发生发展是极其重要的,我们建议对术前PLR>130.8 的患者应格外关注,此类患者术后发生SIRS 的概率更高,在感染早期及时发现,积极采取有效措施来阻止感染的进一步加重,从而提高患者预后及生存质量。术前PLR 评估是一种简单,经济有效且无创的检查,可用于预测SIRS的发展,但目前仍需要进一步完善前瞻性随机研究来比较NLR、PLR 以及其他参数,从而更好的预防PCNL 术后SIRS 的发生。

