超声引导融合虚拟CT导航射频治疗高危部位原发性肝癌
彭宁 陶意文 何松青 杨红 尚丽明 肖开银
作者单位:530021 南宁 广西医科大学第一附属医院肝胆外科
超声引导下射频消融是治疗原发性肝癌(以下简称肝癌)的主要治疗方式之一。目前证据显示,肝癌患者短期生存射频消融与肝切除术相当,但肝切除术长期生存显著优于射频消融,主要原因为射频消融可能导致消融不完全,术后复发率升高[1-2]。近年来,实时超声引导融合虚拟CT导航逐渐应用于肝癌射频消融治疗,但单纯超声引导定位精度不高,消融率偏低。准确的射频定位对高危部位肝癌尤为重要。肿瘤高危部位定义为肿瘤直径5 mm内存在重要的结构或主要静脉(>3 mm)[3]。本研究采用实时超声引导融合虚拟CT导航下射频消融治疗高危部位肝癌,评价其肿瘤定位率、消融率、并发症发生率和复发进展率,以期提高疗效。
1 资料与方法
1.1 一般资料
前瞻性分析2017年1月至2018年6月在广西医科大学第一附属医院接受射频消融治疗的80例高危部位肝癌患者。所有患者均为首发肝癌患者,未接受任何肿瘤治疗。纳入标准:⑴经超声造影和CT检查确诊或病理学检查确诊为肝癌,肝癌诊断符合原发性肝癌诊疗规范(2017年版)诊断标准[4];⑵肿瘤数目≤3个且最大肿瘤直径≤3 cm;⑶肿瘤位于肝脏高危部位(距离肝门血管、胆管和肝脏周围器官5 mm以内,肝脏周围器官包括胃肠道、胆囊、膈肌、肾脏);⑷肿瘤BCLC分期均为A期,无血管、胆管侵犯和远处转移;⑸Child-Pugh肝功能A级或B级。排除标准:⑴合并严重的黄疸、腹水;⑵凝血功能障碍;⑶门静脉癌栓;⑷远处器官转移。将患者分为实时超声引导融合虚拟CT导航下射频消融治疗组(观察组)和单纯超声引导治疗组(对照组)。本研究获本院医学伦理委员会批准,所有患者均签署射频治疗知情同意书。
1.2 方法
超声机采用美国GE LOGIQ E9;虚拟CT导航定位仪使用GCX公司仪器;射频机为Cool-tipTMRF ablation system内冷型射频电极针。观察组术前将CT图像载入超声导航系统,图像融合成功后,CT图像与超声引导的实时位置重叠,形成立体定位图像,超声屏幕上同时显示超声引导图像和CT对应的层面位置(图1和图2)。根据超声导航系统虚拟融合三维图像,制定进针计划。在实时超声引导融合虚拟CT导航下进针,对病灶进行消融治疗(图3)。对照组采用单纯超声引导治疗。两组患者均于消融结束后第2天复查超声造影,检查有无病灶残留,如有病灶残留,再次行射频消融。
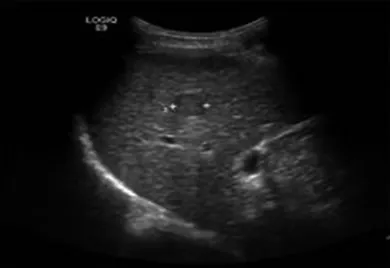
图1 超声发现肿瘤病灶Fig.1 Ultrasound revealed tumor lesions
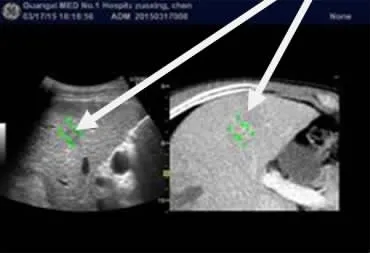
图2 超声融合CT对肿瘤导航Fig.2 Ultrasound fusion CT for tumor navigation

图3 肿瘤射频消融Fig.3 Radiofrequency ablation of tumor
1.3 疗效评价
比较两组患者的肿瘤定位率、消融率、围手术期并发症发生情况和复发进展率。所有患者接受射频消融术后3个月复查超声造影和增强CT,消融病灶未出现强化视为消融治疗完全(图4)。肿瘤局部复发指射频消融术后随访3个月内发现消融病灶2 cm内出现新发病灶。

图4 术后CT复查病灶Fig.4 Postoperative CT reexamination showed inactivation of the lesion
1.4 统计学方法
采用SPSS 16.0软件进行数据分析。计量资料采用均数±标准差(±s)表示,组间比较采用独立样本t检验。计数资料采用n(%)表示,组间比较采用χ2检验或Fisher确切概率法。以P<0.05为差异有统计学意义。
2 结果
2.1 一般情况
共80例患者符合入组标准,其中男性65例,女性 15例;年龄 32~74岁,平均(48.00±8.23)岁。观察组42例患者病灶共50个,对照组38例患者病灶45个。两组患者性别、年龄、肿瘤大小、肿瘤邻近位置、甲胎蛋白、肝功能Child-Pugh分级等比较差异均无统计学意义(P>0.05),见表 1。
表1 两组患者一般资料比较[n(%)±s]Tab.1 Comparison of general data between the two groups of patients[n(%),±s]

表1 两组患者一般资料比较[n(%)±s]Tab.1 Comparison of general data between the two groups of patients[n(%),±s]
General information ControlResearcht/χ2 P groupgroup Gender— >0.999 Male 31(81.6) 34(81.0)Female 7(18.4) 8(19.0)Age(year) 45.03±9.51 50.32±8.22 0.786 0.463 Tumor size(cm)2.10±0.41 1.71±0.20 0.645 0.571 Tumor number45 50 Adjacent location of tumor11(24.4) 12(24.0) 0.003 0.960 Diaphragmatic dome Alimentary canal 15(33.3) 20(40.0) 0.452 0.501 Porta hepatis 16(35.6) 14(28.0) 0.626 0.429 Gallbladder 3(6.7) 4(8.0) <0.001 >0.999 Alpha fetoprotein(ng/mL) 561.32±60.31 610.45±57.34 0.498 0.65 Child-Pugh — 0.495 A 38(100.0)40(95.2)B 02(4.8)
2.2 定位率和消融率情况
观察组一次穿刺定位成功48个病灶,成功率为96.00%(48/50);对照组一次穿刺定位成功36个病灶,成功率为80.00%(36/45),两组比较差异有统计学意义(χ2=4.462,P=0.035)。观察组完全消融48个病灶,消融率为96.00%(48/50);对照组完全消融35个病灶,消融率为77.77%(35/45),两组比较差异有统计学意义(χ2=5.571,P=0.018)。消融结束后第2天复查,残留病灶再次行射频消融。1个月后复查,观察组完全消融49个病灶,消融率为98.00%(49/50),对照组完全消融38个病灶,消融率为84.44%(38/45),两组比较差异有统计学意义(χ2=4.022,P=0.045)。
2.3 并发症和复发率情况
两组患者均未发生膈肌损伤、肝脓肿、邻近器官损伤。观察组发生肝被膜下血肿1例,并发症发生率为2.38%(1/42);对照组出现胸水和胆汁瘤各1例,并发症发生率为5.26%(2/38),两组并发症发生率比较差异无统计学意义(P=0.602)。随访3个月内观察组复发率为 2.38%(1/42),对照组为 21.05%(8/38),两组比较差异有统计学意义(P=0.011)。
3 讨论
射频消融是小肝癌的主要根治性治疗方法之一。射频消融操作方便、治疗时间短、并发症发生率较肝切除术低、术后恢复快、住院时间短、费用较低。部分患者甚至可以进行日间手术,因此射频消融术广泛应用于临床,但如何提高射频消融的消融有效率,降低复发率,成为临床上亟需解决的问题。尤其位于肝脏高危部位肝癌提高射频消融定位准确率和消融率,避免并发症发生,操作更困难。常规超声定位难以清晰分辨病灶大小、范围、边界与周围器官及组织的关系,距离欠清晰,射频时消融范围可能不足,肿瘤残留或复发率较高,且易造成误损伤、胆瘘、肠漏、胆管损伤、出血等并发症。KELOGRIGORIS等[5]报道特殊部位肝癌射频消融并发症的发生率为9.5%。实时超声引导融合虚拟CT导航下射频消融,超声定位时将CT图像融合,利用空间磁场GPS立体定位的方法,在多个层面上多点定位。超声屏幕能同时显示实时超声图像和CT图像,可更好地引导进针,进入病灶底部,囊括病灶的安全范围进行有效消融,提高了定位的精准度和一次消融率,亦可避免误伤特殊部位病灶的周围器官。本研究中两组患者并发症发生率差异无统计学意义,两组患者亦未发生膈肌损伤、肝脓肿、邻近器官损伤,但对照组定位较困难,为避免误损伤,穿刺定位时往往未到达合适位置而导致消融率偏低。因此,超声引导融合虚拟CT可以防止肿瘤消融安全范围不足而导致的病灶残留,有利于降低肿瘤复发率,让患者生存获益。
本研究通过前瞻性分析80例肿瘤位于肝脏高危部位的小肝癌患者共95个病灶,分别采用实时超声引导融合虚拟CT导航下射频消融治疗和单纯超声引导射频消融治疗,结果观察组50个病灶的一次定位率和两次完全消融率均高于对照组;消融率为98.00%,亦高于对照组的84.44%以及SONG等[6]报道的高危部位肝癌射频后的消融率(90.9%),与非高危部位肝癌虚拟导航射频效果相当[7-8]。在并发症发生方面,两组均未发生膈肌损伤、肝脓肿、邻近器官损伤,观察组并发症发生率稍低于对照组,其中观察组发生肝被膜下血肿1例。发生原因是肿瘤靠近肝被膜,且肿瘤表面血运丰富,导致穿刺时出现血肿。建议穿刺时尽量从正常肝组织处进针,退针时消融针道时间适当增加,以减少血肿发生。进一步随访发现术后3个月观察组的复发率亦较低,说明超声引导融合虚拟CT导航下射频消融治疗高危部位肝癌效果良好,是有效、安全的方法,与多项研究[9-10]报道结果一致。分析可能是超声引导融合虚拟CT导航下射频消融较单纯超声引导能更清晰地显示病灶,易于辨认病灶与周围器官、血管、胆管等组织的解剖层次,引导进针时可根据肿瘤大小、位置等准确定位,保证消融安全范围,从而有效提高定位率和消融率,降低复发率。超声引导融合虚拟CT导航相对于常规超声引导和单纯螺旋CT引导不仅消融率较好,且安全性较高,可避免射线对医患双方的伤害[11]。但值得注意的是,融合导航系统要求CT/MRI图像分辨率高,应尽量采取薄层扫描,图像融合时患者体位应与CT/MRI检查体位保持一致,且应了解患者腹腔内病变情况,尽量保持病变稳定,才能精准融合定位准确。此外,高危部位肝癌的消融治疗效果与操作者的经验和临床应变力有关,操作者应尽可能保持准确定位并提前制定详细计划,让患者真正获益。
综上,超声引导融合虚拟CT导航下射频消融治疗高危部位肝癌的定位率和消融率较好,复发率低,是安全、有效的方法,值得临床推广应用。但本研究样本量较少,随访时间较短,高危部位肝癌的消融治疗效果影响因素较多,因此有关结论尚需进一步研究证实。

