输卵管疾病的CT和MRI诊断现状与进展
王成艳, 孙美玉
输卵管解剖
输卵管起自双侧子宫角,横向延伸至同侧卵巢,与腹腔相通,为细长且弯曲的肌性管道,位于子宫阔韧带上缘的腹膜皱褶内,腹膜反折形成输卵管系膜。育龄期女性输卵管长约10~12 cm,直径约1~4 mm。输卵管细而弯曲,分为间质部、峡部、壶腹部、伞部4个部分。间质部、峡部短而窄,壶腹部相对宽大,伞部呈漏斗状,开口于腹膜腔,悬垂于卵巢外上方。组织学上输卵管壁由内向外分别为黏膜层、肌层及浆膜层。
输卵管疾病的诊断方法
输卵管疾病作为常见的女性生殖系统疾病,临床常用超声波检查,但声像图易受到超声波衰减及肠腔气体的影响。子宫输卵管碘水造影属于有创检查,虽可用于输卵管疾病的诊断,但仅能显示管腔内情况。电子计算机断层成像(computed tomography,CT)具有很高的密度分辨率,可在盆腔脂肪组织的衬托下确切的显示输卵管病变的影像,同时多平面重组图像有助于病变检出。磁共振成像(magnetic resonance imaging,MRI)具有多方位、多层面成像的特点及良好的软组织分辨率,可以较清晰的显示输卵管的异常,并能根据病灶的信号特征推测其组织成分,在输卵管疾病的诊断中发挥了重要作用。本文就输卵管疾病(输卵管炎、输卵管妊娠、输卵管子宫内膜异位、输卵管系膜囊肿、输卵管扭转、输卵管癌)的CT和MRI诊断现状与进展进行综述。
输卵管炎性疾病
1.病因与转归
输卵管炎性疾病根据病因分为非特异性炎症和特异性炎症(结核),以非特异性炎症多见。输卵管非特异性炎症多因阴道逆行感染引起子宫内膜炎,进一步发展累及输卵管。如果炎症未能及时治愈,会引起伞端粘连闭锁,液体积聚于管腔内形成输卵管积脓,当炎症消退时,脓细胞和坏死组织的蛋白质分解,形成稀薄的浆液性的液体,输卵管积脓转变为输卵管积液。
2.CT与MRI表现
①输卵管积脓:CT表现为特征性的腊肠状、串珠状、管状或多房状囊实性肿块,囊壁较厚,增强扫描后囊壁、分隔和实性部分呈持续明显强化[1]。分析其明显强化的原因可能是炎症累及输卵管壁,管壁内大量炎细胞浸润,导致管壁充血、水肿;而实质成分由新生的肉芽组织组成,含有大量扩张的新生毛细血管。另外可见子宫和附件周围脂肪模糊、盆腔积液等征象。
MR上表现为扩张扭曲的C形、S形结构,T1WI呈低信号,T2WI呈稍高信号,增强扫描后增厚的管壁明显强化。其中T2WI上扩张的输卵管内显示的“地图样阴影”有助于输卵管积脓的诊断。输卵管积脓在DWI上呈高信号,与脓液内含大量坏死组织、炎性细胞等成分有关[2-3]。Oto等[4]报道将脓液的ADC临界值设为2.0×10-3mm2/s时,DWI与T2WI联合诊断积脓的敏感度为97%,特异度可达100%。
②输卵管积液:CT表现为形态上类似输卵管积脓的囊性肿块,囊壁薄,囊壁厚度多为2~3 mm,增强扫描后囊壁及分隔无强化或轻度强化[1,5]。部分肿块内可见不完全分隔,有助于输卵管积液的正确诊断[6]。通过多排探测器CT扫描及后处理多平面重组(multi-planar reconstruction,MPR)、最大密度投影(maximum intensity projection,MIP)、容积重建(volume rendering,VR)可较准确的识别正常的卵巢,有助于输卵管积脓、积液的及时诊断[7-8]。

图1 女,45岁,右侧输卵管积脓。a) CT平扫示右侧附件区腊肠状低密度影(箭),壁厚,边界模糊; b) 增强扫描示囊壁明显强化(箭),囊内液体无强化。 图2 女,38岁,左侧输卵管积脓。a) 横轴面 T1WI平扫示左侧附件区多囊状肿块(箭),呈均匀低信号; b) 横轴面T2WI抑脂平扫示左侧输卵管呈高信号(箭),囊内可见结节状稍低信号; c) 横轴面 DWI序列呈多个环状高信号(箭); d) 矢状面T2WI平扫示腊肠状肿块(箭),囊内见分隔; e) 横轴面T1WI抑脂增强扫描囊内液体无强化(箭),囊壁增厚且明显强化; f) 冠状面T2WI平扫示盆腔明显扩张的多囊状肿块(箭)。
MRI表现为腊肠样管状结构,呈C形、S形,其内为水样信号,T1WI呈低信号,T2WI呈高信号,DWI呈低或高信号,与积液所含成分有关。增强扫描后囊壁无强化或轻度强化[2]。T2WI上不完全分隔呈低信号,是输卵管积液的特征性表现,可能是固定长度的输卵管系膜的牵拉,使扩张积液的输卵管相邻管壁折叠而成,有助于与有分隔的卵巢囊腺瘤鉴别[9]。因输卵管纵向黏膜皱襞增厚,部分病例在横轴面CT和MRI上可见特征性的“齿轮征”,有助于诊断输卵管积液[1]。
③输卵管结核:输卵管结核是由结核分枝杆菌引起的炎性病变,多由肺结核血行感染输卵管,少数为结核性腹膜炎直接感染输卵管。多累及双侧输卵管及卵巢。病理上输卵管结核分为渗出型、增生粘连型和干酪坏死型,三种病理过程常混合存在,目前CT和MRI尚无法确定病理分型。
CT上输卵管结核表现为子宫旁的蛇形或串珠状囊实性肿块,边界不清楚,多无壁结节,常并发盆腔包裹性积液,由于积液内含蛋白及细胞成分,平扫CT值偏高。增强扫描后实性部分及增厚的囊壁呈环状或蜂窝状明显强化。附件区钙化是诊断输卵管结核的重要征象[9-10]。
输卵管结核MRI表现为腊肠样或多房囊实性肿块,T1WI呈等、低混杂信号,T2WI呈不均匀高信号,增强扫描囊壁、不完全分隔及肉芽肿形成的附壁结节均明显强化[11]。
④Fitz-Hugh-Curtis综合征:如果输卵管卵巢脓肿破裂,炎症沿右结肠旁沟经腹膜上行感染,可引起右上腹膜的炎症,称为Fitz-Hugh-Curtis 综合征,又称肝周围炎(perihepatitis)。Fitz-Hugh-Curtis 综合征是输卵管卵巢脓肿的罕见并发症,被认为是肝脏包膜的炎症,临床上可表现为急性发作的右上腹痛和压痛。CT上表现为伴有多发分隔(腹膜发生粘连所致)的肝周积液和腹腔积液,可伴发胆囊壁增厚、胆囊窝积液。增强扫描表现为增厚的肝前包膜明显强化。门静脉期可见门静脉周围水肿、肝包膜下及门静脉周围血流灌注异常。肝脏血流灌注异常在MRI上表现为动脉期肝包膜下、门静脉周围血供增加,延迟期呈等信号,但平扫多无相应区域的异常信号[1,9]。
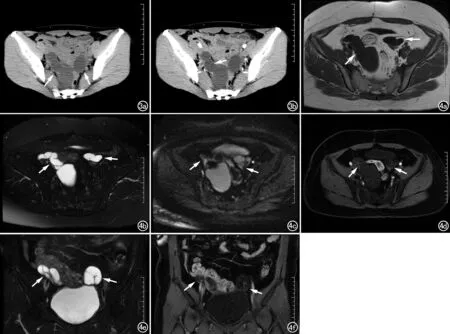
图3 女,40岁,双侧输卵管积液。a) CT平扫示双侧附件区囊性低密度影(箭),呈腊肠状,边界清,壁薄; b) 增强扫描示囊壁轻度强化,囊内可见不完全性分隔且分隔轻度强化(箭)。 图4 女,48岁,双侧输卵管积液。a) 横轴面T1WI示双侧输卵管呈管状扩张(箭),呈低信号; b) 横轴面T2WI抑脂平扫示双侧输卵管呈高信号(箭),右侧扩张输卵管内可见短线状不完全分隔; c) 横轴面DWI序列示双侧输卵管呈低信号、稍高信号(箭); d) 横轴面T1WI抑脂增强扫描示双侧输卵管囊内液体无强化(箭),囊壁轻度强化; e) 冠状面T2WI平扫示双侧输卵管扩张(箭),左侧扩张的输卵管呈“C”形; f) 冠状面T1WI抑脂增强扫描示囊壁增厚(箭),呈轻度强化。
输卵管妊娠
1.病因与转归
受精卵在宫腔外着床与发育称为异位妊娠,输卵管是最常见的异位妊娠部位。异位妊娠占所有妊娠的2%,而输卵管妊娠占异位妊娠的95%~98%。输卵管妊娠好发于壶腹部,常因发生破裂导致腹腔大量出血,是导致妊娠早期孕妇死亡的重要原因。
2.CT与MRI表现
①CT表现:CT表现为附件区混杂密度肿块,肿块内可见环状水样密度孕囊影,中央囊性成分为胚囊,周边实性成分为绒毛组织。增强扫描后呈明显环状强化,称“火环征”。同时可见盆腔积血及内膜增厚等间接征象[12]。
②MRI表现:MRI上妊娠囊表现为T1WI呈等、低信号,T2WI呈高信号,DWI呈点状或环状高信号,增强扫描后多呈不均匀的环状强化[13]。Si等[14]报道T2WI上显示的“three rings”即三环征是诊断输卵管妊娠的特征性表现。中间的环较厚,由大量绒毛组织构成,而绒毛组织间质内含丰富的胎儿毛细血管和母体血液,因而T2WI上呈高信号。薄的外环由邻近的输卵管壁形成呈低信号,薄的内环由无血管成分的羊膜构成,呈等信号。
③输卵管间质部妊娠:间质部是输卵管妊娠最少见的部位,仅占输卵管妊娠的2%~4%,解剖上子宫动脉靠近间质部,间质部妊娠破裂会引起子宫破裂和危及生命的大出血[15-16]。妊娠囊位于宫角外侧,T2WI表现为厚壁的环状妊娠囊样结构,内膜增厚,由于妊娠囊植入在邻近子宫肌层的输卵管管壁内,所以宫腔与间质部妊娠囊之间的结合带是连续的,这是与宫角妊娠区分的重要征象[17]。DWI上妊娠囊呈环状高信号,称“ring of restriction”即限制环征,与妊娠囊的囊壁含大量滋养细胞有关[18]。

图5 女,39岁,左侧输卵管结核。a) CT平扫示左侧附件区蛇形稍低密度影,边界模糊(箭); b) 增强扫描示左侧输卵管管壁增厚,明显强化(箭),同时可见腹腔积液和腹膜增厚。 图6 女,36岁,右侧输卵管妊娠。a) CT平扫示右侧附件区环状稍高密度影(箭),壁厚,边界模糊; b) 邻近层面CT平扫示中央低密度孕囊囊壁不完整,可见破裂口(箭)及盆腔积血(箭头)。 图7 女,40岁,双侧输卵管子宫内膜异位。a) CT平扫示双侧附件区管状稍高密度肿块影(箭),边界模糊; b) 增强扫描示肿块内部无强化,局部管壁轻度强化(箭)。 图8 女,42岁,右侧输卵管子宫内膜异位。a) 横轴面T1WI平扫示右侧附件区结节状高信号肿块(箭),其内形态不规则稍低信号的充盈缺损为异位的子宫内膜腺体; b) 横轴面T2WI抑脂平扫呈高信号,囊内见不规则低信号(箭)。 图9 女,58岁,左侧输卵管系膜囊肿。a) CT平扫示左侧附件区类圆形低密度影(箭),壁薄,边界清晰; b) 增强扫描动脉期囊内液体无强化(箭),囊壁无明显强化。 图10 女,53岁,左侧输卵管高级别浆液性癌。a) CT平扫示左侧附件区囊实混合性肿块(箭),可见盆腔积液; b) 增强扫描动脉期肿块呈腊肠形(箭),呈明显不均匀强化。
输卵管子宫内膜异位
1.病因与转归
输卵管子宫内膜异位好发于育龄期女性,由正常的子宫内膜腺体和间质异位到输卵管所致。异位至输卵管的子宫内膜发生周期性的出血,导致输卵管扩张。最常见的类型是输卵管浆膜和浆膜下的子宫内膜异位,另一种相对少见的类型是管腔内的子宫内膜异位,由于管腔内充满了异位的子宫内膜组织,使输卵管失去正常功能。

图11 女,47岁,左侧输卵管高级别浆液性癌。a) 横轴面T1WI平扫示左侧输卵管腊肠样扩张(长箭),左侧输卵管伞端见均匀低信号肿块(短箭); b) 横轴面T2WI抑脂平扫示扩张的左侧输卵管、伞端肿块呈稍高信号(长箭),伞端肿块信号不均匀(短箭); c) 横轴面DWI示扩张的左侧输卵管和伞端肿块呈明显高信号(箭); d) 横轴面T1WI抑脂增强示左侧扩张的输卵管、伞端肿块呈轻中度强化(箭),伞端肿块边缘明显强化。
2.CT与MRI表现
CT表现为孤立于卵巢的附件区高密度管状或多囊状肿块,CT值多大于50 HU。MRI上T1WI和T2WI表现为附件区多囊状、管状的高信号,部分病例管壁可见不完整的低信号黏膜皱襞。若子宫内膜腺体异位至管腔内,在脂肪抑制T1WI上管状高信号内可见到低信号的充盈缺损[9],T2WI上高信号周围可见特征性的低信号,即“晕征”,形成的原因是异位至输卵管的内膜发生反复周期性出血,其内铁和蛋白质含量极高,缩短T2弛豫时间而呈明显低信号[19-20]。值得注意的是,虽然输卵管积血高度提示输卵管子宫内膜异位,但其他情况下也可发生输卵管积血,如输卵管扭转、输卵管异位妊娠、输卵管恶性肿瘤等。
输卵管系膜囊肿
1.临床与病理
输卵管系膜囊肿又称卵巢旁囊肿、卵巢冠囊肿、阔韧带囊肿或输卵管旁囊肿,位于输卵管与阔韧带之间的输卵管系膜内,目前认为其组织学来源有三种:副中肾管又称米勒氏管来源、中肾管又称沃弗氏管来源、间皮来源。中肾管来源被认为是主要的组织学来源[21]。输卵管系膜囊肿在育龄期女性好发,多为良性,较小时多无临床症状,长大后出现压迫症状,直径大于5 cm的系膜囊肿可发生扭转出现急腹症的临床表现。
2.CT与MRI表现
CT表现为附件区圆形囊性肿块,边界清,壁薄,伴发出血或感染时密度升高,增强扫描后囊壁无强化或轻度强化,囊内液体无强化。典型的输卵管系膜囊肿CT上可见“抱球征”,即子宫阔韧带被输卵管系膜囊肿撑开后呈掌中抱球状[22]。
MRI表现为T1WI低信号,T2WI均匀高信号,合并出血时T1WI呈高信号,边界清,壁薄而光滑,靠近卵巢但与卵巢分界清楚是输卵管系膜囊肿重要的MRI表现[23]。如果囊肿大于5 cm,囊壁见乳头状突起,其恶性风险增加[24]。
输卵管扭转
1.临床与分型
输卵管扭转多单侧发生,好发于育龄期女性,临床上右侧好发,原因可能是乙状结肠可在一定程度上阻止左侧输卵管扭转[25]。输卵管扭转分两种类型:器官轴向型和系膜轴向型。器官轴向型是指输卵管旋转180°或以上时,发生在输卵管远端的扭转。系膜轴向型是发生在输卵管的中间部分围绕系膜轴的扭转,但影像学上难以区分输卵管扭转的类型[26]。输卵管扭转很少单独发生,多与输卵管积液或肿块有关[27]。当患者发生急性腹痛,但显示了正常的卵巢和盆腔囊性肿块,应该考虑到输卵管扭转的可能[28]。
2.CT与MRI表现
输卵管积液并扭转CT表现为管状肿块壁厚超过3 mm,管壁CT值大于50HU,“鸟嘴征”是其特征性表现,增强扫描后无或轻度强化[1],可能是扭转导致管壁发生出血性梗死所致。MRI表现为T1WI低信号,T2WI高信号,增强后无强化,因扭转继发管壁淤血水肿,常可见输卵管管壁增厚。发生扭转的输卵管形态上可类似水流形成的旋涡,T2WI上呈现“漩涡征”为其特征性表现[29-30]。
原发性输卵管癌
原发性输卵管癌(primary fallopian tube carcinoma,PFTC)发病率为女性生殖系统恶性肿瘤的0.14%~1.8%,90%的原发性输卵管癌是高级别浆液性腺癌,由于组织学上与卵巢癌相似常被误诊,因而原发性输卵管癌真实的发病率被低估[31],术前诊断符合率仅约0%~10%[32]。原发性输卵管癌好发年龄为60~70岁,约15%的病例临床出现典型三联征:不规则阴道流液、腹痛和腹部包块。80%以上的患者CA125水平升高[33]。
1.CT与MRI表现
CT表现为附件区腊肠形、C形、不规则形囊实性或实性肿块,部分病例管壁可见乳头状突起,输卵管积液是重要的间接征象。由于肿瘤压迫输卵管淋巴系统致使回流受阻,部分病例患侧子宫圆韧带增粗,增强后实性部分呈轻中度的延迟强化,强化不均匀[34]。
MRI表现为管状或腊肠形肿块,输卵管积液和宫腔积液。位于伞端的输卵管癌常呈结节状。肿块实性部分T1WI呈低信号,T2WI呈等或稍高信号,增强扫描实性部分呈轻度至明显的均匀强化,边缘强化提示肿瘤来源于输卵管[33,35]。
DWI上原发性输卵管癌实性部分呈明显高信号,与肿瘤细胞核浆比增高,细胞数量增多、排列紧密、肿瘤内水分子运动明显受限有关。部分输卵管积液在DWI上呈高信号,分析与积液内含血液、蛋白质或肿瘤细胞成分有关[36]。Kitai等[35]报道输卵管癌的平均ADC值约0.86×10-3mm2/s,但病例数较少。DWI的ADC值定量测量对确定原发性输卵管癌的分化程度有一定价值。Ma等[37]研究发现原发性输卵管癌随着病理级别增加ADC值逐渐降低。由于正常的输卵管无法显示,Grabowska-Derlatka等[38]选择卵巢做为对照组,在不同b值情况下(b=0,50,100,150,200,400,800,1200 s/mm2),对高级别原发性输卵管腺癌进行研究,发现DWI实性部分的信号明显高于对照组正常卵巢组织的信号,平均ADC值明显低于对照组。但由于研究病例数较少,并没有发现信号增加程度与b值的相关性,需要进一步的研究证实。
2.临床分期
MRI可以对输卵管癌进行较准确的临床分期:Ⅰ期肿瘤局限在输卵管,表现为明显强化的腊肠形囊实性肿块。Ⅱ期肿瘤出现盆腔扩散,受累部位T2WI抑脂序列表现为高信号结节,增强后明显强化。Ⅲ期肿瘤出现盆腔外腹膜种植转移/淋巴结转移(淋巴结短径超过1 cm),表现为腹膜结节状增厚,T2WI抑脂序列呈高信号,增强后明显强化。Ⅳ期肿瘤发生远处转移[33,39]。部分微浸润输卵管癌转移至邻近结直肠,在影像学上输卵管可以没有明显的肿块,仅表现为直肠乙状结肠的管状肿块,影像学鉴别肿瘤来源非常困难,需要病理及免疫组化明确肿瘤来源[40]。
3.术后随访
输卵管癌残存肿瘤大小与患者的预后密切相关。残存肿瘤组织小于1 cm,患者的5年生存率为55%;残存肿瘤组织如果大于1 cm,患者5年生存率仅为21%[41]。Liu等[42]研究发现放化疗后残存肿瘤组织的ADC值为(2.14±0.34)×10-3mm2/s,高于放化疗前残存肿瘤组织的ADC值(1.30±0.18)×10-3mm2/s。分析发生此种变化的原因是放化疗破坏了肿瘤细胞的细胞膜,导致细胞外间隙、水分子扩散和细胞凋亡增加,降低了肿瘤细胞的密度,因而ADC值升高。可见DWI有助于评估输卵管癌术后辅助放化疗的近期疗效,进而评价患者的预后。
综上所述,输卵管疾病具有各自特异性的影像学表现。近年来,随着CT和MR设备及技术的不断改进和完善,放射科医生对输卵管疾病的认识明显提高,为临床早期进行合理的干预发挥重要的辅助作用。

