血清脂质过氧化物水平在冠心病合并糖尿病介入治疗后的变化
杨宏飞,鄢高亮
冠状动脉粥样硬化性心脏病简称冠心病,是由于冠状动脉出现粥样硬化病变引起血管狭窄,造成心肌缺血、缺氧而导致的心脏病[1]。糖尿病并发冠心病发病率逐年上升,超过4/5的糖尿病病人是因并发心血管疾病最终导致死亡,冠心病病死率约为非糖尿病病人的3倍[2-3]。目前对糖尿病导致冠状动脉血管的损伤机制仍不是十分清楚,有研究认为[4],胰岛素抵抗在心血管疾病发病中起着重要作用,且可以很好地解释两者之间关系,已被广泛认可。研究表明,氧自由基参与冠脉血管病变的整个过程,其参与脂质过氧化反应引起的血管内皮损伤,是动脉粥样化的主要原因[5]。对比单纯冠心病病人,合并糖尿病者冠状动脉病变更为严重,通常是多支血管同时性损害,并且在每支血管中呈弥漫性损伤[6]。国内目前关于冠心病合并糖尿病病人血管病变脂质过氧化损伤的报道已有许多,但检索发现,探究介入治疗前后糖尿病对血清脂质过氧化物水平影响的文献尚且不多[7]。本研究旨在探究血清脂质过氧化物水平在冠心病合并糖尿病介入治疗后的变化规律,报告如下。
1 资料与方法
1.1 一般资料选取2017年1月至2018年1月东南大学附属中大医院江北院区收治的行经皮冠状动脉介入治疗的冠心病病人94例作为研究对象,将其中单纯冠心病病人41例分为对照组,冠心病合并糖尿病病人53例分为观察组。对照组男26例,女15例;年龄范围为48~84岁,年龄为(60.57±9.57)岁;病程范围为6~19 d,病程为(11.46±3.58)d;Gensini评分范围为38~62分,评分为(51.37±8.53)分。观察组男31例,女22例;年龄范围为46~82岁,年龄为(60.52±9.63)岁;病程范围为 4~17 d,病程为(10.84±3.76)d;Gensini评分范围为39~64分,评分为(51.24±8.38)分。两组一般资料的差异无统计学意义(P>0.05)。本研究符合《世界医学协会赫尔辛基宣言》相关要求。
1.2 入选标准经检查确诊为冠心病病人(有典型胸痛症状,辅助检查发现心肌缺血或冠脉阻塞,心肌损伤标志物判定有心肌坏死);意识及精神状态均正常,配合治疗;病人及其家属签署知情同意书。
1.3 排除标准伴有严重肝、肾等脏器功能障碍;合并良、恶性肿瘤;微生物感染;脑血管疾病;血液、免疫系统障碍;既往有PCI手术史、心力衰竭病史;造血功能障碍;伴有严重感染或风湿免疫疾病;使用维生素、谷胱甘肽等抗氧化药物。
1.4 分组标准将空腹血糖≥7.0 mmol/L,和(或)餐后2 h血糖≥11.1 mmol/L者分为观察组,其余为对照组。
1.5 方法两组在介入手术前根据各自病情进行扩血管(硝酸酯类)、抗血小板(阿司匹林)、调脂(他汀类)治疗,同时给予β肾上腺素受体阻滞药物口服。观察组在此基础上同时进行降糖治疗即予以胰岛素调节治疗。两组均在介入手术前及术后30 min、1 h、12 h、24 h、3 d抽取外周静脉血,再加入30µL浓度为2 g/L的EDTA-Na和40µL抑肽酶,摇晃均匀,以3 000 r/min的转速离心10 min,分离上层血清,置于-80℃待检。丙二醛(MDA)水平采用巴比妥酸比色法测定,超氧化物歧化酶(SOD)水平采用黄嘌呤氧化法测定,操作过程严格按照试剂说明书进行。
1.5.1血清MAD水平测定 采用巴比妥酸比色法检测MAD含量。实验原理:MDA可与硫代巴比妥酸(TBA)缩合形成三甲双酮,这种物质呈紫红色,分光光度计下最大吸收峰为532 nm。研究采用752型分光光度计,测定(532 nm处)三甲双酮吸光光度值,然后根据公式计算MAD水平。
1.5.2血清SOD水平测定 采用黄嘌呤氧化法检测SOD含量。实验原理:SOD可产生超氧阴离子自由基,胺化后会生成亚硫酸盐(酸酐为二氧化硫SO2),与显色剂反应呈紫红色。当样品中含有SOD时标本中的SOD能消除酸酐中的O2-,从而减少亚硝酸盐生成量,降低吸光值,在紫外线可见分光光度计下测定(550 nm处)吸光光度值,然后根据公式计算SOD活力水平。
1.5.3不良事件发生率 通过门诊、电话随访等统计并记录术后6个月内两组出现冠脉再狭窄、急性心肌梗死、卒中及死亡病人例数,分别计算发生率,进行比较分析。
1.6 统计学方法用SPSS 20.0进行数据分析。血清MAD、SOD水平资料均为多时点重复观测数据,均用±s表示,行两因素重复测量方差分析+组间LSD-t检验+组内差值t检验。两组不良事件发生率用n(%)表示,行χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组手术前后血清MAD水平比较整体比较(两因素重复测量方差分析)知:组间、时间及交互作用均差异有统计学意义(P<0.05)。两两精细比较并结合主要数据分析:观察组术后30 min、1 h、12 h、24 h、3 d的MDA水平均低于对照组(P<0.05)。两组术后血清MAD均持续下降,24 h后到达最低值,随后上升;对照组术后12、24 h血清MAD水平、观察组术后各时间段血清MAD水平与两组术前相比差异有统计学意义(P<0.05)。见表1。
2.2 两组手术前后血清SOD水平比较整体比较知:组间、时间及交互作用均差异有统计学意义(P<0.05)。两两精细比较并结合主要数据分析:观察组术后30 min、1 h、12 h、24 h、3 d的SOD水平均高于对照组(P<0.05)。两组术后1 h血清SOD均达到最高值,随后逐渐下降;两组术后各时间段的血清SOD水平与术前相比,差异有统计学意义(P<0.05)。见表1。
表1 经皮冠状动脉介入治疗的冠心病病人94例介入治疗前后血清MAD及SOD水平比较/±s

表1 经皮冠状动脉介入治疗的冠心病病人94例介入治疗前后血清MAD及SOD水平比较/±s
注:整体分析为两因素重复测量方差分析,资料球型性校正采用HF系数法。组间精细比较为LSD-t检验,显著性标记a为两组同时点相比P<0.05。时间精细比较为差值t检验,显著性标记b为和组内手术前比较P<0.05,MDA为丙二醛,SOD为超氧化物歧化酶
血清MAD水平 血清SOD水平时间手术前术后30 min术后1 h术后12 h术后24 h术后3 d整体分析(HF系数)组间F,P值时间F,P值交互F,P值对照组(n=41)74.64±15.63 70.42±12.73 68.38±15.53b 65.39±14.52b 63.59±13.53b 70.53±10.58观察组(n=53)72.49±18.48 53.57±13.48ab 50.38±16.41ab 47.91±16.04ab 45.29±14.59ab 57.41±12.63ab对照组(n=41)17.64±5.63 28.42±6.42b 29.76±5.37b 28.76±5.48b 27.53±6.52b 23.57±5.65b 0.962 8 109.744,0.000 101.849,0.000 5.617,0.000观察组(n=53)19.49±7.48 37.76±6.27ab 38.55±5.65ab 36.96±6.54ab 35.24±6.64ab 29.37±5.65ab 0.915 4 98.031,0.000 21.641,0.000 4.521,0.001
2.3 两组术后6个月不良事件发生率比较观察组冠脉再狭窄、急性心肌梗死、卒中及死亡率均高于对照组(P<0.05)。见表2。
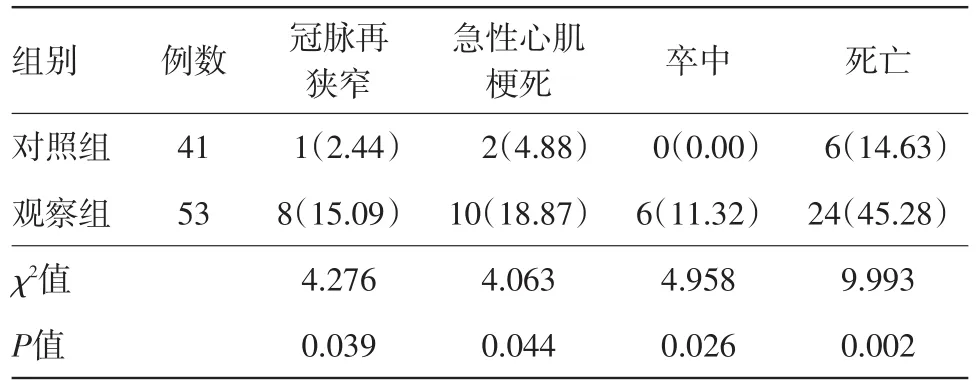
表2 经皮冠状动脉介入治疗的冠心病病人94例介入治疗术后6个月不良事件发生率比较/例(%)
3 讨论
糖尿病是冠心病最为重要的危险因素,统计表明[8],糖尿病病人心血管病发生率高达40%,由此造成的死亡率更是超过了总死亡率的6成以上。持续性的高浓度血糖是冠状动脉损伤且恶化的重要原因,一旦糖基化血红蛋白增多,打破血管舒张平衡,加之脂质过氧化作用便极易导致冠脉弥漫性狭窄[9]。金鹏等[10]通过检测冠脉严重病变需植入支架治疗病人手术前后MDA、D-二聚体的变化,证实介入手术会导致脂质过氧化物水平上升,虽然是暂时的。马建林等[11]研究发现,冠心病病人经介入治疗后会出现脂质过氧化损害,研究中两组病人MDA、SOD水平均较术前均变化明显,且血管内皮功能指标变化显著,实验组更为表现突出,持续时间在1周左右。
近年来,随着血运重建技术不断更新和心肌再灌注损伤研究的深入,临床上对自由基团损伤血管及动脉粥样化导致的脂质过氧化反应动脉斑块形成机制亦有了新的认识,自由基的产生与消除是相互影响的,若机体的氧化代谢效率高,那么其抗氧化能力也会同样强,而当这种平衡关系遭到被破坏后,便会产生氧化应激反应[12]。在本次研究中,观察组术后30 min、1 h、12 h、24 h、3 d的MDA水平均低于对照组(P<0.05),SOD水平均高于对照组(P<0.05)。说明冠心病合并糖尿病病人介入治疗后血清脂质过氧化物水平会出现明显变化,且持续时间较长。同时观察到,两组术后血清MAD均持续下降,24 h后到达最低,随后回升,而SOD则在术后1 h上升至顶峰,后逐渐下降,经统计发现,观察组术后3 d血清MAD、SOD水平变化较对照组更为明显,说明介入治疗对冠心病合并糖尿病病人更能发挥其降低氧化应激反应的作用。MDA和SOD均是抗氧化的重要物质,其通过中和超氧阴离子自由基,以降低活性氧含量,起主要的拮抗作用[13]。众所周知,血脂异常(尤其是低密度脂蛋白水平上升)是动脉粥样化的重要因素,而氧化后的脂蛋白致病作用更强,有研究表明[14],病变血管中可检测出自由基的抗原决定簇,两者结合后会导致局部炎症因子大量释放、活化血小板,刺激细胞外基质过度增生,以促进斑块形成。MDA是脂质氧化反应的终极产物,可通过降低相关酶活性(主要是线粒体呼吸)干涉代谢,对细胞具有一定毒害作用,临床上常根据MDA的检测水平来判断脂质过氧化程度[15]。而SOD作用则与MAD相反,它主要是清除自由基,当SOD含量减少时,自然其对自由基的清除效用便会降低,病人便容易致病,在心血管病变中体现为阻碍低密度脂蛋白氧化的能力降低,导致血管脂质毒性增加[16]。
Smirnova等[17]通过观察介入治疗后冠心病病人主要发生的心血管事件,发现合并糖尿病者心肌梗死及死亡率上均明显高于其他冠心病病人。在本次研究中,观察组冠脉再狭窄、急性心肌梗死、卒中及死亡率均高于对照组(P<0.05)。与上述报道结果相似。考虑可能病人是介入治疗后缺血再灌注损伤再次刺激了自由基含量上升,从而加重脂质过氧化损伤[18]。因此冠心病病人经介入手术治疗后,伴有糖代谢异常者需合理控制血糖,稳定在正常范围内,对改善疾病预后有重要作用。此外,同时重视他汀类药物的使用,以减轻脂质过氧化作用,降低不良事件发生率。
综上所述,冠心病合并糖尿病病人介入治疗后血清脂质过氧化物水平出现明显变化,且持续时间较长,糖尿病或起到一定催化作用。

