两种不同影像学方法对卵巢癌的诊断价值比较
陈炽翔,黄丹江
(台州市第一人民医院放射科,浙江 台州 318020)
卵巢癌是临床常见的恶性肿瘤之一,其在女性生殖系统肿瘤中的患病率居于第3位,且其患病率在近年来呈现逐年升高趋势,手术是目前临床治疗的主要方法之一,已有研究报道卵巢癌患者早期术后5年生存率较高[1]。由于卵巢位置较深,发病早期并无典型的临床表现,同时部分患者临床就诊时已属于晚期,使得其预后状况较差,其死亡率在女性生殖系统恶性肿瘤中居于首位。因此,有效提高早期鉴别及诊断卵巢肿瘤的性质,为后期指导临床治疗方案的制订具有重大意义。影像学技术是目前临床诊断卵巢癌的重要方法,如计算机断层成像技术(computed tomography,CT)与核磁共振成像(magnetic resonance imaging,MRI)等均为临床常用手段,但不同影像学诊断技术各有临床优势[2]。为此,本研究通过回顾性分析台州市第一人民医院78例术前均行CT、MRI检查的卵巢癌患者的临床资料,以手术病理结果为金标准,比较上述两种不同影像学方法对卵巢癌的诊断价值。
1 资料与方法
1.1 一般资料
回顾性分析2016年3月至2018年6月台州市第一人民医院78例卵巢癌患者的临床资料,78例卵巢癌患者年龄为33~64岁,平均为(47.96±10.15)岁;体质量41~68kg,平均(59.96±6.13)kg。患者均行手术治疗,且经术后病理结果证实为卵巢癌,其中透明细胞癌5例,黏液性腺癌22例,颗粒细胞癌3例,子宫内膜样癌12例,浆液性囊膜癌36例。参照国标妇产科联盟标准[3],78例卵巢癌患者中Ⅰ期10例、Ⅱ期12例、Ⅲ期30例、Ⅳ期26例。
1.2 纳入与排除标准
纳入标准:符合卵巢癌的相关诊断标准[4];接受手术治疗,且术前均行CT与MRI检查;具备完整的临床资料,患者知情同意,获得随访者。排除标准:既往行手术或放化疗者;伴有心、脑、肝、肾等重要脏器功能不全;病情危急,预计生存期少于1个月者;存在CT、MRI检查禁忌证;伴有精神性疾病,不配合临床检查及治疗者。
1.3 方法
1.3.1 CT检查方法
CT仪器为西门子Definition as 64排螺旋CT,检查前嘱患者禁食8h,CT扫描前为了使膀胱适度充盈,嘱患者适量饮水(约800mL),以仰卧位为检查体位,先行CT平扫,扫描参数设置如下:管电压120kV,管电流210mA,矩阵512×512,层厚5mm。以全盆腔为扫描部位,扫描间隔约3mm,平扫后行CT增强扫描,准备非离子对比剂碘海醇100mL,采用高压注射器经肘静脉注入,在静脉推注后30s行增强扫描,期间行多层面和曲面重建。
1.3.2 MRI检查方法
MRI仪器为西门子avanto1.5T MRI,常规矢状位像进行定位,接着分别采用T1加权像、T2加权像轴位和矢状位成像。对扫描参数进行设置,其中T1加权像重复时间540ms,回波时间15ms;T2加权像重复时间3 600ms,回波时间90ms,以10个快速成像为回波链,间隔2mm,矩阵192×256,层厚5mm,视野28cm,激励3次。为尽可能减少患者呼吸运动和血液流速等造成的伪影,检查期间可采取呼吸补偿和流动补偿等方法。采用扎喷酸葡胺注射液20mL为造影剂,于静脉注射,行MRI增强扫描。
1.3.3 观察指标
记录CT、MRI两种不同影像学方法对卵巢癌的检出情况,并与病理结果进行对照,统计两者诊断准确率;记录CT、MRI对诊断卵巢癌分期的准确率;术后通过复诊及电话随访的形式,随访至术后12个月,记录CT、MRI对卵巢癌复发及转移的检出情况;由本院两名资深的影像科医师对两种影像学图像进行阅片及图像分析,在意见不一致时,由两人协商确定。
1.4 统计学方法
2 结果
2.1 CT、MRI诊断卵巢癌的准确率比较
根据术后病理结果,CT检查诊断卵巢癌的准确率为76.92%(60/78),MRI检查的准确率为91.03%(71/78),MRI诊断卵巢癌的准确率较CT检查明显升高,差异有统计学意义(χ2=4.76,P<0.05)。
2.2 CT、MRI诊断卵巢癌分期的准确率比较
相比CT检查,MRI检查诊断卵巢癌患者病理分期准确率(87.18% vs.69.23%)明显升高,差异有统计学意义(χ2=6.36,P<0.05),见表1。
2.3 CT、MRI对卵巢癌复发转移检出情况的比较
术后12个月,卵巢癌复发及转移者23例,MRI检查对卵巢癌复发和转移的检出率显著高于CT检查,差异均有统计学意义(均P<0.05),见表2。
2.4 CT、MRI诊断卵巢癌的影像学图像分析
影像学图像显示方面,相比CT检查,MRI显示卵巢癌病灶细节方面更具优势,MRI对肿瘤分隔、壁结节、囊性病变、实性病变的显示率均明显优于CT(均P<0.05),见表3,见图1。
表1CT、MRI对诊断卵巢癌分期的准确率比较 [n(%)]
Table 1 Comparison of the accuracy of CT and MRI in the diagnosis of ovarian cancer staging [n(%)]
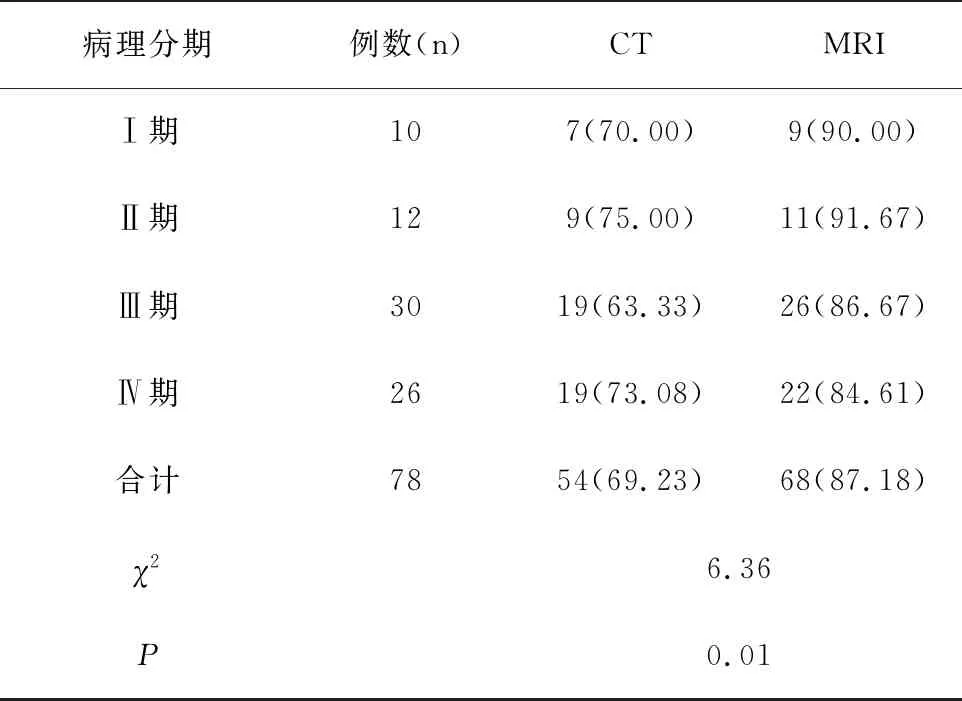
病理分期例数(n)CTMRIⅠ期107(70.00)9(90.00)Ⅱ期129(75.00)11(91.67)Ⅲ期3019(63.33)26(86.67)Ⅳ期2619(73.08)22(84.61)合计7854(69.23)68(87.18)χ26.36P0.01

表2 CT、MRI对卵巢癌复发转移检出情况的比较 [n(%)]
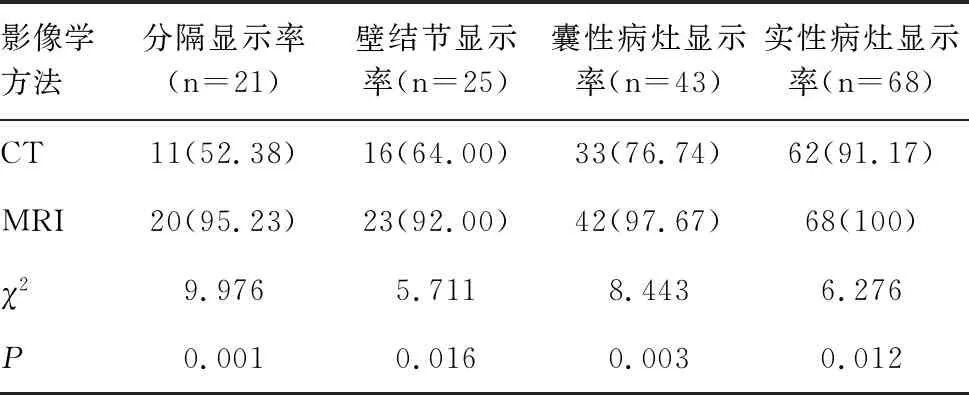
表3 CT、MRI诊断卵巢癌图像显示情况的比较 [n(%)]
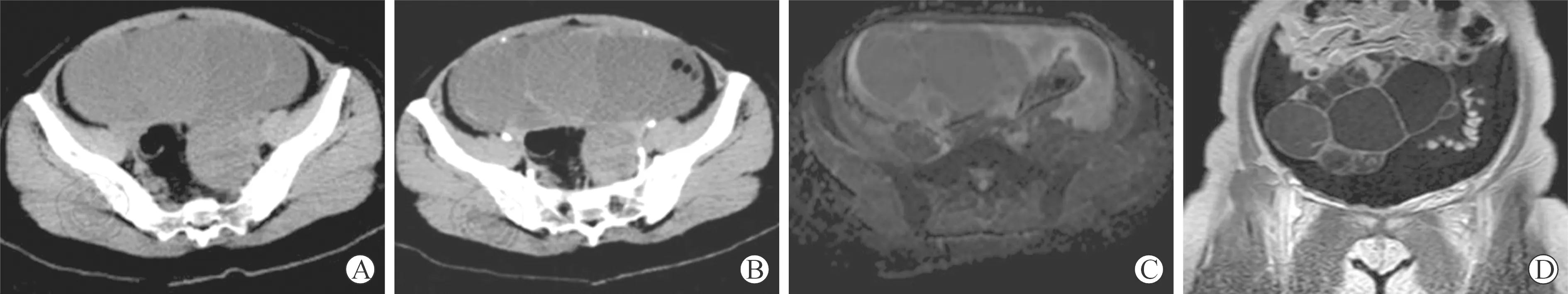
注:图A为卵巢癌患者CT平扫图像,所示盆腔囊性肿块,且出现分隔;图B为患者CT增强扫描图像,所示分隔处明显强化;图C、D为患者MRI图像,所示病灶为囊性,出现壁结节,且存在强化特征,提示MRI对卵巢癌病灶的细节显示明显优于CT。
图1卵巢癌患者CT、MRI图像
Fig.1 CT and MRI images of patients with ovarian cancer
3 讨论
3.1 CT与MRI是诊断卵巢癌的常用影像学手段
近年来,卵巢癌已成为严重威胁女性生命安全的一种常见恶性肿瘤,其患病率及死亡率均较高,使得患者预后状况较差。由于肿瘤早期并无典型的症状表现,早期确诊难度较大,使得临床误诊率及漏诊率较高,且治疗后易出现肿瘤复发、转移,对患者的生命健康造成极大危害。病理活检是目前临床诊断卵巢癌的重要方法,除此之外,CT、MRI等影像学检查是临床常用的诊断方法。随着医学影像学技术的不断提高及检查仪器的不断改进,近年来有关CT与MRI对卵巢癌诊断价值的研究报道逐渐增多,这两种影像学诊断技术对卵巢癌的诊断均具有良好的应用价值。
3.2 CT与MRI对卵巢癌的诊断各有优势
既往研究认为,CT检查便捷且迅速,可有效辨别肿瘤成分,判断是否为原发肿瘤,同时可较好地显示肿瘤转移状况[5]。但有研究表明,CT在鉴别及诊断卵巢癌方面虽具有一定的临床优势[6],但不免存在一定不足,如检查中仅呈现横断图像,且仅有一个X线吸收系数为成像参数,因此在临床应用中受到一定限制。相比CT,MRI在准确诊断卵巢癌病理分期和肿瘤复发、侵犯、转移等方面的优势更为明显,因此已有诸多研究认为MRI对卵巢癌的诊断价值明显优于CT[7],但目前有关这两种影像学复发诊断卵巢癌的差异方面仍看法不一。而随着近年来临床医师对影像学技术操作水平的不断提高,采用CT、MRI临床诊断卵巢癌准确率方面亦会随之升高。既往研究表明,采用CT检查,可准确定位盆腔各脏器解剖结构与肿瘤具体部位,且可较好地显示肿瘤囊实性特征,亦能较好地显示肿瘤与周围器官组织的侵犯和淋巴结转移状况,但其成像参数较少,且仅提供横断面图像[8];而采取MRI检查,其较CT则具有多层面、多方位成像的优势,对卵巢结构及异常病变情况可较好地显示,因此可较好地判断肿瘤结构及分期状况,且具有高对比分辨率的优势,可为临床诊断提供肿瘤与邻近正常组织关系的重要信息,有助于临床医师术前评估患者手术难度及预后状况。
3.3 MRI较CT在准确诊断卵巢癌临床分期及复发转移上更具优势
本研究以术后病理结果为依据,结果发现CT检查对诊断卵巢癌的准确率为76.92%(60/78),MRI检查的准确率为91.03%(71/78),与既往研究报道的诊断准确率基本一致[9]。结果显示,MRI诊断卵巢癌的准确率较CT检查明显升高。此外,相比CT检查(69.23%),MRI检查诊断卵巢癌患者病理分期准确率(87.18%)明显升高,与既往研究报道的病理分期诊断准确率基本相符[10]。术后12个月,卵巢癌复发及转移23例,MRI检查对卵巢癌复发和转移检出率显著高于CT检查。其次,从影像学图像显示方面上看,相比CT检查,MRI显示卵巢癌病灶细节方面更具优势。结果表明,与CT影像学技术相比,MRI在临床诊断卵巢癌、病理分期及肿瘤复发转移方面的优势更为明显。病理分期是目前对卵巢癌进行分期的重要依据,但随着影像学诊断技术的迅速和便捷性,该项技术在初步评估卵巢癌患者临床分期方面具有重要价值,且MRI对卵巢癌的分期评估价值明显优于CT,但不排除存在假阴性及假阳性的可能性。分析其原因,可能是由于双侧肿瘤紧贴而误诊为单侧肿瘤,容易将对侧卵巢出现囊肿误诊为双侧肿瘤。从这点上看,术后病理分期仍是临床重要诊断依据,即MRI的诊断结果不能取代术后病理分期结果,因而临床上在影像学诊断的同时,仍应根据术后病理分期进一步明确肿瘤的分期情况。
综上所述,CT与MRI对卵巢癌的诊断各有优势,但相比CT,MRI在准确诊断卵巢癌临床分期及复发转移上的效能更高,对病灶细节的显示更有价值,因此具有较高的临床应用价值。

