高炉内兰炭与焦炭之间的交互作用
边城, 刘燕军, 刘迎立, 王京彬, 罗明锁, 佘雪峰
(1.北京科技大学钢铁冶金新技术国家重点实验室,北京100083;2.德龙钢铁有限公司,河北 邢台054009)
目前,由于生产优质冶金焦的炼焦煤资源紧缺问题越来越严重,同时焦炭价格始终居高不下,寻找能够适应高炉生产的焦炭替代品仍然是当今研究的热点.随着高炉喷吹煤粉工艺的成熟,也有许多企业将兰炭作为喷吹燃料吹入高炉[1-4],并且取得良好的经济效益;一些学者研究兰炭代替焦粉运用于烧结[5];同时兰炭还可以作为炼焦煤的改性原料运用于炼焦[6].但是将兰炭作为焦炭加入高炉的研究较少,因此有必要研究兰炭的加入对焦炭的影响.同时氧气高炉炼铁工艺日益成熟[7-10],氧气高炉全氧操作能够增加煤比、降低焦比、对含铁原料的质量要求降低,实现钢铁行业的节能减排和可持续发展[11-13],由于煤气成分发生较大变化,需探索新工艺下焦炭性能变化规律[14-16].
兰炭是一种中低温碳化处理的半焦产品,其化学成分和结构更接近高炉冶金用焦,具有价格低廉固定碳含量高、灰分低、多气孔、化学活性高等特点,但是其反应性较高,反应后强度较差[17-20].本实验用热重分析仪探究兰炭与焦炭之间作用;并且模拟氧气高炉条件将兰炭与焦炭混合加入,探究兰炭对焦炭的影响,为其在高炉中运用提供参考.
1 实 验
1.1 实验原料
实验原料为某大型钢厂提供的焦炭和新疆哈密地区的一种块状兰炭,其工业分析见表1.

表1 原料的工业分析和元素分析Table 1 Industrial analysis and elemental analysis of raw mateials
1.2 实验装置
实验由2部分组成,第1部分为对CO2条件下焦炭和兰炭的反应性进行热重检测以及两者交互作用的探究;第2部分为模拟氧气高炉混合气氛条件探究兰炭和焦炭之间交互作用的影响.
在热重实验中,采用进口TA热重分析仪(SDTQ600,美国)来测定单一气氛条件下焦炭和兰炭的反应性.炉体最高温度为1400℃,最大升温速率为50℃/min,精度为0.0001 mg.实验过程中热重分析仪自动记录样品质量,反应时间和温度,实验结束后数据处理可以得到TG(失重率)、DTG(失重速率)曲线.
模拟高炉气氛条件实验,采用自主设计的实验装置来测定混合气氛(实际高炉)条件下焦炭和兰炭的反应性.具体实验装置如图1所示.高温合金管的最高使用温度是1200℃,采用内径为80 mm,高度1200 mm的刚玉管作为反应器.反应器底部铺一层高铝球,使反应气体在整个反应管截面上可以均匀分布,将选取的焦炭放置在高铝球上部.该实验装置,能够实现 CO、CO2、H2、H2O 和 N2多种气体下的焦炭气化反应,加热元件采用硅钼棒,控制柜能够设定多段温度,以实现温度的程序控制.
1.3 实验方法
1.3.1 热重实验
通过热重实验探究CO2条件下焦炭和兰炭的反应性.实验前将所选取的原料破碎至粒度小于150 μm的粉末,然后每个样品取约10 mg均匀地分散在氧化铝坩埚中,并以10 K/min和20 K/min的升温速率分别从室温加热到1100℃,直到样品质量没有进一步的变化为止.以60 mL/min恒定的流速通入CO2气体.在每次实验前使用空盘单独的空白运行,进行基线校准,以确保实验数据的准确性.
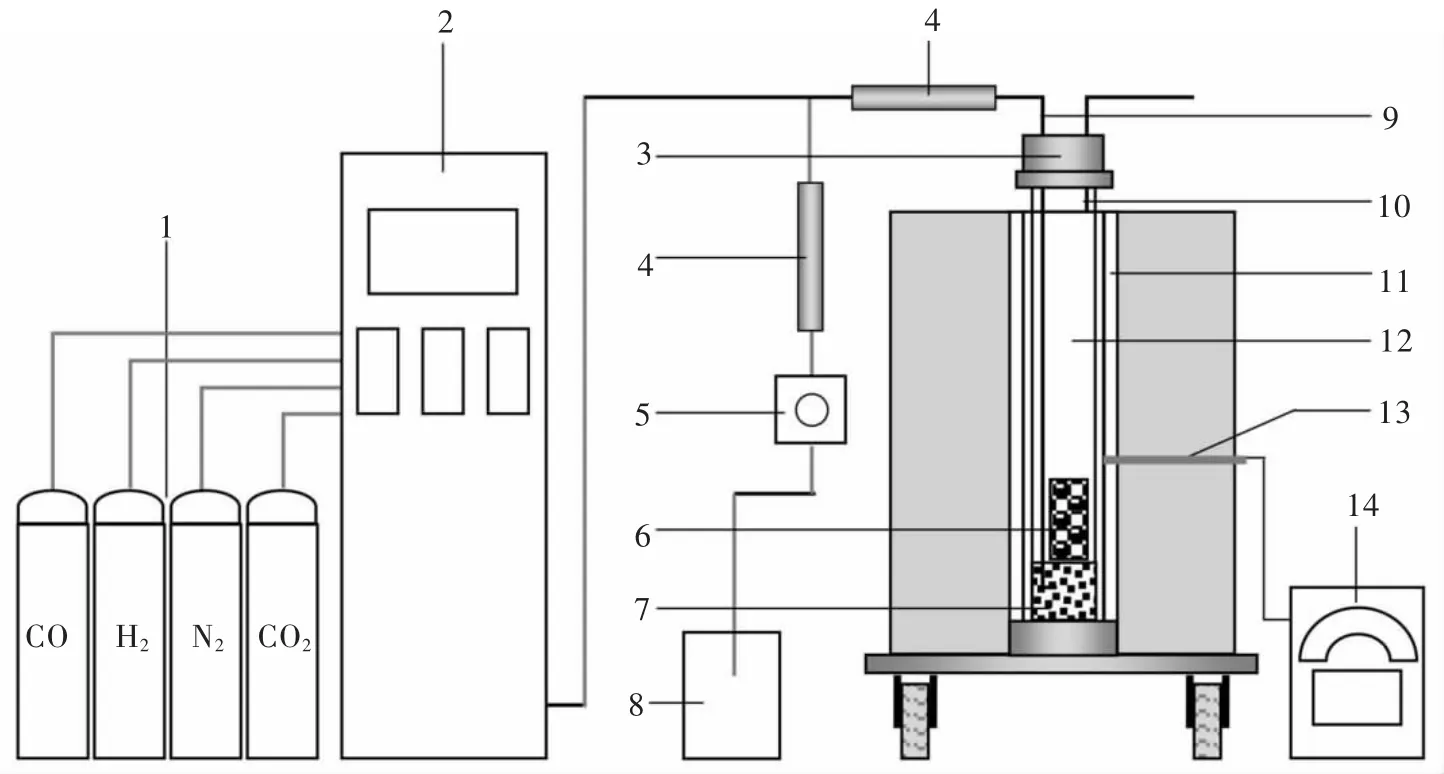
图1 高温气化反应装置Fig.1 Experimental facility
1.3.2 模拟高炉实验
为了探究模拟高炉气氛条件下兰炭和焦炭的交互作用,实验选取粒度为20~23 mm范围的焦炭和兰炭按照成分为100%焦炭和50%焦炭+50%兰炭配料,分别记为Case1和Case2,配料后装入石墨坩埚.为了模拟实际高炉气氛条件,设定炉温应当覆盖高炉内焦炭气化所涉及的全部温度,所以本实验的升温制度为:炉料从室温升温到900℃的升温速率为12℃/min,热储备区的温度范围为900~1100℃,升温速率为2℃/min,温度1100~1200℃为6℃/min.结合高炉内不同区域的气体成分,设定不同温度区间对应着不同气体成分,如表2所列.
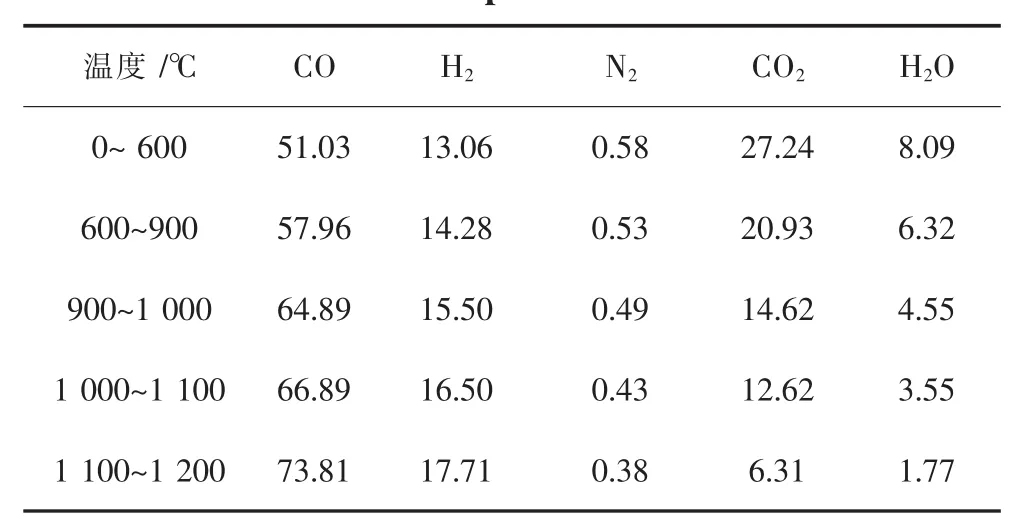
表2 气体成分和温度之间关系/%Table 2 Relationship between gas composition and temperature/%
1.4 评价指标
1)兰炭与焦炭交互作用评价方法
样品a、样品b失重率分别可以表示为:
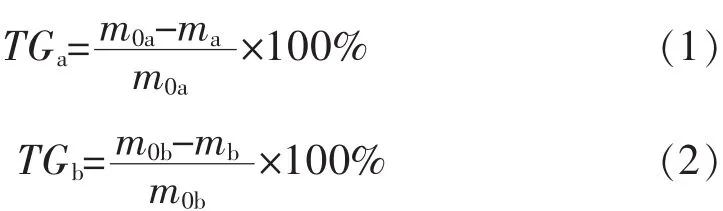
式(1)与式(2)中,ma为样品 a 任意时刻质量,mg;mb为样品b任意时刻质量,mg;m0a为样品a初始样品质量,mg;m0b为样品b初始样品质量,mg.
若样品为a和b混合物,且a和b之间无交互作用,则其失重率可表示为:
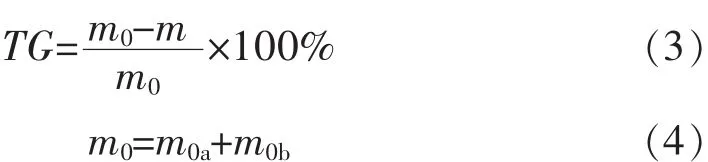
式(3)中,m0为初始样品质量,mg;m为任意时刻总样品质量,mg;


由式(1)和式(2)经推导可得:记m0a=m0×A,m0b=m0×B,并将式(5)、式(6)代入
式(3)、式(4)整理可得理论TG计算公式:
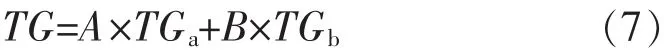
式(7)中,A为a占总样品质量,%;B为b占总样品质量,%.
2)反应性及反应强度
将反应后的焦炭装入Φ130 mm×170 mm的I型转鼓内,以20 r/min的转速转30 min,转数为600转.采用Φ10 mm圆孔筛筛分、称量并记录筛上物质的重量,以大于10 mm粒级焦炭占反应后残余焦炭的质量百分数表示焦炭的反应后强度.计算公式如式(8)、式(9)所示:
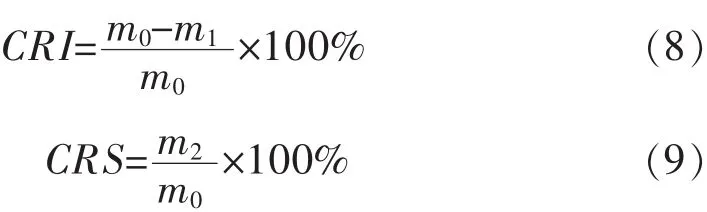
式(8)、式(9),中CRI为焦炭反应性,%;CRS为焦炭反应后强度,%;m0为反应前焦炭试样质量,g;m1为反应后残余的焦炭质量,g;m2为转鼓后>10 mm粒级的焦炭质量,g.
2 结果与讨论
2.1 CO2气氛条件下焦炭和兰炭的反应性

图2 焦炭和兰炭与CO2反应的TG曲线Fig.2 TG curve of Coke and semi-Coke reacting with CO2
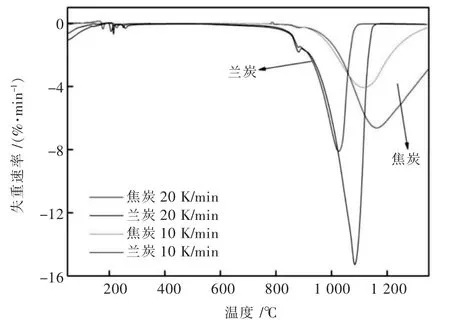
图3 焦炭和兰炭与CO2反应的DTG曲线Fig.3 DTG curve of Coke and semi-Coke reacting with CO2
焦炭和兰炭的失重率曲线如图2所示,对失重率求导可得焦炭和兰炭的失重速率曲线,如图3所示.由图2可知,升温速率为10 K/min时,温度在800℃之前兰炭失重率达到10%,而焦炭在800℃之前变化很小,这是由于兰炭在生产中热解不够完全,进入高炉后进一步发生热解.兰炭的DTG曲线在870℃出现第1个峰值,这是由于兰炭的反应阶段发生变化,由第1阶段的热解反应变为第2阶段的热解和气化耦合反应.温度在1050℃时,兰炭基本反应完全,而焦炭反应率不到20%.升温速率为20 K/min时,在800℃之前,兰炭失重曲线基本和10 K/min的失重曲线重合,说明在800℃之前升温速率对兰炭的热解无影响.但焦炭和兰炭的开始反应温度均增加,反应结束后焦炭的失重量也相对减少.这是由于升温速率增加,焦炭得到的能量总量降低,达不到开始反应需要的能量,所以反应滞后;同时升温速率增加反应时间减少导致失重量减少.
根据图2和图3可以得到焦炭和兰炭与CO2反应的特征参数,如表3所列.兰炭的最大失重速率远高于焦炭.升温速率的增加,燃料的开始反应温度和最大失重率速率温度都增加,这时兰炭的平均反应速率也增加.2种升温速率下,焦炭在温度为1350℃时未完全反应,而兰炭则完全反应.由此可见兰炭的反应性明显强于焦炭.
2.2 热重分析焦炭和兰炭的交互作用
通过热重实验得到混合料 (50%焦炭+50%兰炭)在10 K/min、20 K/min条件下的实际TG和DTG曲线,再根据图2中焦炭与兰炭的热重数据,由式(7)计算获得样品的理论TG和DTG曲线,如图4与图5所示.
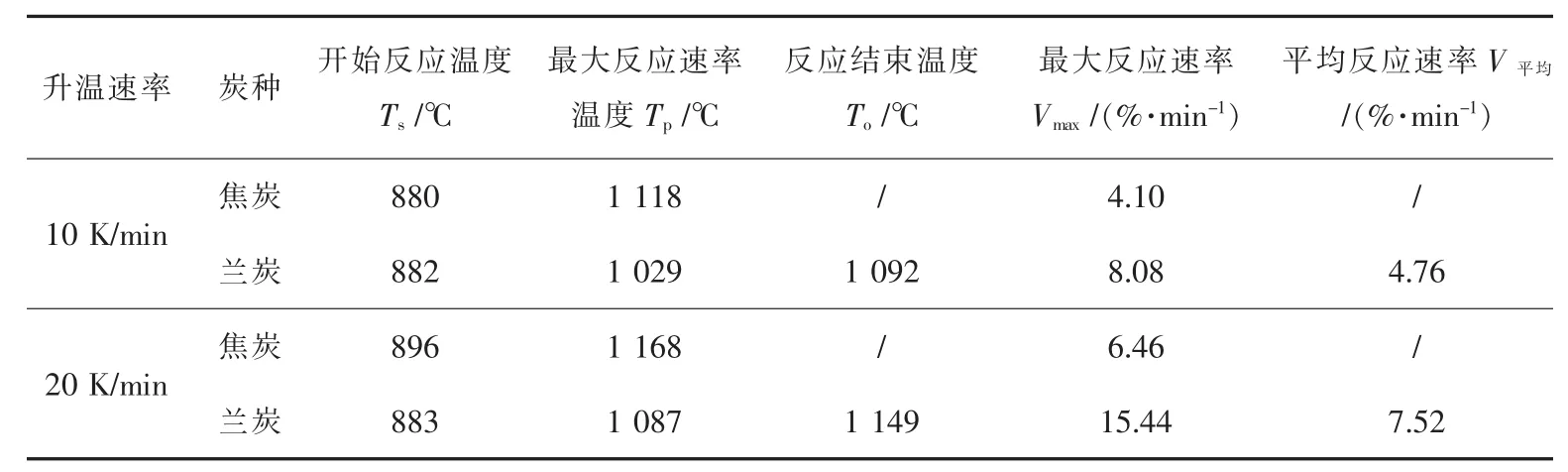
表3 焦炭和兰炭与CO2反应的特征参数Table 3 Characteristic parameters of reaction between coke and semi-coke with CO2

图4 在10 K/min升温速率下的理论TG、DTG和实际TG、DTGFig.4 Theoretical TG、DTG and actual TG、DTG at 10 K/min heating rate

图5 在20 K/min升温速率下的理论TG、DTG和实际TG、DTGFig.5 Theoretical TG、DTG and actual TG、DTG at 20 K/min heating rate
在10 K/min条件下,在850℃之前样品的理论反应和实际反应的曲线基本重合,温度在850~1150℃,实际TG大于理论TG,温度在1150~1350℃,实际TG小于理论TG,在1350℃实际反应和理论反应基本一样.样品的最大理论DTG数值大于其最大实际DTG数值,理论DTG曲线中的第2个峰DTG数值小于实际DTG曲线中的第2个峰DTG数值.说明兰炭和焦炭混合反应前期,他们之间有抑制作用,实际反应速率小于理论反应速率,随着温度增加,其抑制作用不断减弱,温度进一步增加,兰炭和焦炭变成相互促进作用,实际反应速率大于反应速率.在20 K/min条件下,在800℃之前理论曲线和实际曲线基本重合;800℃之后,实际TG曲线小于理论TG曲线,说明在800℃之后兰炭和焦炭之间存在促进作用.
为了对比分析兰炭和焦炭的交互作用,根据图4与图5的TG和DTG曲线可以得出多个反应特征量,如表4所列.由表4可知,随着升温速率的增加,混料的理论和实际开始反应温度、最大失重率温度以及反应结束剩余量均增加.这是由于升温速率增大,使得混料没有足够的时间达到反应所需的能量,从而导致反应所需的温度增加.同时,反应速率的升高使得反应进行不彻底,从而导致反应结束剩余量增加.但是由于兰炭与焦炭存在交互作用,导致实际平均反应速率大于理论平均反应速率.并且随着升温速率的增加,实际反应交互作用增强.

表4 不同升温速率下混料的实际和理论参数Table 4 Actual and theoretical parameters of the mixture at different heating rates
2.3 模拟高炉条件下兰炭对焦炭的影响
图6所示为模拟高炉气氛条件下兰炭和焦炭的反应率.由图 6可知,Case1-焦炭的反应率为5.65%,Case2-焦炭的反应率为3.84%,比Case降低了1.61%,兰炭的反应率为28.64%.由于兰炭的反应性优于焦炭,在模拟高炉气氛条件下兰炭比气煤焦更优先反应,兰炭的加入能够降低焦炭的反应率,减少焦炭在高炉中的消耗,在一定程度上对焦炭起了保护作用.
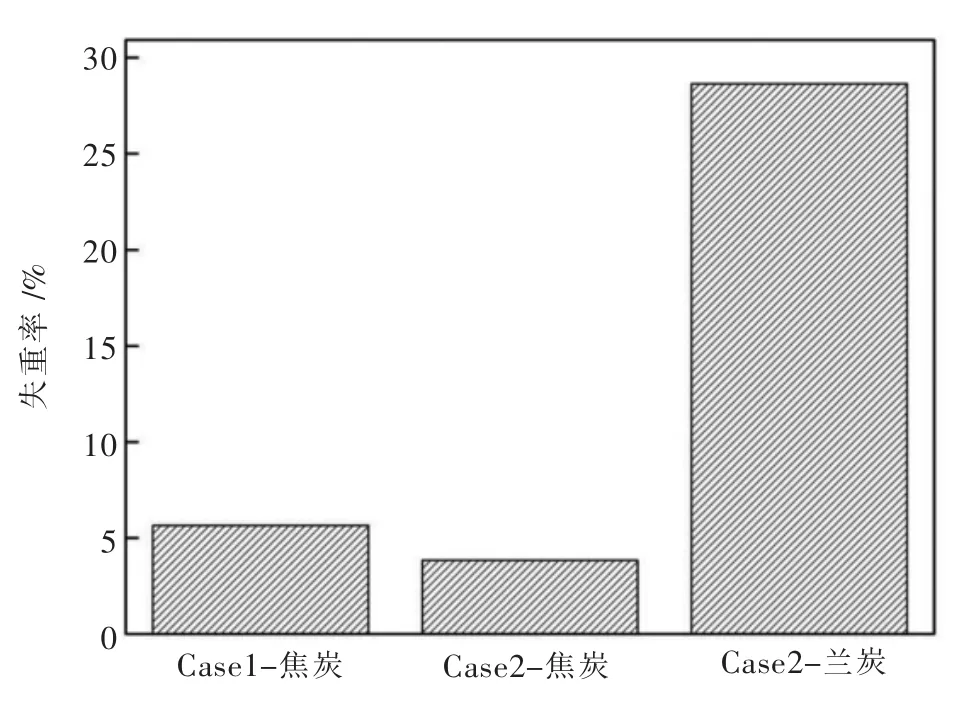
图6 模拟高炉条件下焦炭和兰炭的反应率Fig.6 Reaction rate of coke and semi-coke under simulated blast furnace conditions
焦炭的反应行为不同必然会导致其强度的差异,表5所列为反应后的焦炭转鼓实验的焦炭粒径分布.由表5可知,Case2中焦炭CSR比Case1中CSR提高1.45%,兰炭的加入会导致气煤焦CSR的提高;Case2中焦炭大于3.2 mm的焦粉含量比Case1中提高2.1%;Case2中焦炭小于3.2 mm的焦粉含量比Case1中降低2.11%;其中Case2中焦炭小于0.6 mm的焦粉含量比Case1中降低2.86%,兰炭的加入降低小颗粒焦炭的量.
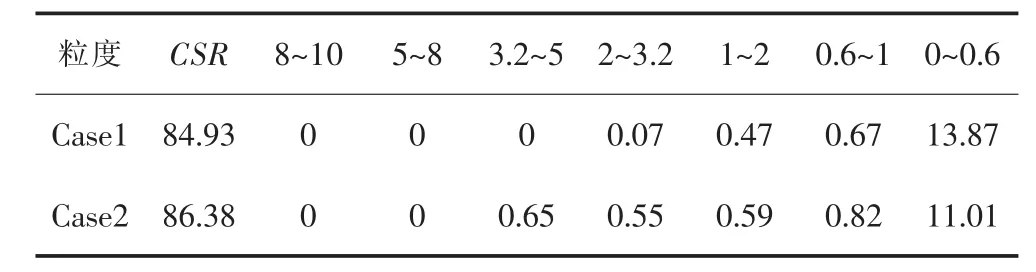
表5 转鼓实验后焦炭粒径分布/%Table 5 Particle size distribution of gas coal after drum test/%
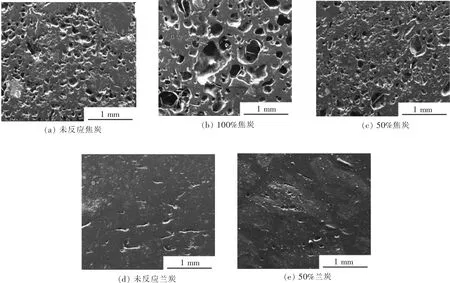
图7 焦炭和兰炭反应前后的微观形貌变化Fig.7 Microscopic morphology changes before and after reaction of coke and semi-coke
反应前后焦炭与兰炭微观结构如图7所示,可以看出未反应焦炭气孔分布较为均匀且以小气孔居多(图 7(a));但是在 Case1混料条件下,由于焦炭与煤气中H2O和CO2的气化反应,焦炭的孔径增大(图7(b)).同时由于气孔壁的反应导致焦炭出现串孔现象,对其强度产生不利影响.在Case2混料条件下,由于兰炭的反应性比焦炭要好,CO2和H2O优先于兰炭反应,导致Case2炉况下的焦炭的孔隙率和大孔径数目比Case1要小(图7(c)),气孔壁消耗较焦炭不易破碎,强度增加.反应后兰炭的孔径和孔隙(图 7(e))相较反应前(图 7(d))相比有略微的增加.由此可知,兰炭的加入能够保护焦炭,降低焦炭的反应和减少气孔率,使焦炭的强度增加,有利于焦炭在高炉中的运用.
兰炭和焦炭反应前后平均孔径如图8所示,对比反应前后平均孔径可以看出,Case1和Case2两种混料条件下反应后焦炭的平均孔径均增大,但Case2中焦炭平均孔隙比Case1中减小0.75 μm;而兰炭在反应后其平均孔径也略微增加但不明显.可以得知兰炭的加入能够降低焦炭的平均孔径,减少大孔的数量,从而增加焦炭的强度;同时兰炭本身平均孔径变化不明显,对其本身强度影响不大.
3 结 论
1)在CO2气氛条件下,兰炭反应性优于焦炭.兰炭在整个反应过程中出现2个DTG峰,第1个DTG峰是由于2次热解反应,第2个DTG峰是由于兰炭热解与气化耦合反应.
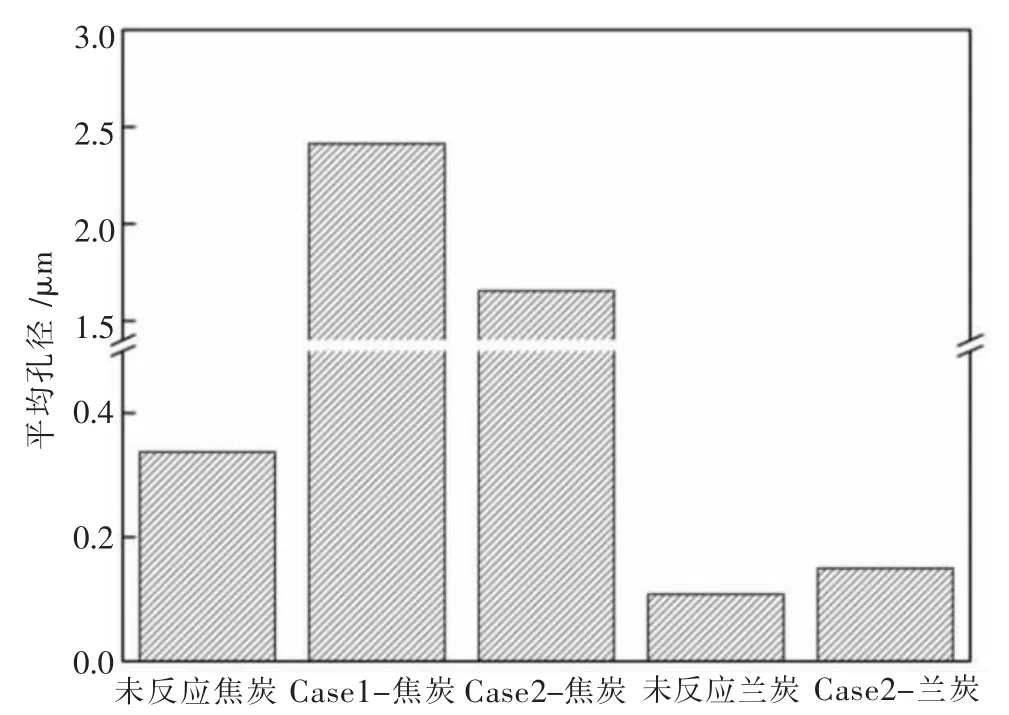
图8 反应前后焦炭和兰炭平均孔径分布Fig.8 Average pore size distribution of coke and semi-coke before and after reaction
2)兰炭与焦炭之间在800℃之前没有交互作用,这主要是因为这一阶段只有兰炭发生热解反应.温度在800℃之后兰炭与焦炭之间存在交互作用,并且在20 K/min的升温速率下交互作用要比10 K/min更强.
3)模拟高炉实验中,兰炭的加入能够降低焦炭的反应率,降低焦炭的粉化,从而对焦炭起到保护作用.兰炭能够降低煤气中CO2和H2O对焦炭气孔壁的侵蚀作用,降低气孔率.兰炭的加入能够降低反应后焦炭的平均孔径,改变焦炭的孔径分布.

