色素上皮衍生因子、血管内皮生长因子及其比值预测子痫前期的价值
戴 蕾 赵丽娜 董 武
子痫前期(PE)对母亲及胎儿均会产生负面影响,是孕妇围生期死亡的主要原因,并可导致包括脑瘫、新生儿呼吸窘迫综合征在内的多种不良胎儿结局[1~3]。目前PE的病因尚未明确,其发生、发展可能与肥胖、高血压、糖尿病等多种危险因素相关[1]。研究表明,VEGF与PEDF间的不平衡是PE发病的重要因素之一[4]。PEDF是具有抗增殖和促凋亡活性的内源性血管生成抑制剂,VEGF是一种二聚体蛋白,可促进血管新生,还能增加血管的通透性[5,6]。目前应用PEDF及VEGF预测PE发生的相关研究相对较少,其应用价值尚未十分明确。因此,本研究通过比较PE孕妇与正常孕妇的临床资料和孕早期血清PEDF、VEGF水平及PEDF/VEGF值等情况,以分析其中影响PE发生的独立危险因素及其对PE发生预测的诊断效能。
资料与方法
1.研究对象及分组:将2016年1月~2018年1月于笔者医院行早期产检并分娩的398例孕妇为研究对象。纳入标准:①单胎妊娠;②规律产检;③临床资料完整。排除标准:①既往有高血压病史;②合并严重心脏、脑、肾脏疾病;③合并自身免疫系统疾病;④伴全身感染性疾病;⑤伴严重精神-神经系统疾病。本研究获得笔者医院伦理学委员会批准同意,全部孕妇均对研究知情,并在知情同意书上签字。依据妊娠结局和《妊娠期高血压疾病诊治指南(2015)》中PE的诊断标准[7]:①妊娠20周后出现血压升高,收缩压≥140mmHg(1mmHg=0.133kPa)和(或)舒张压≥90mmHg并伴有尿蛋白≥0.3g/24h或尿蛋白/肌酐≥0.3或随机尿蛋白≥(+)等情况中的任一种;②无蛋白尿但伴有以下任意一种的心脏、肺、肝脏、肾脏等重要靶器官损害,或伴血液系统、消化系统及神经系统的异常,或累及胎盘-胎儿等,将398例孕妇中确诊为PE的86例孕妇归为子痫前期组,剩余的312例正常孕妇归为对照组。
2.临床资料分析:收集两组孕妇的年龄、孕次、产次、BMI和血糖异常人数情况。
3.血清指标检查:抽取两组孕妇孕早期(10~12周)的空腹静脉晨血4ml,置于无抗凝剂的试管中,待其自然凝固30min后,在4℃环境下以3000r/min的转速离心处理10min,收集血清,置于-80℃的冰箱中保存备用,采用ELISA法检测血清中的sFlt-1、PLGF、VEGF及PEDF水平,并计算PEDF/VEGF值,仪器及试剂盒为深圳晶美生物有效公司产品,操作过程严格按照产品说明书进行。
结 果
1.两组孕妇临床资料的比较:两组孕妇年龄、孕产次相比较差异无统计学意义(P均>0.05),子痫前期组的BMI值及血糖异常人数明显高于对照组(P均<0.05),详见表1。
表1 两组孕妇一般资料的比较
2.两组孕妇孕早期血清sFlt-1及PLGF水平的比较:子痫前期组孕早期的sFlt-1高于对照组(P<0.05),PLGF低于对照组(P<0.05),详见表2。

表2 两组孕妇孕早期血清sFlt-1、PLGF水平的比较
3.两组孕妇孕早期血清PEDF、VEGF水平及PEDF/VEGF值比较:子痫前期组的PEDF及PEDF/VEGF值均明显高于对照组(P<0.05),VEGF明显低于对照组(P<0.05),详见表3。
表3 两组孕妇孕早期血清PEDF、VEGF水平及PEDF/VEGF值比较
4.PE发生的多因素分析:多因素Logistic回归分析显示sFlt-1、PEDF、PEDF/VEGF值及BMI均是PE的独立危险因素,而PLGF及VEGF则是其保护因素,详见表4。
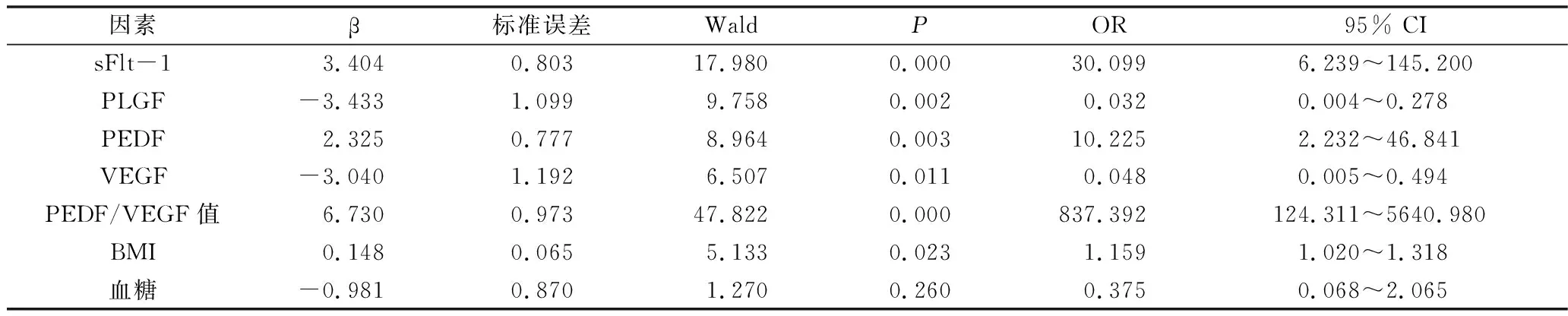
表4 PE发生的多因素分析
5.不同指标预测PE的ROC曲线分析:ROC曲线分析显示,PEDF/VEGF值预测PE的AUC明显高于sFlt-1、PEDF及BMI(P均<0.05),其最佳截点为>1.4,此时其敏感度和特异性分别为83.7%和92.6%,详见图1、表5。
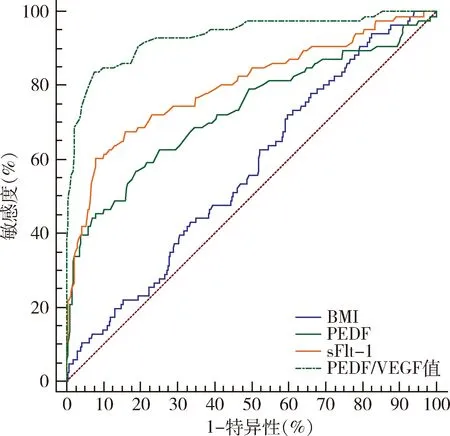
图1 不同指标预测PE的ROC曲线

表5 不同指标预测PE的曲线下面积
讨 论
PE的发病机制尚不明确,胎盘的娩出是目前PE唯一有效的治疗方式,而对有PE风险的孕妇进行筛查及早期鉴定,可及时对具有患病风险的孕妇进行适当的产前保健、管理和治疗,以降低PE的发生率[4]。PE的筛查包括评估临床风险因素如年龄、BMI及家族史等,但最近一项国际研究团队的研究项目证实临床风险因素预测PE的预测能力不高[8]。PEDF是目前已知的作用最强的血管生成抑制剂,VEGF则是最重要的血管生成调节因子[9,10]。江敏等[9]研究结果表明,孕20周前孕妇体内的PEDF水平升高,提示PEDF可能与PE的发病密切相关。陶娅玲等[11]研究则认为VEGF水平能预测PE的发生,且VEGF水平与PE的病情程度呈负相关。
根据目前对子痫发病机制的研究认为,子痫前期分为两个阶段,第一阶段是患者无明显临床症状,但胎盘血管已出现形成不良的病理表现。第二阶段是胎盘功能损伤,胎盘合成受损并释放多种循环因子,致使孕产妇出现子痫的临床症状。在第一阶段,孕妇体内就可能存在胎盘血管发育不良的病理改变,因此理论上即可从孕妇体内检测出相应的循环因子,且大量研究表明,孕早、中期的血清生化标志物等在预测子痫前期方面具有重要意义[12]。为尽早对PE进行有效预测,本研究分析了孕妇孕早期血清PEDF、VEGF水平及PEDF/VEGF值等指标预测PE的诊断效能。
PEDF是具有多种生物作用的丝氨酸蛋白酶抑制剂,是一种有效的内源性血管生成抑制剂[13,14]。研究表明,PEDF在健康孕妇的滋养细胞及血管内皮细胞内高度表达,而PEDF表达水平下降会导致死胎及胎盘血管生成失衡[15]。有研究显示,在PE组孕妇胎盘组织中的PEDF水平显著上升,提示PEDF可能与PE的发生、发展密切相关[16]。VEGF被认为是PE发病机制的重要分子系统之一,VEFG165是VEFG家族中最常见的同种型物质,其与VEGFR-2受体相结合可以增加血管通透性,使血管舒张及血管合成[17,18]。有研究表明VEGF蛋白家族在PE的病理生理过程中发挥了重要作用,是具有高度临床价值的PE的风险标志物[17]。PLGF具有诱导血管内皮细胞增殖、迁移并激活血管内皮细胞的生物学特性,可促进血管生成,并抑制内皮细胞凋亡[19]。而sFlt-1可抑制并下调PLGF的生物活性,从而影响血管壁的完整性及通透性,导致血管生成障碍,此外,其还能阻断VEGF的生物学效应,具有抑制血管生长的作用。相关研究表明,子痫前期组孕妇血清中的sFlt-1明显上升,提示sFlt-1可能参与了PE的病理生理过程。
本研究中两组的对比结果显示,PE组的BMI值、血糖异常人数、血清sFlt-1水平、血清PEDF水平及PEDF/VEGF值均明显高于对照组(P<0.05),血清PLGF和VEGF水平明显低于对照组(P<0.05);多因素Logistic回归分析显示,sFlt-1、PEDF、PEDF/VEGF值及BMI是PE的独立危险因素,PLGF及VEGF则是其保护因素。ROC曲线分析显示,PEDF/VEGF值预测PE的AUC明显高于BMI、sFlt-1及PEDF(P<0.05),其诊断的最佳截点为>1.4,此时其敏感度和特异性分别为83.7%和92.6%。结果分析认为可能与PEDF及VEGF间存在的反馈机制相关,即VEGF可与VEGF-R受体相结合,使血管内皮细胞分化,而PE孕妇体内的VEGF水平下降,会阻碍内皮细胞增生及浸润;PEDF又可抑制血管紧张素Ⅱ上调VEGF,表明PEDF是VEGF的负性调节剂,PEDF的上调会使VEGF水平降低,使胎盘内皮细胞增生、浸润不良,阻碍胎盘形成。同时,采用二者的比值能够获得更大的差异性,故PEDF/VEGF值在预测PE发生方面具有较高的诊断效能。
综上所述,孕早期的PEDF/VEGF值对预测PE的发生具有较高的诊断效能及临床价值,可用于PE的预测。但本试验为单中心、小样本研究,具有一定的局限性,因此应继续开展多中心、大样本的研究进一步证实。此外,还应对其他指标的联合检测进一步分析,以便比较其诊断效能,为临床预测PE提供高效、敏感的预测指标。

