射频消融术联合小剂量胶原酶化学溶解术治疗神经根型颈椎病的疗效评价*
幸泽艇 王 梅 张春元 章 勇 张学学 张达颖△
(1中山市博爱医院麻醉疼痛科,中山528403;2南昌大学第一附属医院疼痛科,南昌330006)
颈椎病(cervical spondylosis, CS)发病率13.76%[1],40~60岁为高发年龄,40~50岁组高于50~60岁组,且呈年轻化趋势[2]。其中,神经根型颈椎病(cervical spondylotic radiculopathy, CSR)在CS中发病率最高,约占CS的50%~60%[3]。Salemi等[4]认为CSR多为颈椎间盘突出导致的,同时Kuijper等[5]认为多数CSR病人不需要开放手术,微创治疗技术在CSR中的治疗日益成熟,正逐渐成为CSR的主要治疗方法之一。现国内临床上已经普遍使用胶原酶化学溶解术治疗颈椎间盘突出症,但围术期因髓核溶解容易出现高张期,剂量过大容易导致椎间盘高度降低等,而射频技术也用于椎间盘病变的治疗中,如何评价两者联合运用治疗CSR的效果及安全性?2005年Carlisle等提出通过应用磁共振成像 (magnetic resonance imaging, MRI) 测量突出物体积及其与椎管占比来指导手术,龚国华[6]报道了两者联合运用与单纯射频热凝术比较,采用MRI突出物体积变化来评价,部分学者采用X线[7]、CT[8]颈椎间盘高度变化来评价,而国内外暂未见报道采用MRI测量突出物部位的三维立体数据来评价该联合手术治疗方法的相关文献。故本研究试图通过利用MRI影像学三维测量联合视觉模拟评分法(visual analogue scale, VAS)、Odom评价标准评价经颈前外侧入路射频消融术 (radiofrequency ablation, RA) 联合小剂量胶原酶化学溶解术 (collagenase chemonucleolysis, CC,简称RC)治疗CSR的效果及安全性,并试图在临床推广运用。
方 法
1.一般资料
本研究经南昌大学第一附属医院伦理委员会批准后,病人自愿签署知情同意书。
CSR的诊断标准[9]:①具有较典型的神经根症状(手臂麻木、疼痛),其范围与颈脊神经所支配的区域一致,体检示压颈试验或臂丛牵拉试验阳性;②影像学检查所见与临床表现相符合;③除外颈椎以外病变( 胸廓出口综合征、网球肘、腕管综合征、肩周炎、肱二头肌腱鞘炎及肺尖部肿瘤等)所致以上肢疼痛为主的疾患。
入选标准:诊断明确的神经根型颈椎病病人;年龄20~65岁;经3个月严格保守治疗无效;病人自愿并知情同意进行本研究;能坚持完成整个治疗过程;根据胡有谷区域定位法[10],选择CSR中MRI示突出物在旁正中区(2区)或外侧区(3区)及a或b域内的病人;既往有干扰本手术治疗的病人(如硬膜外消炎镇痛药液治疗),必须经过5天洗脱期。
参考金星等[11]的排除标准:CS其他类型;突出物巨大或有明显钙化者;伴严重神经功能障碍如完全手下垂、上肢轻瘫者;椎间盘炎或椎间隙感染者;骨性椎管或侧隐窝狭窄者;椎管内肿瘤、骨关节结核者;严重凝血功能障碍者;严重过敏体质者;有明显的社会心理疾病者;高血压病人血压未控制者;糖尿病病人血糖未控制者;安装心脏起搏器者或伴有严重心功能不全者等。
所有病人ASA分级为I-II级,部分病人合并基础疾病,经过内科治疗后均能耐受局部麻醉和手术。按照纳入和排除标准筛选病人,随机数字表法进行分组,如因术中情况确实需要调整手术方式的均采用胶原酶化学溶解术,共纳入25例CSR病人行射频消融术联合小剂量胶原酶化学溶解术(RC组),30例行胶原酶化学溶解术(M组)。观察并记录病人术前(入院时)、治疗终末时及术后3~40个月的随访情况。
2.主要的仪器、材料
Somapho 1.5T超导磁共振机及PACS系统;大型C形臂机、数字减影系统;射频控温热凝仪R-2000B及穿刺针(北琪医疗科技有限公司,北京)。
3.主要的药物
注射用胶原酶600 U粉针剂(国药准字H31022658,上海乔源生物制药有限公司),造影剂:碘海醇注射液,商品名:欧乃派克(国药准字H20000592,上海通用电气药业有限公司)。
4.手术操作及嘱托
联合组(RC组):病人仰卧于DSA机床上,肩下垫一薄枕并用约束带向下绑紧肩膀以便X线显示下颈段。根据术前X线、MRI检查及术中X线动态观察,初步确认病变椎间盘,并在突出物对应椎间盘间隙对侧的胸锁乳突肌及气管间标记穿刺点。常规消毒布巾后,局部浸润后选择合适射频穿刺针,在X线监测下调整进针方向和角度,通常是与中轴矢状线成45°角,避开周围的甲状腺、迷走神经、气管、食管等器官组织,一般可顺利进入间隙直至目标位置,并经影像证实。穿刺时针尖一般位于椎间盘中后1/3、椎体后缘近突出物处,给予造影剂碘海醇0.1~0.3 ml(平均约0.2 ml左右),造影并术中诊断。根据术前影像资料、突出物大小、术中显影情况,DSA设备下再次确定穿刺深度、部位,调整针芯使其辐射范围(半径5 mm)必须为突出物组织,避免损失神经,选择射频参数,置入射频电极并测试。行感觉及运动刺激,未诱发出四肢感觉及肌肉运动异感,给予70℃ 30 s × 1次;80℃ 30 s × 1 次;90℃ 60 s × 1 次;95℃ 90 s × 2次模拟连续射频。射频结束温度下降至45~50℃后,拔出针芯。配制胶原酶600 U/1.2 ml,突出物内给予小剂量胶原酶100 U/0.2 ml,拔针按压后无出血送病房。
胶原酶组(M组):未行射频治疗,穿刺方法基本同联合组,穿刺到突出物内注射药物胶原酶200 U/0.4 ml。
围术期绝对卧床,沙袋固定颈椎。根据病人情况进行脱水消炎,术后7~10天开始佩戴颈围起床、适应性锻炼,2周后开始锻炼,先颈部活动,后力量锻炼,3月后可逐渐恢复劳动。出院后颈托护颈1~1.5月,术毕1月以卧床休息为主,术后3月随访并复查MRI。
5.评价指标
采用VAS、MRI椎间孔孔径 (intervertebral foramen diameter, IFD)、椎间盘高度 (intervertebral disc height, IDH)、突出物长度 (protrusions length, PL) 及宽度 (protrusions width, PW)、突出物面积 (protrusion area, PA)及面积治疗指数,观察手术治疗前、治疗终末、术后3至40个月随访情况并进行疗效评价。两组的术前、治疗终末、术后3月、术后6月、术后1年的VAS分别为VAS1~5。研究者观察记录时,采用双盲法,隐藏,由主刀医师向病人解释病情。
MRI图像测量:通过在影像科MRI仪器的PACS系统软件,在轴向MRI图像上椎间盘突出物最大时,测量各项指标,重复多次测量取均值,两组病人的数据由同一人进行测量。
根据Carlisle测量方法,本研究采用MRI突出物面积及其治疗指数,使用PACS系统测量治疗前与3个月后复查的MRI突出物面积,并计算突出物的治疗指数 =(治疗后突出物面积-治疗前突出物面积)/治疗前突出物面积×100%(见图1)。
根据Dabbs测量方法,采用MRI测量椎间盘高度(见图2),椎间孔孔径(见图3)、突出物长度及宽度(见图4),其中椎间盘高度IDH =(Ha+Hp)/2,Ha椎间盘前侧高度,Hp椎间盘后侧高度(见图2)。
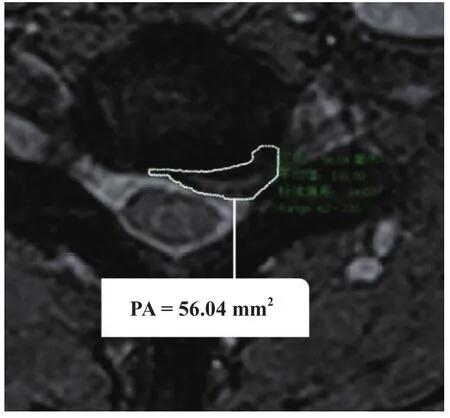
图1 突出物面积PAFig.1 Protrusion area (PA)

图2 椎间盘高度IHDFig.2 Intervertebral disc height (IDH)
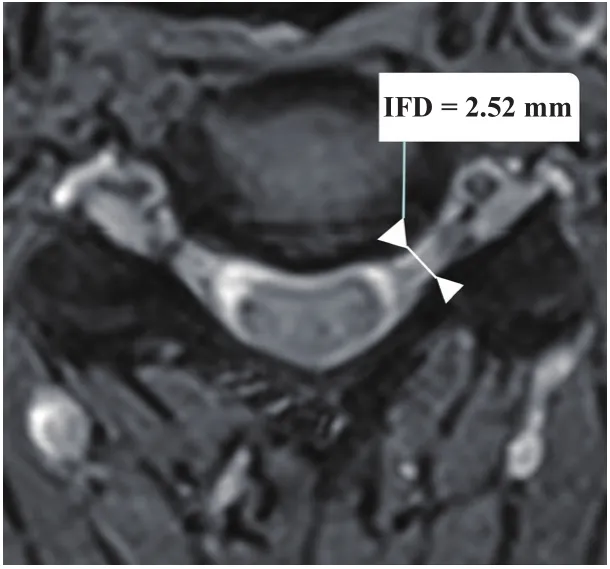
图3 椎间孔孔径IFDFig.3 Intervertebral foramen diameter (IFD)

图4 突出物长度PL及宽度PWFig.4 Protrusions length (PL) and protrusions width (PW)
Odom标准:优:无颈神经根受压症状,恢复原工作;良:仍遗留少许症状,不影响工作;可:症状明显改善,但临床检查活动仍有限制;差:术后症状与术前相比无改善或加重。术后随访,均进行评价。
6.统计学分析
应用SPSS 19.0统计软件对试验数据进行统计学分析,计量数据采用均数±标准差(D)表示,两组间比较采用t检验,重复测量资料比较采用重复测量方差分析(双因素方差分析),当资料满足球对称性等条件时可采用单因素方差分析法,两组优良率比较采用卡方检验(X2),按照α = 0.05水准,P< 0.05为差异有统计学意义。
结 果
1.本研究两组病人的性别、年龄、身高、体重、术前治疗及合并症等一般情况无统计学意义(P>0.05)。所有病人注射造影剂时颈肩臂部均能复制出原来的症状、体征,并确定责任椎间盘。胶原酶组中有一例病人胶原酶化学溶解术后第一天未按照术后医嘱及护理要求,擅自起床,致溶解的髓核急性疝出卡压神经,立即开放手术治疗,已剔除。其他所有病人术后随访,均未发现有明显并发症、后遗症。
2.两组VAS病人治疗终末、术后3月~1年时的疼痛评分较术前VAS1显著降低(均P<0.001),两组中VAS2与VAS3、VAS4与VAS5间比较无差异。术后1.5~3.5年M组随访了11人,其VAS6为2.0±2.1;RC组随访了8人,其VAS6为1.3±1.0。与M组比较,RC组VAS评分差异有统计学意义(F= 5.234,P< 0.05),各时间点均较M组同期VAS小(见表1),则整体上RC治疗后VAS更低。
3.MRI图像
(1)RC组病人术后3个月时的椎间盘高度IDH2与术前IDH1比较差异有统计学意义(P< 0.001)。下降差值= IDH1-IDH2,下降值范围为0~0.44 mm,平均下降0.15 mm (3.57%),最大下降幅度为9.28%(见表2)。与M组术后3月比较,RC组IDH下降程度更轻 (P< 0.05)。
(2)RC组病人术后3个月时的椎间孔孔径IFD2较术前IFD1显著增大(P< 0.001);与M组术后3月比较,RC组IFD无明显差异(P> 0.05,见表2)。
(3)RC组病人术后3个月时的突出物矢状位长度PL2、宽度PW2较术前PL1、PW1均显著减小(均P< 0.001);与M组术后3月比较,RC组PL、PW无明显差异(P> 0.05,见表2)。
(4)RC组25例CSR病人中,颈椎间盘突出消失0%~35%有1例,35%~75%有15例,75%~100%有9例。病人术后3个月时的突出物面积PA2比术前PA1显著减小(P< 0.001,见表2),PA1-PA2为34.29±14.91,平均治疗指数 =70.49%。与M组术后3月比较,RC组PA无明显差异 (P> 0.05)。
4.治疗效果
所有病例于微创手术后1年内进行电话等随访,部分病人随访达40个月,均采用Odom标准评定疗效,计算优良率(见表3)。与M组比较,RC组在各时间点的优良率均更高,差异有统计学意义。随访18~40个月的两组病人,胶原酶组共11人(优5人、良3人、可2人、差1人),优良率72.7%,联合组共8人(优5人、良2人、可1人、差0人),优良率87.5%,RC组优良率更高(P< 0.05)。
讨 论
椎间盘射频多数是靶点射频,单一使用时突出物消融较小,而单纯使用胶原酶溶解突出物,常常采用较大剂量,髓核溶解后张力容易出现高峰期,疼痛症状加重,为避免这些不足,近年来张达颖团队报道了采用射频消融术联合小剂量胶原酶化学溶解术治疗腰椎间盘突出症取得了很好的效果,该团队中Wang等[12]报道了RC治疗CSR术后7天情况,但本人前期研究发现目前不能全面、系统地评价CS损害程度及治疗效果,尤其在评价治疗CSR新开展的技术、方法[13]。因此本研究综合分析后采用包括MRI影像学等多参数综合评价该方法治疗CSR的效果及安全性,较Wang延长随访时间。
表1 病人术前、治疗终末和术后3月、6月、1年VAS评分(D)Table 1 VAS scores before surgery, at the end of treatment, 3 months, 6 months, one year after surgery (D)

表1 病人术前、治疗终末和术后3月、6月、1年VAS评分(D)Table 1 VAS scores before surgery, at the end of treatment, 3 months, 6 months, one year after surgery (D)
*P < 0.001,与同组术前相比,compared with before operation;#P < 0.05,与M组术后同期比较,compared with the same period after operation in M group.
组别G术前(V1)Before operation治疗终末(V2)Terminal treatment术后3月(V3)Three months post-operation术后6月(V4)Six months post-operation 1.0±0.6*#(n = 23)1.6±1.0*(n = 25)RC 4.1±0.4(n = 25)术后1年(V5)One year post-operation M 4.2±0.5(n = 30)2.1±1.3*(n = 30)1.3±1.0*(n = 30)1.4±1.0*(n = 28)0.7±0.7*#(n = 25)0.7±0.5*#(n = 25)1.0±0.7*#(n = 24)
表2 病人术前、术后3月椎间孔孔径、椎间盘高度、突出物矢状位长度、宽度的情况(D)Table 2 Intervertebral foramen aperture, intervertebral disc height,f protrusion lenght and width before operation and three months post-operation (D)

表2 病人术前、术后3月椎间孔孔径、椎间盘高度、突出物矢状位长度、宽度的情况(D)Table 2 Intervertebral foramen aperture, intervertebral disc height,f protrusion lenght and width before operation and three months post-operation (D)
*P < 0.001,与同组术前的比较,compared with before operation,#P < 0.05,与M组术后3月的比较,compared with three months after post-operation of M group.
术后3月Three months post-operation椎间盘高度mm Intervertebral disc height, IDH 4.22±0.42 3.52±1.36* 4.20±0.42 4.05±0.40*#椎间孔孔径mm Intervertebral foramen aperture,IFD M组Group M (n = 30) RC组Group RC (n = 27)术前Before operation术后3月Three months post-operation术前Before operation 0.72±1.09 3.13±0.83* 0.65±1.11 3.06±0.67*突出物长度mm Protrusion length, PL 8.52±1.26 3.96±1.55* 8.32±0.96 4.02±1.35*突出物宽度mm Protrusion width, PW 5.87±1.47 2.56±0.63* 5.97±1.77 2.61±0.56*突出物面积mm2 Protrusion area, PA 50.05±25.20 13.54±9.87* 48.65±23.08 14.36±10.59*
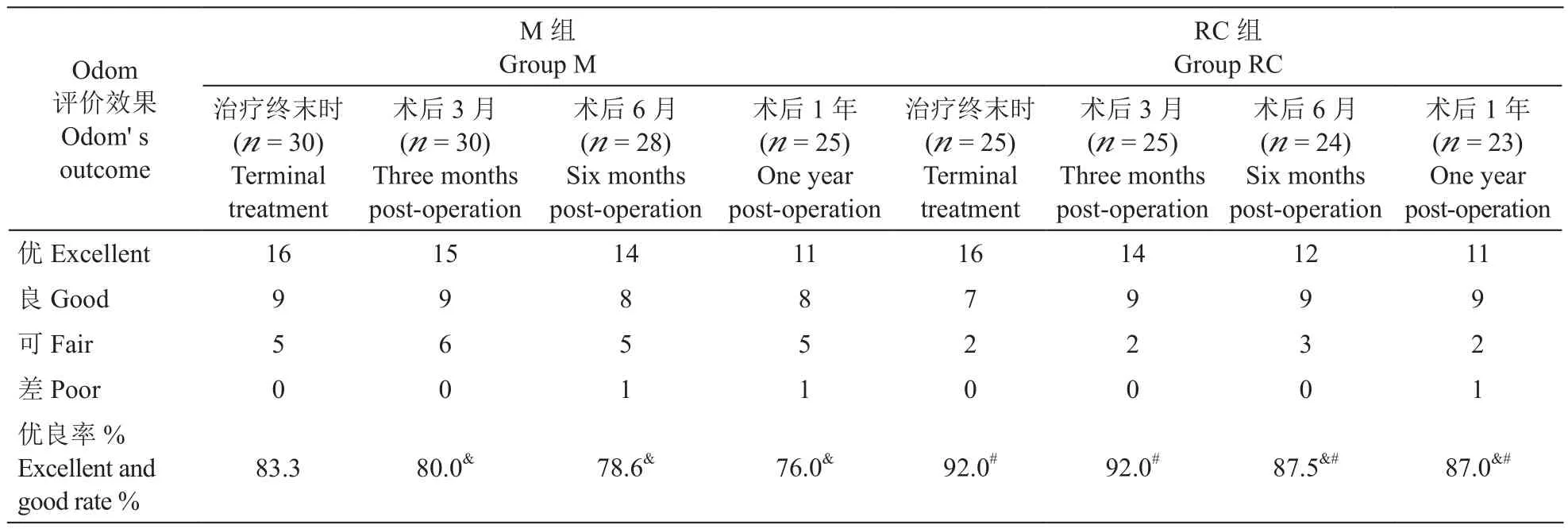
表3 病人治疗终末时至术后1年Odom评价Table 3 Evaluation of Odom at the end of treatment to one year post-operation
Okazaki等[14]采用X线对23例椎间盘切除钛网植入术病人测量责任椎间盘相邻的上、下椎间盘高度,术后1月与术前比较分别为6.5±0.8 mm、6.6±0.8 mm 和 6.4±1.0 mm、6.5±1.1 mm。曾岩等[15]随访66例颈椎前路融合术病人10.5年,结果相邻节段不稳定发生率为72.7%,有明显颈部症状者占40.9%。Bydon等[16]对888例行前路颈椎间盘切除椎间融合术(anterior cervical discectomy and fusion, ACDF)病人进行平均94个月的术后随访,发现108例病人术后出现相邻节段病变(Adjacent segment disease, ASD),并需二次手术治疗。开放手术均提示相邻椎间盘有退变的情况。与单纯胶原酶化学溶解术比较,射频消融术联合小剂量胶原酶化学溶解术治疗CSR椎间盘高度下降更小。与之相一致,本研究采用射频消融术联合小剂量胶原酶化学溶解术治疗CSR,虽然病人术后3个月时的椎间盘高度与术前比较差异有统计学意义,但是病人3个月时的椎间盘高度4.05±0.40 mm较治疗前4.20±0.42 mm,下降幅度为0%~9.28%,平均下降2.2%,相邻椎间盘高度无变化,由于MRI对软组织的测量优于X线,且无一例病人出现颈椎失稳或滑脱的,相邻椎间盘也无明显失稳、滑脱及疼痛等症状,脊柱活动基本正常。故认为该联合微创手术保留了椎间盘的高度,保留了椎间盘维持稳定作用。
本研究中利用MRI对椎间盘、突出物等软组织显示清晰的优点,比较了病人手术治疗前、后在侧隐窝处的孔径大小、突出物大小的变化情况。颈椎MRI发现术后3个月突出物长度、突出物宽度、突出物面积4.02±1.35 mm,2.61±0.56 mm,14.36±10.59 mm2均 较 治 疗 前 8.32±0.96 mm,5.97±1.77 mm,48.65±23.08 mm2显著减小,25例CSR病人3月后复查中结果为颈椎间盘突出物面积治疗指数0%~35% 1例,35%~75%有15例,75%~100% 9例,平均面积治疗指数为70.49%。CSR病人术后3月复查颈椎MRI后发现,突出物内的髓核组织信号强度(T2)显著变化,体积明显缩小甚至消失,基本解除神经根及周围组织的压迫。与1994年Maigne[17]和1997年Bush[18]采用CT评价突出物缩小率的结果比较,相对更客观、合理。本研究病人治疗3月后复查MRI发现椎间孔孔径3.06±0.67 mm较治疗前0.65±1.11 mm显著增大,基本上与2010年陈佩祥[19]等报道解剖15例正常颈椎椎间孔处神经根前后直径3.0±0.7 mm大小相当,根袖及神经根受压解除,说明RC治疗CSR有效,达到了解除突出物压迫神经根的目的。与单纯胶原酶化学溶解术比较,射频消融术联合小剂量胶原酶化学溶解术治疗CSR突出物长度、突出物宽度、突出物面积无明显差异。但与龚国华等[6]的研究比较,术前CSR突出面积大一倍 (48.65±23.08 mm2vs.24.63 ±4.24 mm2),术后3月VAS明显减轻(0.70±0.58vs.2.02±0.51),且治疗效果好(96%vs.97.5%),同时提示可以适当拓宽治疗CSR的适应症。Wang等[12]对该手术治疗效果采用VAS、JOA、MRI评价,但未采用影像学数据详细描述,尤其是椎间盘高度及侧隐窝的情况,且JOA颈椎病评价表中涉及的脊髓、躯干的参数,可能会影响该评价的效度。
本研究中采用门诊、电话随访,最长达约40个月,RC治疗对所有CSR病人均有效,术前、术后治疗终末时、术后3个月至1年的VAS评分,分别为4.18±0.46 cm、0.73±0.71 cm、0.70±0.58 cm、1.02±1.18 cm和1.25±1.67 cm,治疗后VAS评分明显降低,疼痛明显缓解稳定,与单纯胶原酶化学溶解术比较,射频消融术联合小剂量胶原酶化学溶解术治疗CSR,术后3个月至1年VAS更小。采用Odom标准评价疗效,与单纯胶原酶化学溶解术比较,射频消融术联合小剂量胶原酶化学溶解术治疗CSR在治疗终末时及3~40个月的优良率均更高。椎间孔切开术报道52~99%的成功率,但症状复发率高达30%,该技术治疗的有效性也存在争议[10]。而本研究发现术后1年内RC手术治疗优良率与治疗终末时相当,随访达1.5~3.5年RC手术治疗优良率达87.5%,说明其手术治疗效果比较好。
1996年杨述华等[20]研究发现部分病人单纯胶原酶溶解术后高涨期疼痛较术前严重,压迫神经严重,持续时间长。本研究联合微创手术治疗CSR病人,疼痛缓解快且稳定,未发现并发症或不良反应。可能减轻了椎间盘内压力,突出物充分溶解,疼痛明显缓解;同时椎间盘高度降低较小,椎间盘的退变和髓核以及纤维环所受应力相对保持稳定,相邻椎间盘无影响,未发生颈椎不稳定,该手术方式优化,病人治疗安全性及效果优良率高。目前多数学者认为其作用机制可能是:射频消融,灭活了椎间盘内外靶点处的神经炎性因子,疼痛减轻,同时热凝退变椎间盘裂隙、炎性血管,使椎间盘修复,同时胶原酶能使盘外较大的突出物溶解,减少溶解有作用的内层纤维环,稳定椎间盘的粘弹特性。推测可能是三者共同作用的结果,一是椎间盘内压力降低致使部分椎间盘回缩,二是椎间盘高度变化较小而保留颈椎间盘稳定的功能,三是突出物溶解后侧隐窝处神经根及周围组织受压减轻,改善神经周围血液循环,减轻压迫缺血导致的水肿,较少炎性渗出,减轻炎性细胞聚集及炎性反应。
综上所述,本研究采用MRI评价疗效,其对软组织分辨率高,评价更全面,结果相对更客观真实;术后VAS显著降低,Odom标准评价评分显著增加,无明显并发症,则说明RC治疗CSR是安全有效的。综合两种手术的优点,避免使用较大剂量的胶原酶,减小椎间隙高度的下降,同时保证病变部位髓核被射频消融和溶解,突出物被消除,恢复椎间孔的空间结构,避免神经根及周围组织受压。由此推测,该联合微创手术治疗CSR在效果和安全性有其自身的优势,以期在临床上推广应用。本研究也存在样本量相对较小等不足,后期继续深入研究,增加样本量并争取与其他中心共同研究,探讨此联合手术的治疗机制并为临床提供理论依据。

