机器人辅助胰腺手术中血管变异的处理方式
苏秉蔚 翁原驰 许志伟 邓侠兴
上海交通大学医学院附属瑞金医院普外科 胰腺外科中心,上海 200025
【提要】 达芬奇机器人系统目前已广泛应用于胰腺手术。胰腺手术因其手术难度大,解剖复杂,术后并发症多,围术期病死率高,成为普外科手术中的一大难点。血管变异又是外科手术中需仔细甄别、小心处理的另一项关键。生理状态下腹腔血管可存在不同表现型的血管变异,变异的血管在手术中常常会造成手术医师的困扰,导致血管损伤、围术期出血、肝脏及胆管系统缺血和继发性胆漏等手术相关风险的发生概率增加。结合既往研究和笔者所在胰腺中心手术经验,推荐在机器人胰腺手术中通过特定手术路径和技巧处理变异血管。
达芬奇机器人手术作为21世纪新的外科手术方式之一,目前已广泛应用于普外科、心外科、胸外科、泌尿外科、妇产科等多个科室。上海瑞金医院胰腺外科中心自2010年引进达芬奇机器人外科技术以来,已实施1 569例胰腺手术,其中包括495例胰十二指肠切除术(pancreato duodenectomy, PD),693例胰体尾切除术,151例胰中段切除术,130例胰腺肿瘤剜除术。胰腺手术中明确血管解剖尤为重要。生理状态下腹腔血管可存在不同表现型的血管变异,这给手术医师造成困扰,导致手术风险增加。荟萃分析显示,PD中血管变异可使损伤血管、围术期出血、肝脏及胆管系统缺血、继发性胆漏和吻合口狭窄的发生率增加[1-2],因此关注患者的血管解剖状态成为胰腺手术中必不可少的一环。达芬奇机器人不仅具有将胰腺手术视野光学放大10~20倍及合成高清3D立体图像的优势,且具备7个自由度的机械臂自动滤除颤动[3],故在血管的处理方面较传统剖腹手术更为灵活、安全。本文结合笔者所在胰腺中心的手术经验,探讨机器人胰腺手术中血管变异的识别、判断和处理方式。
一、胰腺手术中需警惕的血管变异
胰腺位于腹腔深部,与周围脏器关系紧密,且周围血管解剖极为复杂。胰腺手术常常需要采用血管显露、血管离断、血管骨骼化、血管重建等操作,因此要求术者对胰腺相关血管的解剖具有清晰的认识,对于血管处理具有准确精细的手法,对于出血、血管变异等情况具有精准果断的处理能力。血管变异是胰腺手术中常见的现象,辨识及合理处理血管变异对于胰腺手术至关重要,以下对胰腺外科几种经典术式相关的血管变异简要概述。
1.胰十二指肠切除术:常规PD切除范围包括胰头、十二指肠、胆囊、部分胃及部分空肠。手术时首先通过Kocher切口游离胰头和十二指肠,此时应注意变异肝动脉的存在。正常左、右肝动脉自起源于腹腔干的肝固有动脉分出(Hiatt Ⅰ型),约占75.7%;小部分人群的左肝动脉或副左肝动脉自胃左动脉发出(Hiatt Ⅱ型),约占9.7%;右肝动脉自肠系膜上动脉(Hiatt Ⅲ型),约占10.6%,此变异血管一般穿过肝后十二指肠韧带;左、右肝动脉分别自胃左动脉和肠系膜上动脉发出(Hiatt Ⅳ型),约占2.3%;左、右肝动脉仍自肝固有动脉发出,但肝总动脉起自肠系膜上动脉发出(Hiatt Ⅴ型),约占1.5%;肝总动脉为腹主动脉的独立分支,不构成腹腔干(Hiatt Ⅵ型),约占0.2%[4-5]。此外,还存在极少数Hiatt分型外的肝动脉变异,在术前检查及术中应注意仔细辨认。分离肝十二指肠韧带时遇到进入半肝的孤立的动脉,应考虑变异肝动脉的存在。第二步,游离胰头和腔静脉之间间隙,分离出肠系膜上静脉。脾静脉与肠系膜上静脉汇合成门静脉处对侧往往有胰腺静脉支汇入,在游离胰头时应注意结扎或凝断小血管。第三步,游离胆囊、胃窦和十二指肠,离断胃右动脉和胃十二指肠动脉。胰头的血供主要来自胃十二指肠动脉和肠系膜上动脉的分支,较为恒定的营养动脉有胰十二指肠上前、上后动脉,胰十二指肠下前、下后动脉,胰十二指肠前、后动脉弓[6]。在离断胰腺前,应注意供应血管分支的存在,管径较大的血管应予以结扎或夹闭,避免离断胰腺后胰腺残面出现能量器械难以控制的渗血。胃左动脉主要起源于腹腔干,也可发自肝总动脉或脾动脉[7]。另外应注意静脉血管变异,约70%的人群拥有胃结肠静脉干(Henle 干),主要由胃网膜右静脉、右半结肠引流静脉、胰十二指肠静脉属支中的1条或几条汇合而成,走行于胰头前方并常于脾门静脉汇合处下方约3 cm处汇入肠系膜上静脉总干或其右主干[8-9],其中最常见的是胃网膜右静脉与上右结肠静脉汇合形成的Henle干[8]。手术中游离胃大弯时,可沿胃网膜右静脉游离Henle干,避免手术误伤或血管撕裂。切除胃小弯约第3根静脉水平处和胃大弯最接近胃壁处网膜血管后,断半胃和空肠,移除标本。
2.远端胰腺切除术:位于胰腺体尾部的肿瘤一般行远端胰腺切除术(distal pancreatectomy, DP)。根据2019年NCCN(V1版)胰腺癌指南[10]推荐,胰体尾恶性肿瘤需联合完整脾脏切除。打开大网膜后,将胃向上翻起,暴露胰腺体尾部。游离胰腺上下缘,断胰颈,此时应小心肠系膜上静脉。肠系膜上静脉一般位于肠系膜上动脉右侧,也可位于其左侧或前方。Sakaguchi等[8]将肠系膜上静脉分为单支主干型(Ⅰ型)和双支主干型(Ⅱ型),Ⅰ型约占76.5%,Ⅱ型表现为左右双主干,根据左主干的汇入位置,还可以细分为Ⅱm亚型和Ⅱp亚型。结扎肠系膜上静脉,游离脾血管。脾动脉起源较恒定,但仍有少数报道显示脾动脉也可起自肠系膜上动脉[11]。夹闭胃网膜左动脉,向上仔细分离并结扎所有胃短动脉,游离脾脏,将胰体尾连同脾脏一并移除。
3.联合血管切除术:对于局部进展、侵犯或包绕血管的胰腺肿瘤,为达到R0根治,需行联合血管切除术。笔者认为,对于同时存在血管变异和动脉受侵的胰腺癌患者,不应教条地将其归为交界可切除或局部进展期胰腺癌,应根据血管变异和动脉受侵的实际情况,评估手术的可切除性。血管变异有时会成为胰腺肿瘤根治手术的有利因素。笔者所在中心1例患者行机器人PD,肿瘤位于胰头、胰颈交界处,肿块侵犯肝总动脉、肝固有动脉,但因患者存在发自肠系膜上动脉的变异右肝动脉,且右肝动脉呈优势血供(图1),故行联合肝总动脉、肝固有动脉、左肝动脉切除的PD,得到了R0切除,术后患者肝功能指标轻度升高,3 d后恢复正常。
血管变异也可能成为血管切除重建的可行条件。笔者所在中心1例PD联合血管重建的手术中,自肠系膜上动脉发出的右肝动脉受肿瘤侵犯,手术医师离断右肝动脉及胃十二指肠动脉,移除标本后,行右肝动脉-胃十二指肠动脉吻合术(图2),术后患者肝功能指标均在正常范围内。
二、机器人辅助胰腺手术中血管变异的处理
近年来,随着微创外科的发展,腹腔镜及机器人越来越多地应用于胰腺手术。机器人手术系统由于视野光学放大、3D立体图像、7个自由度的机械臂及自动滤除颤动等优势,成为笔者所在中心微创胰腺手术的主要选择。然而在处理胰腺外科常见的血管变异方面,机器人胰腺手术与剖腹胰腺手术存在一定的区别。
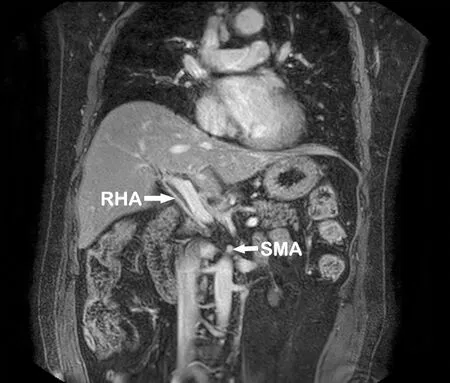
图1 右肝动脉自肠系膜上动脉发出。RHA:右肝动脉;SMA:肠系膜上动脉
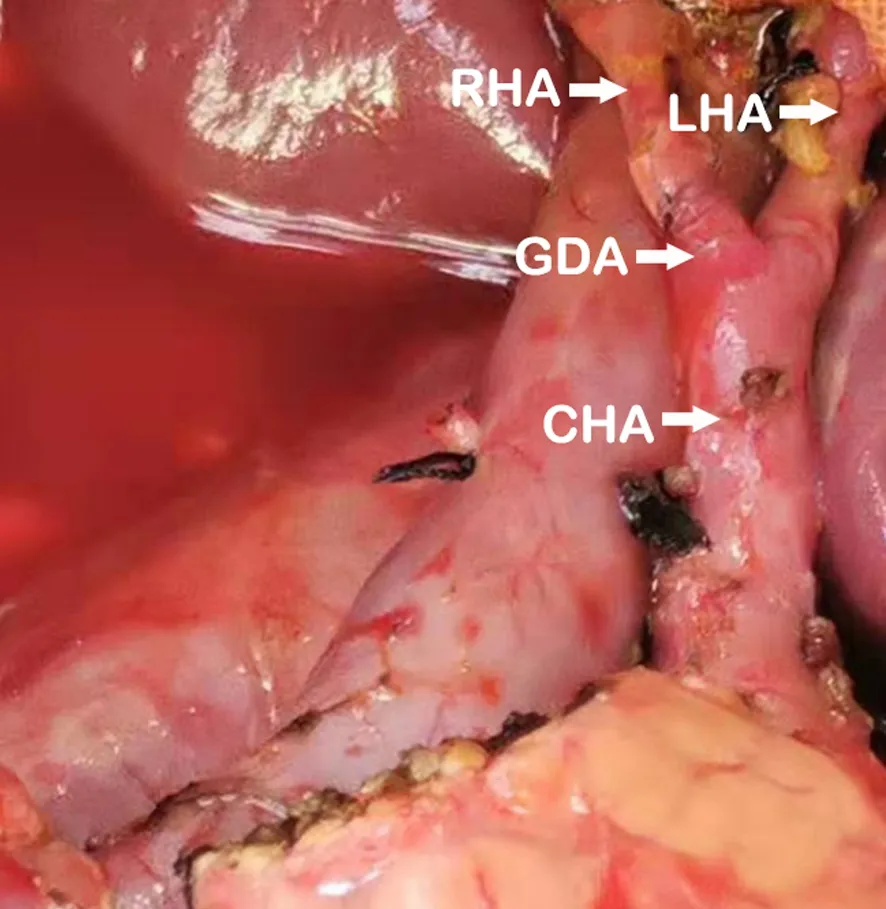
图2 右肝动脉-胃十二指肠动脉吻合。RHA:右肝动脉;LHA:左肝动脉;LHA:胃十二指肠动脉;GDA:肝总动脉
多数胰腺外科医师常习惯于通过手指触觉来感知动脉搏动,从而判断解剖区域动脉变异的存在。其实无论剖腹、腹腔镜还是机器人胰腺手术,都必须强调术前影像学检查,尤其是血管重建成像的重要性。相比剖腹胰腺手术,机器人手术系统缺乏力反馈,术者及助手无法通过手的触觉感知动脉搏动,术前影像学检查提前认知血管变异的存在,对于存在血管变异的机器人胰腺手术尤为重要。胰腺增强CT检查能较为精准地显示上腹部腹腔血管的分支走向,为术前明确血管变异的存在提供了一种安全无创且快捷有效的方法[1,12],帮助术者预知血管变异存在与否及血管变异的类型,避免因盲目解剖导致血管损伤。有条件的中心应在完成胰腺平面增强CT的同时,常规进行血管三维重建,能更立体直观地展现血管解剖[13]。
机器人胰腺手术分离解剖时,需极为重视解剖层次。助手通过辅助孔操作吸引器或分离钳、肠钳,轻柔地推移、牵拉组织,取得手术视野的良好暴露,术者使用超声刀或电钩、电剪刀,沿秋耕管解剖分离,常常能获得比剖腹手术更精细的解剖层次。笔者所在的机器人胰腺团队,主要采用超声刀进行分离解剖。因机械臂无法传导触觉,故对于解剖不明的结缔组织团,先以超声刀逐层分离出血管周围淋巴脂肪组织,明确血管走行后,沿血管解剖分离,从而获得更清晰的解剖层次,避免血管损伤。在腹腔镜PD中,对于起自肠系膜上动脉的肝动脉,Ogiso等[14]推荐沿Kocher切口,从十二指肠后方暴露肠系膜上动脉的后侧壁,即胰后入路,借此显露肝动脉分支。机器人PD与之类似,助手从辅助孔推挡牵引十二指肠,使之朝中上方翻起,充分暴露后腹膜间隙,超声刀沿肠系膜上动脉根部血管的走行自下而上分离,通常可以清晰地显露变异的肝动脉,随后沿肝动脉向上解剖,直至完全游离出肝动脉。此种“围管性解剖”处理动脉变异,不仅能减少变异血管损伤,同时也更有利于廓清血管周围淋巴脂肪组织,更好实现血管骨骼化。
机器人胰腺手术如遇到动脉受侵的情况,同样应根据实际情况判断动脉的可切除性。在机器人视野下,对已完成骨骼化的动脉可以清晰地辨识其管径大小,粗略判断其血流量,也可置入腔镜下超声探头探测血管的血流速度,评估是否可以进行血管切除。对于“不可剥离”的动脉则需行整段血管切除以及机器人动脉吻合术。切除后对于血管直径≥3 mm者,予5-0 prolene自血管后壁向前壁连续外翻缝合;血管直径<3 mm者,予6-0或7-0 prolene行间断外翻缝合[15]。机器人手术中若意外损伤重要血管,如肝动脉、门静脉,需吸引器配合吸引暴露,保持手术视野干净,明确出血点,6-0或5-0 prolene缝合血管壁。进出针时带入血管壁不宜过多,1 mm左右为宜,避免血管狭窄,造成组织缺血。
三、小结
本文从胰腺手术的基本方式出发,以达芬奇手术机器人系统的临床应用为立足点,结合笔者所在胰腺中心的手术经验,探讨了机器人胰腺手术中血管变异的处理技巧。对于机器人胰腺手术中的血管变异,应注意:(1)所有胰腺手术术前均建议行胰腺增强CT血管造影检查。术者需养成术前仔细读片的习惯,明确个体的血管走行及分支变异情况,在手术时做到脑中有图、心中有数。(2)手术中注意解剖层次,充分游离重要血管,骨骼化大血管,强调“围管操作”。 (3)根据手术要求和术中实际情况,选择保留或离断血管,充分利用血管变异带来的好处、实现手术利益最大化。(4)切忌盲目猜测,导致对变异血管的误伤、误断。(5)术后注意并发症,常规监测脏器功能,评估手术相关脏器的血供情况,警惕术后出血,对手术中血管处理的结果进行回顾性评价。
利益冲突所有作者均声明不存在利益冲突

