维生素C多重乳状液的制备及其稳定性研究
兰宏兵 余述燕 黄秋荣 麻怡 梁雯敏 尹志刚

摘要:以液体石蜡为内乳液油相、Tween|80为外水相乳化剂、明胶为高分子增黏剂,采用两步乳化法制备多重乳状液并对维生素C进行包裹,以离心前后多重乳状液相对体积比和放置2周期间维生素C包裹率的变化值为稳定性衡量标准,通过单因素试验考察乳化剂种类和用量、外内相用量比、乳化温度、均质速度和高分子材料用量等因素对多重乳液稳定性的影响,并确定其中具有显著性影响的3个因素.通过正交试验确立了多重乳状液的最佳配方和制备工艺:以Tween|80和P135分别为外内相乳化剂,Tween|80质量分数为2%,外内相用量比1.0,乳化温度45 ℃,均质转速2000 r/min,明胶用量0.5%.该条件下,制得的多重乳状液相对体积比为0.966 4,性能稳定,对维生素C的包裹率可达98%,具有令人满意的包裹稳定性.
Abstract:Through two|step emulsification method,the multiple emulsions were firstly prepared with paraffin as internal oil phase,Tween|80 as hydrophilic emulsifier and gelatin as thickener,and then were used to encapsulate Vitamin C.The effect of various parameters on the stability of multiple emulsions was investigated by determiningthe volume changes after centrifugation and the encapsulation changes of Vitamin C during two weeks.These factors included the species and amount of emulsifier,the dosage ratio of two phases,emulsion temperature,homogenization speed and the dosage of polymer,three of which were most influential.The optimal formula and preparation process were obtained through orthogonal experiment,that was,Tween|80 and P135 as foreign and internal emulsifiers,respectively,the mass ratio of Tween|80 was 2%, the dosage of external phase was 1.0, and the emulsification temperature was 45 ℃,homogeneous speed was 2000 r/min,gelatin dosage was 0.5%.Under this condition, the relative volume ratio of multiple emulsions was 0.966 4, the performance was stable, and the encapsulation rate of Vitamin C could reach 98%,and the multiple emulsions had a satisfactory package stability.
关键词:维生素C;多重乳状液;稳定性;包裹率
Key words:Vitamin C; multiple emulsions;stability;encapsulation rate
中图分类号:TQ658;TS974.1文献标识码:ADOI:10.3969/j.issn.2096-1553.2019.04.007
文章编号:2096-1553(2019)04-0043-09
0 引言
维生素C,又名抗坏血酸,是一种易溶于水的无色晶体,广泛存在于新鲜水果和蔬菜中.由于其分子中存在烯二醇结构,具有很强的还原能力[1],同时能够有效地抑制酪氨酸酶的活性,是人们最早用于化妆品的美白成分之一,也是被皮肤科医生认可的安全无毒、可淡化色斑的口服型药剂[2].但由于其自身的不稳定性,易受到过渡金属离子(如Cu2+和Fe3+)、热、光、pH值、高浓度氧和高水分活度的影响发生氧化或水解反应而丧失美白活性,加之其脂溶性差的特点,使它在化妆品领域的应用受到极大的限制[3].因此,研究人员一直在寻求理想的解决途径,使化妆品既能保留维生素C的美白还原活性,又能最大程度地提高其稳定性和配伍性.
目前,已經报道的解决途径大致可以分为两类:一是将维生素C衍生化,生成如维生素C脂肪酸酯衍生物、维生素C磷酸酯衍生物和维生素C脂肪醚类化合物等[4-8].研究表明,这些衍生物大部分能在一定程度上改善维生素C的脂溶性和稳定性,但是其还原性和美白功效却有不同程度的降低,并且衍生化过程需要使用大量的有机试剂,而维生素C又具有多个反应位点,因此衍生化过程通常需要繁琐的合成和提纯工艺,从而增加了成本投入,也造成了一定的环境污染.二是采用合适的材料或技术将维生素C进行包裹[9-13],使之与外部环境隔断,由此达到提高其稳定性和配伍性的目的,相比于将维生素C衍生化,该方法具有更大的优势.
多重乳状液是1925年由Seifritz发现并提出的,是将初级乳状液分散在另外的连续相后形成的 O/W 型和 W/O 型乳液共存的复合体系[14-16].多重乳液不仅规避了单一乳化体系的缺点,还同时保留了两者的优点,展现出令人满意的使用效果和肤感.此外,利用多重乳状液3个被膜分隔开的相区溶解不同的活性物质,可防止它们之间相互作用,为那些不稳定的物质和难以共存的功效成分的应用提供理想的载体,亦可实现有效成分的缓慢释放.因此,多重乳状液被认为是目前最有前途的3种化妆品体系之一.但由于其本身固有的复杂性,特别是多重乳状液的稳定性问题,包括乳化体系的稳定性和包裹效能的稳定性,是实现其工业化应用前必须要解决的难题[17].
本文拟以液体石蜡为内乳液油相,Tween|80为外水相乳化剂,明胶为高分子增黏剂,制备多重乳状液并对维生素C进行包裹,以离心前后多重乳状液的相对体积比和放置2周的维生素C的包裹率之变化值作为衡量多重乳状液稳定性的指标,通过单因素试验和正交试验法确定维生素C多重乳状液的最佳配方和制备工艺,以期为多重乳状液在化妆品领域的应用提供参考,为提高维生素C的稳定性和配伍性提供一条可行的途径.
1 材料与方法
1.1 试剂与仪器
主要试剂:维生素C(分析标准品),抗坏血酸(分析纯),明胶(分析纯),Tween|80(分析纯),Span 80(分析纯),Span 60(分析纯),Brij 72(分析纯),阿拉丁试剂有限公司产;液体石蜡,聚乙二醇(30)二聚羟基硬酯酸酯(P135),均为分析纯,天津市恒宇精细化工有限公司产.
主要仪器: JJ-1 增力电动搅拌器,金坛市医疗仪器厂产;XP400C 电脑型偏光显微镜,上海万衡精密仪器有限公司产;TDL80-2B 台式离心机,上海安亭科学仪器厂产;SGX500/750封闭式高剪切乳化机,上海尚贵流体设备有限公司产;AL104 电子天平,梅特勒-托利多仪器(上海)有限公司产.
1.2 实验方法
1.2.1 多重乳状液的制备
采用两步乳化法制备维生素C多重乳状液.
W/O型初级乳状液的制备:将一定质量分数的维生素C水溶液加入到含有亲油性乳化剂的液体石蜡溶液中,50 ℃条件下,3000 r/min均质3 min,得初级乳状液.
W/O/W型多重乳状液的制备:将上述制备的初级乳状液滴加到含有亲水性乳化剂Tween|80的外水相中,2000 r/min均质3 min,即可获得多重乳状液.
1.2.2 相对体积比的测定
将制备的多重乳状液在3000 r/min条件下离心30 min,分别记录离心前后多重乳状液体积V0和Vt,并计算相对体积比φ=Vt
V0,φ值越大,离心后分层越少,表明多重乳状液越稳定.
1.2.3 维生素C包裹率的测定[18-19]
维生素C质量浓度测定方法的选择:维生素C在紫外区265 nm处有最大吸收峰,并且在质量浓度0~120 μg/mL的范围内满足比尔定律,即吸光度与质量浓度呈良好的线形关系.因此本实验采用分光光度法测定各样品溶液的吸光度,并依据维生素C标准曲线,计算维生素C质量浓度.
维生素C标准曲线的绘制:首先配制标准溶液.准确称取维生素C标准品0.102 2 g,置于洁净的三角烧瓶中,用去离子水完全溶解后,转移至100 mL容量瓶中,定容、摇匀后即得质量浓度为1.022 mg/mL的维生素C标准溶液;然后分别量取0.00 mL,0.20 mL,0.40 mL,0.60 mL,0.80 mL和1.00 mL标准溶液,将其置于50 mL容量瓶中,用去离子水定容,以去离子水作为参比,在265 nm波长处测定上述各质量浓度维生素C溶液的吸光度A,并以吸光度对质量浓度作图,即得维生素C标准曲线.
维生素C包裹率的测定:取 10 g 多重乳液放入透析袋,浸于一定量去离子水中,在室温、避光和搅拌条件下透析 24 h,将未被包裹的维生素 C 去除.精确吸取透析液 5 mL 置于10 mL 容量瓶中,用去离子水定容,于265 nm 处测定吸光度.
包裹率=(1-2W1/W2)×100%
式中,W1为测定的透析液中维生素C的质量浓度,W2为多重乳状液中添加维生素C的质量浓度.
1.2.4 单因素试验
以液体石蜡为内乳液油相,在两步乳化法制备多重乳状液的过程中,考察内乳液乳化剂种类、外内相用量比、外水相乳化剂质量分数、第二步乳化温度和均质转速、高分子增黏剂用量对多重乳状液稳定性的影响,为正交试验的设计提供依据.
1.2.5 正交试验
以单因素试验结果为依据,选择具有显著性影响的3个因素,设计三因素三水平正交试验,获得最佳试验方案,并通过验证试验确定多重乳状液的最佳配方和制备工艺.
2 结果与讨论
2.1 内乳液乳化剂种类的选择
固定外水相与内乳液质量比为1.0,内乳液中石蜡油用量为60%(百分数均指质量分数,下同),乳化剂用量为5%,1%维生素C水溶液用量为35%,外水相乳化剂Tween|80用量为5%(若无特别说明,单因素试验中均设置乳化温度为40 ℃, 均质转速为3000 r/min).
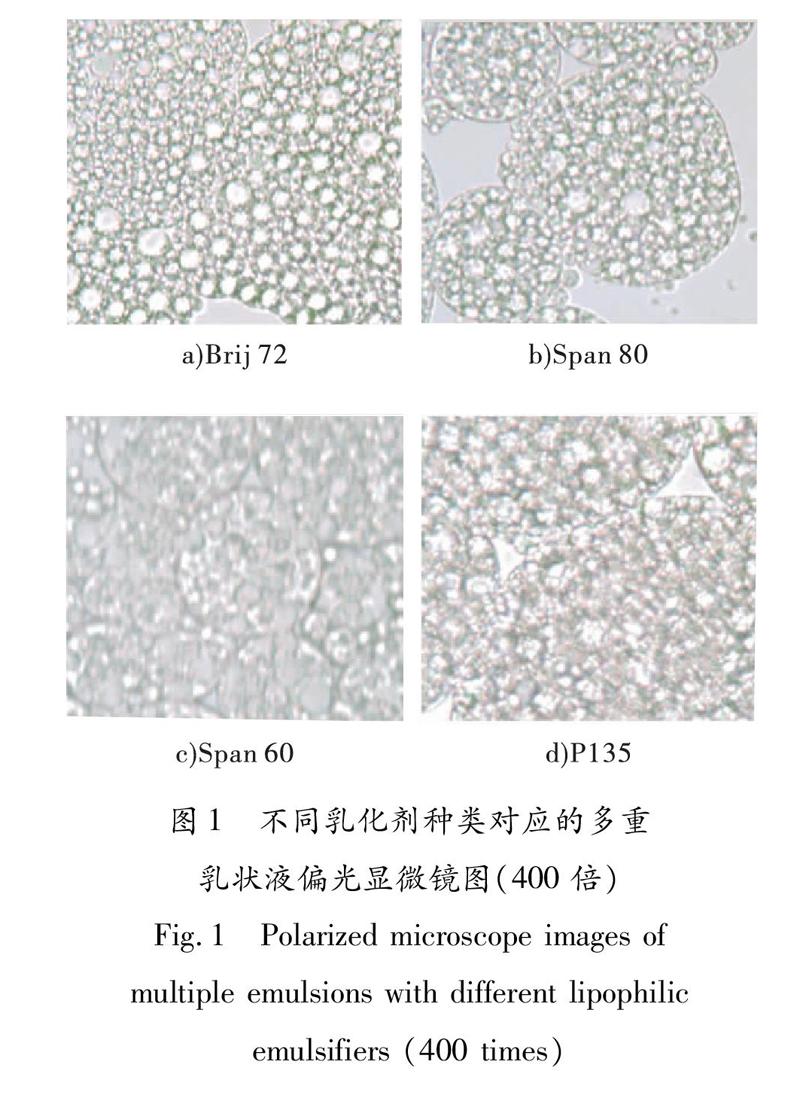
分别使用不同的内乳液乳化剂,考察其对多重乳状液稳定性的影响,得到
Brij 72,Span 80,Span 60,P135的相对体积比分别为0.734 4,0.901 8,0.878 9和0.921 1
,对应的偏光显微镜图见图1.从图1可以看出,当Brij 72和 Span 60为乳化剂时,形成的多重乳状液液滴之间相互聚结现象明显,
Span 80為乳化剂时,形成的多重乳状液液滴尺寸大小不均匀,
而当P135为乳化剂时,
离心前后多重乳状液相对体积比最大,
多重乳状液稳定性好,液滴尺寸较小,且没有明显的黏结现象,因此适宜的内乳液乳化剂为P135.
2.2 外内相用量比对多重乳状液稳定性的影响
固定内乳液中石蜡油用量为60%,外水相中1%维生素C溶液用量为35%,内乳液乳化剂P135用量为5%,外水相乳化剂Tween|80用量为5%,
分别测定m(外水相)GA6FAm(内乳液)分别为0.6,0.8,1.0,1.2和1.4时多重乳状液离心前后的相对体积比,分别为 0.907 0,0.924 8,0.921 1,0.893 7和0.838 8,对应的微观结构偏光显微镜图如图2所示.由图2可知,随着外水相占比的增加,多重乳状液的稳定性先上升后下降,外内相用量比在 0.6~1.0范围内乳状液稳定性较好.这可能是由于当外水相用量小时,没有足够多的水相将内乳液油滴进行分散,油滴间相互接近,容易聚集破裂,但外水相过多,乳化剂乳化能力有限,导致多重乳状液黏度降低,乳状液稳定性下降.从图2可以看出,当两者比值为0.6时,没有形成明显的W/O/W结构,相比于1.0,两者比值为0.8时多重乳状液液滴界限更加明显,尺寸均匀,稳定性更为理想.因此,选择适宜的外内相用量比为0.8.
2.3 外水相乳化剂质量分数对多重乳状液稳定性的影响
固定内乳液中石蜡油用量为60%,外水相中1%维生素C溶液用量为35%,外水相与内乳液用量比为0.8和内乳液乳化剂P135用量为5%,考察质量分数分别为1%,2%,3%,4%,5%的Tween|80对多重乳状液稳定性的影响,得到相对体积比分别为0.723 8,0.878 7,0.954 0,0.931 0,0.924 8,对应的偏光显微镜图见图3.由图3可知,随着外水相乳化剂质量分数的增加,多重乳状液的稳定性先显著上升后有缓慢下降的趋势.当Tween|80质量分数为1%时,乳状液稳定性较差.从图3中也没有观察到明显的多重乳状液包裹结构,这可能是由于乳化剂质量分数低时,乳化能力有限,不利于W/O/W型復相乳状液的形成.当乳化剂质量分数超过3%时,多重乳状液稳定性开始呈下降趋势.这可能是由于有部分的乳化剂吸附在W/O油滴界面上,破坏了第一相稳定性.因此,选择适宜的外水相乳化剂Tween|80的质量分数为3%.
2.4 第二步乳化温度和均质转速对多重乳状液稳定性的影响
在外水相与内乳液用量比为0.8,内乳液中石蜡油用量为60%,外水相中1%维生素C溶液用量为35%,内乳液乳化剂P135用量为5%和外水相乳化剂Tween|80用量为3%条件下,进一步考察第二步乳化温度和均质转速对多重乳状液稳定性的影响.首先,设定第二步乳化温度分别为35 ℃,45 ℃,55 ℃和65 ℃,得到的多重乳状液在3000 r/min条件下离心30 min,计算它们的相
对体积比分别为 0.914 5,0.960 0,0.937 6和0.940 8.升高第二步乳化温度,多重乳状液的稳定性有增加的趋势.当乳化温度为45 ℃时,乳状液稳定性最好.
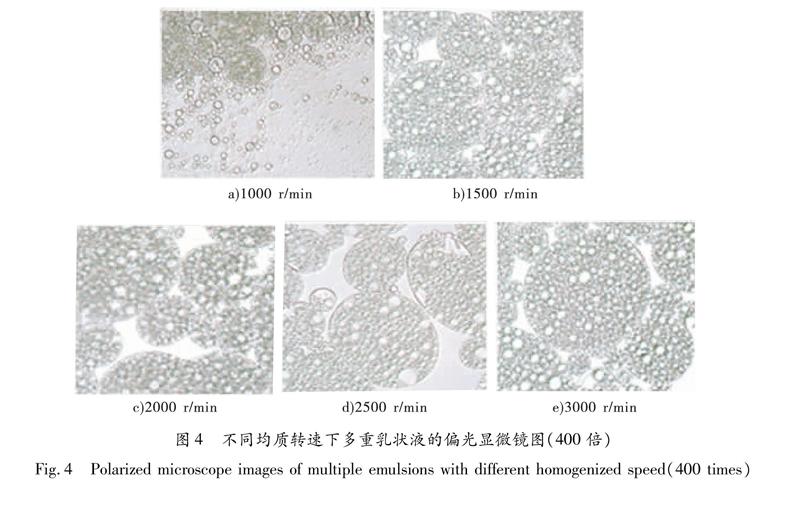
在其他条件相同的情况下,改变第二步乳化时均质器转速,设置均质器转速分别为1000 r/min,1500 r/min,2000 r/min,2500 r/min和3000 r/min,测定上述转速下的相对体积比分别为0.790 8,0.912 0,0.969 7,0.954 3和0.960 0,对应的偏光显微镜图见图4.从图4可看出,随着均质器转速的增大,多重乳状液的稳定性也随之增强,当均质器的转速达到2000 r/min时,多重乳状液的稳定性最好.结合图4可以发现,当均质转速较高时得到的多重乳液的结构大小更均匀,但是转速在2500 r/min时,有少部分W/O乳液未能被包裹住,所以2000 r/min为适宜的第二步均质转速.
2.5 高分子增黏剂用量对多重乳状液稳定性的影响
高分子材料通常应用在乳状液类产品中,利用其可增加乳液黏度的特性提高乳状液稳定性.在上述实验结果的基础上,即固定外水相与内乳液用量比为0.8,内乳液中石蜡油用量为60%,外水相中1%维生素C溶液用量为35%,内乳液乳化剂P135用量为5%和外水相乳化剂Tween|80用量为3%,设定乳化温度为45 ℃和均质转速为2000 r/min的条件下,通过在外水相中分别添加0.2%,0.5%,1.0%,1.5%和2.0%的明胶,考察其对乳状液稳定性的影响,结果发现:多重乳状液的稳定性随着明胶质量分数的增大而有所提高(上述5种明胶用量下的相对体积比分别为0.943 3,0.961 0,0.959 5,0.960 7,0.964 3),但当明胶用量为 1.0%时,稳定性没有明显上升反而有所降低,且多重乳状液黏度明显增加.考虑到该体系在使用方面的便捷性,实际应用中添加0.5%左右明胶是比较适合的.
2.6 正交试验确定多重乳状液最佳配方和制备工艺
通过上述单因素试验可以确定影响多重乳状液稳定性的主要因素为外内相用量比(A)、外水相乳化剂的用量(B)和乳化温度(C).采用正交试验法获得最佳的试验配比,正交试验因素水平见表1,结果见表2.
从表2可知,影响多重乳状液稳定性因素的主次顺序为:外水相乳化剂的用量>外内相的用量比>乳化温度,最佳试验方案为B1 A2 C2,
即外水相乳化剂Tween|80的用量为2 %,外内相质量比为1.0,乳化温度为45 ℃.为了验证该结果的准确性,采用两步乳化法,对该配方进行验证试验,所得多重乳状液的相对体积比为0.966 4,且在偏光显微镜下展现出良好的结构形态(见图5).
2.7 维生素C的包裹率及包裹稳定性分析
通过测定不同质量浓度维生素C溶液的吸光度,获得维生素C标准工作曲线,见图6.从图6
可以看出,吸光度和维生素C质量浓度在0~20 μg/mL范围内具有良好的线性关系,回归方程为
Y =0.065 1X + 0.029 7, R2=0.999 8
在此基础上,依据最佳配方和制备工艺,分别使用质量分数为1%,2%,4%和6%的维生素C水溶液制备多重乳状液,测定并计算不同时间点4种多重乳状液样品的维生素C包裹率及其随时间的变化情况,结果如图7所示.由图7可以看出,在最佳配方和制备工艺下,多重乳状液中4种质量分数维生素C的包裹率没有明显的差别(分别为98.77%, 98.83%, 98.18%, 97.59%).而随着时间的延长,包裹率都有所下降.这可能是随着时间的延长,有部分不稳定的油滴发生破裂,包裹的内水相扩散至外水相所致.但当维生素C的质量分数为1%和2%时,包裹率下降非常缓慢,14 d后包裹率还能保持在95%以上,而当维生素C的质量分数较大时,包裹率下降比较明显,且多重乳液颜色有加深的趋势.这可能是由于浓度差增大时,内乳液中未包裹的维生素C和不稳定油滴破裂导致内水相中释放出的维生素C向外水相中扩散速度加快.
3 结论
本文以液体石蜡为内乳液油相,Tween|80为外水相乳化剂,明胶为高分子增黏剂,采用两步乳化法制备了多重乳状液并对维生素C进行包裹,以离心前后多重乳状液相对体积比和放置2周期间维生素C包裹率的变化值为稳定性衡量标准,通过单因素试验确定了影响多重乳状液稳定性的主要因素是外内相质量比、外水相乳比剂用量、乳化温度、均质速度和高分子材料用量,结合正交试验获得了多重乳状液的最佳配方和制备工艺: 以Tween|80和P135分别为外内相乳化剂,Tween|80質量分数为2%,乳化温度为45 ℃,均质转速2000 r/min,明胶用量0.5%,在外内相用量比为1.0的条件下,制得的多重乳状液相对体积比0.966 4,性能稳定.该条件下维生素C的包裹率可达98%,具有令人满意的包裹稳定性.本文研究结果为多重乳状液的制备及其在化妆品、农药和医药等领域的应用提供了一定的理论依据.
参考文献:
[1] 葛颖华,钟晓明.维生素C和维生素E抗氧化机制及其应用的研究进展[J].吉林医学,2007,28(5):707.
[2] 张建友,方艳燕,吴晓琴,等.天然活性美白化妆品研究现状及发展前景[J].精细化工,2008,25(1):72.
[3] 郝志耘,夏惠娟.维生素C稳定性实验研究[J].牡丹江医学院学报,1997,18(1):13.
[4] 董瑞娟.抗氧化维生素衍生物的制备[D].北京:北京化工大学,2015.
[5] 谷雪贤.维生素C衍生物的制备及其在化妆品中的应用[J].化学试剂,2011,33(4):325.
[6] 李诚让,朱文元.维生素C衍生物研究进展[J].临床皮肤科杂志,2005,34(7):487.
[7] 闫世梁,史小利,户言峰,等.维生素C衍生物的合成与研究[J].低碳世界,2018(5):357.
[8] 贾博.维生素C及其衍生物的制备工艺和应用[J].河北化工,2011,34(8):25.
[9] KARIM A A,TAN E,LOH X J.Encapsulation of Vitamin C with its protection from oxidation by poly(vinyl alcohol) [J].Journal of Molecular and Engineering Materials,2017,5(4):175.
[10]李思琪,张晓庆,吐马拉·吐尔洪,等.维生素C脂质体的制备[J].轻工科技,2018,34(4):15.
[11]王婷婷.海藻酸钠微球包封L-抗坏血酸的制备及其在化妆品中的应用[D].无锡:江南大学,2014.
[12]李芳芳,贾红娇,田永红,等.多重结构乳状液的研究进展[J].日用化学工业,2014,44(4):222.
[13]王传好,曹光群,孙谦.W/O/W型多重乳状液的制备及应用概述[J].日用化学工业,1991(8):23.
[14]曾兰兰.多重乳液的制备及其包裹能力的研究[D].无锡:江南大学,2009.
[15]罗昌荣,侯亚龙.多重乳状液技术及其在香料物质缓释中的应用[J].中国食品添加剂,2003(Z1):65.
[16]文静.含多重结构的亲水性成分包覆载体技术及其应用[D].上海:上海应用技术大学,2017.
[17]李光水,邵国泉,雍国平,等.提高W/O/W多重乳状液的稳定性研究[J].食品科学,2002,23(1):51.
[18]刘彬,赵惠新.维生素C含量测定方法综述及其比较[J].课程教育研究,2018(42):178.
[19]李秋菊,王亚红,刘秀萍.维生素C的测定方法[J].太原师范学院学报(自然科学版),2005,4(1):89.

