3例16p11.2微缺失综合征胎儿的产前诊断及其产前超声分析*
(湖北省妇幼保健院 优生遗传科,湖北 武汉 430070)
16p11.2 微缺失综合征是因为16号染色体p11.2存在复发性杂合缺失区域而引起的一类综合征。16p11.2微缺失综合征于2008年由KUMAR等在自闭症谱系障碍病因的研究中首次提出[1]。国外流行病学研究其人群发病率为0.3‰[2]。患者的主要临床症状包括:发育迟缓、智力障碍和/或自闭症谱系障碍。患者的智商通常在轻度智力障碍到正常之间,但智力正常的也往往有其他发育问题,如语言发育迟缓或者自闭症谱系障碍[3]。大部分患者还有发生超重和肥胖的风险[4]。20%患者有癫痫发作,2岁之前常出现巨头畸形。16p11.2微缺失综合征的各种出生缺陷均略微增加,但以椎体畸形最为常见。
16p11.2 微缺失综合征可以由拷贝数变异的方法如染色体微阵列(chromosomal microarray analysis,CMA)或目标缺失分析方法如荧光原位杂交(fluorescence in situ hybridization,FISH)技术检出。单核苷酸多态性微阵列(single nucleotide polymorphism array,SNP array)技术能够检出 >50 kb 的 CNVs,能准确地检测出16p11.2微缺失综合征。目前,16p11.2微缺失综合征的产前诊断报道较少,本研究通过对3例16p11.2微缺失综合征胎儿的产前遗传学分析,结合其超声异常特点,探讨其基因型与表型的对应关系。
1 资料与方法
1.1 研究对象
病例1,汉族,G4P1,孕23周因胎儿超声提示胸腰段脊柱侧弯,L12~S1呈半椎体畸形,单脐动脉(右侧缺如),右心室强光斑,经孕妇知情同意后于孕24周行羊水穿刺术。病例2,汉族,G3P1,孕24周因胎儿超声提示胎儿脊柱侧弯(L11~12,S1椎体向右侧侧弯),椎体排列不整齐(半椎体),羊水指数位于正常值上限,经孕妇知情同意后于孕25周行羊水穿刺术。病例3,汉族,G1P0,孕13周因胎儿超声提示NT 4.8 mm,胎儿鼻骨显示不清,经孕妇知情同意后于孕18周行羊水刺术。病例4,汉族,G3P1,胎儿系统超声检测未见异常,孕19周因高龄(41岁)经孕妇知情同意后行羊水穿刺术,为正常对照组。4个病例所抽取的羊水均行常规G显带染色体核型分析和SNP array检测。
1.2 方法
1.2.1 常规羊水染色体核型分析孕妇在超声连续引导定位下行羊膜腔穿刺术,抽取胎儿羊水28 ml,无菌操作下分别进行体外培养。培养好的羊水细胞经收获、固定、核型制备和G显带。染色体异常的描述依据《人类细胞遗传学国际命名体制2016版》。
1.2.2 全基因组DNA 提取 使用 QIAamp ® DNA Mini Kit(250)试剂盒抽提取羊水的全基因组DNA,提取的DNA置于-20℃冰箱冷冻储存备用。芯片实验前使用Nanodrop one分光光度计定量,标准化并稀释样本浓度至 50 ng/μl。
1.2.3 SNParray 检测缺失基因 采用 Cyto Scan 750K芯片(包括55万个拷贝数探针和20万个SNP探针)进行检测。芯片检测所需DNA总量为250 ng。采用Affymetrix公司配套检测试剂盒及优化的标准操作流程,进行酶切、连接、PCR、PCR产物纯化、片段化、标记、杂交、洗染、扫描等几个步骤。整个过程严格按照质控标准进行。用 Affymetrix Chromosome Analysis Suite Software进行分析。利用国际基因组变异数据库DGV(http://dgv.tcag.ca/dgv/app/home)剔除常见的多态性CNV,其余CNV与CNVs数据库DECIPHER(https://decipher.sanger.ac.uk/patient/)、OMIM(https://omim.org)、ISCA(https://www.iscaconsortium.org/)比对分析,在 PubMed数 据 库(https://www.ncbi.nlm.nih.gov/pubmed)上检索相同或相似区段的CNV研究的文献。
1.2.4 实时荧光定量聚合酶链反应(quantitativerealtime polymerase chain reaction,qRT-PCR) 根据 3个16p11.2微缺失病例DNA缺失区域,选择共有缺失序列区域为扩增子,设计正反向引物,选择ALB基因为内参,作为靶标拷贝数相对定量的依据;所有引物设计及序列特异性比对均使用Primer 5.0 and National Center for Biotechnology Information Basic Local Alignment Search Tool software(blast.ncbi.nlm.nih.gov/Blast.cgi)。该验证靶标及内参引物序列见表1,扩增体系使用 ABI SYBR Green PCR Master Mix,样本均使用TE稀释成5 ng/μl,加样时取2 μl作模板;使用ABI 7500 荧光定量 PCR 仪,选择 SYBR Green Reagent模式。扩增条件:95℃预变性5 min及热启动酶激活,95℃变性 15 s、60℃退火 40 s,45个循环。每个样品检测3个复孔,实验进行3次重复。
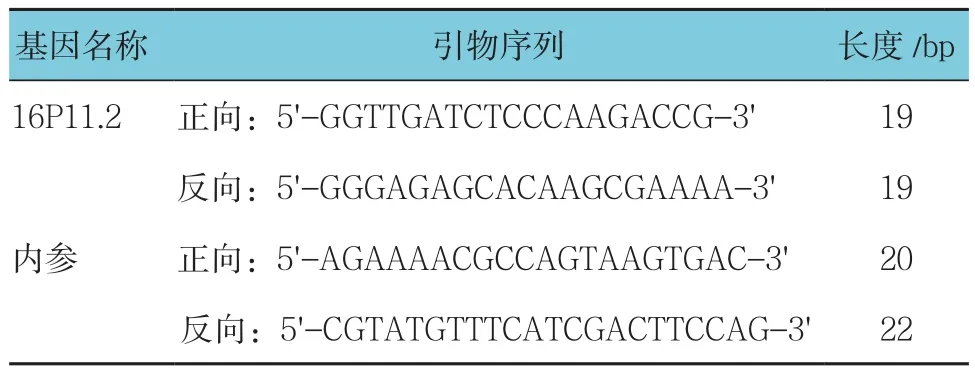
表1 16p11.2(hg19)微缺失区域实时荧光定量PCR检测所用引物序列
1.3 统计学方法
数据分析采用 Microsoft Office Excel 2010 统计软件,计算相对值、均值及标准差。
2 结果
2.1 G显带核型分析结果
病例1和病例2胎儿羊水染色体核型为46,XX,病例3和病例4胎儿羊水染色体核型为46,XY。见图1。
2.2 SNP array分析结果
病例 1 的 SNP array结果为 arr [hg19]16p11.2(29,428,531 ~ 30,350,748)X1,即 16p11.2 存在 922 kb的缺失。病例2的SNP array结果为arr[hg19]16p11.2(29,591,326~30,176,508)X1,即16p11.2存在585 kb 的缺失。病例 3 的 SNP array结果为 arr[hg19]16p11.2(29,428,531~30,176,508)X1,即16p 11.2存在748 kb的缺失(见图2)。3个病例均未检测到其他基因组位点的致病性或可疑致病性变异。病例4的SNP array结果未检测到致病性或可疑致病性变异。
2.3 qRT-PCR结果
病例1~3在16p11.2(hg19)相对拷贝数几乎均是病例4的50%,病例1~3胎儿羊水细胞存在16p11.2杂合缺失,而病例4不存在缺失。见表2。
2.4 妊娠结局
病例1、病例2和病例3分别于孕27周、孕28周和孕21周行引产术,但均未同意进行引产后的病理解剖。病例4于孕38+2周剖宫产健康男婴1例。
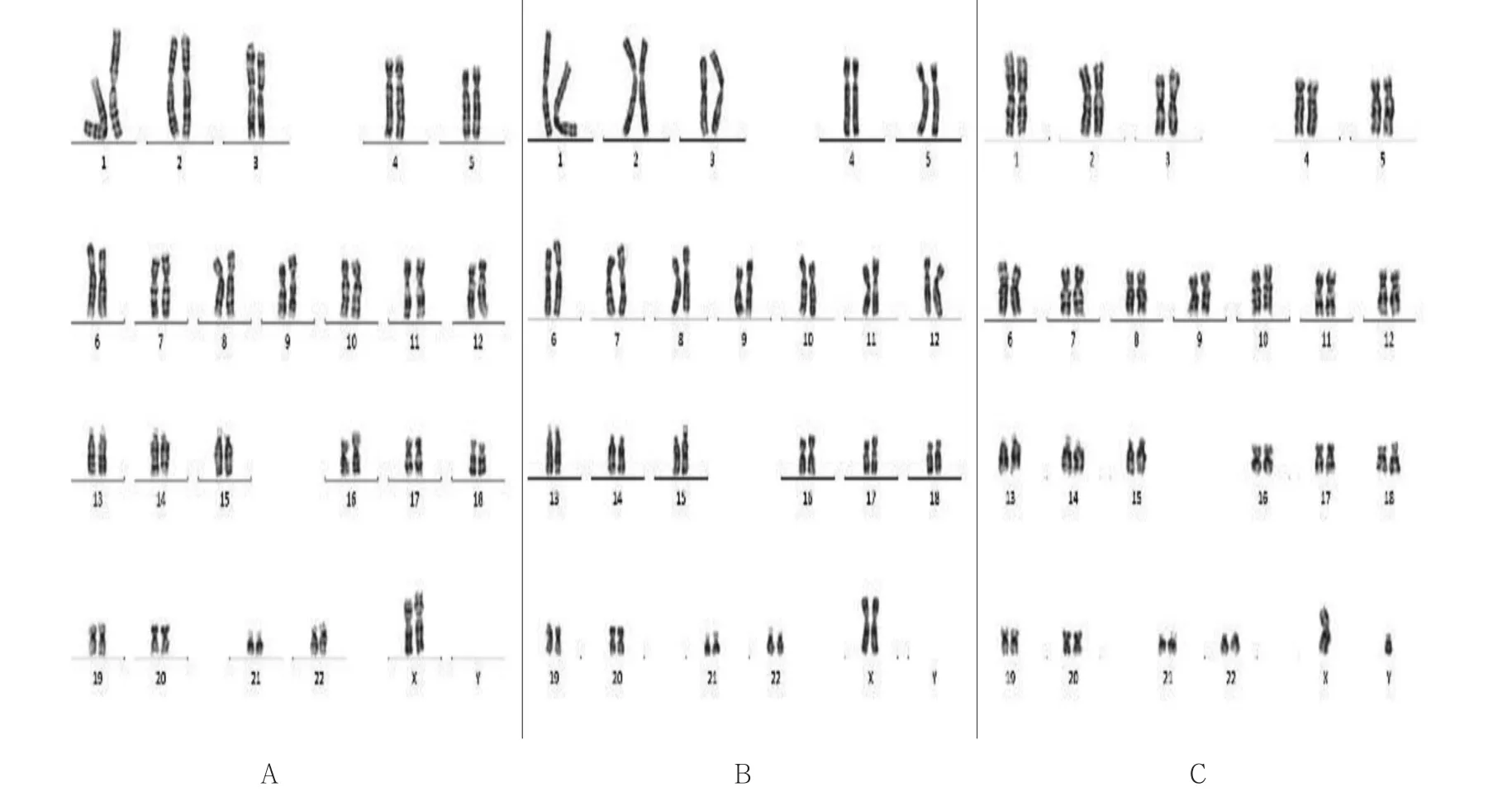
图1 胎儿羊水染色体核型
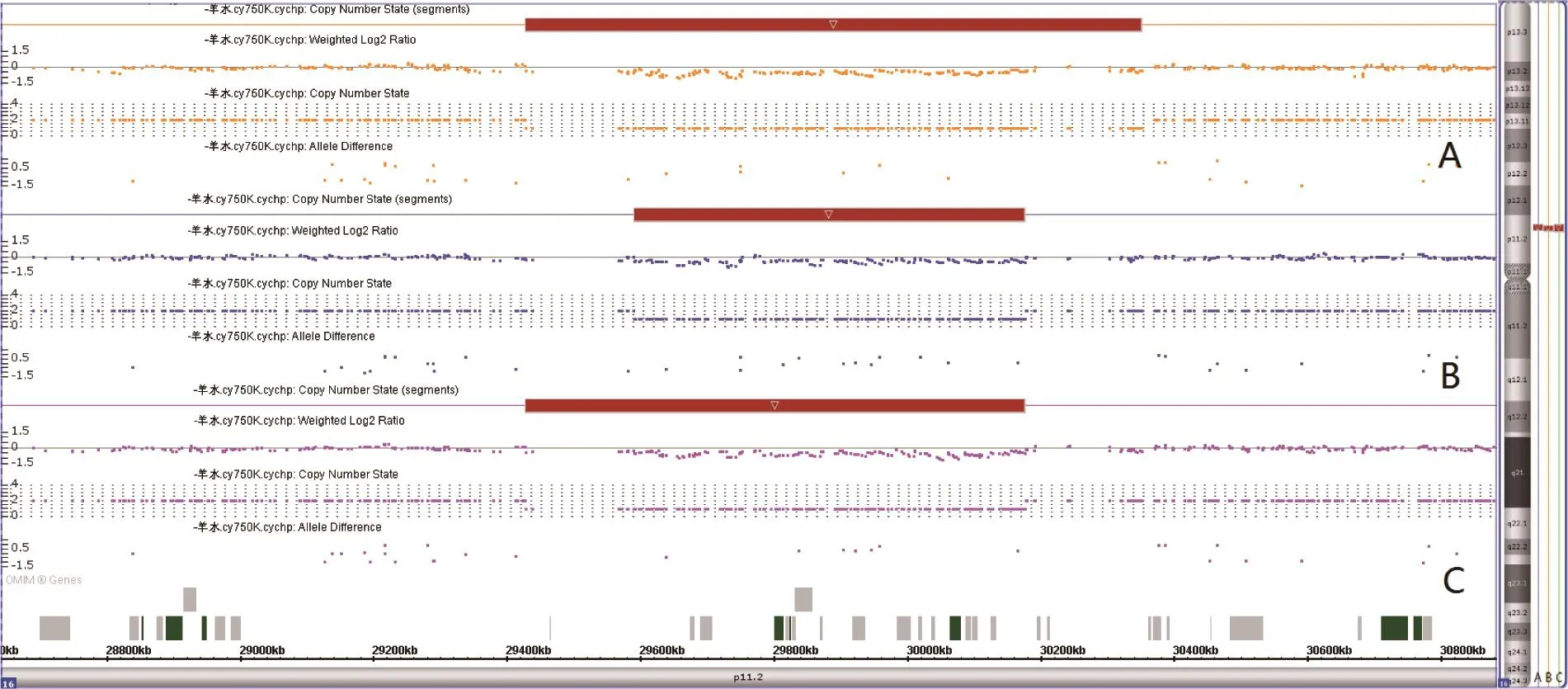
图2 3例SNP array结果
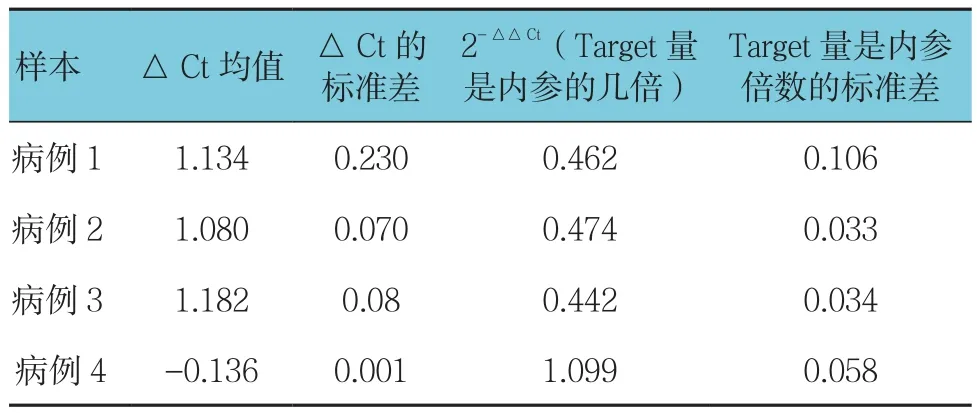
表2 qRT-PCR数据统计
3 讨论
16p11.2 微缺失综合征根据缺失区域主要分为2类:①典型16p11.2缺失综合征(OMIM:611913),为 16 号染色体 29.5~ 30.1 Mb 区域上 500 ~ 600 kb的缺失,是最常见的类型。该区域覆盖有:PRRT2、KCTD13、TBX6、HIRIP3、SEZ6L2等29个基因。②非典型16p11.2缺失(OMIM:613444),为16p11.2末端28.73~28.95 Mb区域上200~220 kb的缺失,这类型缺失较少见。此区域包含SH2B1、CD19、SPNS1等9个基因[5]。两种类型16p11.2微缺失综合征因为缺失区域的基因不同,临床症状也不同,本文主要讨论典型16p11.2缺失综合征。
16p11.2 微缺失综合征的发生是因为在16p11.2区域两端有低拷贝重复序列(low copy repeats,LCRs),它位于微缺失区域两端,长约147 kb片段(147A和147B),它们之间有99.5%序列同源[6]。2段低拷贝重复序列造成基因组的不稳定性,使得在细胞减数分裂过程中易引起同源染色体上非等位基因的重组(nonallelic homologous recombination,NAHR),从而导致微缺失和微重复的产生。
16p11.2 微缺失内部包含25个注释基因或转录子,同时在低拷贝重复序列中还包含4个额外的基因,其中包含几个重要的功能基因如PRRT2、KCTD13、TBX6、HIRIP3、SEZ6L2等。目前,这些基因的缺失是如何导致患者表型的机制尚不明确,但是最近的一些研究逐步揭示该关键基因的作用以及它们引起表型的功能通路。PRRT2基因可能是引起16p11.2微缺失综合征患者癫痫或婴儿性惊厥的关键基因。PRRT2基因杂合功能丢失型致病变异可以导致发作性运动诱导性运动障碍及引起良性家族性婴儿性癫痫与舞蹈手足徐动综合征[7]。KCTD13基因是斑马鱼和小鼠神经元增殖的关键驱动因子,也是引起16p11.2微缺失综合征巨头畸形的主要驱动因子,缺失区域内的MAPK3和MVP基因可能作为修饰基因增强KCTD13基因的表达[8]。HIRIP3基因产物和HIRA结合形成HIRA-HIRIP3复合物,在染色质和组蛋白代谢中发挥重要的功能,16p11.2缺失后可能因为HIRIP3基因单倍剂量不足,从而导致主动脉瓣畸形的发生[9]。SEZL6L2基因的单倍剂量不足可能是导致16p11.2微缺失综合征语言迟缓、认知障碍和自闭症的重要因素。与SEZL6L2基因同源的SEZ6基因缺陷性小鼠显示出空间记忆受损、运动障碍和焦虑程度降低。SEZ6L2基因不仅在人类大脑中有高表达,且与导致癫痫和言语障碍的SRPX2基因高度同源[10]。TXB6基因是引起16p11.2微缺失综合征患者椎体畸形的关键基因[11]。TBX6基因编码一个转录因子,它在小鼠的体节发生中发挥了关键作用[12]。POURQUIE等[13]研究发现TXB6基因敲除小鼠出现与人类相同的脊椎肋骨发育不全和先天性脊柱侧弯等表型。SPARROW等[14]证明TXB6基因突变后影响TBX6蛋白的转录活性从而导致脊椎肋骨发育不全,并发现携带1个TBX6无功能等位基因的小鼠胚胎,46%有轻度的颈椎缺陷,30%存在骶骨缺损。FEI等[15]研究发现,在中国汉族人群中TBX6基因上的2个单核苷酸多态性位点:rs2289292和rs3809624,这2个位点的多态性在先天性脊柱侧弯的发病机制中起重要的作用。WU等[16]进一步研究发现在中国汉族人群中TBX6基因以一种特殊的作用形式:无功能等位基因(包括16p11.2微缺失综合征中TBX6基因的缺失)合并另一个常见的亚效等位基因单体型T-C-A(3个常见的单核苷酸多态性位点:rs2289292、rs3809624、rs3809627)而导致半椎体和脊柱侧弯。
16p11.2 微缺失综合征患者有明显表型异质性和不同的外显率。ROSENFELD等报道16p11.2微缺失综合征(TBX6)的外显率46.8%(31.5%~64.2%),这可能与TBX6基因的特殊致病方式(1个无功能等位基因合并另一个常见的亚效等位基因单体型T-C-A)相关[16-17]。在千人数据库中,TBX6基因T-C-A单体型在中国汉族人群中占44%,因此,理论上在中国汉族人群中16p11.2微缺失综合征(TBX6)的外显率应为44%。而且TBX6基因杂合性缺失的表型在不同种族中也不尽相同,在中国汉族人群主要导致半椎体畸形、脊柱侧弯[16,18]。
目前,16p11.2微缺失综合征的产前诊断报道较少,仅有少数文献报道其超声异常征象有心脏畸形、单侧多囊肾、鼻骨缺失、单脐动脉、宫内发育迟缓等[19-20]。16p11.2微缺失综合征的其他表型如发育迟缓、智力障碍和/或自闭症谱系障碍、肥胖等表型具有年龄依赖性,无法在宫内诊断,而半椎体畸形、脊柱侧弯在中国汉族人群中外显率较高,可以依靠产前超声进行诊断。笔者所报告2例的病例均表现为半椎体畸形、脊柱侧弯。病例1超声提示胎儿胸腰段脊柱侧弯,L12~S1呈半椎体畸形,单脐动脉(右侧缺如),右心室强光斑。病例2超声提示胎儿脊柱侧弯(L11~12,S1椎体向右侧侧弯),椎体排列不整齐(半椎体),羊水指数位于正常值上限。而病例3超声仅提示胎儿颈部半透明膜4.8 mm,鼻骨显示不清。一方面可能是由于16p11.2微缺失综合征存在外显率与表现度的差异;另一方面也可能是由于患者后续未行胎儿系统彩超进一步监测病情的进展。在本研究中,笔者采用全基因组SNP array技术对3个病例进行分析,不仅在分子水平准确地检出胎儿16p11.2微缺失综合征,而且排除其他基因组位点的异常。
综上所述,16p11.2 微缺失综合征在产前可出现各个系统超声异常,但椎体畸形最为常见。中国汉族人群产前超声中如果出现胎儿半椎体畸形、脊柱侧弯,应考虑16p11.2微缺失综合征的可能。SNP array分析可以有效地诊断16p11.2微缺失综合征,明确其断裂点以及所涉及的基因,有助于分析其基因型与表型的对应关系。

