几种食品添加剂对黑胡萝卜红色素热稳定性的影响
赵 昕,韩宗博,王智宇,李治城,展亚莉,常秀莲
(1.烟台大学生命科学学院,山东 烟台 264005;2.青岛鹏远康华天然产物有限公司,山东 莱西 266612)
黑胡萝卜外观为紫黑色,含有的红色素为花青素[1],花青素属于黄酮类化合物的一种,是自然界中普遍且广泛存在于植物中的天然水溶性色素,也是植物的主要呈色物质之一[2],主要作为食品和化妆品的着色剂[3].花青素类物质具有多种生物学活性,如抗衰老[4]、抗炎[5]、抗肿瘤[6]、抗突变[7]、化学预防[8]、抑制血小板凝集[9]和脂质过氧化[10]、保护视力[11]和预防糖尿病[12]等.花青素在自然条件下非常不稳定,游离状态的花色苷元极少见,一般会与单个或多个糖类在3,5位置上以化学键形式结合,形成花色苷,因此该色素也属于花色苷类.
国内对黑胡萝卜红色素的研究报道较少,主要集中在色素的提取[13]和稳定性研究.刘楠[14]研究了pH值、光、热、金属离子、抗坏血酸、氧化剂H2O2、还原剂Na2SO3、防腐剂苯甲酸钠对黑胡萝卜色素稳定性的影响.ALGARRA M[15]研究了黑胡萝卜红色素的结构.另外,田喜强[16]对黑米色素在不同温度、光照、氧化剂条件下的稳定性进行了研究, XU H G等[17]在葡萄皮色素中添加栎草亭(六羟基黄酮)、表没食子儿茶素、没食子酸酯、茶多酚、杨梅树皮甙和芸香苷,结果表明辅色剂对葡萄皮色素的稳定性有不同程度的影响.YAWADIO R等[18]研究了芳香族和脂肪族羧酸对花青素的增色效果,表明芥子酸、阿魏酸、对香豆酸能增强黑米汁的颜色,效果最强的是芥子酸(二甲基肉桂酸酯衍生物),加入后,颜色由红色向蓝色偏移.工业化生产中,70 ℃是色素真空浓缩的温度上限,热处理对色素有很大损失,为探讨食品添加剂对黑胡萝卜红色素热稳定性的影响,采用柠檬酸、草酸、阿魏酸、酒石酸、乳酸、乙酸、抗坏血酸、没食子酸、苹果酸、对香豆酸10种酸类添加剂和乳糖、β-环状糊精、壳多糖、糊精4种糖类添加剂,研究食品添加剂对黑胡萝卜红色素热稳定性的影响及其热降解动力学,以期寻找实际生产中可以维持花青素稳定的添加剂,从而为企业减少生产过程中造成的损失的同时,也为企业节约了成本.
1 材料和方法
1.1 实验仪器
SC-15数控超级恒温槽,宁波天恒仪器厂;pH211酸度计,意大利哈纳公司;WGJ7200可见分光光度计,尤尼柯(上海)仪器有限公司;TU-1900双光束紫外可见分光光度计,北京普析通用仪器有限责任公司;AR1530分析天平,奥豪斯国际贸易(上海)有限公司.
1.2 实验材料
黑胡萝卜红色素、糊精,青岛鹏远康华天然产物有限公司提供;无水乙酸钠、氯化钾、冰乙酸、草酸、柠檬酸、乳酸、酒石酸、没食子酸、抗坏血酸试剂均为分析纯,对香豆酸、阿魏酸、DL-苹果酸试剂均为食品级.
1.3 分析和试验方法
1.3.1 花色苷总量的测定 黑胡萝卜中的红色素属于花色苷类,花色苷总量的测定采用pH示差法[16],以矢车菊-3-葡萄糖苷计.
分别以pH值 1.0 和4.5 的缓冲溶液对储备样品进行适当稀释.以水做空白,分别测定 520和 700 nm 波长下的吸光度.
在700 nm波长下测定吸光度是为了校正混浊对测定结果的干扰.如果稀释后的样品过于混浊,测定前采用离心或过滤的方法进行澄清处理.采用的过滤器不能吸收花青素.测量前先用pH值 1.0 的溶液稀释,确定合适的稀释倍数,使其吸光度在0.2~0.7的范围内,再用pH值 4.5 的溶液测量其吸光度.
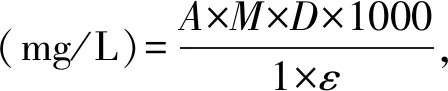
式中:吸光度A=(A520-A700)pH1.0-(A520-A700)pH 4.5,
M(摩尔质量)为449.2 g/mol,以矢车菊-3-葡萄糖苷为基准;D为样品储备液的稀释倍数;1为光路长,cm,测试中采用1 cm 光路长的比色皿;ε为矢车菊-3-葡萄糖苷的摩尔消光系数,为26 900 L·mol-1·cm-1;1 000为由g换算成mg的转换系数.
1.3.2 不同酸类添加剂对黑胡萝卜色素稳定性的影响 在1.0 mg/mL黑胡萝卜红色素溶液中添加相同量的柠檬酸、草酸、阿魏酸、酒石酸、乳酸、乙酸、抗坏血酸、没食子酸、苹果酸和对香豆酸10种酸类添加剂,在水浴锅中70 ℃条件下水浴120 min,每隔30 min取样测定溶液花青素含量.
1.3.3 糖类添加剂对黑胡萝卜色素稳定性的影响 在1.0 mg/mL黑胡萝卜红色素溶液中添加相同量的乳糖、糊精、β-环状糊精和壳多糖4种糖类添加剂,在水浴锅中70 ℃条件下水浴180 min,每隔30 min取样测其花青素含量,通过热降解动力学实验来比较不同酸类添加剂对色素的影响.
1.3.4 热降解动力学分析 由于黑胡萝卜红色素为花色苷类色素,所以其降解动力学反应为零级动力学[19]或者一级动力学[20-21].
(1) 零级动力学
零级反应动力学的方程式及半衰期t1/2为
Ct=C0-kt,t1/2=C0/2k,
式中:C0为初始时刻花色苷的含量;Ct为一定温度下加热t时间后花色苷含量;K为反应动力学常数;t1/2为反应半衰期即花色苷降解一半时所需要的时间.
(2) 一级动力学
一级反应动力学方程经常用来表征食品品质的变化过程.
一级反应速度常数k及半衰期t1/2为
ln(Ct/C0)=ln(At/A0)=-kt,
t1/2=-ln 0.5×k-1,
式中:C0为初始时刻花色苷的含量;Ct为一定温度下加热t时间后花色苷含量;其中C0和Ct可用A0和At代替.A0为初始时刻花色苷样品液在最大吸收波长处的吸光度;At为一定温度下加热t时间后花色苷样品液在最大吸收波长处的吸光度.
2 结果与讨论
2.1 不同酸类添加剂存在下黑胡萝卜红色素的热稳定性
10种酸类添加剂在70 ℃下加热120 min后黑胡萝卜残余花色苷的含量在草酸、柠檬酸、乳酸、乙酸、酒石酸、没食子酸、苹果酸中明显高于空白(图1(a)),而在抗坏血酸、对香豆酸、阿魏酸这3种添加剂中要明显低于空白(图1(b)).
图1(a)为70 ℃下加热120 min后,残余花色苷含量高于空白值的有机酸.由图1(a)知,黑胡萝卜红色素在前30 min下降低最快,可能是由于高温引起色素分子上糖基的破坏,从而导致其降解[22];在第2个30 min下基本没有变化,以后除空白和没食子酸外,其他有机酸的存在使所测得的花青素含量在逐渐增加,颜色加深,目前,文献上尚未有此现象的报道,推测其原因为:高温使有机酸跟色素的羟基发生酯化反应,随着加热时间延长,酯化反应程度增加,花色苷更稳定存在.其中草酸、柠檬酸、乳酸和酒石酸存在的情况下,黑胡萝卜红色素在高温环境中的稳定性较好,草酸效果最好.
热降解动力学数据采用零级和一级动力学模型进行拟合,表1中很低的相关系数表明零级和一级动力学方程都不能很好的表征动力学数据,可能是由于发生了酯化反应,所以不遵循此热降解动力学规律.因此,根据实验结果采用多项式拟合的方法,拟合了有机酸的热降解动力学数据,如图2所示,拟合的方程以及R2在表1右列中,方程与实验数据的相关系数均高于0.9,拟合结果较好.总之,草酸最有利于黑胡萝卜红色素的稳定,而抗坏血酸最不利于其稳定.
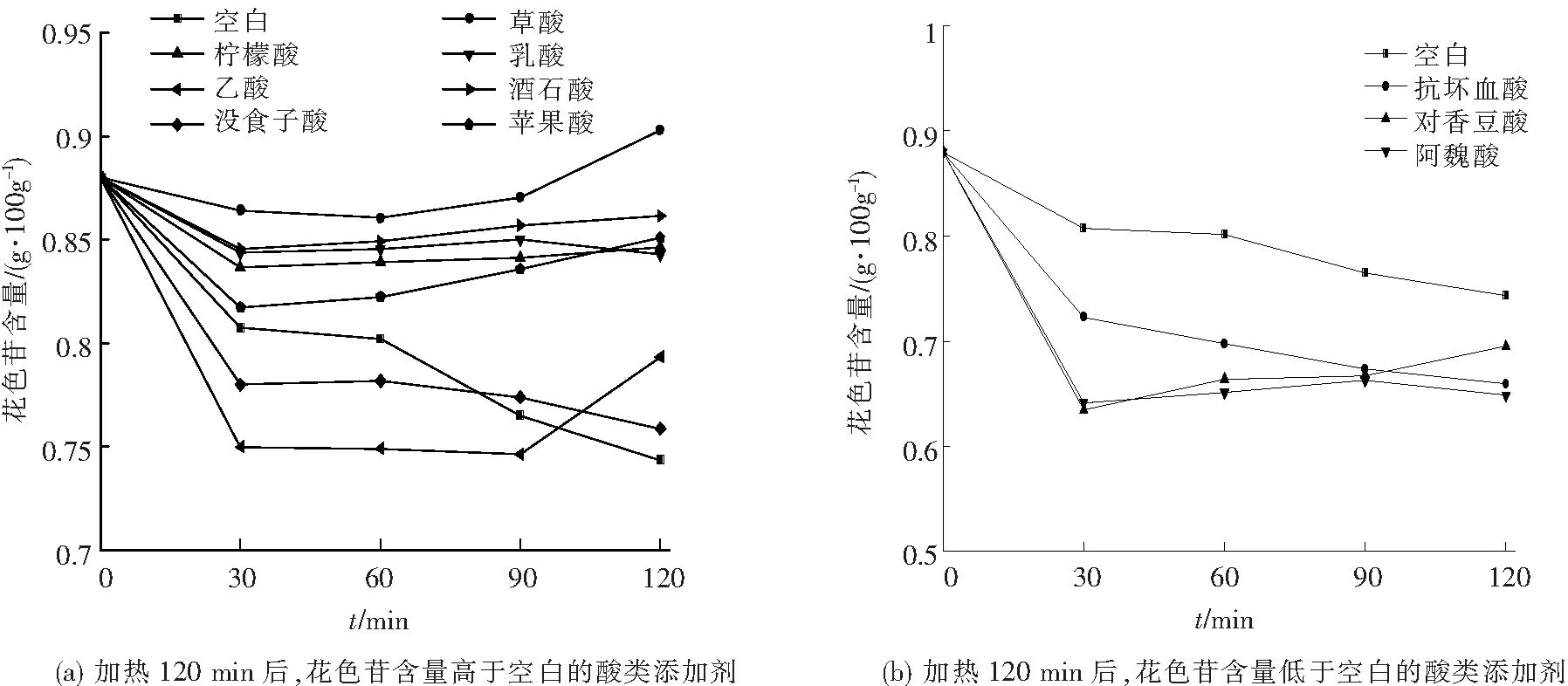
图1 不同酸类添加剂对黑胡萝卜红色素稳定性的影响
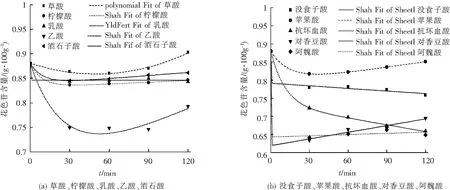
图2 不同酸类添加剂对黑胡萝卜红色素热降解动力学的影响
2.2 不同糖类添加剂存在下黑胡萝卜红色素的热稳定性
乳糖、β-环状糊精、壳多糖和糊精4种糖类添加剂加入到黑胡萝卜红色素溶液中,70 ℃下作用不同时间,色素残留量随时间的变化关系如图3所示.图3可知,随着加热时间的延长,包括空白在内的5组样品中的花色苷含量均呈现下降趋势,其中糊精在短时间内加热(30 min)色素溶液花色苷含量上升,添加β-环状糊精、乳糖和壳多糖的溶液中花色苷含量下降明显.因此,除糊精可以增强稳定性外,其他糖类添加剂的存在并不能增强色素溶液的稳定性.用色素的零级和一级热降解动力学方程来拟合实验数据,拟合参数如表2所示,零级和一级动力学方程都能很好地拟合实验数据,且拟合效果相近,综合考虑零级和一级动力学的R2,色素的热降解一级动力学稍显优势,因此将一级动力学数据进行作图拟合,如图4所示,可以清楚看出除β-环状糊精外,其他糖类添加剂的拟合效果很好.

表1 黑胡萝卜红色素在不同酸类添加剂中的热降解动力学参数
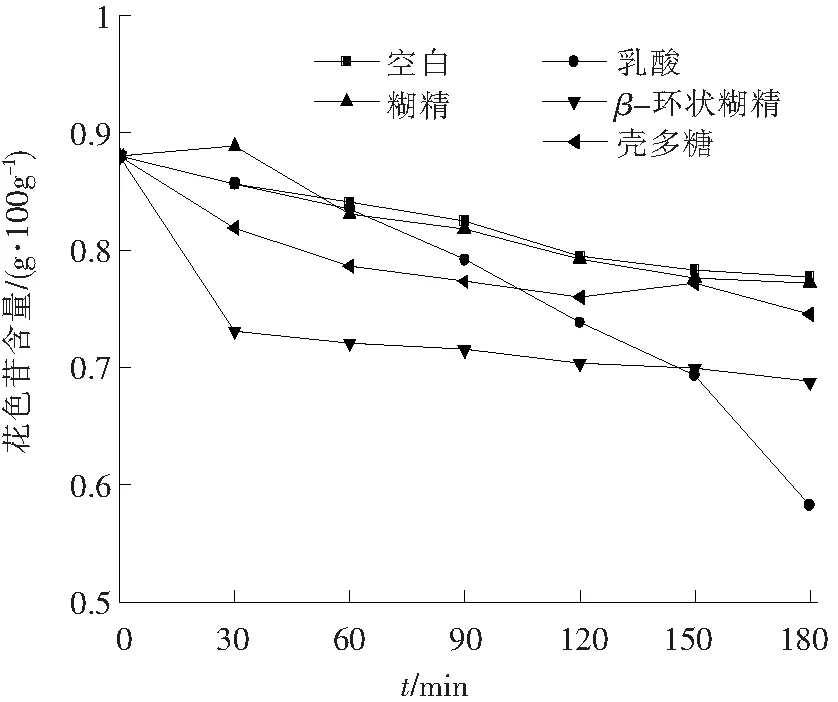
图3 不同糖类添加剂对黑胡萝卜红色素稳定性的影响

图4不同糖类添加剂对黑胡萝卜红色素热降解动力学的影响
Fig.4 Effect of different sugar additives on the thermal degrada-tion kinetics of black carrot color
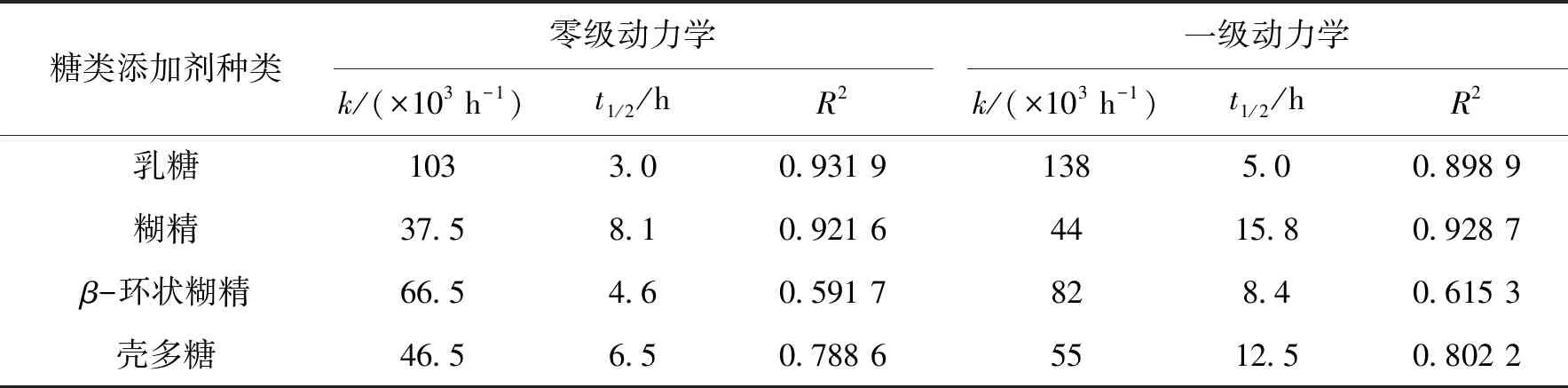
表2 色素在不同糖类添加剂中的热降解动力学参数
2.5 草酸和糊精对黑胡萝卜红色素的热稳定性比较
实际工业化浓缩过程中,热处理的时间与待处理浓缩的物料量的多少及浓度有关,由于物料量及浓度不定,因此需要的处理时间不同.通过上述实验可以看出,长时间加热下,加入酸性添加剂草酸效果最好,对于需要短时间处理的溶液(30 min以内),草酸和糊精都能够增加花色苷含量,因此将二者进行实验比较,30 min内70 ℃的实验结果如表3所示.表3结果表明,在黑胡萝卜红色素中糊精的存在使色素损失仅约1%,而酸性添加剂草酸的存在与空白结果类似,色素损失分别为7.09%和8.3%,差异不大.因此,短时间加热时,糊精对色素稳定性的增强效果明显好于草酸.

表3 色素在草酸和糊精存在下的稳定性比较
3 结 论
10种酸类添加剂对黑胡萝卜红色素热稳定性的影响不同,草酸最有利于色素的稳定,而抗坏血酸使色素的稳定性更差,且酸类添加剂对色素热稳定性的影响适合用多项式方程表达;相同条件下,4种糖类添加剂均不利于色素长时间的热稳定,但糊精在30 min内对色素的热稳定性起到很好的保护效果,且稳定性高于草酸,在糖类添加剂存在下色素的热降解用零级或一级动力学方程均能较好的描述,且2种方程拟合效果相差不大.

