乳腺炎冲剂质量标准研究
段松冷 刘敏 刘礼斌


[摘要] 目的 建立乳腺炎沖剂质量标准。 方法 高效液相色谱(HPLC)法测定乳腺炎冲剂中芍药苷含量。采用Agilent EClipse SB-C18色谱柱(4.6 mm×250 mm,5 μm),甲醇-0.05 mol/L磷酸二氢钾溶液(40∶60)为流动相,流速为1.0 mL/min,检测波长230 nm,柱温30℃,进样量10 μL;薄层色谱鉴别乳腺炎冲剂中香附、当归和赤芍;重金属检查法和砷盐检查法测定乳腺炎冲剂中重金属和砷盐限度。 结果 HPLC法测定芍药苷含量:芍药苷质量浓度在5.01~501 μg/mL(r = 0.9996)范围内与峰面积呈良好的线性关系,平均回收率为99.92%,RSD = 1.26%(n = 6);薄层色谱法:样品斑点清晰,无阴性干扰;乳腺炎冲剂重金属和砷盐限度检查,结果符合规定。 结论 HPLC法测定结果准确、灵敏度高、重复性好;薄层色谱法操作简便,试验周期短,结果清晰可靠;现行药典中重金属和砷盐检查法可以用于乳腺炎冲剂重金属和砷盐的的限度检查,以上方法为建立乳腺炎冲剂治疗标准提供了依据。
[关键词] 乳腺炎冲剂;质量标准;高效液相色谱法;薄层色谱;重金属砷盐限度检查
[中图分类号] R282 [文献标识码] A [文章编号] 1673-7210(2019)12(c)-0111-04
[Abstract] Objective To establish the quality standard of Mastitis Granules. Methods Paeoniflorin content in Mastitis Granules was determined by high performance liquid chromatography (HPLC). Agilent EClipse SB-C18 column (4.6 mm×250 mm, 5 μm) was used as the column, methanol-0.05 mol/L potassium dihydrogen phosphate solution (40∶60) was used as the mobile phase, the volume flow rate of 1.0 mL/min, with the detection wavelength of 230 nm. The colomn temperature maintained at 30℃. The injection volume was 10 μL. The identification of Cyperus rotundus L., Angelica sinensis and Paeoniae Radix Rubra in Mastitis Granules were determined by thin-layer chromatography (TLC). The limits of heavy metals and arsenic salts in Mastitis Granules were determined by heavy metal test method and arsenate test separately. Results The content of paeoniflorin was determined by HPLC. The paeoniflorin in the range of 5.01-501 μg/mL(r = 0.9996) showed a good linear relationship with the peak area. The average recovery rate was 99.92%, RSD = 1.26% (n = 6). The spots of TLC samples were clear and there was no negative interference, the limit tests of heavy metals and arsenic salts in Mastitis Granules were in accordance with the regulations. Conclusion The results of determination by HPLC are accurate, sensitive and reproducible. TLC method is simple and easy to operate, with short test period and clear and reliable results. The current pharmacopoeia method for heavy metals and arsenic salts can be used for the limit examination of heavy metals and arsenic salts in Mastitis Granules. The above methods provide a basis for establishing the treatment standard of Mastitis Granules.
[Key words] Mastitis Granules; Quality standard; High performance liquid chromatography; Thin-layer chromatography; Limit examination of heavy metal arsenic salt
乳腺炎冲剂是北京市医疗机构的法定中药制剂,北京市多家医疗机构具有该制剂的批准文号,用于治疗乳腺炎等疾病。本制剂收载于《医疗单位制剂规程》[1],是由柴胡、桔叶、炙香附、川楝子、瓜蒌、败酱草、丝瓜络、当归、赤芍、陈皮组成的复方制剂。《医疗单位制剂规程》[1]没有关于该制剂定性定量的控制项目,亦没有对乳腺炎冲剂质量标准其他项目提出要求,查阅文献,尚缺乏对乳腺炎冲剂质量标准研究的相关收载。因此,本研究参考首都医科大学附属北京世纪坛医院(以下简称“我院”)乳腺炎冲剂生产工艺规程,以我院制剂室生产的乳腺炎冲剂为研究对象,以加强乳腺炎冲剂质量控制为目的,建立了乳腺炎冲剂中芍药苷含量测定的高效液相色谱(HPLC)法,对柴胡、瓜蒌、香附、川楝子、当归、赤芍的薄层色谱鉴别进行了研究,建立了香附、当归和赤芍的薄层色谱鉴别方法,并考察了该制剂重金属及砷盐情况。该研究结果为重新修订《医疗单位制剂规程》提供了的试验依据。
1 仪器、试剂与试药
高效液相色谱仪(导津公司 LC-20A),千分之一电子分析天平(梅特勒GB303),甲醇、甲苯等试剂均为分析纯。柴胡(批号:120992-201108)、瓜蒌(批号:120836-201211)、香附(批号:121059-200706)、当归(批号:120927-201315)对照药材及芍药苷对照品(批号:110736-201136)均购自中国食品药品检定研究院。乳腺炎冲剂样品(批号:20180622、20180623、2018 0624)为我院制剂室制备。柴胡阴性(批号:20180622)、瓜蒌阴性(批号:20180622)、香附阴性(批号:20180629)、当归阴性(批号:20180829)及赤芍阴性(批号:0180706)样品为实验室制备。
2 方法与结果
2.1 HPLC法测定芍药苷含量
2.1.1 色谱条件 Agilent EClipse SB-C18色谱柱(4.6 mm×250 mm,5 μm),甲醇-0.05 mol/L磷酸二氢钾溶液(40∶60)为流动相,检测波长230 nm,柱温30℃,流速1.0 mL/min,进样量10 μL。理论板数按芍药苷峰计算应不低于3000。
2.1.2 溶液的制备 取芍药苷对照品适量,精密称定,加甲醇制成0.501 mg/mL芍药苷的溶液作为对照品溶液。取研细后的乳腺炎样品0.5 g,精密称定,置于锥形瓶中,加甲醇25 mL,称重,浸泡30 min,超声提取30 min,放冷,补重,滤过作为供试品溶液。照供试品溶液制备方法取赤芍阴性样品制备赤芍阴性对照溶液。
2.1.3 专属性考察 吸取芍药苷对照品溶液、供试品溶液、芍药苷阴性对照溶液各10 μL,结果阴性对照无干扰,与相邻峰分离度良好。见图1。
2.1.4 线性关系考察 取上述制备的对照品溶液,逐级稀释成浓度为5.01、10.02、20.04、50.1、100.2、200.4、501 μg/mL的芍药苷标准品溶液,各吸取10 μL,注入高效液相色譜仪,测定,绘制标准曲线,得到回归方程:Y = 14 052X-63 298,R2 = 0.9996。
2.1.5 精密度试验 精密吸取芍药苷对照品溶液(0.501 mg/mL)适量,连续进样6次,测定对照品的峰面积,平均值为1 059 998,RSD值为0.23(n = 6),提示仪器的精密度良好。
2.1.6 稳定性研究 取研细后的乳腺炎细粉0.5 g,精密称定,依法制备芍药苷供试品溶液,分别在制备后0、2、4、8、14、24 h进样进行分析,峰面积平均值为1 060 353,RSD值为0.59(n = 6),提示供试品溶液在24 h内稳定性良好。
2.1.7 重复性试验 均匀取研细后的乳腺炎细粉0.5 g,精密称定,依法制备供试品溶液6份,记录峰面积,计算芍药苷含量,测得供试品中的芍药苷含量平均值为4.09 mg/g,相对标准偏差RSD = 1.30%,提示方法的重复性良好。
2.1.8 加样回收率试验 分别精密称取9份已知含量的乳腺炎细粉0.25 g于容量瓶中,精密加入低、中、高3个水平的芍药苷对照品溶液,每个水平制备3份。按“2.1.3”项中的方法进行加样回收率试验,按“2.1.1”项中的方法测定芍药苷含量,计算加样回收率。见表4。
2.2 薄层色谱研究
2.2.1 香附的薄层色谱鉴别 取样品10 g,加乙醚40 mL,超声处理20 min,滤过,滤液挥干,残渣加乙酸乙酯1 mL使溶解,作为供试品溶液[2]。取香附对照药材1 g,同法制成对照药材溶液。取香附阴性样品10 g,按“2.2.1”项下供试品溶液制备方法制备阴性样品溶液。照薄层色谱法(中华人民共和国药典以下简称“中国药典”2015年版附录Ⅵ B)试验,吸取上述3种溶液各4 μL,分别点于同一硅胶GF254薄层板上,以二氯甲烷-乙酸乙酯-冰醋酸(80∶1∶1)为展开剂,展开,取出,晾干。置紫外光灯(254 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点,无阴性干扰。见图3。
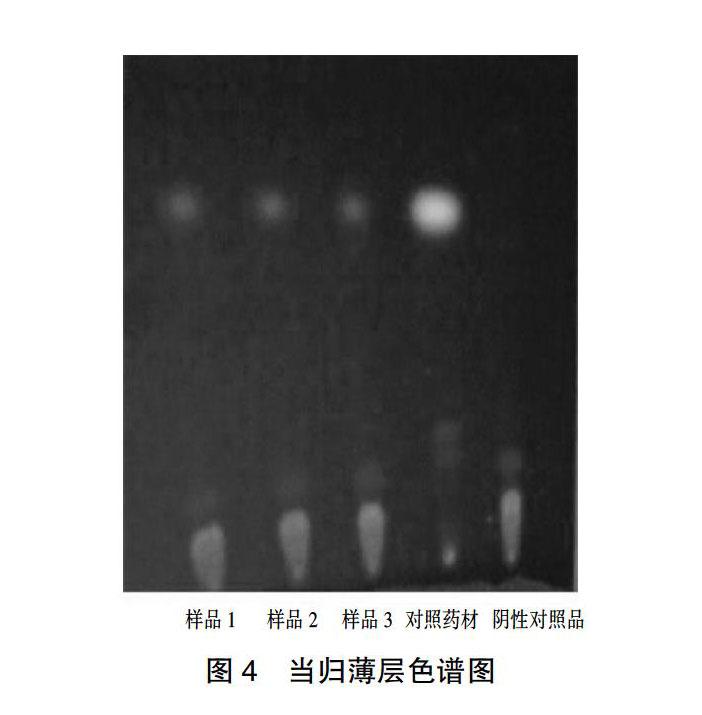
2.2.2 当归的薄层色谱鉴别 取“2.2.1”项下供试品溶液待检。取当归对照药材1 g,按“2.2.1”项下供试品溶液制备方法制成对照药材溶液。取当归阴性样品10 g,同法制成阴性样品溶液。照“2.2.1”中薄层色谱法,吸取上述3种溶液各10 μL,分别点于同一硅胶G薄层板上,以正己烷-乙酸乙酯(4∶1)为展开剂,展开,取出,晾干。置紫外光灯(365 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点,无阴性干扰。见图4。
2.2.3 赤芍的薄层色谱鉴别 取样品10 g,加乙醇40 mL,超声处理10 min,滤过,滤液挥干,残渣加乙醇1 mL使溶解,作为供试品溶液。取芍药苷对照品适量,加乙醇制成2 mg/mL的溶液,作为对照品溶液。取赤芍阴性样品10 g,按“2.2.1”项目供试品溶液制备方法制备阴性对照品溶液。照“2.2.1”中薄层色谱法,吸取上述3种溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)为展开剂,展开,取出,晾干。喷以5%香草醛硫酸溶液,加热至斑点显色清晰,日光下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点,无阴性干扰。见图5。
2.3 重金属、砷盐考察
2.3.1 重金属 取本品3批,每批各1 g,称定重量,置坩埚中,缓缓加热至完全碳化,放冷,加硫酸1 mL,低温加热至硫酸蒸气除尽后,加硝酸0.5 mL,蒸干,至氧化氮蒸气除尽后,在500~600℃炽灼使完全灰化,照《中国药典》2015版4部[3]重金属检查法第二法,对3批样品进行了测定,结果重金属检查(ppm)<10,均符合规定。
2.3.2 砷盐 取本品3批,每批各1 g,称定重量,置坩埚中,加氢氧化钙1 g,缓缓加热至完全碳化,放冷,在500~600℃炽灼使完全灰化,照《中国药典》2015版4部[3]砷盐检查法第一法,对3批样品进行了测定,结果砷盐检查(ppm)<2,均符合规定。砷斑照片。见图6。
3 讨论
本研究最初拟用HPLC法测定乳腺炎冲剂中柴胡皂苷a及皂苷d含量,查阅多篇相关文献[4-9],尝试多种色谱条件,在柴胡皂苷a保留时间处仍有干扰峰,曾尝试用大孔吸附树脂对柴胡皂苷a和皂苷d进行分离提纯[10],仍无法消除干扰。分析原因可能是因为乳腺炎冲剂药味较多,并采取煎煮法提取,大量水溶性成分的溶出使得干扰较多,较难去除。故本研究选择测定芍药苷含量对乳腺炎冲剂进行质量控制,得到了满意的结果。乳腺炎冲剂共含10味中药,无质量标准,曾对方中柴胡[11-13]、川楝子[14-15]、瓜蒌[16-17]、败酱草[18-19]、陈皮[20-21]进行薄层色谱鉴别研究,尝试中国药典及多篇文献方法皆不能取得满意效果,分析原因可能是由于乳腺炎冲剂在煎煮过程中多种药味发生化学变化,使原有药味化学成分转变,导致薄层色谱无法检识。因此,本研究仅建立了香附、当归和赤芍薄层色谱法鉴别法。医院制剂多为中药复方制剂,成分复杂,中药制剂有时重金属与砷盐的含量很高,危害人体健康,如铅在人体和动物组织中能够蓄积,人若每天摄入1 mg铅,长期则有中毒危险,过量的铅可引起贫血、神经功能失调及肾损伤[22],因此对医院制剂进行重金属与砷盐的限量检查意义重大。
[参考文献]
[1] 北京市卫生局.医疗单位制剂制规程[Z].北京:北京市卫生局,1985.
[2] 国家药典委员会.中华人民共和国药典[S].一部.北京:中国医药科技出版社,2015:158,258.
[3] 国家药典委员会.中华人民共和国药典[S].四部.北京:中国医药科技出版社,2015:101-102.
[4] 孟杰,陈兴福,杨文钰,等.柴胡主根与侧根中柴胡皂苷a及皂苷d含量测定[J].药物分析杂志,2013,33(7):1218-1212.
[5] 刘伟,杨艳玲,刘乃强,等.柴胡口服液HPLC指纹图谱及柴胡皂苷b2的含量测定[J].中国试验方剂学杂志,2013, 19(8):134-137.
[6] 李軍,姜华,张延萍,等.柴胡口服液工艺药渣中5种柴胡皂苷的含量测定[J].中国药学杂志,2012,47(16):1337-1340.
[7] 马泽刚,黄春花,钟辉云.HPLC法对不同产地柴胡根中柴胡皂苷a及柴胡皂苷d的含量测定[J].湖北农业科学,2017,56(13):2519-2520.
[8] 李竞,高英,李海龙,等.太行山区柴胡中总皂苷及柴胡皂苷a、d的含量测定[J].中国医药导报,2013,10(8):124-129.
[9] 陈新梅,王集会.无名异的质量控制.中国试验方剂学杂志[J],2013,19(7):107-109.
[10] 宋海妹,苏小凤,李楠,等,柴胡皂苷的提取与鉴定[J].大连轻工业学院学报,2015(1):15-18.
[11] 严华,董亚娟,程显隆,等.南柴胡与常见混伪品的鉴别方法研究[J].中国药学,2015,50(2):109-114.
[12] 戴培慧,马瑞莲,高佳丽,等.基于HPLC分析柴胡黄芩配伍的主要化学成分研究[J].世界中医药,2017,12(7):1660-1663.
[13] 李腾,高展,孙玉侠,等.柴胡及其制剂中皂苷类成分的研究[J].中成药,2011,33(11):1840-1843.
[14] 王志朝,丁志民,张孟佑,等.三子胶囊的制备及质量标准研究[J].中国药房,2007,18(9):665-666.
[15] 杜怡昊,刘建华,李计龙,等.川楝子中香草酸含量测定研究[J].天然产物研究与开发,2011,23(6):1103-1106.
[15] 韩毅,于艳,吴振起,等.清肺膏的质量标准研究[J].山西医科大学学报,2018,49(1):31-35.
[16] 陈秀敏,靳凤云,彭小冰,等.消疬胶囊质量标准研究[J].中药材,2016,39(5):1094-1097.
[17] 陈惠玲,曾荣洁.妇炎消胶囊质量标准的研究[J].中国药品标准,2014,15(4):272-275.
[18] 罗玉鸿,梁飞华,黄好武,等.复方妇炎平胶囊质量标准控制[J].中国医院药学,2009,29(1):73-75.
[19] 韩冬,程东岩,王隶书.百苑止咳颗粒质量标准的建立[J].中国药师,2018,21(8):1471-1473.
[20] 莫结丽,张靖,宫璐,等.陈皮精准煮散饮片与市售饮片的质量[J].世界中医药,2017,12(11):2786-2790.
[21] 徐乐,孔亚萍,孙慧珠,等.舒肝丸质量标准中薄层和液相方法完善研究[J].中国药事,2018,32(4):516-521.
[22] 圭源.药理学[M].北京:中国医药出版社,2003:316-336.
(收稿日期:2019-08-21 本文编辑:刘永巧)

