不同性别OSAHS合并高血压患者的危险因素分析
于阅尽 黄卫 郝亚楠 李佩 高轶昳 徐迎辉
(上海中医药大学附属第七人民医院,(1.耳鼻喉科;(2.心血管内科,上海 200137)
研究[1]发现,阻塞性睡眠呼吸暂停低通气综合征(OSAHS)患者常以心血管系统异常表现为首发症状和体征,而且OSAHS合并高血压患者的晨起血压较单独性高血压患者升高明显。OSAHS是除年龄、性别、肥胖、吸烟、酗酒、心脏、肾脏疾病及精神因素以外引起高血压的一个独立危险因素[2]。多项研究指出[3],OSAHS 的患病率男性多于女性,OSAHS合并高血压患者也呈现男性多于女性的差异,但是目前的治疗没有因为性别差异而有所不同。不同性别OSAHS合并高血压患者的发病危险因素是否在共性中也存在差异性?本研究主要探讨不同性别OSAHS合并高血压患者的危险因素。
1 资料与方法
1.1一般资料 连续选择2015年12月至2017年12月入我院诊断OSAHS合并高血压男性和女性各90例,纳入标准:符合中华医学会耳鼻咽喉头颈外科学分会制定的OSAHS诊断标准[4]和2014年《中国高血压基层管理指南》关于原发性高血压的诊断标准;年龄18~75岁;OSAHS和高血压均未行任何药物或手术干预;OSAHS和高血压病程至少>1个月;临床资料完善,取得知情同意权。排除标准:继发性高血压、严重心、肝、肺、肾、脑等脏器功能障碍;依从性差,同时参与其他研究或存在可能影响结果的因素等。
1.2方法 由同一经严格培训的调查团队完成资料搜集,观察指标包括患病年龄(确诊OSAHS和高血压的起始年龄)、OSAHS病程和分级、高血压分级、体质量指数(BMI)、打鼾分级、Epworth嗜睡量表评分,吸烟、饮酒、运动、钠盐摄入量,高血压、糖尿病以及心脑肺家族史,血生化指标包括巨细胞病毒感染、C反应蛋白(CRP)、血糖、血脂、尿酸和内皮素-1(ET-1)水平。采用多导睡眠图(PSG)监测睡眠呼吸暂停低通气指数(AHI)将OSAHS分为轻度(5~15)、中度(15~30)及重度(>30)。高血压分级包括轻度(140~149/80~89 mmHg)、中度(150~159/90~99 mmHg)和重度(≥160/100 mmHg)。打鼾分级分为0级(从不打鼾)、1级(较正常人呼吸音粗重)、2级(较正常人说话声音响亮)、3 级(同房间人无法入睡)和4级(伴睡眠呼吸间歇现象)。Epworth嗜睡量表共8个项目,每项设置0~3分,分数相加,总分0~24分,分数越高代表白天嗜睡情况越严重。采用常规生化法检测血糖、血脂和尿酸水平,日立3700型全自动生化检测仪及配套试剂;胶体金法检测巨细胞病毒感染,试剂购自美国Sigma公司;ELISA法检测hs-CRP和ET-1水平,试剂购自美国R&D公司;均严格按照说明书步骤进行,分别测量3次取平均值。
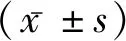
2 结 果
2.1两组患者的病情比较 男性组患者年龄较轻、OSAHS病程较长和分级较重、高血压分级较高、BMI值较大、打鼾分级和Epworth评分较高,差异均有统计学意义(P<0.05)。见表1。

表1 两组患者的病情比较
2.2两组患者的生活方式和家族史比较 男性组患者吸烟、饮酒、钠盐摄入量较高,差异有统计学意义(P<0.05)。见表2。
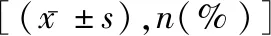
表2 两组患者的生活方式和家族史比较
2.3两组患者的血生化指标比较 男性组患者hs-CRP、尿酸和ET-1水平较高,而女性组患者血巨细胞病毒感染率较高,差异有统计学意义(P<0.05)。见表3。进一步对各组血清ET-1浓度变化进行比较:轻度OSAHS,男性为(39.7±7.3) ng/L,女性为(38.6±6.16) ng/L;中重度OSAHS,男性为(44.5±9.4) ng/L,女性为(45.4±5.24) ng/L。男女中重度OSAHS组明显高于轻度OSAHS组(t=4.61,4.23,P均<0.05)。
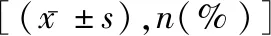
表3 两组患者的血生化指标比较
3 讨 论
研究[5]显示,绝经期后未使用激素替代治疗的女性睡眠呼吸暂停发病率明显上升,接近男性发病率,性激素在OSAHS的发生中可能起到重要作用。吸烟、喝酒、钠摄入量可能也是引起OSAHS的危险因素。吸烟、饮酒在本组病例中均占有相当成分,且男性比例显著高于女性,尤其是吸烟。吸烟可导致咽部慢性炎症、上气道阻力增加,致使打鼾的危险性增加。酒精可抑制醒觉反应,延长呼吸暂停时间,同时降低上气道扩张肌对低氧和高碳酸血症的反应性,使上气道易于塌陷。这可能是也男性OSAHS患者较女性患者病情更严重的部分原因。
hs-CRP被公认为是最有价值的急性时相反应蛋白,是反映非特异性炎症的最主要、最敏感的指标之一。本研究发现,患者hs-CRP、尿酸和ET-1水平均较高(P<0.05),且男女中重度OSAHS组血清ET-1水平明显高于轻度OSAHS组,这可能是呼吸暂停引起反复低氧血症、高碳酸血症和pH值失代偿,导致了血管内皮细胞损伤和功能紊乱,这些因素通过刺激中枢和外周化学感受器兴奋交感神经系统,导致夜间及醒后血压升高,低氧-化学感受器-交感神经兴奋,激活某些内生血管活性肽,使内皮细胞分泌过多的ET-1[6]。有研究[7]发现,OSAHS患者血清ET-1水平并不升高,认为ET-1可能在OSAHS发病的病理生理中不起重要作用。总之目前大多数研究认为OSAHS反复发生的呼吸暂停低通气引起的低氧血症,以及睡眠结构紊乱均可引起血管内皮细胞的损伤,这时候血管内皮细胞产生过多的ET-1进一步诱发高血压;同时高血压又能加重血管内皮细胞的损伤,产生过多的ET-1,形成恶性循环。
本研究显示,女性组患者高血压家族史的比例高于男性组,血巨细胞病毒感染率较高(P<0.05),王立曼等[8]的研究也发现,性别不同的患者在患病率、发病年龄、临床表现及生物学行为等方面均存在一定差异;因此,我们认为不同性别OSAHS合并高血压患者的危险因素可能不同。超重和肥胖不仅是导致OSAHS的主要原因,也是我国高血压患病率增长的一个重要危险因素。BMI正常者高血压的患病率为30.0%,超重者为43.2%,而肥胖者为高达59.2%[9]。饮酒、钠盐摄人量、体力活动等生活方式[10-11],以及血脂异常、糖尿病、高尿酸血症也是目前明确导致高血压的可变危险因素[12]。此外,炎症标记物hs-CRP、巨细胞病毒感染、血管内皮细胞损伤和功能紊乱等指标对OSAHS及高血压的发生都有一定程度的影响[13]。

