喹诺酮和喹啉类化合物的抗单纯疱疹病毒活性
张姝,李红,梅敏,冯连顺,刘明亮,郭慧元,*
(1 武汉谱尼科技有限公司,武汉 430014;2 中国医学科学院北京协和医学院医药生物技术研究所,北京 100050)
1 前言
单纯疱疹病毒(HSV)根据其抗原性质的差异可分为HSV-1和HSV-2两个亚型,两亚型病毒核苷酸序列有50%同源性[1,2]。HSV可经口腔、呼吸道、生殖器以及皮肤破损处侵入体内,潜居于人体正常黏膜、血液、唾液、神经组织和各种器官内,引起人类多种疾病如龈口炎、角膜结膜炎、脑炎以及生殖系统感染和新生儿的感染等[3,4]。HSV-1主要侵犯面、脑及腰以上部位,而HSV-2主要侵犯生殖器及腰以下部位[5]。HSV感染人群极为普遍,据世界卫生组织(WHO)统计全球50岁以下人群约有37亿人感染过HSV-1和HSV-2,70~90%的成人曾感染过HSV-1[6]。目前,对HSV感染的控制尚无特异性有效措施[7,8]。疫苗对阻止原发HSV感染有效,但重组HSV-2糖蛋白疫苗却不能保护生殖器的再感染[9]。而临床上使用的抗HSV药物如无环鸟苷、阿糖腺苷等虽能通过抑制HSV DNA合成,减轻临床症状,但不能从根本上防止潜伏感染的再发[10]。
喹诺酮和喹啉类化合物具有抗菌[11,12]、抗结核[13,14]、抗肿瘤[15,16]、抗疟疾[17-19]和抗病毒(包括HSV)[20,21]等多种生物活性。喹诺酮类药物在临床上广泛用于各种细菌感染的治疗,而喹啉类化合物是治疗疟疾的常见药物。除此之外,某些喹诺酮和喹啉类化合物如voreloxin、quarf l oxin、贝达喹啉和evitegravir等已在临床上用于治疗肿瘤、结核病和HIV等各种疾病[22]。目前,使用过喹诺酮和喹啉疗法的患者已达数十亿人次,为人类健康做出了巨大贡献[23]。
喹诺酮和喹啉结构骨架可修饰的位点较多,几乎所有位点均可被修饰。因此,在发现全新结构骨架愈发困难的今天,喹诺酮和喹啉类化合物已成为科学家竞相研究的热点[24,25]。近年来,药物化学家对喹诺酮和喹啉进行了系统而广泛的结构修饰,这类化合物的生物活性不断拓展,构-效关系(SAR)不断完善。本文将着重介绍近年来喹诺酮和喹啉类化合物在抗HSV领域的最新研究进展,并归纳此类药物的SAR,以启迪科学家设计活性更高的候选物。
2 喹诺酮衍生物
喹诺酮具有生物活性谱广、药代动力学性质和安全性良好等诸多优点,在药物化学领域占据重要位置[26,27]。喹诺酮可分为2-喹诺酮和4-喹诺酮,其中目前临床上使用的喹诺酮类药物均属于4-喹诺酮,而某些2-喹诺酮类化合物如viridicatol和tipifarnib等目前正处于临床评价阶段,也引起了药物化学家的极大关注[28,29]。
Pandey等评价了2-喹诺酮三聚体1(图1)的体外抗乙脑病毒、HSV-1和体内抗高血压活性,发现三聚体1a对乙脑病毒和HSV-1无活性,而1b则具有潜在的体外抗乙脑病毒、HSV-1和体内抗高血压活性[30]。三聚体1b抗乙脑病毒和HSV-1的半数效应浓度(EC50)分别为15.62和62.5 μg/mL,且对VERO细胞无毒,值得进一步优化。

图1 2-喹诺酮衍生物1的化学结构
氟喹诺酮类药物环丙沙星、洛美沙星、氧氟沙星、培氟沙星和如氟沙星也具有微弱的抗HSV-2活性,但不具备进一步研究价值[31]。研究表明,氟喹诺酮2 (K-12)具有广谱抗病毒活性(图2),对HIV-1(包括耐药株)、HIV-2、猴免疫缺陷病毒(SIV)、松鼠猴疱疹病毒(HVS)、人类巨细胞病毒(HCMV)和带状疱疹病毒(VZV)的活性较高,EC50为0.2~6.9 μmol/L,但对HSV-1和HSV-2的活性较弱,EC50为98 μmol/L[32]。
Lecero等研究了一系列喹诺酮羧酸酯(3)及其羧酸衍生物(4)的体外抗HSV-1活性,发现所有衍生物对HSV-1均显示出潜在的活性,在浓度为50 μmol/L时的抑制率为58~99%[33]。对活性最高的9个化合物(3b~d, 3f, 3j, 4a, 4d, 4i和4j)抗HSV-1的EC50和对VERO细胞系的细胞毒性测定结果表明,所选化合物对HSV-1的EC50较低(EC50: 0.7~3.2 μmol/L),且对VERO细胞无毒(半数细胞毒性浓度/CC50: >500 μmol/L),安全性良好。SAR显示,总体而言,羧酸酯的活性略优于相应的羧酸;对于羧酸酯3而言,向喹诺酮母核的C-6位引入卤素氟、氯和溴对活性有利;对羧酸衍生物4而言,向喹诺酮母核的C-7位引入卤素氟、氯和溴可提高活性。活性最高的化合物3d, 3j和4j对HSV-1的EC50分别为0.80, 0.87和0.70 μmol/L,CC50分别为1250, 1196和1200 μmol/L,选择性指数(SI)分别为1562, 1375和1714,活性和毒性优于无环鸟苷(EC50: 1.09 μmol/L和CC50: 960 μmol/L)。良好的活性和安全性,使得三者极具进一步研究价值。喹诺酮衍生物5具有潜在的抗HIV-1和HSV-1活性,其抗HIV-1活性是抗HSV-1活性的上百倍[34]。
Wentland等对一系列6-氨基喹诺酮-3-酰胺的体内外抗包括耐药株在内的HSV-1和HSV-2活性评价结果显示,这类化合物对所测病毒株具有潜在的体内外活性,但抗HSV-1活性远优于抗HSV-2[35,36]。其中,代表物6对所测包括耐药株在内的7株HSV-1和HSV-2的EC50低至0.13~0.32 μmol/L,对其中6株病毒的活性是对照药无环鸟苷(EC50: 0.29~77 μmol/L)的2.2~592.3倍。在小鼠感染HSV-2模型中,代表物6在口服给药剂量为25 mg/kg时的体内活性与无环鸟苷在口服给药剂量为400 mg/kg时的活性相当。总之,代表物6对包括耐药株在内的HSV-1和HSV-2均具有良好的体外活性,在小鼠感染HSV-2模型中也显示出优秀的体内活性,可作为先导物进一步研究。
喹诺酮并吡咯衍生物7对HCMV、VZV和HSV-1具有广谱抗病毒活性,IC50为0.03~2.1 μmol/L[37]。对抗HSV-1而言,吡咯环上的取代基链越短对活性越有利。其中,化合物7a的抗HSV-1活性最高,IC50为0.8 μmol/L,优于对照药无环鸟苷(IC50: 2.1 μmol/L),值得进一步优化。
4-喹诺酮衍生物8抗HSV-1和HSV-2的SAR显示,N-1位取代基对活性至关重要,无取代基衍生物的活性普遍优于甲基衍生物[38]。向喹诺酮母核的C-8为引入甲基和甲氧基均会导致抗HSV-2活性的消失,甲氧基的引入对抗HSV-1也不利,但甲基的引入对抗HSV-1有利。化合物8d的活性最高,抗HSV-1和HSV-2的IC50均为29.4 μmol/L,但远弱于对照药无环鸟苷(EC50: 0.2和2.1 μmol/L)。
研究表明,C-6位取代的喹诺酮-呋喃核糖杂合体9及其位置异构体10具有良好的抗HSV活性[39-41](图3)。其中,杂合体9b的活性最高,其抗HSV-1 (KOS), HSV-1 (AR29)和HSV-2的EC50分别为1.3,1.4和1.1μmol/L,活性与对照药无环鸟苷(EC50: 0.99,5.8和1.4 μmol/L)相当或更优[41]。不仅如此,杂合体9b(CC50: 1500 μmol/L)对VERO细胞系的毒性弱于无环鸟苷(CC50: 860 μmol/L)[41]。而喹诺酮-腙杂合体11对HIV-1和HSV-1 DNA聚合酶均有潜在的抑制活性,值得进一步研究[42]。
3 喹啉衍生物
喹啉结构骨架是重要的药效团,在抗疟疾领域有着极为广泛的应用[43,44]。除具有抗疟疾活性外,某些喹啉类化合物还具有潜在的抗HSV活性。吡唑类化合物具有潜在的抗HSV活性,将其与喹啉杂合可能会进一步提高此类化合物的活性[45]。喹啉并吡唑杂合体12(图4)具有良好的抗HSV活性,SAR显示,向R位引入供电子基甲基和甲氧基时可提高活性[46]。其中,杂合体12c的体外抗HSV-1活性略优于无环鸟苷,而在小鼠体内的急性毒性与无环鸟苷相当,值得进一步开发。进一步研究发现,向吡唑C-3位的氨基引入D-葡萄糖、D-半乳糖、D-甘露糖、D-阿拉伯糖和D-木糖所得的杂合体13并不能提高这类化合物的抗HSV-1活性[47]。喹啉并吡唑烷酮-呋喃核糖杂合体14仅显示出微弱的抗HSV-1活性,其在浓度为100 μmol/L时对HSV-1的抑制率仅为15~35%[48]。

图2 4-喹诺酮衍生物2~8的化学结构
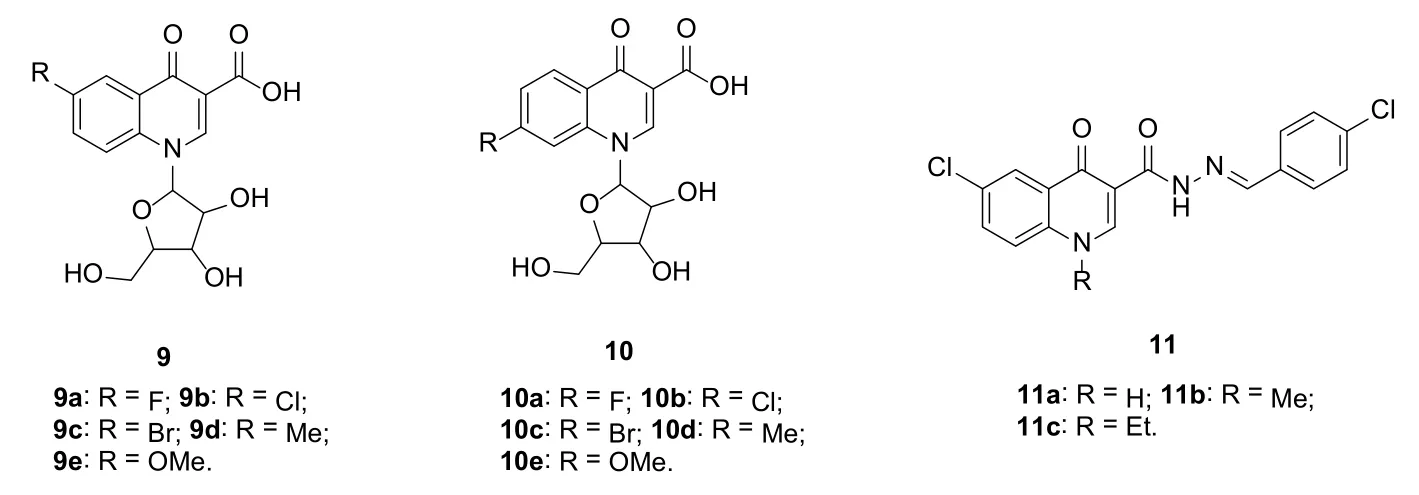
图3 喹诺酮杂合体衍生物9~11的化学结构
咪唑类化合物也具有广泛的生物活性[49],某些喹啉-咪唑杂合体如咪喹莫特(15a)和雷西莫特(15b)具有一定的抗HSV活性[50,51](图5)。因此,有必要研究这类杂合体的抗HSV活性。喹啉并咪唑16a对HSV-1 (KOS)和HSV-2 (G)具有潜在活性,EC50分别为5.4和2.4 μmol/L,与Cidofovir (EC50为2 μmol/L)相当[52]。SAR显示,氮原子的引入将导致活性消失,如杂合体16b,c对HSV-1 (KOS)和HSV-2 (G)的EC50>100 μmol/L。喹啉并咪唑-呋喃核糖杂合体17及其位置异构体18 (EC50: 70~>100 μmol/L)对HSV-1无活性或活性较弱,杂合体17b的活性最高,EC50仅为70 μmol/L[53]。
绝大多数喹啉-三氮唑和喹啉-噁唑杂合体未显示出任何抗HSV活性,不具备进一步研究价值[54-56]。四氢喹啉衍生物19具有潜在的抗HSV-1和HSV-2活性,其中,化合物19a对HSV-1和HSV-2的EC50分别为1.92和0.53 μg/mL,活性与无环鸟苷(EC50: 0.5和1.0 μg/mL)相当,可作为先导物进一步优化[57]。
4 结束语
单纯疱疹病毒(HSV)感染人群极为普遍,超过70%的成人曾感染过HSV。目前,对HSV感染的控制尚无特异性有效措施,故亟需研发抗HSV新药。喹诺酮和喹啉类化合物具有药效强、毒副作用低和药代动力学性质良好等诸多优点,广泛应用于临床。不仅如此,喹诺酮和喹啉结构骨架可修饰的位点较多,在发现全新结构骨架愈发困难的今天,喹诺酮和喹啉类化合物已成为科学家竞相研究的热点。
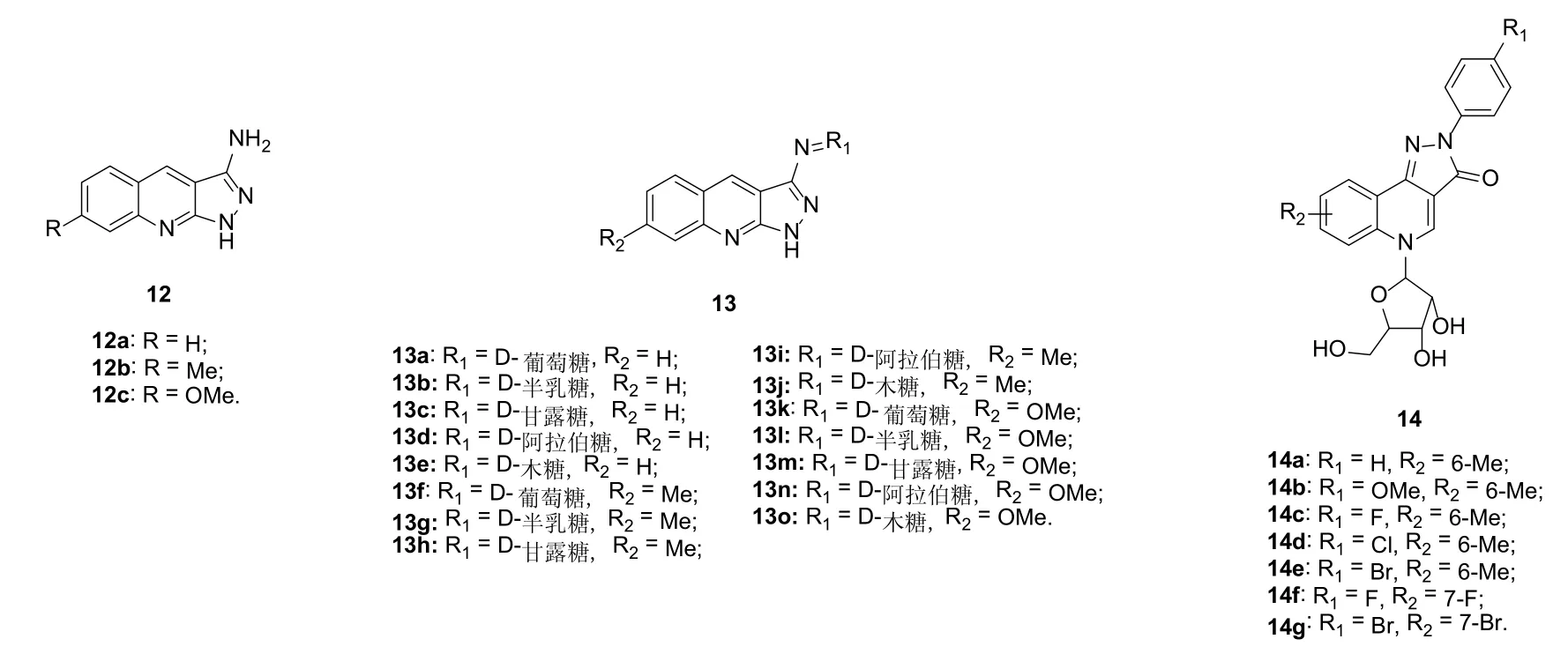
图4 喹啉并吡唑(酮)衍生物12~14的化学结构
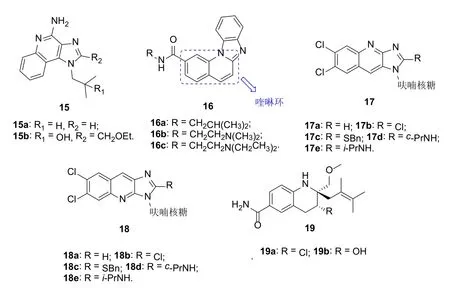
图5 喹啉并咪唑衍生物15~18及四氢喹啉衍生物19化学结构
喹诺酮和喹啉类化合物具有潜在的抗HSV活性,其中的某些化合物如6显示出良好的体内外抗HSV活性,值得进一步研究。本文着重了介绍近年来喹诺酮和喹啉类化合物在抗HSV领域的最新研究进展,并归纳了此类化合物的构-效关系,以启迪科学家设计活性更高的候选物。

