重复经颅磁刺激治疗不完全脊髓损伤后神经病理性疼痛的临床观察
何予工,杨 蕾,宋 斌
(郑州大学第一附属医院康复科,郑州 450052)
神经病理性疼痛(neuropathic pain,NP)是躯体感觉系统的损害或疾病引起的疼痛,主要表现为自发痛、痛觉过敏、感觉异常等[1]。NP是脊髓损伤最常见的并发症。相关研究表明,65%~85%的脊髓损伤患者存在慢性疼痛,其中约1/3为重度疼痛[2],且迁延不愈,严重影响患者生活质量,部分患者因疼痛难以忍受而产生抑郁情绪,甚至有自杀倾向。有研究表明,重复经颅磁刺激(petitive transcranial magnetic stimulation,rTMS)可有效缓解脊髓损伤后NP[3];但相关临床研究较少,缺乏有力证据支持。本研究采用rTMS对脊髓损伤后NP进行治疗,并与常规康复治疗进行对比,旨在为临床应用提供理论依据。
1 资料与方法
1.1一般资料 选取2017年6月至2018年7月在本院康复医学科住院治疗且符合以上标准的30例患者,按照随机数字表法将其分为治疗组和对照组,每组15例。2组患者性别、年龄、病程、损伤平面、ASIA分级等一般资料比较,差异无统计学意义(P>0.05),具有对比性,见表1。
1.2纳入标准 经CT或MRI确诊为脊髓损伤,临床表现为截瘫或四肢瘫,美国脊髓损伤协会(american spinal injury association,ASIA)分级B、C、D 级患者;神经病理性疼痛符合国际疼痛研究协会(international association for the study of pain,IASP)诊断标准[4];患者出现抑郁障碍、睡眠障碍:汉密尔顿抑郁量表(hamilton depression scale,HAMD)评分大于8分,匹兹堡睡眠质量指数量表(pittsburgh sleep quality index,PSQI)评分大于7分;无诊断明确的焦虑状态,即汉密尔顿焦虑量表(HAMA)评定小于14分;患者及家属签署知情同意书。
1.3排除标准 合并有其他原因所致的疼痛,包括脊髓损伤平面以下各类损伤性、退行性骨关节疾病,糖尿病周围神经痛等;近3个月服用过抗抑郁药物或进行过心理治疗;有认知障碍[智力状态检查量表(MMSE)<20分]或严重精神障碍不能配合评估者;存在rTMS禁忌证:有癫痫、精神分裂症等精神疾病史患者;头颈部附近有金属材料或电子仪器患者,如:心脏起搏器、电子耳蜗、金属支架等;有严重脑外伤、脑肿瘤、脑血管病、脑代谢性疾病、脑炎等患者;有严重心、肺、肝、肾等重要脏器功能衰竭患者;妊娠期妇女;长期酗酒者等。
1.4治疗方法 2组患者均给予常规康复治疗,治疗组在常规疗法的基础上增加重复经颅磁刺激治疗。
1.4.1常规康复治疗 根据患者疼痛程度、损伤程度、功能障碍程度及并发症情况,给予等速肌力训练、坐位训练、转移训练、步行训练、轮椅训练、矫形器的使用、日常生活能力训练及各种并发症的处理;同时行电刺激、气压治疗、针灸治疗、蜡疗等物理治疗。

表1 2组患者一般资料比较
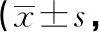
表2 2组各指标在治疗前后的比较分)
a:P<0.05,与组内治疗前比较;b:P<0.05,与对照组治疗后比较
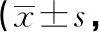
表3 2组各指标治疗前后差值组间比较分)
a:P<0.05,与对照组比较
1.4.2rTMS治疗 采用CCY-IA型rTMS治疗仪(武汉依瑞德公司)。患者取仰卧位或半卧位、闭目、放松,由治疗师测定静息运动阈值(resting motor threshold,RMT):单个rTMS脉冲刺激一侧大脑M1区,用表面电极在对侧手第一骨间背侧肌处记录运动诱发电位,调试最佳刺激点。在连续10个试次中,有5个试次诱发出至少50 mV的运动诱发电位的最低刺激强度,通过RMT来确定rTMS的刺激强度。然后将圆形线圈置于与患者颅骨表面相切对应的M1区,给予rTMS刺激。参数设置:频率 10 Hz;刺激10 s,间隔50 s;每天1次,每次15 min,每周治疗5 d,共治疗6周[5]。
1.5疗效评定 于治疗前和治疗6周后,由同一经过专门培训治疗师分别对2组患者进行疼痛程度、抑郁程度、睡眠质量评分。疼痛程度采用简易McGill 疼痛问卷(short-form of McGill pain questionnaire,SF-MPQ)进行评定[6]。该量表由疼痛评级指数(in rating index-sensory,PRI),视觉模拟评分(visual analogue scale,VAS),现实疼痛指数(present pain index,PPI)3部分组成。抑郁程度采用汉密尔顿抑郁量表(HAMD)[7],包括24项评定内容,总分大于24分,重度抑郁;总分21~24分,中等抑郁;总分8~<21分,可能抑郁;总分小于8分,无抑郁。 睡眠质量采用匹兹堡睡眠质量指数量表(pitts-burgh sleep quality index,PSQI)进行评定[8]:分值0~21分,总分大于或等于6分表示睡眠质量差,得分越高,表示睡眠质量越差。

2 结 果
治疗前,2组患者一般资料、SF-MPQ评分、HAMD评分、PSQI评分之间比较,差异无统计学意义(P>0.05)。治疗6周后,rTMS组患者SF-MPQ评分、HAMD评分、PSQI评分与组内治疗前、对照组治疗后比较,差异均有统计学意义(P<0.05);对照组患者HAMD评分、PSQI评分、SF-MPQ量表中子项目VAS评分与组内治疗前比较,差异有统计学意义(P<0.05);2组治疗前、后各项评分差值比较,差异有统计学意义(P<0.05)。见表2、3。
3 讨 论
脊髓损伤后疼痛比较公认的分类为:神经病理性疼痛、肌肉骨骼性疼痛、内脏性疼痛以及其他类型的疼痛,其中肌肉骨骼性疼痛、内脏性疼痛对症治疗后可以缓解,而神经病理性疼痛是最复杂难治的一种,可能持续存在、反复发作,需要长期治疗[9]。传统药物治疗效果有限,仅1/3的患者NP可以减轻50%[10-11];侵入性治疗,如脑深部电刺激(DBS)和硬膜外运动皮层电刺激(MCS),有治疗神经痛及患肢疼痛的相关报道,然而,其疗效仍不确定,且存在费用高、风险高等缺点;非侵入性治疗,尤其是重复经颅磁刺激,因安全、有效、不良反应少,且患者依从性较好,被认为有发展前景[12]。脊髓损伤后NP发病机制仍不明确,可能与脊髓的解剖重塑、中枢敏化、中枢去抑制有关[13]。
本研究选取30例脊髓损伤后NP患者作为研究对象,对照组患者在常规康复治疗下,疼痛程度、抑郁状态、睡眠质量有所改善;治疗组患者在rTMS治疗下疼痛程度、睡眠质量、抑郁状态显著改善,提示rTMS有利脊髓损伤后NP的康复。该结论与既往研究结论一致,YILMAZ等[14]将17例脊髓损伤后NP患者分为2组,治疗组给予rTMS刺激:频率 10 Hz,刺激强度110% RMT,每次持续15 min,疗程6周,研究结论显示 rTMS对脊髓损伤后神经病理性疼痛有显著性的疗效,但对NP后继发的抑郁情绪、睡眠障碍未进行进一步观察。有关数据显示脊髓损伤后NP与抑郁、睡眠质量之间存在着相关联,对于轻、中度抑郁患者,随着疼痛程度的减轻,抑郁程度、睡眠障碍也有所改善[15-16],本研究中补充了这一观点。李向哲等[17]采用重复经颅磁刺激(刺激靶点为 M1区,刺激频率为10 Hz,刺激强度为90%RMT,每天治疗1次,每周治疗5 d,连续治疗6周)治疗18例脊髓损伤后NP患者,发现rTMS可以缓解脊髓损伤后NP,并能改善患者疼痛相关情绪障碍和生活质量,但未使用统计学方法量化分析常规康复治疗对脊髓损伤后NP的治疗效果。DEFRIN等[18]采用rTMS治疗11例胸髓损伤后疼痛患者,疼痛程度均有不同程度的降低,一系列研究表明经颅磁刺激对脊髓损伤后NP及其继发抑郁情绪、睡眠障碍有肯定疗效。
而KANG等[19]将11例患者(其中6例患者有截瘫,5例患者有四肢瘫痪;完全性脊髓损伤 5例,不完全脊髓损伤 6例)分为2组,治疗组给予高频rTMS刺激:频率10 Hz,刺激强度80% RMT,统计结果显示高频rTMS刺激无临床意义,分析认为可能与入选患者脊髓损伤程度、损伤节段等有关。脊髓完全性损伤患者运动神经传导束严重受损,下肢感觉功能严重缺失,神经灵敏度低,治疗效果差,另外rTMS的刺激强度低可能会影响其疗效。本研究中入组标准均为脊髓不完全损伤患者,且rTMS刺激强度的设置由治疗师个体化测量确定。相关研究认为,rTMS改善脊髓损伤后神经病理性疼痛的机制可能是:改善大脑兴奋性;改善脑部血流和代谢神经;调节神经递质和基因表达;神经系统可塑性改变;降低背根神经节内过度表达的神经元型一氧化氮合酶,抑制星形胶质细胞活性[20]。
综上所述,rTMS作为一种安全、无创的新型康复治疗方法,可有效缓解脊髓损伤后NP,同时可改善慢性疼痛后继发抑郁情绪及睡眠障碍。由于本研究时间短,涉及样本量偏少,缺乏一些客观的评定方法,因此对于rTMS改善NP的长期疗效有待进一步研究来阐明。

