麻疯树籽酶解液纳米乳液体系构建及其稳定性研究
王 勇 许 晶 连子腾 郭明辉
(1.东北林业大学生物质材料科学与技术教育部重点实验室, 哈尔滨 150040;2.东北农业大学学生工作处, 哈尔滨 150030; 3.东北农业大学文理学院, 哈尔滨 150030;4.东北农业大学食品学院, 哈尔滨 150030)
0 引言
麻疯树(JatrophacurcasL.)属于大戟科麻疯树属的灌木或者小乔木,在我国主要种植或半野生于热带、亚热带地区,分布广泛,资源丰富。麻疯树籽大,结实多,含有丰富的油脂,约占其质量的50%左右,是制备生物柴油的一种理想原料[1-4]。同时麻疯树籽含有萜类、酚类、黄酮类等多种活性成分,具有杀螺、杀虫、抗菌等功效[5]。目前,常见的油料提油方法主要分为机械压榨法和溶剂浸提法,这两种方法均不能有效分离细胞壁和包裹在细胞壁中的蛋白质,容易使油脂残留在饼粕中,导致残油率较高[6-7]。随着近年来生物技术的快速发展,酶剂制备工艺简化、价格大幅降低。由于水酶法提油技术具有作用条件温和、环境友好等特性,同时能够降低高温对油脂中活性生物质的破坏,已被认为是一项极具前途的植物油提取技术[8]。
水酶法处理麻疯树籽后,可得到游离麻疯树籽油、酶解液及残渣。酶解液中含有佛波醇酯、植物凝集素、胰蛋白酶抑制剂等抗营养因子和毒素。佛波醇酯是麻疯树中的一类二萜酯,常溶解于麻疯树籽油中,被认为是麻疯树籽中的主要毒性物质之一,不仅能导致温血动物中毒,而且对无脊椎动物的虾、蟹和多种软体动物也具有杀灭作用[9-10]。许多学者对麻疯树籽油中佛波醇酯的杀虫活性以及对人体细胞毒性机制进行了研究[11-13]。佛波醇酯可作为植物源生物农药的有效成分,但其化合物不稳定,对热、光、氧气、酸和碱较敏感,容易发生氧化、酯化和差向异构化,因此,使用过程中需要在无氧环境、避光等条件下贮存[14]。
纳米乳液以纳米材料吸附或包裹活性物质,其具有纳米级粒径和较大比表面积,可以有效提高活性物质的分散性和稳定性,具有在储藏、运输过程中无絮凝、无聚集的优点,可作为有效酯类物质载体[15-19]。目前,纳米乳液制备技术已经逐渐成熟,纳米乳液具有抗沉降和乳析的动力学稳定特性,吸收迅速完全,能增强保健效果,降低毒副作用,具有很大的发展潜力,在特定条件下能长期保持动力学稳定性,在储存过程中无絮凝、聚集、沉淀、奥斯特瓦尔德成熟现象,被看成是一种近热力学稳定体系。高压均质机在食品领域中常用于制备纳米乳剂、纳米粒、脂质体等,制备工艺一般为先进行粗乳制备,再经高压均质得到较小粒径和均匀一致的制剂。高压均质机的可控设备参数有均质压力、循环次数、循环时间和温度等,制剂粒子大小和分布一般随着均质压力增大和循环次数增多明显下降,到达一定压力和循环次数后渐趋平衡;也有的制剂当压力和循环次数超过一定值后,平均粒径和分布反而增大;在制备纳米乳液时需选择合适的均质压力、均值次数等。
鉴于此,本文对高压均质纳米乳液的制备工艺进行优化,以获得高稳定性、高功能性纳米乳液。应用麻疯树籽水酶法产物中的乳状液及水解液为复合乳化剂,通过高压均质技术制备麻疯树籽酶解液纳米乳液,评价其平均粒径及分散性、ζ-电位变化、浊度以及稳定性。
1 材料与方法
1.1 材料与试剂
麻疯树(JatrophacurcasL.)籽,云南神宇新能源有限公司;酸性蛋白酶(200 000 U/g),北京索莱宝科技有限公司;其他试剂均为分析纯。
1.2 仪器与设备
FW-200型万能粉碎机,北京中兴伟业仪器有限公司;索氏提取仪,瑞士步琪公司;HH-S型数显恒温水浴锅,济南海能仪器股份有限公司;SPX-250B-Z型生化培养箱,宁波江南仪器厂;101-1A型数显恒温干燥箱,上海东美建材试验设备有限公司;RE-52B型旋转蒸发器,上海隆拓仪器设备有限公司;AL204型电子天平,梅特勒-托利多仪器(上海)有限公司;分样筛(40目),Zetasizer Nano-ZS 90型光散射粒度分析仪,英国马尔文仪器有限公司;紫外-可见分光光度计,上海光谱仪器有限公司;Turbiscan Lab Expert 型浓缩体系稳定性分析仪,法国Formulaction公司;BX53型OLYMPUS显微镜,日本奥林巴斯公司;激光共聚焦显微镜,汇佳生物股份(中国)有限公司。
1.3 试验方法
1.3.1麻疯树籽酶解液
将麻疯树籽剥壳除杂后,先经粉碎机粉碎,过40目分样筛,得到麻疯树籽仁粉。称取10 g麻疯树籽仁粉,常压蒸汽热处理5 min灭酶,冷却后,调节液料比为6.31 mL/g、加酶量为3.5%、酶解温度为56℃、酶解时间为2.13 h,酶解结束后升温至90℃、10 min灭酶。灭酶处理后经高速离心分离,获得游离麻疯树籽油、乳状液、水解液及残渣。
1.3.2麻疯树籽酶解液纳米乳液
在1.3.1节制备得到的酶解液(乳状液和水解液)中,加入一定比例的水,采用磁力搅拌器充分搅拌后,用高速分散器在25℃、20 000 r/min下分散5 min,在高压均质机内进行纳米乳液制备。
1.3.3制备工艺优化
以纳米乳液的平均粒径、分散性指数(Polydispersity index, PDI)及乳化产率为考察指标,通过单因素试验考察乳状液添加量、水解液添加量、高压均质压力、均质次数对3个指标的影响。进一步利用Design-Expert软件进行响应面分析设计优化试验,选取乳状液添加量、水解液添加量、高压均质压力3个因素为自变量,以平均粒径R1、乳液稳定性指数(Turbiscan stability index, TSI)R2及乳化产率R3为响应值,设置三因素三水平进行试验。
1.3.4纳米乳液粒径分布、PDI及ζ-电位
用光散射粒度分析仪分别测定纳米乳液的粒径分布规律及ζ-电位变化,油滴折射率设置为1.45,水相溶液折射率设置为1.33。为了降低多重光散射效应,分析前用pH值 7.5的磷酸盐缓冲液稀释纳米乳液1 000倍测定平均粒径及PDI,稀释50倍测定ζ-电位。
1.3.5纳米乳液浊度
将纳米乳液用pH值 7.5的磷酸盐缓冲液溶液稀释40倍,以pH值 7.5的磷酸盐缓冲液为空白对照,用紫外-可见分光光度计测定600 nm处的吸光度,浊度计算公式为
(1)
式中A——稀释纳米乳液在600 nm处的吸光度
V——稀释倍数
I——光程差,取0.01 m
1.3.6纳米乳液乳化产率
以乙醇/正己烷(体积比1∶1)混合有机相分别萃取乳状液、水解液、纳米乳液中的麻疯树籽油,纳米乳液的乳化产率Q计算公式为
(2)
式中W1——纳米乳液中麻疯树籽油质量
W2——乳状液、水解液、纳米乳麻疯树籽油的总质量
1.3.7纳米乳液稳定性
利用浓缩体系稳定性分析仪对纳米乳液的稳定性进行分析。试验中,取18 mL麻疯树籽酶解液纳米乳液于Turbiscan稳定性分析仪专用的圆柱形玻璃杯中。在55℃条件下每30 min扫描一次,扫描6 h。由此获得反映纳米乳液稳定性的差值反射光量(ΔBS)随时间的动态变化,即可作出衡量纳米乳液稳定性的图谱,记录TSI。
1.3.8纳米乳液界面蛋白吸附量
界面蛋白含量测定参照文献[20]的方法。将新制备的纳米乳液经12 000 r/min离心60 min,离心温度为20℃。离心结束后,将离心管顶部的乳清层小心转移到滤纸上,滤去多余水分,然后用水复溶到初始体积。用注射器转移离心管下层的清液,并用0.22 μm的滤膜过滤。采用凯氏定氮法测定下清液中的蛋白含量。界面蛋白吸附量计算公式为
(3)
式中Γ——界面蛋白吸附量,mg/m2
Ctotal——最初乳状液中总的蛋白质量比,g/g
Cserum——乳清层中的蛋白质量比,g/g
S——液滴的比表面积,m2/g
1.3.9纳米乳液显微观察
使用载玻片及盖玻片处理纳米乳液,通过光学显微镜观察纳米乳液的显微结构。
1.3.10纳米乳液激光共聚焦显微观察
分别将0.001 g/mL尼罗红和0.001 g/mL尼罗蓝溶解在丙醇中,漩涡混合30 s后对碱纳米乳液染色30 min。染色结束后取10 μL乳液于载玻片上,采用激光共聚焦显微镜观测纳米乳液的显微结构。
1.3.11数据统计及分析
所有试验均进行3次平行测定,利用SPSS Statistics 22软件对数据进行ANOVA差异显著性分析,P<0.05为显著性差异。采用Origin 9.1软件进行数据分析、图表处理及图谱分析处理。
2 结果与分析
2.1 单因素试验
2.1.1乳状液添加量
控制水解液添加量40%、高压均质压力120 MPa、均质次数3次,调节乳状液添加量分别为5%、10%、15%、20%、25%、30%,考察乳状液添加量对纳米乳液平均粒径、ζ-电位、PDI、乳化产率、浊度及TSI的影响。
由表1可知,随着乳状液添加量的增加,纳米乳液平均粒径及PDI呈先降低后增高的变化趋势。这是由于随着乳状液添加量的提高,麻风树籽蛋白更多地覆盖于油水界面处,降低了界面张力。当乳状液添加量为15%时,麻风树籽蛋白在液滴表面形成紧密的界面膜,纳米乳液液滴粒径相对较小且其分布较为集中,此时纳米乳液处于均一、稳定的状态。而过多添加乳状液会形成局部的麻风树籽蛋白聚集,影响麻风树籽蛋白在界面处的舒张展开,增大纳米乳液的粒径。此情况在浊度随乳状液添加量增加而增大上可以得到印证。ζ-电位绝对值随着乳状液添加量的增加呈现逐渐增大后降低的变化趋势,而纳米乳液TSI呈现先降低后增加的变化趋势。结果表明,适量增大乳状液添加量可稳定纳米乳液,但过量添加乳状液则易造成纳米乳液失稳。纳米乳液的乳化产率呈现先增加后降低的变化趋势,这与其平均粒径及稳定性的变化趋势有关。综合上述结果可知,应选择乳状液添加量为15%进行后续工艺优化研究。

表1 乳状液添加量对纳米乳液稳定性的影响Tab.1 Effect of additive amount of emulsion on stability of nanoemulsion
注:同一列数据后的不同字母代表样品间差异显著(P<0.05),下同。
2.1.2水解液添加量
控制乳状液添加量20%、均质压力120 MPa、均质次数3次,调节水解液添加量分别为30%、35%、40%、45%、50%,考察水解液添加量对纳米乳液平均粒径、ζ-电位、PDI等的影响,如表2所示。
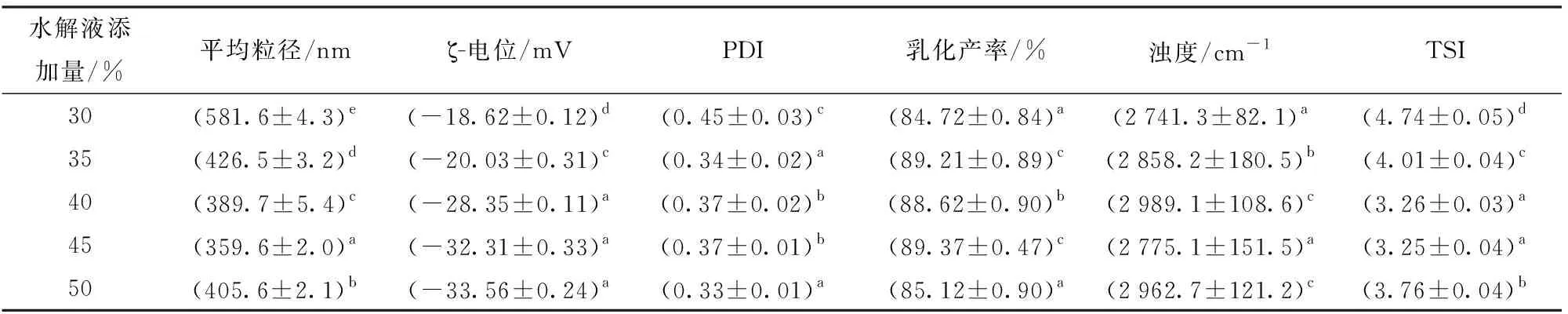
表2 水解液添加量对纳米乳液稳定性的影响Tab.2 Effect of additive amount of hydrolysate on stability of nanoemulsion
由表2可知,随着水解液添加量的增大,纳米乳液的平均粒径呈现先降低后增加的变化趋势,PDI呈现先降低后增大再降低的变化趋势。这可能是由于水解液中的多肽补充了纳米乳液表面蛋白的乳化层间隙,进而提高了纳米乳液的乳液稳定性,但过高的水解液添加量会稀释纳米乳液,不利于纳米乳液的形成。纳米乳液絮凝主要受界面层上发生的吸引和排斥作用影响,增强液滴间的静电可提高纳米乳液抗絮凝能力,液滴ζ-电位越大纳米乳液稳定性越好[21]。随着水解液添加量的增加,更多带负电荷的水解多肽吸附于纳米乳液界面处,提高了纳米乳液的ζ-电位电势,提高了纳米乳液的稳定性,进一步表现于TSI的降低上。虽然50%水解液添加量时乳液的ζ-电位绝对值最大,但却造成了乳滴絮凝程度的增加,故而造成了TSI的增加。由于水解液添加量为45%时,纳米乳液具有最佳的稳定性及乳化特性,采用此值进行后续响应面优化设计试验。
2.1.3高压均质压力
控制乳状液添加量20%、水解液添加量40%、均质次数3次,调节均质压力分别为30、60、90、120、150 MPa,考察高压均质压力对纳米乳液平均粒径、ζ-电位、PDI、乳化产率、浊度及TSI的影响。
表3结果表明,随着均质压力增大,纳米乳液平均粒径呈现先降低后增大的变化趋势。这是由于在高压均质纳米乳液制备过程中,乳液分散相颗粒在巨大剪切、撞击、空穴效应的作用下,逐渐形成纳米粒径乳滴。随着均质压力的不断增加,机械作用力输出强度增大,颗粒粒径减小、分布更为均一。而当均质压力高于90 MPa时,由于均质压力过高机械输出作用过强,分散相粒径的比表面积急剧增加, 有限的乳化剂不能被有效吸附到所有液滴表面上, 乳化作用下降,液滴相互聚集,出现不稳定现象,粒径反而变大,扩大了纳米乳液的粒径分布范围[22]。纳米乳液乳化产率也呈先增大后降低的变化规律,在高均质压力下纳米乳液乳化产率增加与乳滴聚集有关。当均质压力达到90 MPa后,纳米乳液平均粒径增加与乳化产率降低均可能与过高均质压力造成的纳米乳液乳滴裂解营养素流失有关。但过高均质压力(150 MPa)输出下,乳化界面伴随着乳滴裂解发生了失稳现象,此时纳米乳液的ζ-电位绝对值显著降低。均质压力低于90 MPa时,纳米乳液浊度随均质压力增大呈现逐渐降低的变化趋势,表明纳米乳液随压力增大呈现更均一的乳滴分布。而均质压力高于90 MPa时,纳米乳液浊度的增大进一步证实了乳滴裂解现象的发生。综合纳米乳液特性及稳定性考虑,本研究拟选择均质压力为90 MPa进行后续研究。
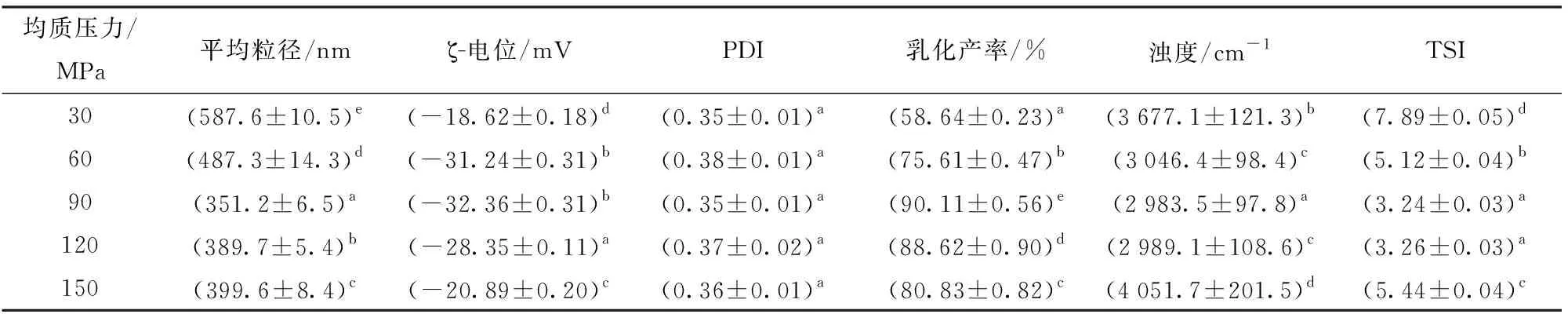
表3 均质压力对纳米乳液稳定性的影响Tab.3 Effect of homogenization pressure on stability of nanoemulsion
2.1.4高压均质次数
控制乳状液添加量20%、水解液添加量40%、均质压力120 MPa,调节均质次数分别为1、2、3、4、5次,考察高压均质次数对纳米乳液平均粒径、ζ-电位、PDI、乳化产率、浊度及TSI的影响,如表4所示。
由表4可以看出,随着均质次数的不断增加,纳米乳液的平均粒径整体呈不断减小的变化规律,ζ-电位绝对值呈现逐渐增大的变化规律。FLOURY等[23]研究指出,在一定均质压力下,随着均质次数的增加,粒径有不断下降的趋势,这可能是由于随着均质循环次数的不断增加,其机械作用的时间变长,之前未被均质细化的大颗粒或小颗粒聚集体在多次均质后粒径减小,乳液乳滴更加稳定。但当纳米乳液均质次数为5次时,纳米乳液的平均粒径增大及ζ-电位绝对值降低,这是由于均质过程中提供大量能量导致新液滴的快速重聚集,即过处理现象[24]。高频的聚集现象和极高的能量密度是产生过处理现象发生的主要原因之一[25-26]。在此条件下的较大纳米乳液浊度也说明了聚集行为的发生。乳液的PDI呈现先降低后增大的变化趋势,这可能与更多小乳滴及过渡态中尺寸乳滴伴随这均质次数增加逐渐形成有关,而均质5次时过处理现象导致的聚集行为则是纳米乳液PDI增大的可能原因。大豆蛋白-磷脂酰胆碱纳米乳液的乳化产率随均质次数增多呈逐渐增大的变化趋势,而均质次数超过4次后,纳米乳液乳化产率不再继续增大。在实际应用中,均质压力与均质次数的合适比率对节约成本、减少机器工作时间、实现目标粒径乳状液的制备有重要作用,但均质压力过高、均质次数过多,乳状液粒径减小趋缓,甚至重新聚集而使平均粒径增大,分布变宽。综合考虑,本研究拟设计均质4次进行后续纳米乳液制备试验。
2.2 响应面优化试验
本试验利用统计软件Design-Expert进行响应曲面法优化,以乳状液添加量、水解液添加量、均质压力为自变量,纳米乳液的平均粒径、TSI 及乳化产率为响应值,根据中心组合设计原理,确定高压均质法制备纳米乳液的最佳工艺条件,响应面试验方案及结果见表5、6,表6中A、B、C分别表示乳状液添加量、水解液添加量、高压均质压力的编码值。
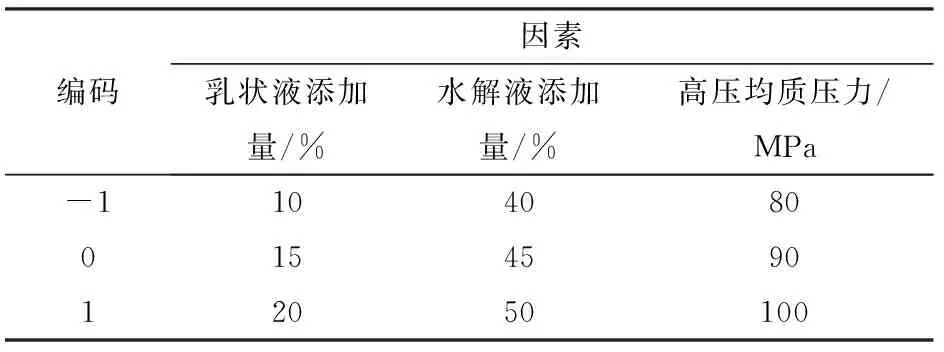
表5 试验因素编码Tab.5 Encode of factors
通过统计分析软件Design-Expert进行数据分析,建立平均粒径R1二次响应面回归模型为
R1=300.68-19.30A-11.04B-10.91C+2.77AB+
13.38AC+1.65BC+31.26A2+25.18B2+ 25.99C2
(4)
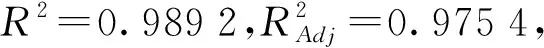
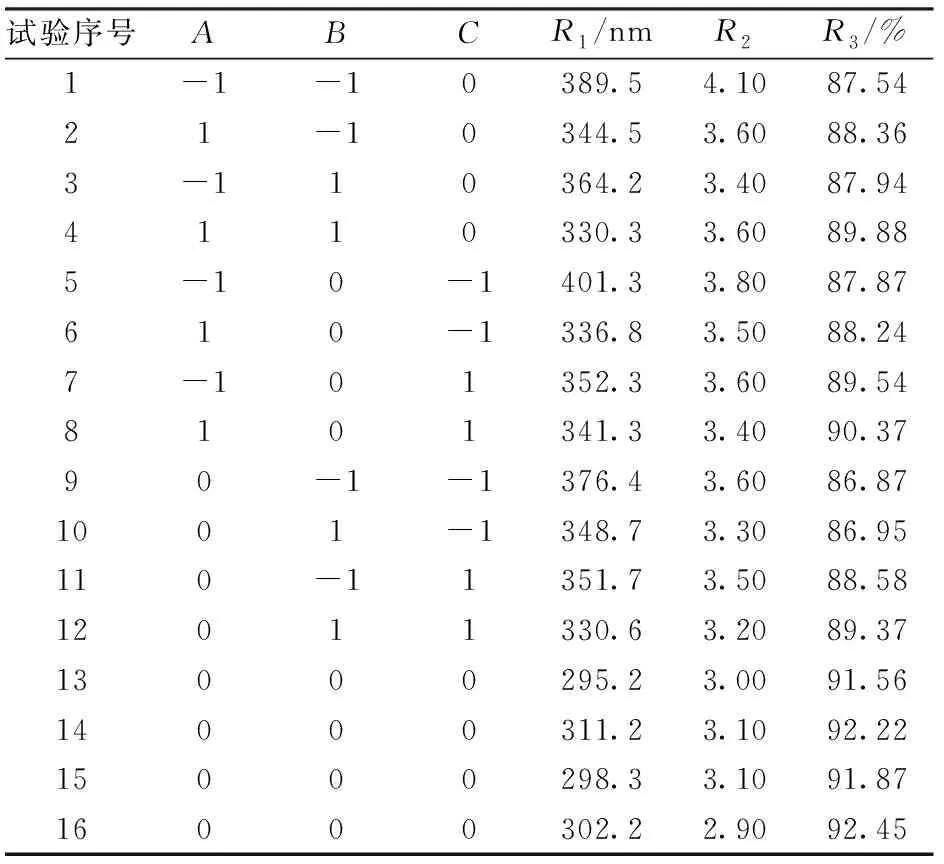
表6 试验安排及结果Tab.6 Experiment scheme and results
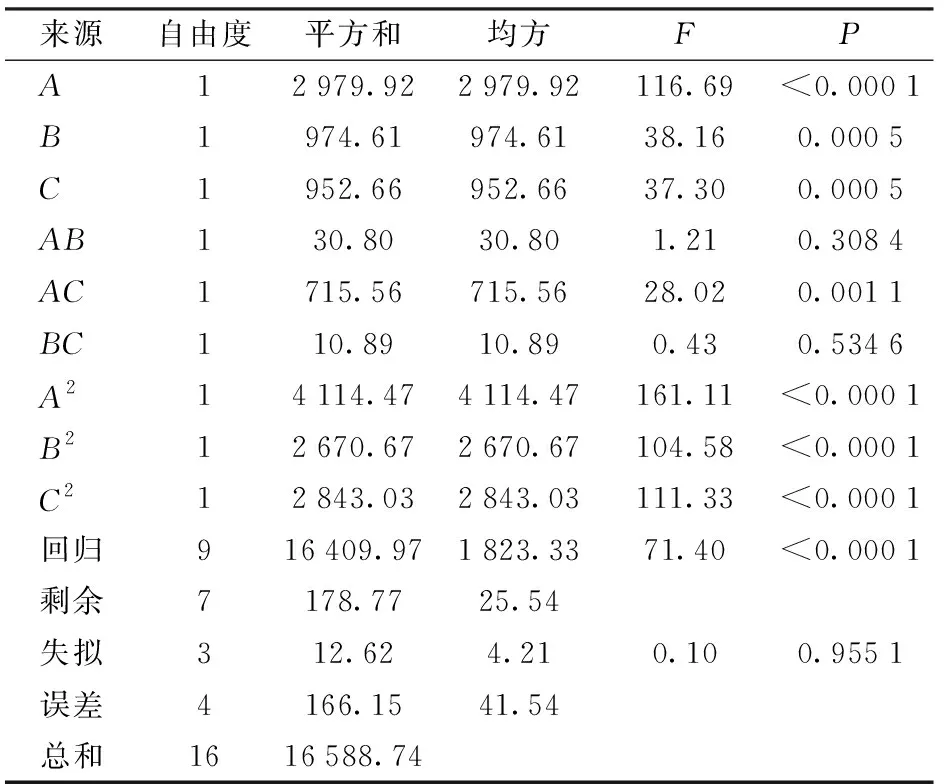
表7 平均粒径回归与方差分析结果Tab.7 Results of regression and variance analysis of average particle size
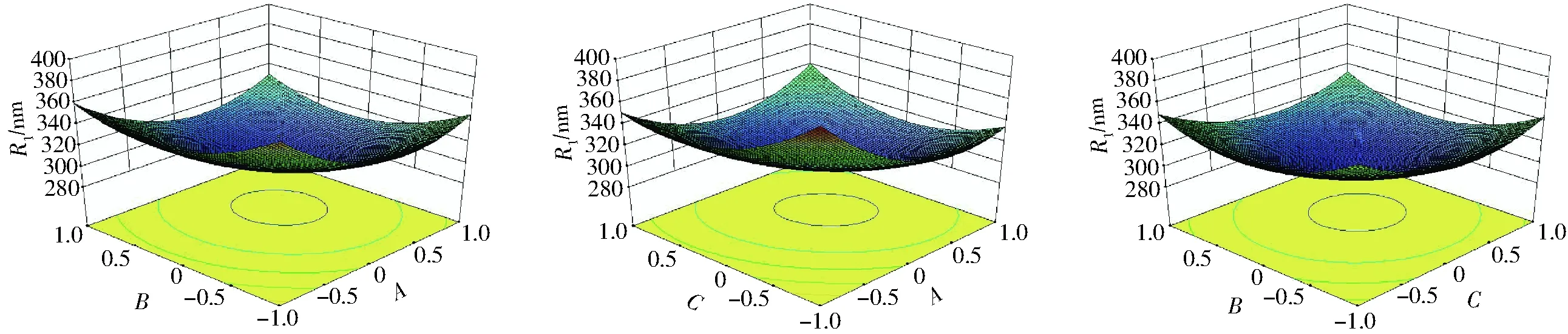
图1 各因素对纳米乳液平均粒径影响的响应面图Fig.1 Response surface diagrams showing effect of factors on average particle size of nanoemulsion
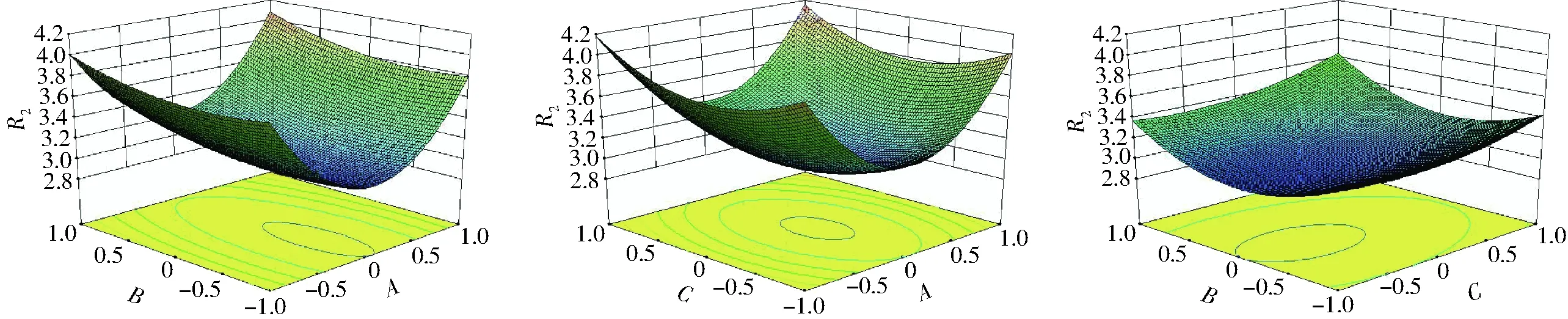
图2 各因素对纳米乳液TSI影响的响应面图Fig.2 Response surface diagrams showing effect of factors on TSI of nanoemulsion
通过统计分析软件Design-Expert进行数据分析,建立TSI(R2)二次响应面回归模型为
R2=3.00+0.013A+0.12B+0.087C+0.025AB-0.01AC+0.020BC+0.81A2+0.12B2+0.30C2
(5)


表8 TSI回归与方差分析结果Tab.8 Results of regression and variance analysis of TSI
通过统计分析软件Design-Expert进行数据分析,建立乳化产率R3二次响应面回归模型为
R3=92.09+0.50A+0.35B+0.99C+0.28AB+
0.12AC+0.18BC-1.30A2-2.36B2-1.78C2
(6)

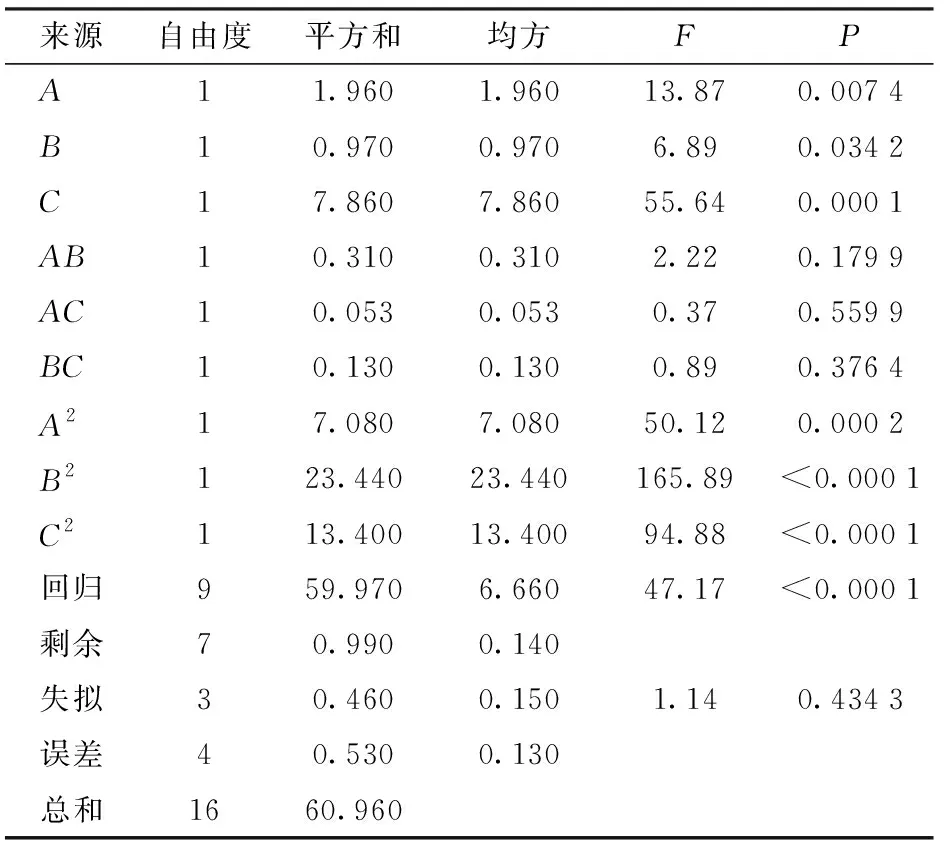
表9 乳化产率回归与方差分析结果Tab.9 Results of regression and variance analysis of emulsion productive rate
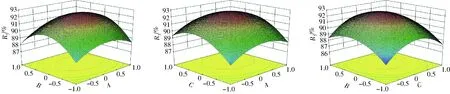
图3 各因素对纳米乳液乳化产率影响的响应面图Fig.3 Response surface diagrams showing effect of factors on emulsion productive rate of nanoemulsion
采用联合求解法确定平均粒径、TSI及乳化产率最优条件为:乳状液添加量15.55%、水解液添加量45.25%、高压均质压力91.3 MPa,此条件下平均粒径297.8 nm,TSI为3.03,乳化产率92.24%。为适应生产,将制备条件优化为乳状液添加量15.55%,水解液添加量45.25%,高压均质压力91 MPa,此条件下纳米乳液平均粒径297.2 nm,TSI为2.98,乳化产率92.47%。说明响应值的试验值与回归方程预测值吻合良好。
通过光学显微镜对纳米乳液进行观察,结果如图4所示。由图可知,通过本研究制备的纳米乳液粒径均一、乳液状态稳定。且通过界面蛋白含量分析,本研究制备的纳米乳液界面蛋白吸附量高达31.20 mg/m2,高界面蛋白含量起到了稳定乳液的作用。

图4 纳米乳液显微及激光共聚焦显微成像图Fig.4 Microscopic observation images of nanoemulsion
3 结束语
通过响应曲面法优化确定了以水酶法处理麻风树籽得到的乳状液及水解液为复合乳化剂,调配制备纳米乳液的工艺,确定的最优工艺为:乳状液添加量15.55%、水解液添加量45.25%、高压均质压力91 MPa、均质次数4 次,此条件下纳米乳液平均粒径297.2 nm,TSI为2.98,乳化产率为92.47%。本研究制备的纳米乳液粒径均一、乳液状态稳定,且纳米乳液界面蛋白吸附量高达31.20 mg/m2,高界面蛋白含量起到了稳定乳液的作用。

