离子液体/H2 O2体系脱硫实验研究
李 梅,孙功成,程雪云,李佳佳,金 权,徐荣声
(1.北方民族大学 化学与化学工程学院,宁夏 银川 750021;2.北方民族大学 宁夏太阳能化学转化技术重点实验室,宁夏 银川 750021;3.北方民族大学 国家民委化工技术基础重点实验室,宁夏 银川 750021)
脱硫方法分为物理方法、化学方法和微生物法,但不同的方法都有其优缺点。物理法脱硫主要针对的是无机硫的脱除,对煤中的有机硫作用效果较小,微生物法脱硫的作用成本较低,但是作用时间过长,并且会导致部分煤结构的变质。化学脱硫法是使用最广泛的脱硫方法,也是研究最多的方法,但是化学药品的大量使用会对环境造成较大的影响。离子液体由于其对有机/无机化合物良好的溶解性,优良的热稳定性与化学稳定性被广泛用于煤和油品的脱硫实验研究[2,3]。Bui等[4]用不同种类的非卤素离子液体萃取模型油中的含硫化合物。实验结果发现,离子液体对油品中硫分有较强的脱除能力。To等[5]使用离子液体/水混合物处理煤,研究发现,离子液体处理后,煤样起始热解温度降低,粒径减小,硫分明显降低。Tian等[6]用合成的三种咪唑类磷酸根离子液体用于萃取脱除模型油中的二甲基二硫醚,实验结果表明,模型油可溶于离子液体且硫分降低明显。Dharaskar等[7]探究了1-丁基-3-甲基咪唑溴化物([Bmim]Br)离子液体对液体燃料中的二苯并噻吩的脱除效果,发现二苯并噻吩的脱除率可达79.5%。Saikia等[8]用H2O2/HCOOH混合溶液进行脱硫实验研究,加入少量离子液体,发现离子液体的加入增强了H2O2/HCOOH的脱硫脱灰效果。巩明月等[9]将离子液体[Hnmp]H2PO4负载到MOF-199上,结果发现,改性后的离子液体对噻吩脱除率可达到96.7%。陈宗定等[10]研究了KNO3体系中离子液体辅助煤浆电解脱硫效果,研究了煤浆电解过程中离子液体的阴阳离子差异、温度和时间对脱硫率的影响。结果发现,阳离子相同时,不同阴离子脱硫率由高到低顺序为:Br->BF4->Cl-,当阴离子同为Br-时,咪唑脱硫效果优于吡啶,且脱硫率随温度的升高和时间的延长而增大。徐永亮等[11]用1-丁基-3-甲基咪唑硫酸氢盐([Bmim]HSO4)联合H2O2溶液进行脱硫实验研究,结果发现,经ILs/H2O2体系作用后煤中硫醚及噻吩含量显著降低。安莹等[12]合成了新型的磷钼杂多酸离子液体[Hmim]3PMo12O40,并将其用于以1-甲基咪唑四氟硼酸盐([Hmim]BF4)为溶剂的模拟油品氧化脱硫实验。结果发现,二苯并噻吩脱硫率达到90%,二苯硫醚、苯甲硫醚和二乙硫醚的脱除率可达100%。
综上所述,前人对离子液体脱除煤及油品中的硫分进行了广泛研究,但是研究离子液体作用后煤中硫形态及含量变化的较少。本研究选用四种不同种类离子液体与H2O2联合对两种脱灰高硫煤(LS、QX)进行脱硫实验研究,并用FT-IR、XPS、SEM以及TG等对离子液体处理前后煤样进行表征,探讨离子液体的加入对H2O2氧化脱硫效果的影响,以及ILs/H2O2对煤中硫铁矿及有机硫的脱除机理。
1 实验部分
1.1 实验样品
研究选用山西灵石(LS-raw)和贵州黔西(QX-raw)两种高硫高灰煤样(粒径≤74 μm)。煤样的工业分析以及元素分析见表1。
由于所选两种煤样的灰分都超过了50%,为使离子液体与煤基质充分接触,防止高灰分对实验的影响,用HCl/HF对两种高灰煤进行脱灰处理,脱灰后,煤中大部分矿物质,包括硫酸盐硫被脱除,剩下的硫分主要为硫铁矿和有机硫,脱灰煤样(LS、QX)的工业分析及元素分析见表2,形态硫分析见表3。
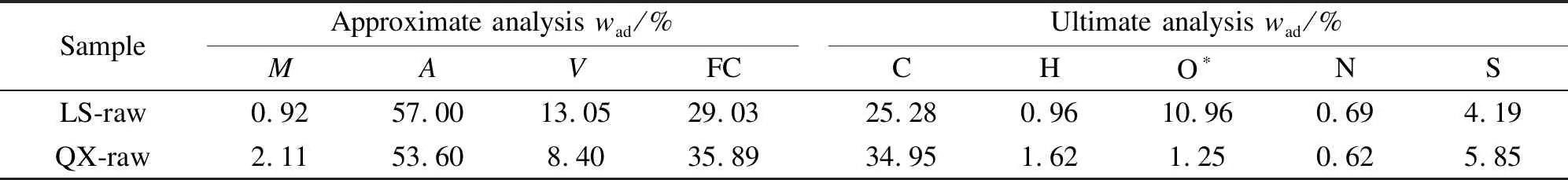
表1 煤样的工业分析和元素分析Table 1 Proximate and ultimate analyses of coal samples
note:ad:air dried;M:moisture;A:ash content;V:volatile;FC:fixed carbon;*:by difference
1.2 实验试剂
实验所用离子液体(ionic liquids,ILs)为1-丁基-3-甲基咪唑溴化物([Bmim]Br,纯度≥99%)、1-丁基-3-甲基咪唑四氟硼酸盐([Bmim]BF4,纯度≥99%)、1-丁基-3-甲基咪唑硫酸氢盐([Bmim]HSO4,纯度≥98%)和1-丁基-3-甲基咪唑磷酸二氢盐([Bmim]H2PO4,纯度≥98%)。离子液体均由兰州物理化学研究所合成,所用离子液体的结构见图1。实验用30%H2O2溶液为分析纯。
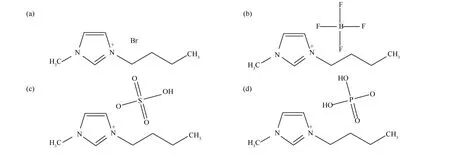
图1 离子液体结构图Figure 1 Structure diagram of ionic liquids(a):[Bmim]Br ;(b):[Bmim]BF4 ;(c):[Bmim]HSO4;(d):[Bmim]H2PO4
1.3 实验过程
将3 g煤样和15 mL H2O2溶液加入烧瓶中,在R-1002-VN旋转蒸发仪中反应,作为对照实验。为了探究离子液体的加入对脱硫效果的影响,取3 g煤样和15 mL H2O2溶液,分别与不同种类离子液体混合,离子液体、煤样、H2O2的用量比为ILs∶coal∶H2O2=1∶1∶5(g∶g∶mL)。为探究离子液体单独作用煤样时的脱硫效果,利用去离子水代替H2O2溶液,离子液体和煤样的质量比不变。实验温度为60 ℃,反应时间为2 h,用蒸馏水洗涤多次直至pH值呈中性,所得滤饼在真空干燥箱中80 ℃干燥24 h,然后放入真空干燥器中备用。
1.4 实验仪器及条件
使用美国LECO S-144 DR红外定硫仪,测定反应前后样品的硫分。
使用美国Thermo Fisher Scientific Nicolet Avatar 380傅里叶变换红外光谱仪(FT-IR)对样品中官能团进行半定量分析。先将样品与光学纯溴化钾按照质量比为1∶100充分混合均匀,然后在红外光谱仪压片机上制成1 mm左右的薄片。波数为400-4000 cm-1,分辨率为4 cm-1,扫描32次。
胖子显然不情愿,但也无计可施。于是每天下午,整个基地的人都会看到蓝天白云间,一个胖子以诡异的“撒尿”姿势在另一个男人的怀抱里尖叫、盘旋,以比翼双飞的姿态翱翔在天地间……好在七哥有着极高的职业素养,胖子每次尖叫的时候,他都会耐心温柔地提醒要领,甚至直接抓住胖子的手帮他摆正姿势……这画面太美,没人敢看。
XPS测试在美国Thermo Fisher Scientific ESCALAB 250Xi型X射线光电子能谱仪上进行,靶材为Al靶,分辨率为0.45 eV,通过能为30 eV,以C 1s(284.6 eV)峰作为内标进行校正。
在德国ZEISS EVO18扫描电子显微镜上观察处理前后样品的形貌特征,测试电压为15.00 kV。
热重实验在德国NETZSCH STA449 F5同步热分析仪上完成,实验用气体为N2,N2流量为100 mL/min,样品质量5 mg左右,测试温度范围为室温到900 ℃,升温速率为10 ℃/min。
1.5 全硫脱硫率计算方法
全硫脱硫率计算公式如下(1):
(1)
式中,η∶全硫脱除率,%;Sj∶精煤全硫,%;St∶原煤全硫,%;w∶收率,%。
2 结果与讨论
2.1 离子液体种类对煤样脱硫率的影响
图2、图3为ILs/H2O2体系在温和条件下分别作用于LS、QX煤的脱硫率变化。
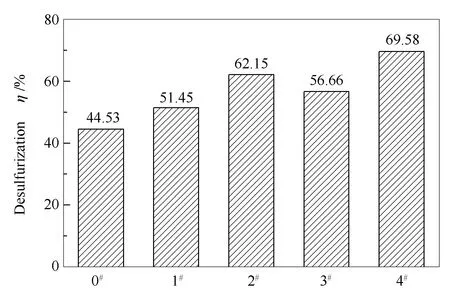
图2 H2O2及ILs/H2O2体系处理LS煤的脱硫率变化Figure 2 Desulfurization rates of LS coal treated by ILs/H2O2 system and H2O20#:LS-H2O2;1#:LS-H2O2-[Bmim]Br;2#:LS-H2O2-[Bmim]BF4;3#:LS- H2O2-[Bmim]HSO4;4#:LS-H2O2-[Bmim] H2PO4

图3 H2O2及ILs/H2O2体系处理QX煤的脱硫率变化Figure 3 Desulfurization rates of QX coal treated by ILs/H2O2 system and H2O2a#:QX-H2O2;b#:QX-H2O2-[Bmim]Br;c#:QX-H2O2-[Bmim]BF4;d#:QX- H2O2-[Bmim]HSO4;e#:QX-H2O2-[Bmim] H2PO4
由图2和图3可知,当ILs/H2O2体系分别作用两种煤样时比仅用H2O2溶液处理的脱硫率均有所升高。不同种类离子液体的脱硫效果存在差异,且同种离子液体作用不同煤样的效果也不同。[Bmim]H2PO4/H2O2体系的作用效果最为理想,当使用[Bmim]H2PO4/H2O2体系处理煤样后,LS与QX的脱硫率分别高达69.58%和84.09%;当用[Bmim]BF4/H2O2体系处理后,LS和QX的脱硫率分别为62.15%、65.29%;[Bmim]Br与[Bmim]HSO4的脱硫作用效果相对于前两种来讲稍小,[Bmim]Br/H2O2体系作用LS煤与QX煤时的脱硫率分别达到了51.45%、49.97%;[Bmim]HSO4/H2O2体系作用LS煤与QX煤时的脱硫率分别为56.66%、54.78%。所使用的四种离子液体脱硫作用强弱依次为[Bmim]H2PO4>[Bmim]BF4>[Bmim]HSO4>[Bmim]Br。
2.2 脱硫前后煤样形态硫的变化
表2为脱灰煤样及用H2O2、ILs/H2O2体系作用后样品的工业分析和元素分析表、表3为H2O2及ILs/H2O2体系脱硫前后LS、QX煤样的形态硫变化。由于是经HCl/HF的脱灰煤样,所以煤中硫主要是硫铁矿以及有机硫,脱灰后LS和QX的硫分分别为8.68%和11.88%。
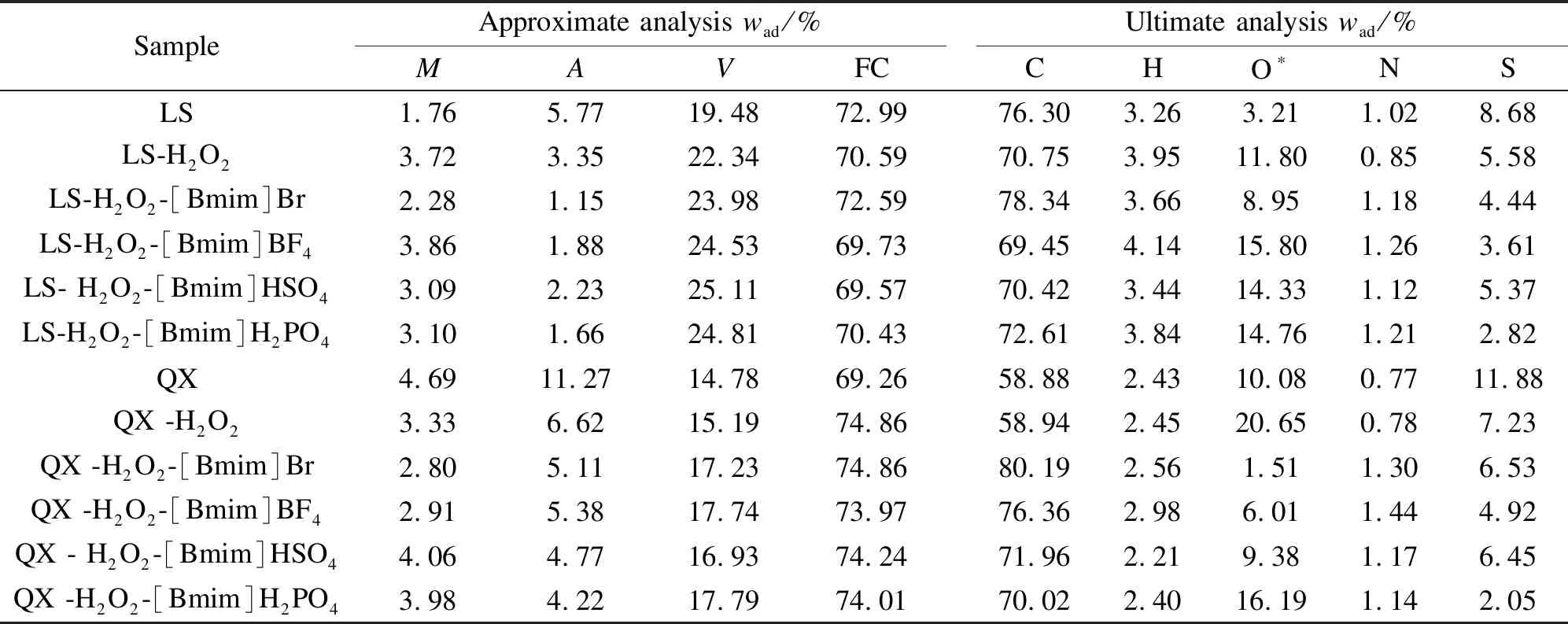
表2 H2O2及ILs/H2O2体系作用前后煤样的工业分析和元素分析Table 2 Proximate and ultimate analyses of deashed coals with and without desulfurization by ILs/H2O2 system and H2O2
note:ad:air dried;M:moisture;A:ash content;V:volatile;FC:fixed carbon;*:by difference
由表3可知,加入离子液体后,煤样中硫铁矿硫以及有机硫显著降低,其中,[Bmim]H2PO4/H2O2体系脱硫效果最为显著,使得QX煤中硫铁矿的脱除率高达96.37%,有机硫的脱除率也达到了68.50%。实验中所用的离子液体阳离子均为咪唑类,对同种煤的脱硫效果的差异应该是由阴离子不同引起的。酸根阴离子可使煤溶胀,促进煤中的含硫结构溶解在ILs/H2O2溶液,且含酸根阴离子的离子液体可以提供酸性环境,从而增强H2O2的氧化性,[Bmim]H2PO4为二氢酸盐,故其脱硫能力比其他离子液体强[3],同种离子液体作用不同煤样的形态硫脱除效果差异可能由于硫形态及其含量不同造成的[13]。
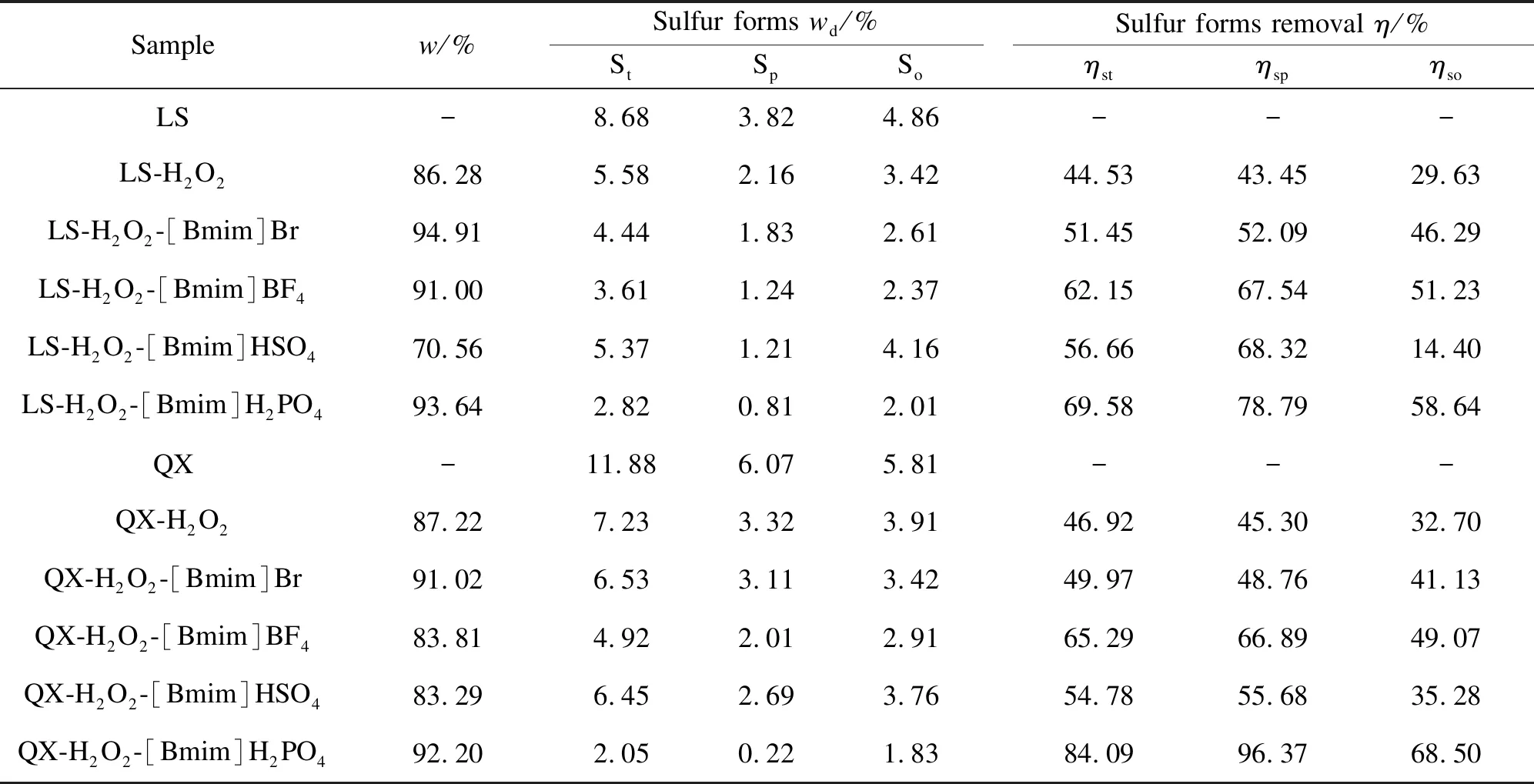
表3 H2O2及ILs/H2O2体系脱硫前后煤样形态硫的变化 Table 3 Changes of sulfur forms in deashed coals with and without desulfurization by ILs/H2O2 system and H2O2
note:St:total sulfur;Sp:pyrite sulfur;So:organic sulfur
2.3 离子液体单独作用时煤样的脱硫率
表4为离子液体单独作用时,煤样的收率及全硫脱硫率。由表4可知,离子液体单独作用时,对硫分脱除作用较弱,脱硫率最高仅为14.80%,说明离子液体单独作用煤样无法高效脱除煤中的硫分,因此,与2.1和2.2节的结果对比可以得出,ILs/H2O2体系作用煤样的高脱硫率可能是由于离子液体加入后,破坏了煤中的弱键合结构,使煤结构更加松散,孔隙率增加,使得H2O2与煤基质接触更充分,氧化脱硫作用增强。

表4 离子液体单独作用下煤样收率及全硫脱硫率Table 4 Yield and ratio of total desulfurization of coals after treatment by individual effect of ILs
2.4 脱硫前后煤样官能团的变化
图4为H2O2和ILs/H2O2体系处理前后LS与QX煤的FT-IR谱图。图5为H2O2和ILs/H2O2体系处理前后LS与QX煤在400-700 cm-1的FT-IR谱图。红外谱图中,波数在3000-3800 cm-1附近的吸收振动峰主要是-OH官能团的振动吸收峰;2800-3000 cm-1波数附近的峰主要为脂肪烃-CHx的吸收振动峰;1490-1620 cm-1为芳环中的C=C的振动吸收峰,700-900 cm-1为芳香烃的伸缩振动峰;在1000-1800 cm-1主要为含氧官能团的振动吸收峰[14],1110-1330 cm-1为醇、酚、酯、醚中-O-的振动吸收峰。由图4可知,离子液体处理前后煤样的红外谱图峰形无明显变化,说明离子液体处理没有改变煤样的基本碳骨架结构。1020-1050 cm-1为煤样中S=O的伸缩振动吸收峰,由图4中可以看出,离子液体作用后煤样在该范围的伸缩振动峰强度相对于原煤更强,这是由于ILs/H2O2体系作用使煤中的部分硫转化成了砜类硫,其中,[Bmim]H2PO4/H2O2体系作用后LS煤在该位置的伸缩振动峰强度最大,说明[Bmim]H2PO4/H2O2体系作用使LS煤中更多其他形式硫转化为砜类硫,这与[Bmim]H2PO4/H2O2体系对硫铁矿硫的高脱除率相对应。471 cm-1处为有机S-H的伸缩振动吸收峰[15],由图5(b)可以看出,离子液体处理后QX煤中属于有机S-H的峰强度明显降低,说明QX煤样中的硫醇、硫醚等有机硫化物硫被脱除;420 cm-1处为硫铁矿的伸缩振动吸收峰[16],从图5可以发现,ILs/H2O2体系处理的煤样中硫铁矿的峰强度明显降低。
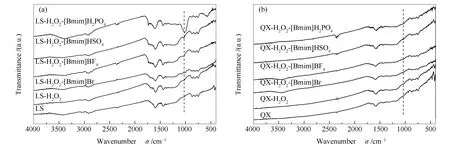
图4 H2O2和ILs/H2O2体系脱硫前后煤样的FT-IR谱图Figure 4 FT-IR spectra of coal samples before and after desulfurized by ILs/H2O2 system and H2O2
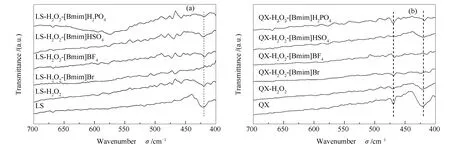
图5 H2O2和ILs/H2O2体系脱硫前后煤样400-700 cm-1的FT-IR谱图Figure 5 400-700 cm-1 FT-IR spectra of coal samples before and after desulfurized by ILs/H2O2 system and H2O2
2.5 脱硫前后煤样硫形态的变化
图6和图7分别为LS和QX煤用H2O2和ILs/H2O2体系脱硫前后煤样S 2p谱图。表5和表6分别为LS和QX煤脱硫前后硫形态的相对含量变化表,不同硫形态的峰位置参考文献[17-20]。不同硫形态的相对含量计算方法如下:A1、A2、A3、A4和A5分别表示XPS谱图中各硫形态的峰面积,各硫形态的相对含量计算公式如下(2):
(2)
式中,A1:有机硫化物硫(organic sulfide);A2:硫铁矿(pyrite);A3:噻吩(thiophene);A4:亚砜(sulfoxide);A5:砜(sulfone);R:硫形态的相对含量。
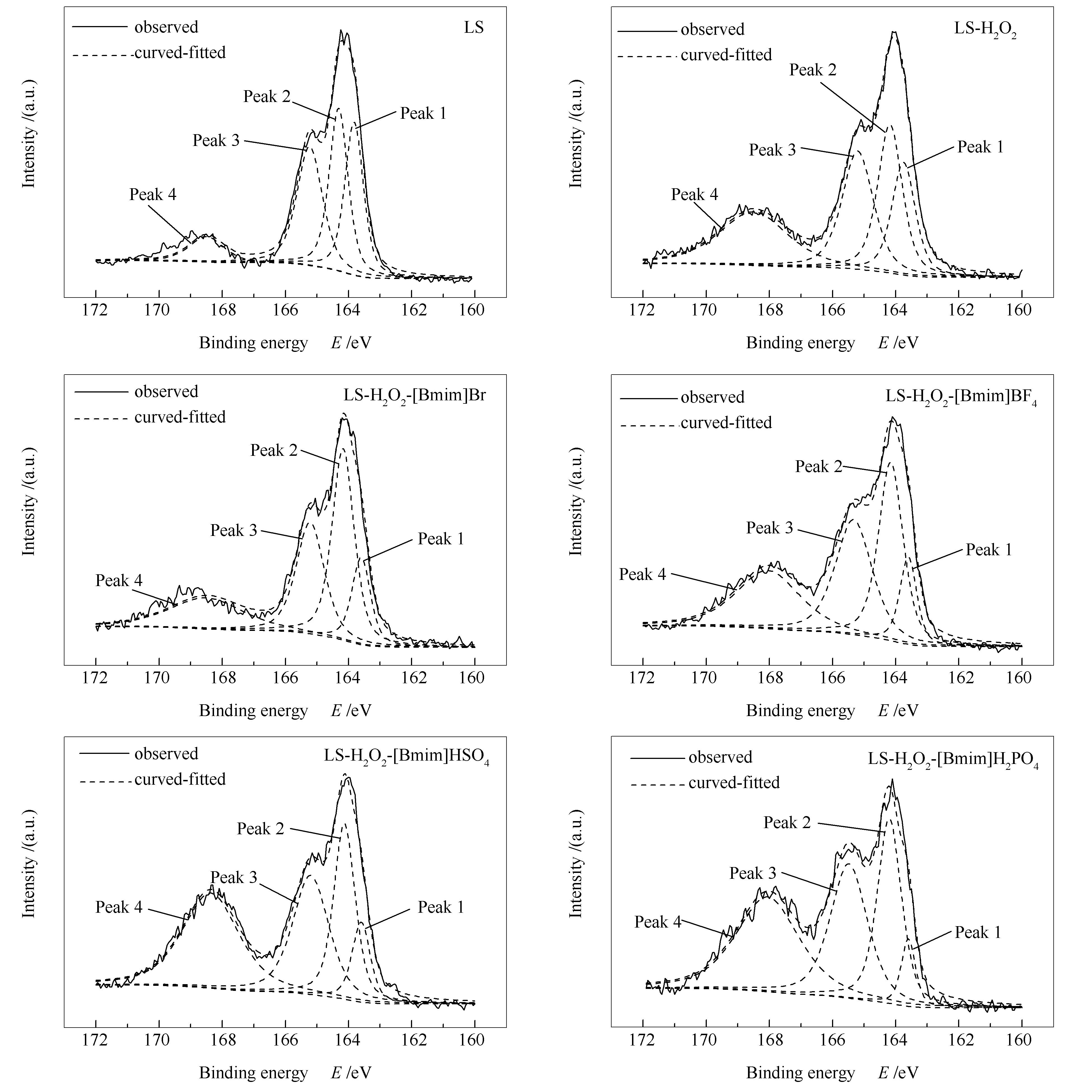
图6 H2O2和ILs/H2O2体系脱硫前后LS煤中硫的XPS谱图Figure 6 XPS spectra of sulfur in LS coal before and after desulfurized by ILs/H2O2 system and H2O2
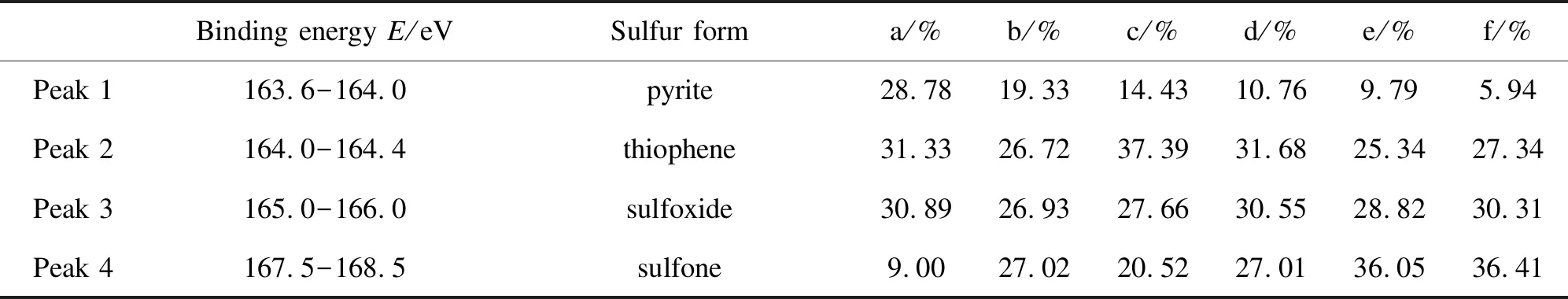
表5 XPS谱图中LS样品的硫形态及相对含量Table 5 Sulfur form and its relative content in LS samples by XPS spectra
a:LS;b:LS-H2O2;c:LS-H2O2-[Bmim]Br;d:LS-H2O2-[Bmim]BF4;e:LS-H2O2-[Bmim]HSO4;f:LS-H2O2-[Bmim]H2PO4
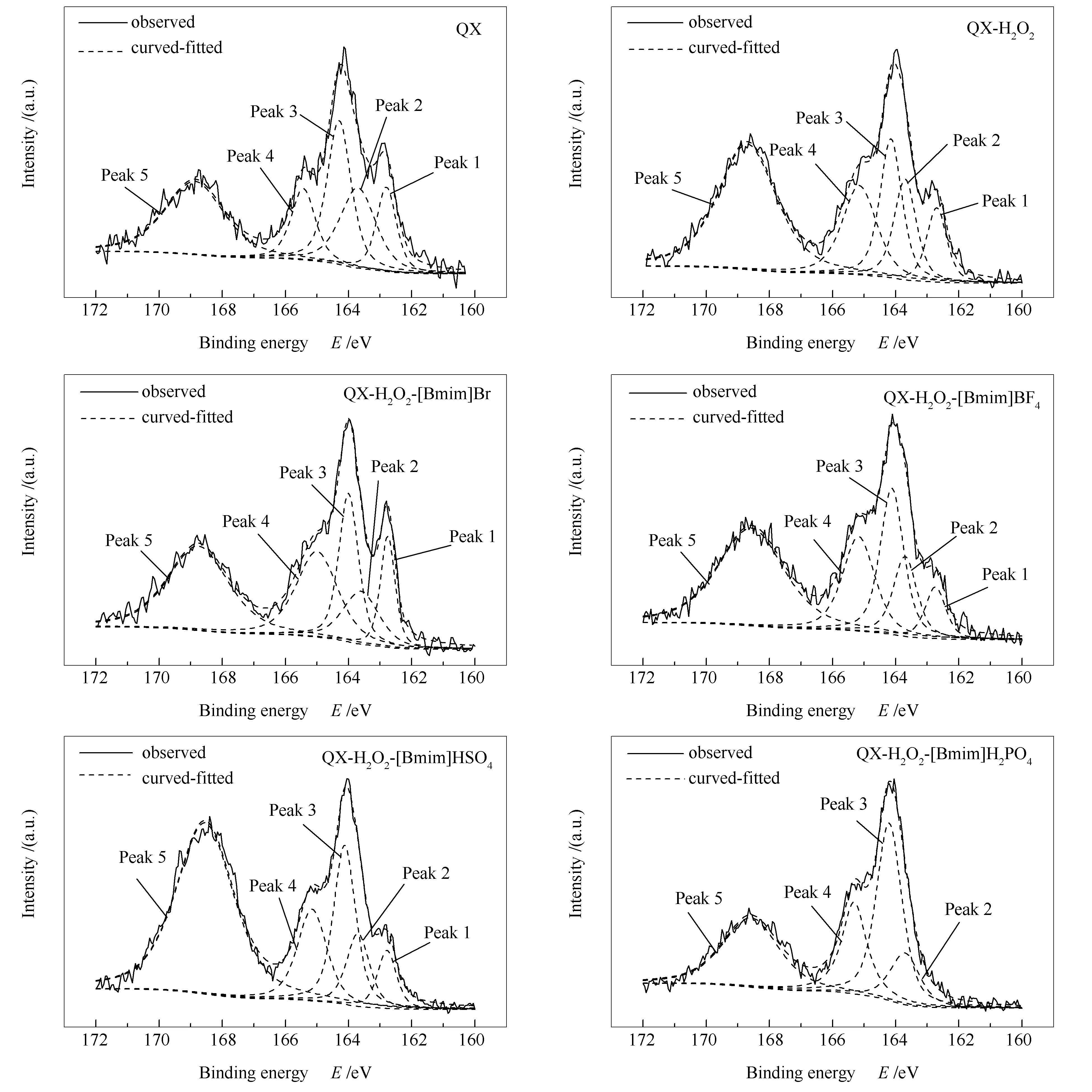
图7 H2O2和ILs/H2O2体系脱硫前后QX煤中硫的XPS谱图Figure 7 XPS spectra of sulfur in QX coal before and after desulfurized by ILs/H2O2 system and H2O2
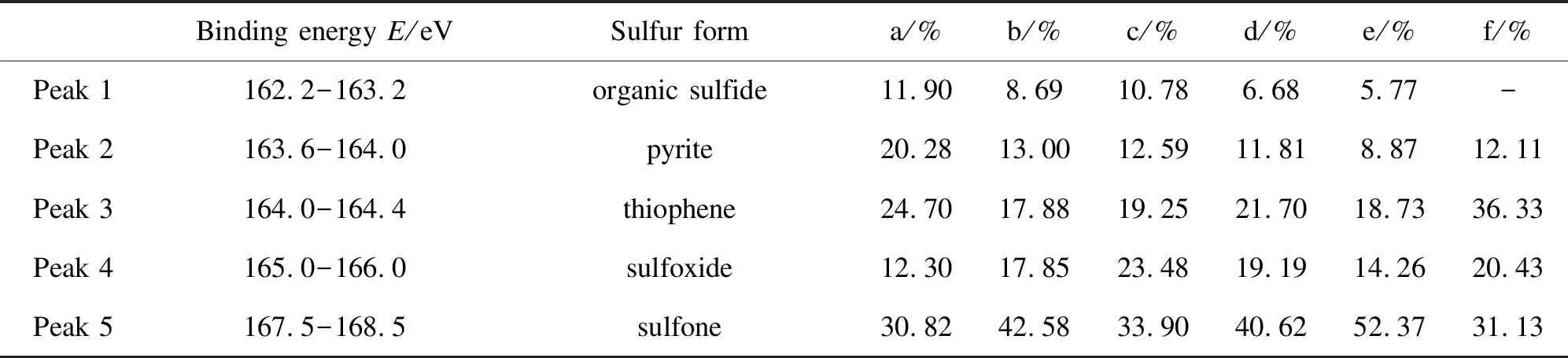
表6 XPS谱图中QX样品的硫形态及相对含量Table 6 Sulfur form and its relative content in QX samples by XPS spectra
a:QX;b:QX-H2O2;c:QX-H2O2-[Bmim]Br;d:QX-H2O2-[Bmim]BF4;e:QX-H2O2-[Bmim]HSO4;f:QX-H2O2-[Bmim]H2PO4
综合分析图6、图7、表5和表6可以发现,两种煤样经过ILs/H2O2体系处理后,有机硫化物硫、黄铁矿硫、噻吩硫的相对含量都有一定程度的降低,其中,有机硫化物硫和黄铁矿硫的降低最为明显,砜类硫的相对含量有所升高,这可能是由于离子液体的加入增强了H2O2对煤样的氧化脱硫作用,离子液体的加入会破坏煤中的弱键合结构,加剧煤中的氢键、弱共价键、π-π键和范德华相互作用等的断裂,使煤中含硫结构与H2O2充分接触,最终导致氧化脱硫作用的加强[8]。煤中砜类硫的含量升高可能是由于煤样中砜类硫较难脱除且煤中部分低价态硫被氧化成更高价态的砜类硫。
2.6 脱硫前后煤样表面形貌的变化
图8中(a)、(b)、(c)、(d)、(g)图为QX煤样的微观形貌图,(e)、(h)图为H2O2氧化处理的QX煤样品的微观形貌图,(f)、(i)图为[Bmim]H2PO4/H2O2体系处理QX煤样品的微观形貌图,从煤样的微观形貌图中可以观察到硫铁矿颗粒的存在,硫铁矿一般是嵌入煤颗粒中(如图(a)),部分硫铁矿聚合成球形团块(如图(b)),也有部分硫铁矿以独特的六角形立方晶体形式存在(如图(c))[21]。其中,图8(d)、(e)、(f)都是500放大倍数下的微观形貌图。从图8可以发现,H2O2氧化后的样品中的硫铁矿颗粒相对于原煤有所减少,而ILs/H2O2体系作用煤样的扫描图中发现硫铁矿颗粒减少的更为明显,说明硫铁矿被脱除,这与FT-IR、XPS的分析结果相对应。图8(g)、(h)、(i)是5000放大倍数下的微观形貌图。从微观形貌图中也可以发现,原煤中粒径大小分布不均匀,经H2O2氧化后小粒径颗粒减少,当使用ILs/H2O2体系处理煤样可以发现小粒径的颗粒减少更为明显,颗粒间的缝隙增大,煤表面的凹坑明显,说明原属于该凹坑位置的物质被脱除。
2.7 脱硫前后煤样热解特性分析
图9为不同种类ILs/H2O2体系作用LS及QX煤的TG-DTG曲线。由图9可知,原煤的热失重均小于ILs/H2O2处理后煤样。从DTG曲线可以看出,在200-350 ℃,ILs/H2O2处理后的煤样相比原煤有明显失重峰,这可能是由于离子液体处理打断了煤样内部的交联结构,使键更容易断裂,小分子更容易逸出;且脱硫后煤结构中含有大量易于裂解的含氧官能团,热解过程中在较低温度下以挥发分的形式逸出。在400-600 ℃,失重最为明显,这主要是由于煤中挥发性物质大量释放及非均相有机物质的分解引起的,在这一阶段含硫气体也随着挥发分一起释放出来[22]。由于ILs/H2O2体系处理后,煤样中硫分大量减少,以及第一阶段挥发性物质的更多释放,所以在该阶段原煤的失重强度大于离子液体处理样的失重强度。
离子液体处理对煤的热解特性有一定的影响,离子液体处理可以打断煤中部分化学键,使煤结构中的活性基团增加,产生更多的自由状态小分子[23],与原煤相比,ILs/H2O2体系作用使煤结构中的含氧官能团,支链和桥键更容易在热解过程中断键并以挥发分的形式释放出来。

图9 ILs/H2O2体系脱硫前后煤样的TG-DTG曲线Figure 9 TG/DTG curves of coal samples before and after desulfurized by ILs/H2O2 system and H2O2
3 结 论
通过使用不同种类的离子液体作用于LS、QX两种煤样,发现离子液体的加入均可以增强H2O2的脱硫能力,且不同种类离子液体的作用效果不同,同种离子液体对不同煤样的作用效果也有差异。[Bmim]H2PO4/H2O2体系分别作用于两种煤样时,LS与QX煤全硫脱硫率分别高达69.58%、84.09%,对于QX煤而言,其硫铁矿的脱除率可达96.37%,有机硫的脱除率也达到了68.50%。ILs/H2O2体系主要脱除的是煤样中的有机硫化物硫和硫铁矿硫,在反应过程中部分低价态硫被氧化成砜类硫,同时发现离子液体处理会使得小粒径煤粒减少,使颗粒间隙增大。离子液体处理会使煤样的热失重相比原煤增大,挥发分释放峰温提前,说明离子液体处理会打断煤中化学键,使煤样中的小分子和含氧官能团更容易逸出。

