掺氮石墨烯-铜基催化剂的制备及催化性能
唐晓宁 邵姣婧
(贵州大学材料与冶金学院,贵阳 550025)
0 引 言
聚氯乙烯是氯乙烯单体(vinyl chloride monomer)通过聚合反应制备的,工业上生产氯乙烯的方法主要有两种:乙烯法和乙炔法.基于我国能源结构现状,我国主要采用乙炔法制备氯乙烯单体[1-2],在该制备工艺中活性炭负载HgCl2催化剂(HgCl2/C)扮演着重要的角色.然而,剧毒HgCl2活性组分极易挥发,不仅造成催化剂失活,还严重危害工人健康,污染环境[3-4].因此,无汞催化剂的研发是聚氯乙烯行业发展的必经之路,也是实现该行业可持续发展的关键环节[5-8].
就催化剂的活性组分而言,在种类多样的无汞催化剂中,AuCl3/C催化剂的研发引起了广泛关注,是因为其具有高活性和选择性.但是,Au基催化剂成本高、稳定性差成为制约其进一步发展的瓶颈问题.近年来,许多学者致力于研究和对比一系列过渡族金属氯化物对乙炔氢氯化反应的催化性能,发现这些金属催化活性顺序为[4]:Pd2+>Hg2+>Cu2+~Cu+>Ag+>Cd2+>Zn2+.由于Cu价格低、毒性低、热力学稳定性好及催化活性优良,使得CuCl2成为理想的催化剂活性组分.然而,与HgCl2或AuCl3相比,Cu基催化剂的反应活性较低 (Cu400Ru/MWCNTs[9],Cu-g-C3N4-AC[10]、Cu-NCNT[11]),成为Cu基催化剂亟待解决的问题.
另一方面是乙炔氢氯化反应催化剂的载体.与二氧化硅、金属氧化物和沸石相比,碳材料由于具有高的电子导电率和大的比表面积,表现出更好的催化活性.掺氮活性炭在氮原子的作用下,可以修饰电子结构,从而提高其润湿性和亲水性.而在碳材料中,自2004年石墨烯被发现以来,备受各领域关注.石墨烯实质就是单层石墨,是sp2杂化碳原子构成的蜂窝状的六元环,有着独特的二维纳米结构.与乙炔氢氯化反应催化剂中常用的载体相比,石墨烯高理论比表面积(2 630 cm2.g-1)表现出更大优势[12].然而,有关掺氮石墨烯与活性组分Cu进行复合的相关报道较少,将Cu与掺氮石墨烯复合制备乙炔氢氯化反应催化剂具有一定研究价值.
基于以上分析,本文以CuCl2.2H2O为活性组分、掺氮石墨烯为载体,采用超声辅助等体积浸渍法制备了乙炔氢氯化反应掺氮石墨烯-铜基催化剂(Cu-N/GN).Cu-N/GN催化剂的微观结构表征证明:该催化剂具有较大的比表面积,且活性组分Cu2+均匀分布于载体N/GN上;催化剂中C、O、N、Cu和Cl元素共存.催化性能测试结果表明:Cu-N/GN表现出良好的催化活性(68%)和对氯乙烯单体优良的选择性(99%).
1 实验部分
1.1 试 剂
CuCl2.2H2O购自上海精化科技研究所;尿素,天津市致远化学试剂有限公司;盐酸,重庆川东化工(集团)有限公司;氧化石墨为课题组自制,详细制备步骤可参考已发表论文[13].
1.2 催化剂制备
1.2.1 载体的制备
称取氧化石墨粉末(GO)400 mg加入到200 mL去离子水中,超声2 h后得到2 mg.mL-1GO分散液.按GO分散液与尿素1∶30的比例进行超声混合,混合均匀后倒入反应釜,在180℃下水热反应12 h.随炉冷却至室温,用去离子水洗涤、干燥后得到掺氮石墨烯(N/GN).作为对比实验,制备了石墨烯(GN),步骤与掺氮石墨烯相似,只是前驱体中没有添加尿素.
1.2.2 催化剂的制备
分别称取GN和N/GN 20 g于2个烧杯中,在烧杯中分别加入含铜量为4%的CuCl2溶液25 mL,然后在恒温水浴锅中75℃下浸渍5 h,之后超声处理1 h;最后将其放到培养皿中进行干燥.干燥处理步骤为:在40℃干燥4 h和120℃干燥12 h,得到样品分别为石墨烯-铜催化剂(Cu-GN)和掺氮石墨烯-铜催化剂(Cu-N/GN).通过ICP-OES测试,在Cu-GN和Cu-N/GN两种催化剂中铜含量分别约为3.3%和3.6%.
1.3 测试仪器
采用X射线衍射仪D-8,(XRD,德国Bruker公司,Cu Kα 射线,λ=0.154 056 nm,管电压 40 kV,管电流100 mA),2θ扫描角度范围是10°~80°,扫描速度为4°.min-1测试催化剂物相.催化剂形貌采用场发射扫描电子显微镜S-4800(SEM,Hitachi公司,操作功率为15 kW)和透射电子显微镜JEM-2100F(TEM,JEOL公司,操作功率为100 kW)进行表征.催化剂元素分析是由X射线光电子能谱(XPS,Perkin Elmer PHI 1600 ESCA,单色Al Kα射线,操作功率为150 W)、扫描电子显微镜配套的能量分布X射线光谱仪(EDS)和电感耦合等离子体原子发射光谱仪(ICP-OES,Agilent 730)进行测试.俄歇电子光谱分析(XAES,AER-200,日美纳米表面分析仪器公司),用Al Kα X射线作为射线源(hν=1486.6 eV).通过BEL-Mini高精度N2吸脱附比表面积分析仪测试催化剂的N2吸附-脱附性能,其比表面积和孔径分别基于Brunauer-Emmett-Teller(BET)理论和密度泛函数理论(DFT)进行计算.
1.4 催化剂的性能测试
评价催化剂的性能优劣首要评价催化剂的活性和稳定性.其中,催化剂的活性方面主要评判乙炔的转化率和氯乙烯的选择性.通过Lw型固定床不锈钢微反应器对GN、Cu-GN、Cu-N/GN进行活性测试,并采用LabSolutions CS气相色谱仪对催化剂性能进行评价.反应条件是:C2H2和HCl混合气的组成比例为 VHCl/VC2H2=1∶1.15、101.325 kPa、温度 150℃、GHSV(C2H2)=360 h-1.反应尾气中的HCl气体用NaOH溶液洗涤2次以除去[14-15],最后进入LabSolutions CS气相色谱进行催化剂活性评价.
在分析时由于体系中HCl被吸收除去,故将整个反应装置内的体积视为恒定,令其为1个体积单位得到乙炔转化率(XA)和氯乙烯选择性(SVC)的计算公式如下[16]:
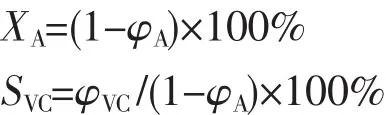
式中φA为装置尾气中剩余乙炔的体积分数、φVC为氯乙烯体积分数.
2 结果与讨论
2.1 催化剂的物相分析
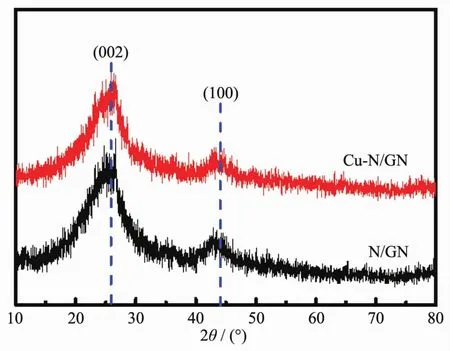
图1 N/GN和Cu-N/GN的XRD图Fig.1 XRD patterns of N/GN and Cu-N/GN
如图1所示,N/GN和 Cu-N/GN均在 2θ=25.3°和2θ=42.5°左右出现特征峰,表现为石墨烯的特征峰[17],分别对应于石墨烯的(002)和(100)晶面[18].其次,与N/GN相比,Cu-N/GN的特征峰略有变宽[19],表明铜的负载对石墨烯微观结构产生了影响.另外,在Cu-N/GN的XRD图中并没有铜的特征吸收峰,可能是铜尺寸小、含量少(3.6%)或是分布均匀的原因造成的[20-21].
2.2 催化剂的微观形貌分析
通过SEM和TEM分析表征Cu-N/GN催化剂的微观形貌,结果如图2所示.图2(a)为Cu-N/GN催化剂的SEM图,表现出石墨烯特有的褶皱片层形貌[13].图2(b)是催化剂的EDS图谱,证明了催化剂中C、O、N、Cu和Cl共同存在,同时表明了N掺杂和Cu负载成功.为了进一步表征催化剂的形貌,又进行了TEM分析.从TEM图中看到(图2(c)),Cu组分均匀分布于N/GN片层上,可能是超声辅助作用有利于活性物质Cu在N/GN上的均匀负载,进而提高催化剂的催化活性.
2.3 催化剂的N2吸附脱附分析
通过N2吸附脱附测试表征新制备的和反应后的N/GN和Cu-N/GN催化剂的比表面积、孔体积和孔径等孔结构特征,测试数据如表1所示.从表1中可以得出:(1)新制备的Cu-N/GN的比表面积、孔体积和孔径(587 m2.g-1、0.41 cm3.g-1、2.21 nm)均小于新制备的N/GN的比表面积、孔体积和孔径(660 m2.g-1、0.46 cm3.g-1、2.30 nm),可能是用于铜负载占据了一定的空间引起的.(2)与新制备的Cu-N/GN的比表面积和孔体积相比,反应后的Cu-N/GN的比表面积和孔体积均明显减小.新制备和反应后N/GN的比表面积和孔体积,也表现出相同的变化趋势.这种现象可能是由于样品在参与催化反应过程中,产生了积碳现象或是载体中部分孔坍塌造成的[3,22].
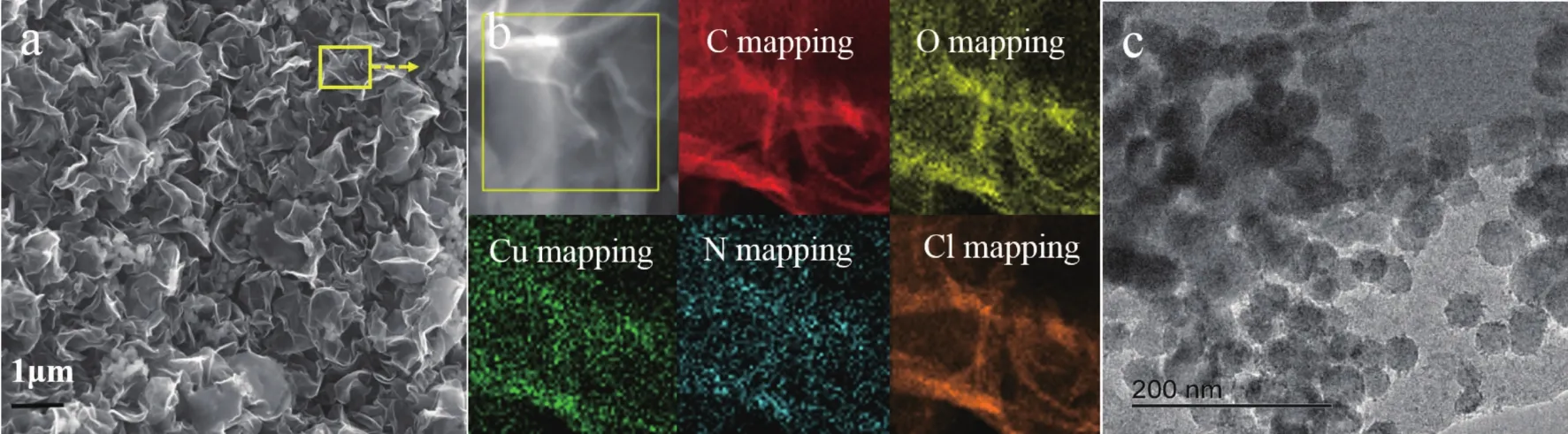
图2 Cu-N/GN催化剂的(a)SEM图,(b)EDS图和(c)TEM图Fig.2 (a)SEM image,(b)EDS mapping and(c)TEM image of Cu-N/GN catalyst
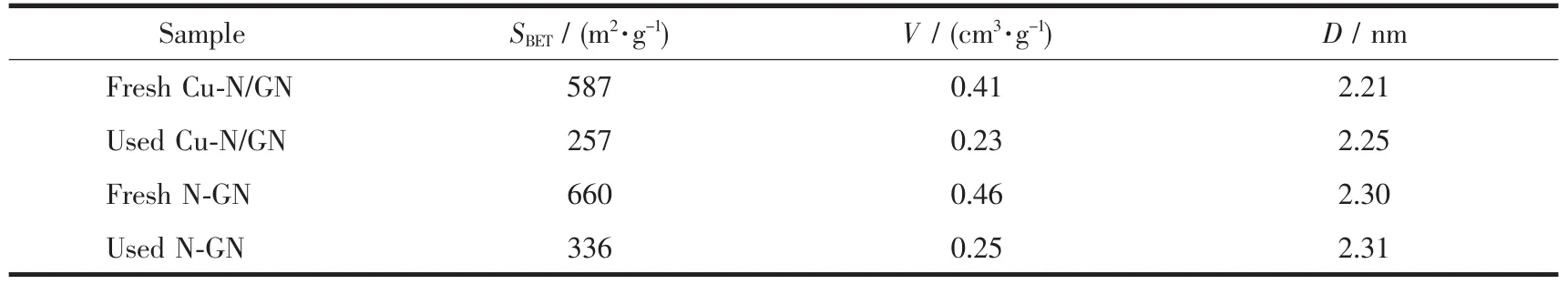
表1 样品的N2吸附脱附测试数据Table 1 N2adsorption/desorption data of the samples
2.4 催化剂的元素、含量及化学价态分析
乙炔氢氯化反应过程中,金属物质价态变化是金属催化剂失活的主要因素之一.因此,通过XPS和XAES表征,研究新制备的和反应后的催化剂中Cu化学价态的变化.如图3a所示,在N/GN图中,有明显的N元素峰,表明通过GO和尿素的水热反应,成功的将N元素掺杂到石墨烯中.Cu-N/GN图中,在 200.4、284.8、399.5、531.7 和 933.6 eV 的 5 个峰分别为 Cl2p、C1s、N1s、O1s和 Cu2p 的峰[13,23-25],表明Cu-N/GN中N和Cu元素的存在,与EDS测试结果一致.其中,N和Cu的百分比分别为6.1%和3.5%,Cu的含量与ICP-OES测试结果相吻合.从Cl2p的高分辨率图(图3b)中可以看出,Cl2p被分成2个峰198.0和199.1 eV,这2个峰分别对应于Cl-2p3/2和Cl-2p1/2[26],表明在催化剂中Cl元素是以离子态存在的.新制备Cu-GN和Cu-N/GN催化剂的XPS和XAES如图3c和3d所示.两种新制备催化剂的Cu2p图中,都有明显的Cu2p3/2、Cu2p1/2峰和伴随峰,表明催化剂中Cu2+的存在[27].拟合曲线中,在930.0~935.1 eV识别出2个峰,分别是934.1和931.8 eV处.前者是Cu2+物质的特征峰,后者是Cu+或Cu0物质[28-29].从Cu2p的XPS图中还可以得出,在两种催化剂中Cu2+是主要的活性成分.因为Cu+和Cu0的结合能非常相似,所以通过XAES图对Cu+和Cu0进行分析,如图3d是Cu LMM俄歇光谱图.从图中可以看出,2个主峰分别为916.6 eV处对应于Cu+和910.5~912.1 eV处代表Cu LMM图中Cu的不同转变态[30],由此得出在新制备的催化剂中只存在Cu+.
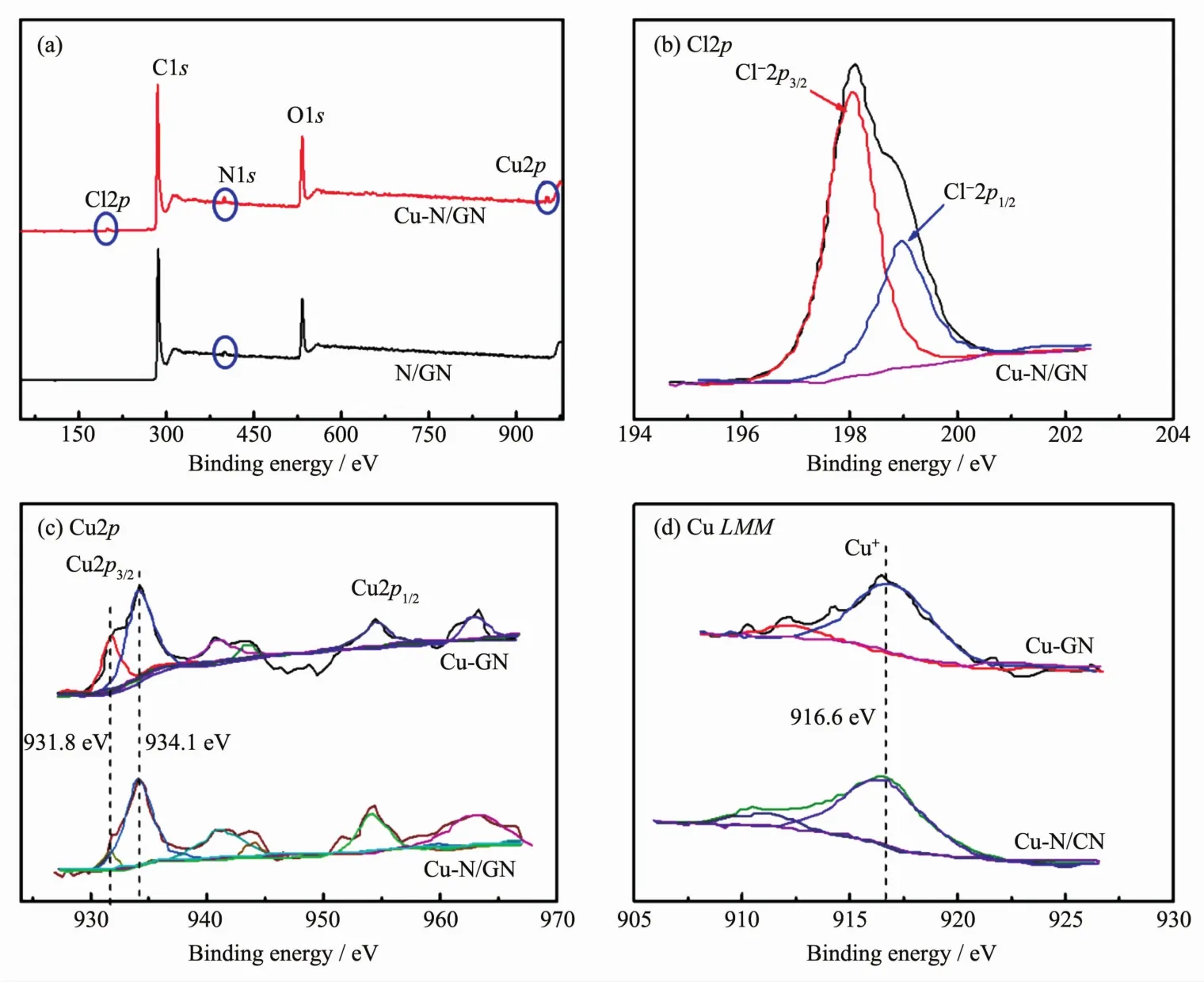
图3 新制备的N/GN和Cu-N/GN催化剂的(a)XPS图;(b)Cu-N/GN中Cl2p的XPS图;Cu-GN和Cu-N/GN的(c)Cu2p XPS图和(d)Cu LMM俄歇光谱图Fig.3 (a)XPS survey spectra of fresh N/GN and Cu-N/GN catalysts;(b)Cl2p XPS spectrum of Cu-N/GN;(c)Cu2p XPS spectra and(d)Cu LMM Auger spectra of Cu-GN and Cu-N/GN
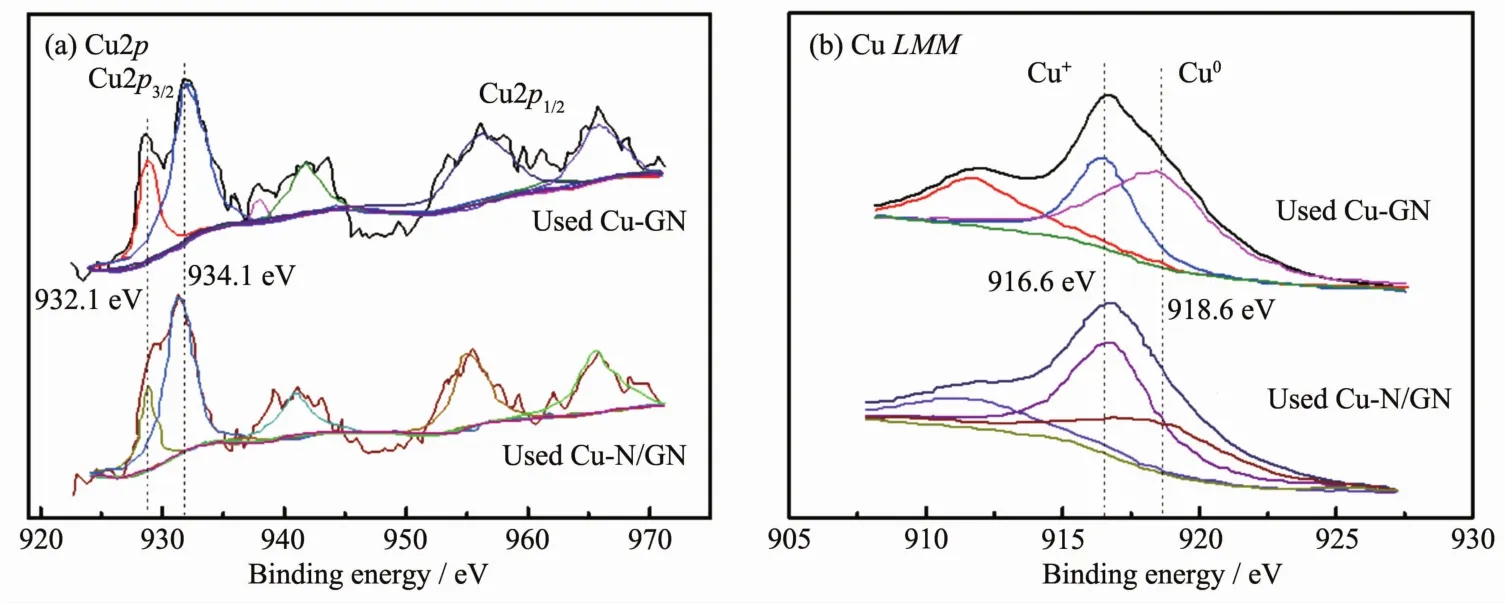
图4 反应后的Cu-GN和Cu-N/GN催化剂的(a)Cu2p XPS和(b)Cu LMM俄歇光谱图Fig.4 (a)Cu2p XPS spectra and(b)Cu LMM Auger spectra of used Cu-GN and Cu-N/GN catalysts
反应后Cu-GN和Cu-N/GN催化剂的XPS和XAES分析结果如图4所示.图4a中可以看出,在934.1 eV处有明显的Cu2+特征峰,并有在940~945 eV处的Cu2+伴随峰,表明反应后的2种催化剂中Cu2+仍然是主要组分.然而,与新制备的催化剂相比,932.1 eV(Cu+或Cu0)处的峰面积增大,表明在反应中部分活性组分被还原了.此外,从反应后的2种催化剂的Cu LMM俄歇光谱图 (图4b)得出,在918.6和916.6 eV处分别是Cu0和Cu+的特征峰,表明在反应后催化剂中含有Cu0(在新制备的催化剂中没有检测到,如图3d).因此,对比图3和图4分析结果得出,催化剂中活性组分的还原可能是催化剂失活的原因.从图4b还可以看出,与反应后Cu-N/GN相比,反应后Cu-GN在918.6 eV(Cu0)处的峰面积更大,可以得出Cu-N/GN中N的存在一定程度上抑制了活性组分还原为Cu0.
2.5 催化剂的催化性能分析
从图5(a)N/GN、Cu-GN和Cu-N/GN样品的催化性能图中可以看出,N/GN对乙炔氢氯化反应的催化活性在25%左右;Cu-GN和Cu-N/GN催化剂在反应50 h后对乙炔氢氯化反应乙炔转化率分别稳定在57%和68%.图5(b)是Cu-GN和Cu-N/GN对氯乙烯选择性图,得出两种催化剂对氯乙烯的选择性相似且都具有高的选择性,在98.0%~99.5%的范围内波动.
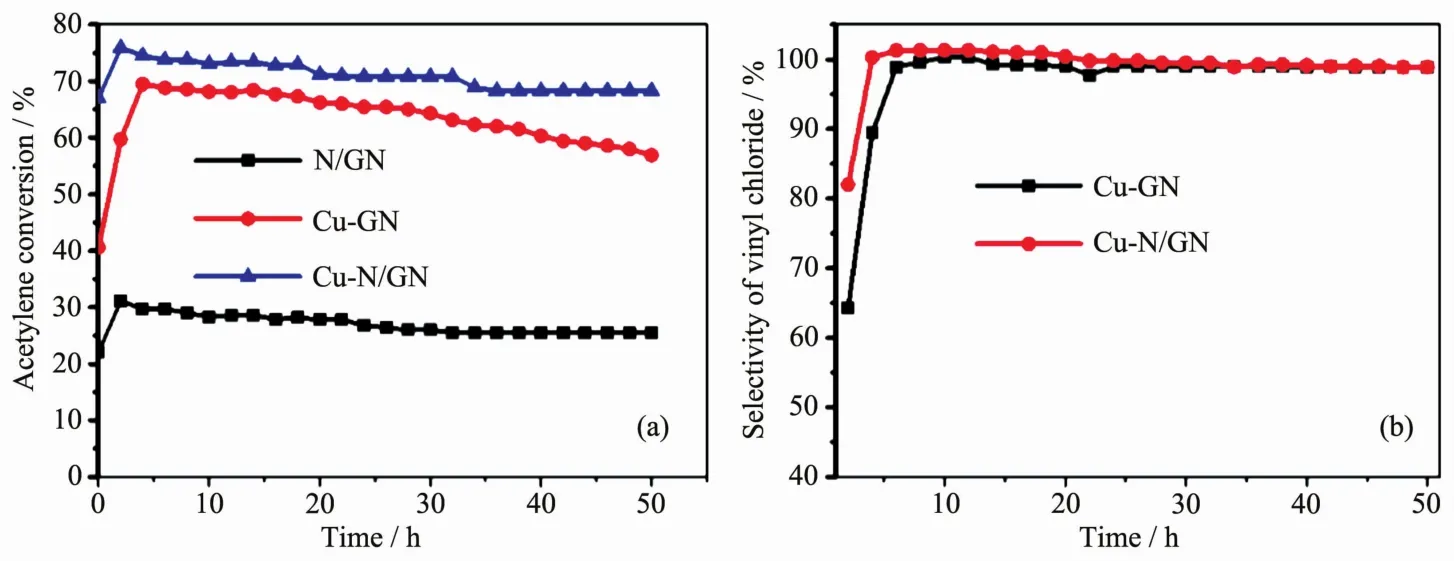
图5 GN、Cu-GN和Cu-N/GN催化剂的催化活性 (a)和选择性 (b)Fig.5 Catalytic activities(a)and selectivities(b)of GN,Cu-GN and Cu-N/GN catalysts
综上所述,(1)Cu-N/GN催化剂不仅做到无汞,还具有良好的催化活性和较长的使用寿命.(2)催化剂Cu-GN和Cu-N/GN中的Cu2+是乙炔氢氯化反应的主要活性组分,且催化剂失活的主要原因是反应过程中部分Cu2+被还原为Cu0.(3)与Cu-GN相比,Cu-N/GN表现出更好的催化性能,可能是由于:N/GN载体中N元素掺杂改变了石墨烯片层的电子结构,增加了石墨烯表面的活性位点,在静电吸附作用下有助于Cu2+均匀分布于石墨烯表面,且活性组分Cu2+的含量较高(图6);N元素的存在还抑制了Cu2+的还原,从而提升了Cu-N/GN对乙炔氢氯化反应的催化活性.
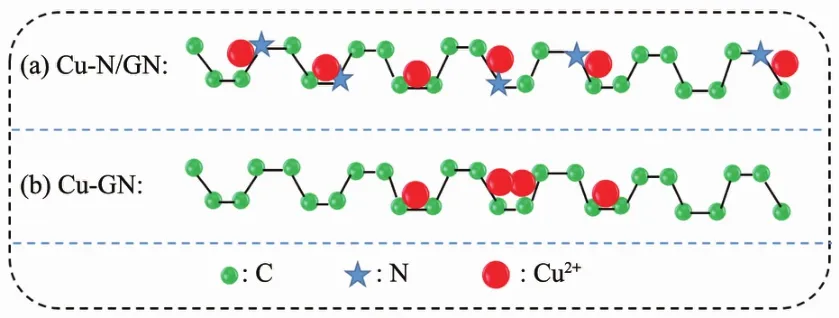
图6 (a)Cu-N/GN和(b)Cu-GN催化剂的结构示意图Fig.6 Structure diagrams of(a)Cu-N/GN and(b)Cu-GN catalysts
3 结 论
(1)采用水热法制备N/GN载体,以CuCl2.2H2O为活性组分,采用超声辅助等体积浸渍法制备了乙炔氢氯化反应所用掺氮石墨烯-铜基催化剂(Cu-N/GN).
(2)测试结果表明,Cu-N/GN催化剂中活性组分Cu尺寸较小、含量较低且均匀分布于载体N/GN上.与Cu-GN相比,在乙炔氢氯化反应中Cu-N/GN表现出良好的催化活性(68%)、高选择性(99%)和稳定性(50 h).
(3)Cu-N/GN催化剂性能优良归因于,N/GN载体中N元素掺杂改变了石墨烯片层的电子结构,增加了石墨烯表面的活性位点,在静电吸附作用下有助于Cu2+均匀分布于石墨烯表面,且活性组分Cu2+的含量较高;N元素的存在还抑制了催化反应过程中Cu2+的还原,从而提升了Cu-N/GN对乙炔氢氯化反应的催化性能.
(4)催化剂Cu-GN和Cu-N/GN中的Cu2+是乙炔氢氯化反应的主要活性组分,且催化剂失活的主要原因是反应过程中部分Cu2+被还原为Cu0.

