糖通饮与穴位埋线对DPN大鼠血清NGF、TGF-β1的影响
屈璐,侯胜开,高楠楠,潘艳伶
(1.贵阳中医学院第一附属医院,贵州 贵阳 550004;2.枣庄市妇幼保健院,山东 枣庄 277100; 3.贵州医科大学,贵州 贵阳 550004;4.贵州医科大学附属医院,贵州 贵阳 550004)
糖尿病周围神经病变(Diabetic peripheral neuropathy,DPN)是糖尿病最常见的并发病之一,也是糖尿病患者致残的首要因素[1-3],常以肢体远端及躯干部分的麻木、疼痛、异样感、肌肉无力及萎缩等为主要临床表现。全国名老中医凌湘力教授自拟临床经验方“糖通饮”在治疗DPN上取得了较好的临床疗效[4],但尚未有进一步的机制研究。本实验即通过动物实验,初步探讨糖通饮及穴位埋线治疗DPN大鼠可能的作用机理和途径,为临床治疗及进一步优选治疗方案提供客观的理论依据。
1 材料
1.1 实验动物
清洁级健康雄性SD大鼠75只,体质量(200±20)g,由贵州医科大学实验动物中心提供,合格证号:SCKK(黔)2012-0001。
1.2 仪器与试剂
稳豪型血糖仪和血糖试纸(德国罗氏);BL-420F生理记录仪(成都泰盟);链脲佐菌霉素(Streptozocin,STZ,美国Sigma);大鼠神经生长因子(nerve growth factor,NGF)、转化生长因子β1(transforming growth factor-β1,TGF-β1)和ELISA检测试剂盒(货号:CK-E30636R、CK-E30643R)(昆明腾昆科技有限公司)。
1.3 动物饲料
动物饲料购置于贵州医科大学实验动物中心。高能量饲料配方[5]:普通饲料64.9%、炼猪油10%、蔗糖20%、蛋黄5%及食盐0.1%,由贵州医科大学实验动物中心按上述配方加工生产。
1.4 糖通饮方
组方:黄芪30 g,地骨皮15 g,熟地黄10 g,泽泻10 g,茯苓10 g,山药15 g,牡丹皮10 g,草决明20 g,丹参12 g,地龙12 g,鸡血藤20 g和路路通10 g。所用中药饮片均购于贵州医科大学附属医院中药房。
2 方法
2.1 分组
75只大鼠适应性喂养1周后,随机分为正常组(15只)、模型组(15只)和治疗组(45只,中药组、穴埋组及药埋组每组各15只)。
2.2 模型制备
模型组及各治疗组大鼠给予高能量饲料喂养2周后,使用0.1%STZ按20 mg/kg、30 mg/kg、30 mg/kg的剂量标准进行2~3次腹腔注射,每次注射72 h后取大鼠尾静脉血检测空腹血糖(fasting blood glucose,FBG),大鼠FBG值≥16.7 mmol/L[6],且连续3天血糖值稳定,则判定为造模成功,血糖值未达标者进行下一次注射(3次注射后血糖值均未达标者,判定模型失败)。最终纳入观察大鼠为正常组12只,模型组9只,中药组9只,穴埋组12只,药理组11只。
2.3 治疗方法
中药组大鼠按8 mL/kg(根据实验动物体表面积剂量换算)的剂量标准,给予糖通饮浓缩煎剂灌胃给药,1次/d;埋线组选取双侧足三里、肝俞及肾俞穴,常规消毒后,将0.2 cm羊肠线埋植在穴位皮下组织或肌肉层内,1次/2 w。药埋组将中药组、穴埋组治疗方法结合进行治疗。正常组和模型组给予生理盐水灌胃,剂量标准同中药组,1次/d。中药干预治疗以5周为1个疗程,共进行2个疗程;穴位埋线2 w/次,共治疗5次。治疗期间所有大鼠均采用普通饲料喂养。
2.4 指标采集及检测
2.4.1 坐骨神经动作电位传导速度
大鼠麻醉后俯卧位固定,钝性分离并暴露左侧坐骨神经,采用BL-420F生物机能实验系统软件“肌肉神经实验”中“神经干兴奋传导速度测定”模块检测坐骨神经干动作电位传导速度。控制参数:刺激参数及模式:细电压,方式:单刺激,延时5.00 ms,波宽0.05,波间隔10,频率10.0 Hz,强度3.000 V。
2.4.2 NGF、TGF-β1检测
麻醉大鼠,取大鼠股动脉血5 mL以3 000 r/min离心(4℃)后取上清液,采用ELISA试剂盒检测。
2.4.3 坐骨神经形态学检测
麻醉大鼠,俯卧位固定,钝性分离并暴露右侧坐骨神经,截取神经节段放入20%福尔马林液中固定72 h后,石蜡制片,HE染色后在光镜下观察。
2.5 统计学处理

3 结果
3.1 各组大鼠一般情况比较
正常组大鼠毛发光泽,毛色正常,活动灵活,精神、饮食、二便均正常,体质量随周龄增加而增加。造模成功后,模型组及治疗组大鼠开始陆续出现程度不等的体质量减轻,饮食、饮水增加,大小便增多,大便溏,毛发杂乱色枯黄并伴有脱毛。在行动上,模型组及治疗组大鼠表现出精神倦怠,少动,行走迟缓,对外界刺激(声音、触碰、针刺等)反应迟钝,部分大鼠出现跛行。进行干预治疗后,治疗组大鼠进食饮水及二便增多症状有所好转,体质量逐渐稳定,并有所增加,大鼠毛色、精神、活动等方面均得到不同程度改善。
3.2 各组大鼠血清神经生长因子(NGF)及转化生长因子β1(TGF-β1)水平比较
与正常组比较,模型组大鼠血清NGF含量明显降低,血清TGF-β1含量明显增高(P<0.01)。经干预治疗后,各治疗组大鼠血清NGF含量较模型组明显升高(P<0.01),且中药埋组血清NGF含量升高最为明显(P<0.01);各治疗组大鼠血清TGF-β1含量均显著低于模型组(P<0.01),其中药埋组血清TGF-β1含量降低最为明显(P<0.01)。见表1。

表1 各组大鼠血清NGF及TGF-β1含量比较
注:与正常组比较,1)P<0.01;与模型组比较,2)P<0.01;与药埋组相比,3)P<0.01。
3.3 各组大鼠空腹血糖及坐骨神经动作电位传导速度比较
与正常组比较,模型组大鼠空腹血糖明显升高,且动作电位传导速度明显降低(P<0.01)。与模型组比较,各治疗组大鼠FBG值均降低(P<0.05或P<0.01),其中药埋组下降最为明显(P<0.01)。经干预治疗后,治疗组大鼠坐骨神经动作电位传导速度较模型组均有所升高(P<0.05),但各治疗组间神经动作电位传导速度未见明显差异(P>0.05)。见表2。
表2 各组大鼠空腹血糖及坐骨神经动作电位传导速度比较
注:与正常组比较,1)P<0.01;与模型组比较,2)P<0.05,3)P<0.01;与药埋组相比,4)P<0.01。
3.4 各组大鼠坐骨神经光镜检查情况
正常组大鼠坐骨神经切面可见神经组织结构正常,神经纤维排列规则整齐,雪旺细胞、髓鞘及轴索结构完整清晰,神经束膜组织结构正常。模型组大鼠神经纤维排列紊乱,雪旺细胞数量中度减少、形态不规则、部分退变和排列紊乱;髓鞘形态不规则、中度水肿,郎飞结组织结构不清;轴突形态不规则、粗细不等及连续中断,神经束膜血管扩张充血,并伴有少量炎细胞浸润。治疗组大鼠神经纤维轻度排列紊乱,雪旺细胞数量轻度减少,轻度排列紊乱,轴突形态不规则、粗细不等及连续中断;髓鞘形态不规则、轻度水肿,郎飞结结构较模型组清晰;中药组和穴埋组神经束膜血管轻度扩张充血,并伴有炎细胞浸润,药埋组神经束膜血管未见明显扩张充血。见图1。
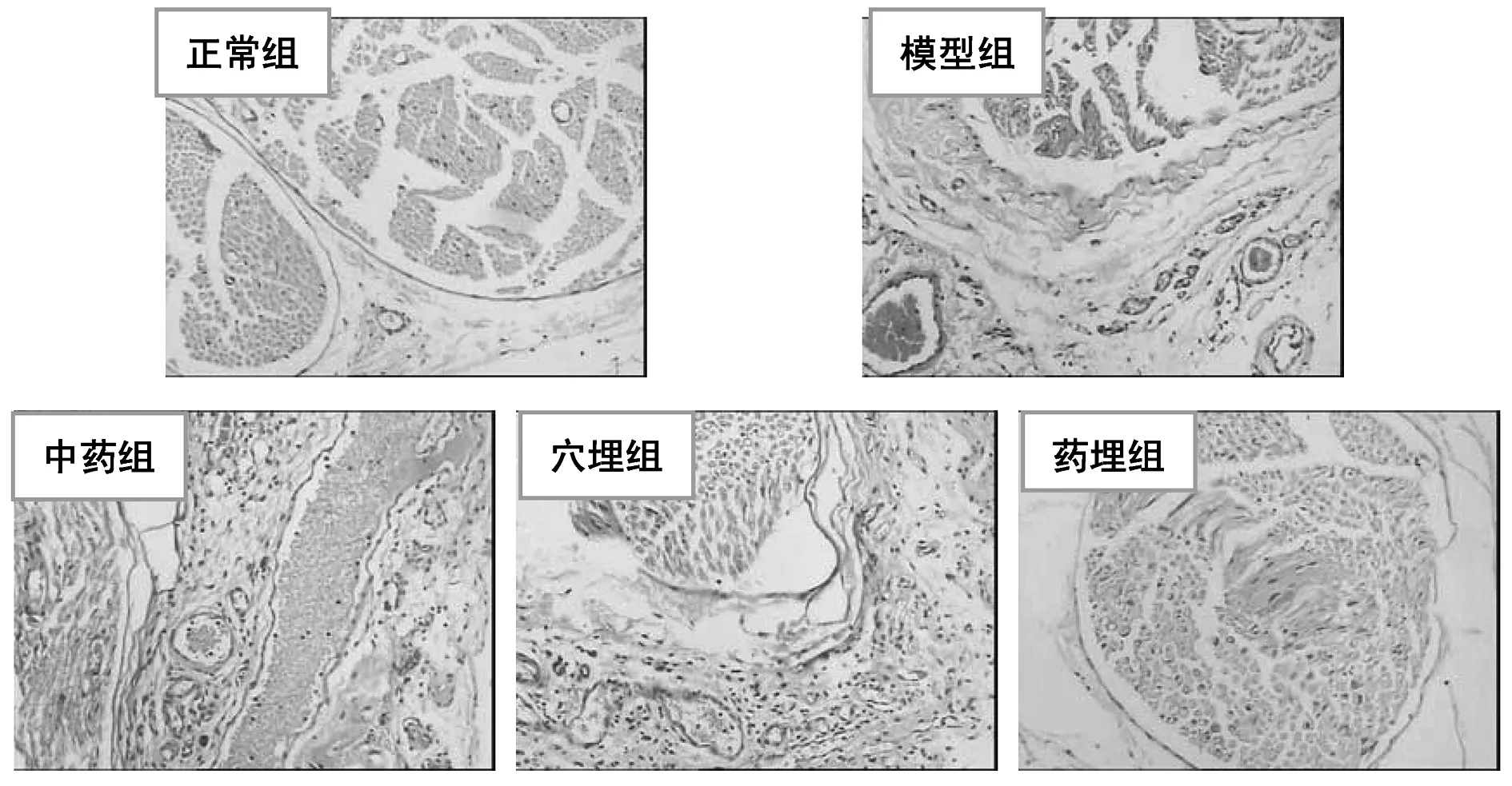
图1 各组大鼠坐骨神经HE图(HE,×100)
4 讨论
现代医学认为DPN是代谢紊乱、血管损害、神经营养因子缺乏、氧化应激和免疫损伤等多因素共同作用的结果[7-9]。其中,高血糖是DPN发病的基础性因素,研究表明[10-11],机体血糖长期处于较高水平,不仅会出现微血管病变,雪旺细胞受损,还可导致活性氧自由基、糖基化终产物等产生过多,激活机体多条旁代谢途径,进而导致神经组织功能受损。NGF的缺乏则被认为是DPN发病的主要原因之一[12],神经营养因子学说认为神经营养因子的合成、分泌和代谢障碍是DPN发病的重要原因,而NGF是神经营养因子家族中与神经系统活动关系最密切的一员。研究表明[13-16],NGF除了对周围感觉神经节和交感神经的生长、维持及存活有重要作用以外,还可促进神经中血管的再生和血管活性因子的产生,对加速受损神经修复、促进神经功能恢复、改善患者周围神经症状等具有积极作用,因而在DPN的发病机制和防治中,NGF的作用极其重要。
TGF-β1一直被作为研究糖尿病肾病的重要指标[17],但Anjaneyulu等[18]研究显示,TGF-β1介导了糖尿病动物模型的周围神经细胞的损伤后,TGF-β1与DPN之间的关系开始被重视。研究证明[19-22],TGF-β1可能通过介导核转录因子-κB的活化、影响谷胱甘肽形成和维持相关的基因、促进细胞外基质积聚等方面参与DPN的发生发展,抑制TGF-β1的生成可改善周围神经病变。
中医学中并没有关于糖尿病周围神经病变病名的记载,但关于该病临床表现的描述可散见于诸多医学文献中,如《丹溪心法》有“肾虚受之,腿膝枯细,骨节烦疼”的记载,清代《王旭高医案》也记载了消渴患者“消渴日久,但见手足麻木,肢冷如冰”的临床表现,这些记载都描述了本病具有凉、麻、痛和痿等特点,结合其发病机制,可将其归入中医的“消渴痹证”“消渴痿证”等证范畴[23]。
近年来,众多医家分别从阴虚津亏、脏腑虚弱和痰瘀为患等角度对DPN的病因病机进行了深入研究[24-27],偏重各有不同。全国名老中医凌湘力教授则认为,该病的基本病机是病久耗伤气阴,致气血运行不畅,瘀血阻络;或消渴日久,阴损及阳,痰瘀互结,痹阻脉络,导致阳气不能通达四末,肌肉筋脉失于濡养,发为病,虽其病变在筋脉,但究其内涉脏腑乃肝、肾、脾三脏虚损。凌老认为,该病病机为肝、脾、肾气阴不足、痰瘀互结,具有本虚标实的病机特征,其中痰瘀互结为糖尿病周围神经病变的直接病因,故而在治疗上应重在滋肾补肝健脾、益气活血通络,并据此创立糖通饮方。方中重用黄芪益气活血,熟地黄滋阴补肾、填精益髓,山药气阴双补,一可与黄芪配伍补益脾气,补后天而充先天,二可与熟地黄相伍滋补肝肾之阴,三者同用并补肾、肝、脾三阴以治本虚,共为君药;鸡血藤、地龙相伍活血通络,路路通通经化瘀,丹参引药入心经助血上行,四者共用活血化瘀、通经疏络,共为臣药;佐药牡丹皮、地骨皮、泽泻、茯苓、草决明清热利湿泄痰浊,一则防阴虚日久生热,二则防阴损及阳,水津不布,日久生痰浊之弊,全方补虚泻实,标本兼治,祛邪而不伤正,扶正而不敛邪,诸药合用,共奏滋肾补肝健脾、益气活血通络之效。
现代药理学研究证实[28-31],黄芪、山药、牡丹皮等药物中的有效成分可以通过调节糖、脂代谢,在一定程度上延缓糖尿病及其并发症的发展。另有报道[32-33],熟地黄能明显促进皮质神经元轴突生长,具有保护神经和抑制中枢神经系统作用;地龙中的水溶性提取物可以显著激发NGF生物活性以诱导神经轴突增生,也能有效的促进神经修复、再生。
穴位埋线主要是通过埋入羊肠线对穴位产生持久、平和的生理和生物化学刺激,以调节机体脏腑功能。足三里穴位于下肢,是足阳明胃经合穴,也是胃的下合穴,既可补益气血以润宗筋,又可滋肾健脾,以助消除痰浊瘀血,标本兼顾,故选为主穴;肾为消渴发病之根本,且肝肾同源,肾俞穴可起到培补元气、滋水涵木、补肝肾之阴精的作用,脾胃为气血生化之源,脾俞穴具有益气健脾、化湿泄浊之效,且与肾俞穴同用可以补后天而充先天,故选取肾俞、脾俞两穴为配穴。三穴同用可滋肝补肾健脾,以益气活血、化瘀泄浊,使脏腑气血通畅、宗筋得养。
本实验结果提示,DPN大鼠经治疗后,FBG、血清NGF、血清TGF-β1含量均较模型组改善,其中药埋组改善最为明显,说明中药糖通饮和穴位埋线均能有效治疗DPN,延缓DPN病情进展,两者合用时疗效最佳,值得临床推广应用,其可能的作用途径为通过降低血糖,改善糖代谢,增加NGF含量,降低TGF-β1含量,直接或间接促进受损神经的生长和修复,来实现延缓DPN病情进展的目的。
——从一道浙江选考生物学试题谈起

