肢体骨肉瘤长期生存患者子女健康状况分析
鞠晓聪 郑凯 徐明 韩加 王文剑 王景明 宋帅 李泉 鲁亚杰 于秀淳
自规范性化疗及广泛性肿瘤切除手术的联合应用以来,国内外文献报道骨肉瘤患者 5 年生存率从30 年前的不足 20% 提高到 60%~80%[1-4]。新辅助化疗药物包括顺铂 ( D )、多柔比星 ( A )、甲氨蝶呤( M ) 和异环磷酰胺 ( I ),足够的化疗药物剂量和恰当的化疗方案是保证患者治疗效果的基础[5]。随着生存率的提高,患者的生存质量是需要关注的一个问题。1948 年,Spitz[6]首次报道高剂量化疗药物会对患者性腺造成损伤,部分损伤甚至不可逆,对患者心理及生活产生不良影响[7]。
目前肢体骨肉瘤患者接受化疗后顺利生育子女的文献报道较少[8-11],2000 年 Longhi 等[8]报道长期生存的 92 例女性骨肉瘤中,有 14 例共生育 19 名子女;2003 年 Longhi 等[9]报道 96 例男性骨肉瘤中,8 例共生育 12 名子女;2004 年,Durrieu 等[10]报道1 例骨肉瘤生育 1 名后代;同年 Harish 等[11]报道长期生存的 36 例骨肉瘤中,接受治疗后有生育需求的15 例共生育 22 名子女,但对肢体骨肉瘤患者子女健康状况的随访尚无报道。骨肉瘤患者体细胞存在染色体不稳定性,具有较高的肿瘤发生风险,这种不稳定性可能通过遗传方式传给子代,使子代对肿瘤的易感性增加[12]。
本研究目的:( 1 ) 评价规范化治疗肢体骨肉瘤长期生存患者的生育能力;( 2 ) 评价骨肉瘤患者子女健康状况。
材料与方法
一、纳入标准与排除标准
1. 纳入标准:( 1 ) 2000 年 6 至 2016 年 3 月在解放军九六○医院和西京医院行肢体骨肉瘤规范化治疗后长期生存并可能生育者;( 2 ) 原发部位为四肢长骨骨肉瘤者;( 3 ) 接受规范化治疗者;( 4 ) 生存时间>5 年者;( 5 ) 发病治疗后符合生育年龄 ( <40岁 ) 者。
2. 排除标准:( 1 ) 随访资料不全者;( 2 ) 不愿意接受相关咨询和评价者;( 3 ) 不公开相关资料者。
二、一般资料
本研究共纳入 35 例。具有生育要求的患者13 例,初诊年龄 10~24 岁,平均年龄 18.5 岁;术后生存时间 7~21 年,平均术后生存时间 13.2 年;发病部位:股骨远端 8 例,胫骨近端 5 例;Enneking分期:均为 IIB 型;治疗方式:活检病理明确诊断后行术前化疗、手术、术后化疗,根据患者对化疗药物的耐受程度调整化疗剂量及化疗次数;化疗药物包括:顺铂 ( D )、多柔比星 ( A )、甲氨蝶呤 ( M )和异环磷酰胺 ( I ),具体化疗方案[13-14]:MMIA 化疗方案 8 例,MIDA 化疗方案 1 例,DIA 化疗方案4 例;手术方式:瘤段骨切除灭活再植术 7 例,瘤段骨切除特制肿瘤型人工假体置换术 6 例。
三、研究方法
电话随访 13 例具有生育要求的肢体骨肉瘤长期生存患者生育情况。查询所接受化疗方案,统计化疗药物累积量。
家庭随访肢体骨肉瘤长期生存患者生育子女,记录年龄、身高、体重,计算体质量指数 ( BMI ),参考 WHO 2006 年公布 0~5 岁儿童生长标准,以及 2007 年美国国家营养调查数据为蓝本所修订的5~19 岁的生长标准评价身体发育速度[15],营养状况 ( 消瘦或超重 )[16-17]。
应用量表评价患者子女智力发育情况:3 个月~3 岁患者子女应用盖塞尔智力量表[18]( 不包括3 岁 );3~6 岁患者子女应用韦氏幼儿智力量表[19]( 不包含 6 岁 );6~16 岁患者子女应用韦氏儿童智力量表[20]( 不包括 16 岁 )。
采集 6 例子女外周血液样本送往深圳华大生物公司行染色体检测。6 例患者子女及父母自愿接受基因检测,均签署自愿同意书,运用高通量测序技术进行全基因组测序 ( 染色体非整倍体、100Kb 以上缺失 / 重复检测 ),其检测结果参考基因组为 GRCh37 / hg,检索数据库包括 UCSC、DGV、OMIM、HGMD、DECIPHER、PubMed 和 ISCA 等。本次检测尚无法检测染色体高度重复、高度固缩区域 ( 如近着丝粒、端粒区域的染色体异常:罗氏易位等 )、多倍体变异、100Kb 以下缺失 / 重复、易位、倒位、低比例嵌合体、单亲二倍体等情况。
本研究严格遵循我国伦理学标准,充分告知研究对象及家属本次研究目的,严格保护研究对象及家属的个人身份等隐私,在获得研究对象及家属许可且研究对象及家属自愿签署知情同意书的前提下进行研究。
结 果
一、13 例有生育要求的肢体骨肉瘤长期生存患者生育及接受化疗药物情况
通过电话随访得知 4 例未完成生育,2 例男性分别于当地医院诊断为无精症和少精症,1 例未孕女性化疗结束后长期月经不调 ( 未对该患者配偶进行生殖功能评估 ),1 例男性患者妻子怀孕 42 周 ( 截至本次研究时间 );初诊年龄 10~19 岁,平均年龄16 岁;生存时间 6~17 年,平均生存时间 9.5 年;发病部位:股骨远端 3 例,胫骨近端 1 例;Enneking分期:均为 IIB 型;化疗方案:MMIA 化疗方案1 例,DIA 化疗方案 2 例,MIDA 化疗方案 1 例;接受化疗累计药物 ( 表1 )[21]:甲氨蝶呤 ( M ):0~80 g / m2,顺铂 ( D ):0~1320 mg / m2,异环磷酰胺( I ):10~110 g / m2,阿霉素 ( A ):90~990 mg /m2;手术方式:瘤段骨切除灭活再植术 1 例,瘤段骨切除特制肿瘤型人工假体置换术 3 例。
9 例完成生育,男 1 例,女 8 例;初诊年龄14~24 岁,平均年龄 19.1 岁;生存时间 7~21 年,平均生存时间 13.7 年;发病部位:股骨远端 5 例,胫骨近端 4 例;Enneking 分期:均为 IIB 型;化疗方案:MMIA 化疗方案 7 例,DIA 化疗方案 2 例;接受化疗累计药物 ( 表1 ):甲氨蝶呤 ( M ):0~180 g /m2,顺铂 ( D ):0~1440 mg / m2,异环磷酰胺 ( I ):10~120 g / m2,阿霉素 ( A ):90~1080 mg / m2;手术方式:瘤段骨切除灭活再植术 5 例,瘤段骨切除特制肿瘤型人工假体置换术 4 例。

表1 13 例有生育要求患者接受化疗情况Tab.1 Chemotherapy for 11 patients with fertility wish
9 例共生育 12 名子女,男女比例 7∶5;1 例男性患者生育 2 名子女,8 例女性患者成功怀孕 9次,共生育 10 名子女 ( 1 例双胞胎 );年龄:10 个月~13 岁 4 个月,平均年龄 6 岁 1 个月;生产方式:顺产 6 例,剖腹产 6 例;妊娠情况:无孕后流产,足月妊娠 11 例,早产儿 1 例,12 例子女均无出生缺陷,APGAR 评分均正常。
二、肢体骨肉瘤长期生存患者子女生长发育结果
9 例完成生育的长期生存肢体骨肉瘤患者及配偶均属于中国汉族,排除不同种族间的生长发育差异。12 名肢体骨肉瘤长期生存患者子女生长发育情况见表2,年龄分布为 0~5 岁 5 例,6~19 岁7 例,所有儿童生长发育正常,无生长发育迟缓、低体重、超重。
三、肢体骨肉瘤长期生存患者子女智力发育结果
12 例子女智力发育结果 ( 表2 ),年龄<3 岁共 5 名,应用盖塞尔智力量表评分分别为 89 分、96 分、94 分、95 分、94 分,测评为智力正常;年龄>3岁<6 岁共 1 名,应用韦氏幼儿智力表评分 108 分,测评为智力正常;年龄>6 岁<16 岁共6 名,应用韦氏儿童智力量表评分分别为:96 分、109 分、108 分、101 分、110 分、105 分,测评为智力正常。
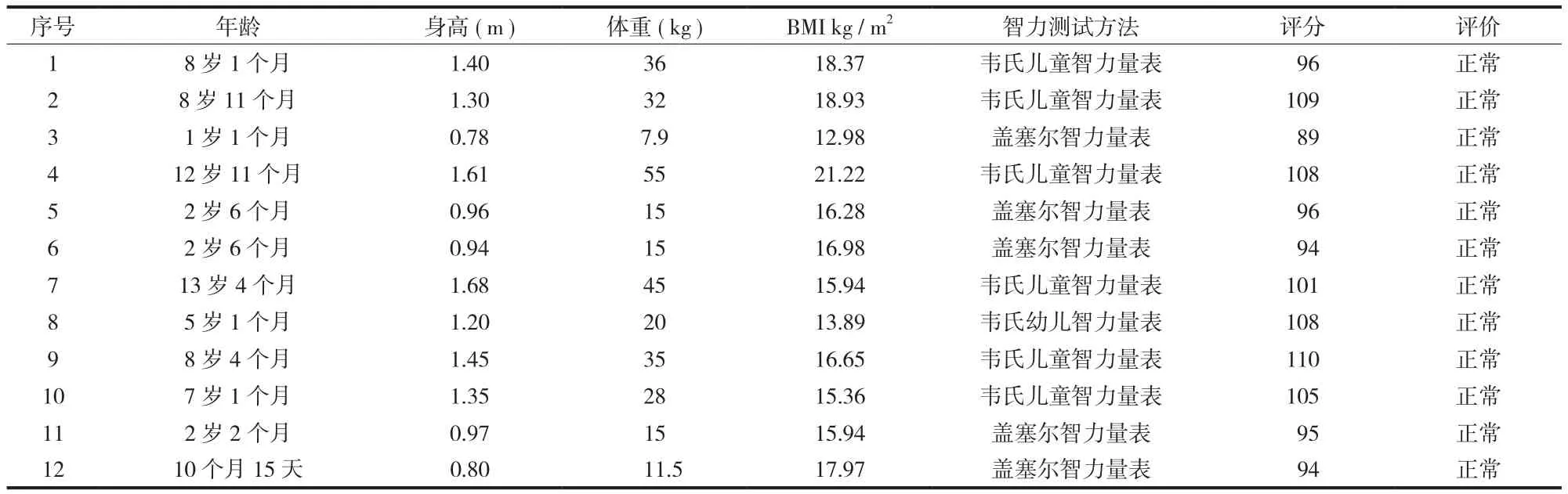
表2 12 名子女生长发育及智力发育情况Tab.2 Growth and Intellectual Development of 11 Children
四、染色体检测结果
6 例子女血液样本均检测成功,检测结果见表3,对应染色体核型分析 ( 图1 )。6 例子女的染色体异常率 100%,结果重复率达 133%,缺失率达33.3%,6 例染色体重复或缺失片段区域内相关基因在检索数据库 ( UCSC、DGV、OMIM、HGMD、DECIPHER、PubMed 和 ISCA 等 ) 中均未发现骨肉瘤及其它疾病的致病基因出现,未发现染色体非整倍体变异及已知的、致病性明确的 100Kb 以上的微缺失 / 微重复变异。
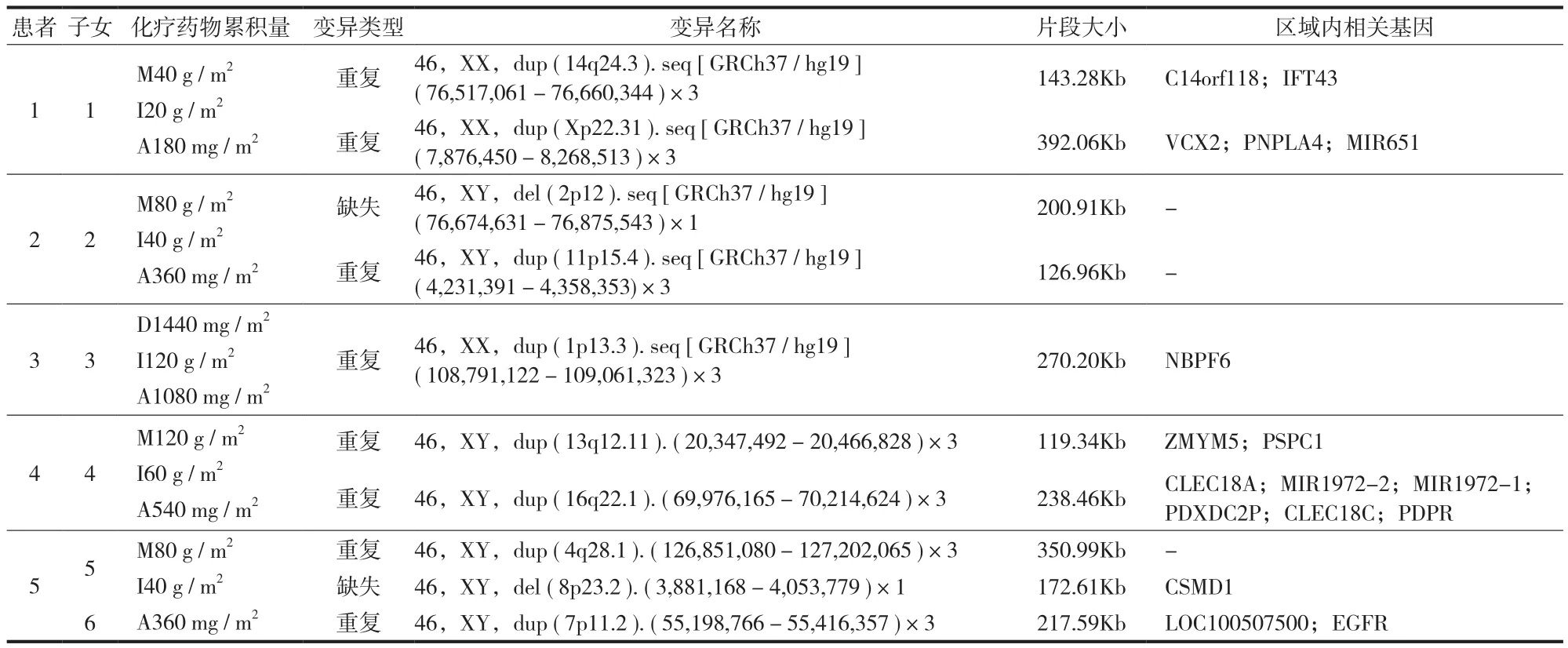
表3 染色体检测结果Tab.3 Results of chromosome detection

图1 6 例染色体核型分析Fig.1 Karyotype analysis of 6 cases
讨 论
一、骨肉瘤长期生存患者子女健康状况评价
儿童期和青春期是人体快速生长发育时期,遗传因素是影响子女生长发育和智力发育的重要因素。骨肉瘤是儿童期和青春期最常见的原发性恶性骨肿瘤[22]。由于化疗药物及方案的不断改进,儿童期和青春期肢体骨肉瘤患者得以长期生存,部分长期生存患者已生育子女[8-11],但对肢体骨肉瘤患者子女健康状况的随访尚无报道。本研究从身体发育和智力发育两方面评价 12 名子女 ( 幼儿期 5 例,学龄前期 1 例,学龄期 5 例,青春期 1 例 ) 的健康状况。11 名子女生长发育均正常,未发现发育迟缓或低体重事件;12 名子女智力发育评价均在正常水平,未发现智力发育障碍事件。接受规范化疗的骨肉瘤长期生存患者子女儿童期和青春期未出现骨肉瘤病变或其它病变,健康状况评价为正常。
二、染色体变异探讨
目前骨肉瘤常用化疗药物 ( 甲氨蝶呤、顺铂、异环磷酰胺、阿霉素 ) 具有细胞毒性和遗传毒性[23-26],会对接受化疗药物治疗的骨肉瘤患者 DNA 造成损伤,可能会诱导其它疾病的发生[27-28]。目前尚不明确肢体骨肉瘤患者接受化疗药物造成的 DNA 损伤是否会遗传子女。25 岁以下患有骨肉瘤的患者中,约有20% 患者存在生殖系统基因改变[29]。骨肉瘤患者染色体具有高度非整倍性、不平衡性染色体重排的聚集、多区域的扩增与缺失在内的基因组不稳定性[30],考虑长期生存的肢体骨肉瘤患者生育子女是否会遗传骨肉瘤患者染色体不稳定的特性。6 例染色体检测结果都存在异常,重复率达 133%,缺失率达 33.3%,但在染色体重复或缺失区域内未发现骨肉瘤或其它疾病致病基因出现,这种现象称为染色体多态性[31]。传统观点认为这种现象属于正常变异,不引起表型异常,因而不具有临床病理意义,但是近年来有报道不断有证据表明染色体多态性改变与多种疾病的发生有关[32-37]。2007 年,王小荣等[38]对1414 例咨询者血液样本经 G、C 显带行核型分析,发现多态性变异 180 例,占 12.73%,既往文献未报道正常人群运用本研究方法来进行畸变率统计。有研究认为,细胞在冷、热、缺氧等应激状态下,会发生致病性改变[39]。6 例子女均出现了染色体多态性改变,虽未有致病性基因出现,但可能在某种因素刺激下会表现出致病性,随着研究的进一步深入可能会有更多的发现。长期生存的肢体骨肉瘤患者生育子女染色体虽未发现致病基因,但尚不能排除长期生存肢体骨肉瘤患者子女染色体对肿瘤的易感性增加。笔者推测长期生存肢体骨肉瘤患者子女染色体多态性改变与患者治疗期间接受化疗药物治疗密切相关,笔者尝试证明某种化疗药物会造成相应染色体片段的缺失或重复,结果发现每位患者子女染色体多态性改变都是独立的,不具备共性,因而笔者进一步推测高剂量的化疗药物只会造成个体染色体片段重复或缺失几率增加,而不会造成特定某个染色体片段的缺失或者重复。
三、化疗药物对肢体骨肉瘤长期生存患者生育能力及其生育子女健康影响探讨
目前报道骨肉瘤患者生育子女文献较少,既往文献[8-11]累计报道 38 例肢体骨肉瘤长期生存患者共生育 54 名子女且出生子女无缺陷,其中 Longhi等[8]于 2000 年报道了 92 例女性骨肉瘤,22 例有生育要求的女性,20 例怀孕,2 例未能怀孕,14 例完成生育;25 例在化疗结束后出现永久性不规则月经周期,2 人永久性闭经,研究结论称化疗对女性骨肉患者生育影响不大。2003 年该作者报道的 96 例男性骨肉瘤患者中 8 例患者共生育 12 名子女,26例未完成生育的男性患者接受精子质量检测,19 例患者 ( 中位随访时间为 6 年 ) 诊断为无精症,1 例患者诊断为少精症,文献提到顺铂、阿霉素、甲氨蝶呤、异环磷酰胺四种化疗药物都会导致男性患者出现无精症,其中异环磷酰胺化疗药物对男性不育风险影响最大[9]。2004 年 Harish 等[11]报道 15 例有生育要求的患者均完成生育,共生育 22 名子女,研究结论称化疗不会影响肢体骨肉瘤患者生育。本研究报道了 13 例有生育要求,4 例未完成生育,9 例完成生育,共生育 12 名子女,出生子女均无缺陷。既往文献未具体提及每例骨肉瘤患者接受化疗药物累积量,本研究 2 例未完成生育的男性患者均接受异环磷酰胺化疗药物累积量均超过 100 g / m2,顺铂化疗药物累计量均超过 1000 mg / m2,阿霉素药物累积量均超过 900 mg / m2,生存时间均超过 7 年;1 例未孕女性患者仅接受了 2 次疗程的 MMIA 化疗,12 名子女在儿童期和青春期身体健康未见异常。化疗药物对骨肉瘤长期生存患者造成的生殖功能损伤会逐步恢复,男性化疗后出现无精症一般在2~3 年内是可逆的[40],女性化疗时出现闭经一般在化疗结束后月经活动会再次开始[8],但是接受高剂量化疗药物可能会造成骨肉瘤患者不能生育。从化疗药物对患者性腺损伤和生育影响角度来看,虽然我科与文献报道药物累积量均超出了药物累计安全范围[41-44],但是大部分骨肉瘤患者都保留了生育能力,生育子女健康不受影响,只有少部分患者未能完成生育,这可能与患者自身性腺耐受程度和恢复能力有关。笔者可以推测化疗药物的应用,会对长期生存骨肉瘤患者自身生育能力造成影响,但是不会对子女健康产生影响。
本研究发现规范化治疗长期生存大部分骨肉瘤患者仍可正常生育子女,但少部分患者可能丧失生育能力,个体差异可能是影响患者生育的因素。肢体骨肉瘤长期生存患者的子女身体、智力均表现健康状态,但染色体分析提示存在染色体片段的重复或缺失,发生原因和可能导致的后果不甚明确,笔者需要运用更精确的检测技术去验证。临床工作中应充分告知患者接受化疗后的潜在风险,包括不育风险和生育后代存在染色体多态性改变的警告。
本研究存在不足之处,受多方面条件限制,研究样本少,肢体骨肉瘤长期生存患者子女健康状况未能充分反映,笔者在今后工作中,加强各骨肿瘤协作组之间的协作,进一步完善对骨肉瘤患者术后的随访工作,增加病例的积累,以求更客观的反映肢体骨肉瘤长期生存患者子女健康状况。

