改质长焰煤与松木共热解协同效应及动力学分析*
赵璐涵 何选明 李 昊 范贵平
0 引 言
能源在人类文明进步和社会经济发展中有着举足轻重的地位,其中,煤炭资源是世界上储量最多、分布最广的常规能源[1]。我国是世界上少有的以煤炭作为主要能源的国家之一,煤炭产量已经超过了世界总产量的1/3[2]。随着优质煤炭资源日益短缺,传统煤炭利用方式所带来的环境污染、温室气体排放增多等问题日益严重,寻找高效清洁煤炭利用技术对于构建资源节约型、环境友好型社会有重要意义。
生物质与煤低温共热解是目前倍受关注的一种煤炭综合利用的方式。作为一种对环境友好的可再生资源,生物质能源燃烧产生的COx,SOx,NOx等有害气体较少;同时生物质具有富氢的特点可减少煤热解后自由基再缩聚从而达到热解产物轻质化的效果,且生物质灰中含高碱金属和碱土金属,可大大提高煤热解过程的反应活性。WANG et al[3]发现,与生物质共热解时的平朔煤挥发分析出温度以及析出速率最快时的温度都低于煤样单独热解时相对应的温度。严东等[4]发现在煤与稻壳共热解过程中,活化能随稻壳掺混比例的增加而减小,混合物料共热解过程活化能和指前因子呈现补偿效应。ZHANG et al[5]通过气相色谱仪分析褐煤与豆秆共热解产生的热解气时,发现共热解时气相产物的组成并不是单独热解时气相产物组成的简单叠加。刘玥[6]利用Miura积分法,通过失重率α对活化能E求导,计算得到活化能分布曲线,发现活化能分布区间会随着生物质掺混比的增大而左移。TARO et al[7]发现,将泰国褐煤和玉米芯在固定床反应器中共热解时,两者之间存在协同效应。目前对生物质与煤共热解反应动力学研究多采用Coats-Redfern模型法求解动力学参数[8],本研究利用热重分析仪考察改质长焰煤和松木混燃时的反应特性,并通过结合Coats-Redfern和Satava-Sestak两种模型法对此反应进行动力学分析,且利用等转化率Ozawa法[9]检验合理性,以期更深入地了解其共热解特性。
1 实验部分
1.1 实验原料
本实验所选用的原料为改质新疆淖毛湖长焰煤(CY)和江苏扬州木材市场的松木木屑(SM)。此改质长焰煤为新疆淖毛湖长焰煤经内热式气体导热干馏技术在150 ℃~350 ℃条件下干燥提质所得。改质长焰煤参照GB 474-2008自然干燥后经磨煤机破碎,过80目标准筛后封存待用。松木经粉碎机破碎后过80目标准筛,筛下物经自然干燥后封存待用。改质长焰煤与松木的工业分析与元素分析如表1所示。
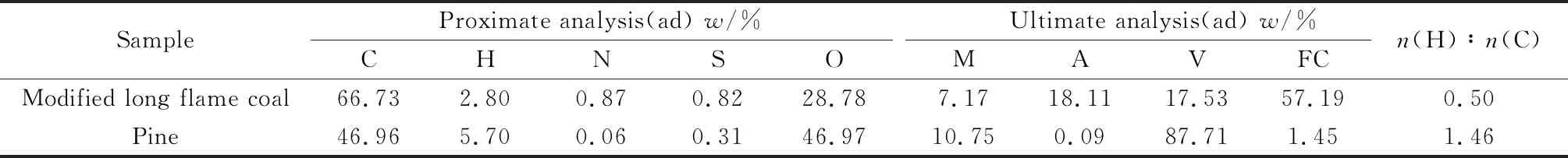
表1 改质长焰煤和松木的工业分析及元素分析Table 1 Proximate and ultimate analysis of modified long flame coal and pine
1.2 实验装置
TG与DTG分析采用德国NETZSCH公司所生产的STA449F3型热重分析仪。热解装置采用武汉科技大学自制铝甑热解炉,其装置如图1所示。
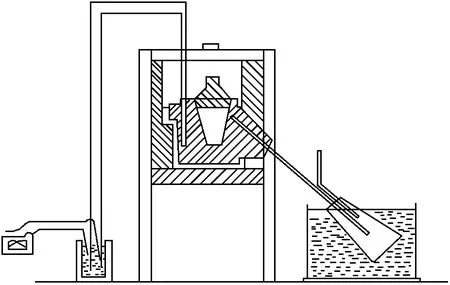
图1 铝甑热解炉试验装置Fig.1 Aluminum crucible pyrolysis furnace device 1—Aluminum crucible lid;2—Aluminum crucible body;3—Ducting tube;4—Air guiding tube;5—Conical flask;6—Cooling trough; 7—Thermocouple;8—Thermoelectric sleeve;9—Heating device;10—Milliometer pyrometer;11— Cold junction thermostat
1.3 实验方法
将松木与煤样按不同掺混比例(松木掺混比例分别为0%,10%,20%,30%,40%,50%,100%)混合均匀,取20 g置于铝甑热解炉内,在初始温度为20 ℃,终温为400 ℃,升温速率为10 ℃/min,保温时间为30 min条件下进行低温干馏实验。通过对比热解产物产量的实验值与理论值,可确定松木与改质长焰煤共热解时是否存在协同作用。分别对煤样、松木及其混合物(记为CS,混合物中煤样与松木掺混质量比分别为3∶1,1∶1,1∶3,混合物样品分别编号为C3S1,C1S1,C1S3)进行热重分析实验及动力学分析。热重分析实验的条件参照文献[10],每次样品质量为6 mg~7 mg,通入流量为8 mL/min的N2作为实验保护气, 升温速率分别为10 ℃/min,20 ℃/min,30 ℃/min,热解终温为1 000 ℃。
1.4 相关计算公式及参数
1.4.1 计算公式
热解失重率:
(1)
热解转化率:
(2)
式中:w为失重率,%;α为转化率,%;m0为共热解开始时混合原料的质量,mg;mt为共热解反应至t时刻剩余样品的质量,mg;m∞为反应结束后最终剩余样品的质量,mg。
1.4.2 热解参数
松木的热重曲线如图2所示,以此图为例示意各热解特征参数。挥发分开始析出温度Ta、挥发分析出终止温度Tb、最大失重速率温度Tmax所对应的温度等热解特性参数采用切线法[11]求得。
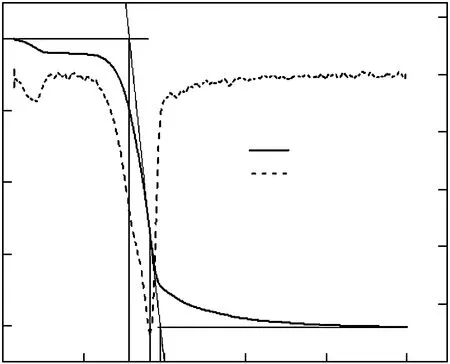
图2 松木单独热解时的TG-DTG曲线Fig.2 TG-DTG curves of pine pyrolysis
2 结果与讨论
2.1 热解产物分布
改质长焰煤与松木共热解产物分布理论值与实际值的对比见图3。产物产率加权平均计算公式为ω=ωCY×xi+ωSM×(1-xi),其中,xi为改质长焰煤的质量分数(%),ωCY,ωSM分别为改质长焰煤和松木的产率(%)。
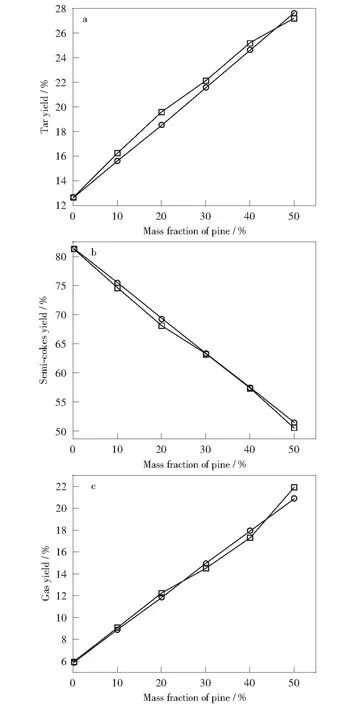
图3 改质长焰煤与松木共热解产物产率的实验值与理论值Fig.3 Experimental value and theoretical value of co-pyrolysis products yield □—Experimental value;○—Theoretical value

2.2 热解特性分析
2.2.1 改质长焰煤单独热解特性
图4所示为不同升温速率条件下改质长烟煤单独热解的TG和DTG曲线。
由图4a可以看出,在不同升温速率下改质长焰煤单独热解的TG曲线拥有相同的趋势且非常接近。在室温到大概200 ℃的温度区间,随着温度的升高,曲线出现第一个肩状峰,失重速率开始加快,此时为改质长焰煤干燥脱气阶段。在120 ℃以前主要是脱除试样水分,120 ℃~200 ℃温度区间内,改质长焰煤表面微孔内吸附的CH4,CO2和N2等气体受热脱除[14]。待温度升至244.82 ℃时开始一次热解,此阶段以解聚和分解反应为主。该阶段TG曲线变化较快,失重明显,在450 ℃左右时失重速率达到峰值,这是因为较高的温度使得改质长焰煤中侧链官能团受热断裂,煤的化学结构和物理结构均受到破坏,煤中的碳和氢反应生成排出大量挥发物(焦油和热解气)。温度继续升高,在600 ℃左右时,又出现了一个较快的失重阶段,此时为二次脱气阶段,这一阶段是半焦缩聚成焦炭的过程,会产生H2和少量CH4,CO,CO2[14]。
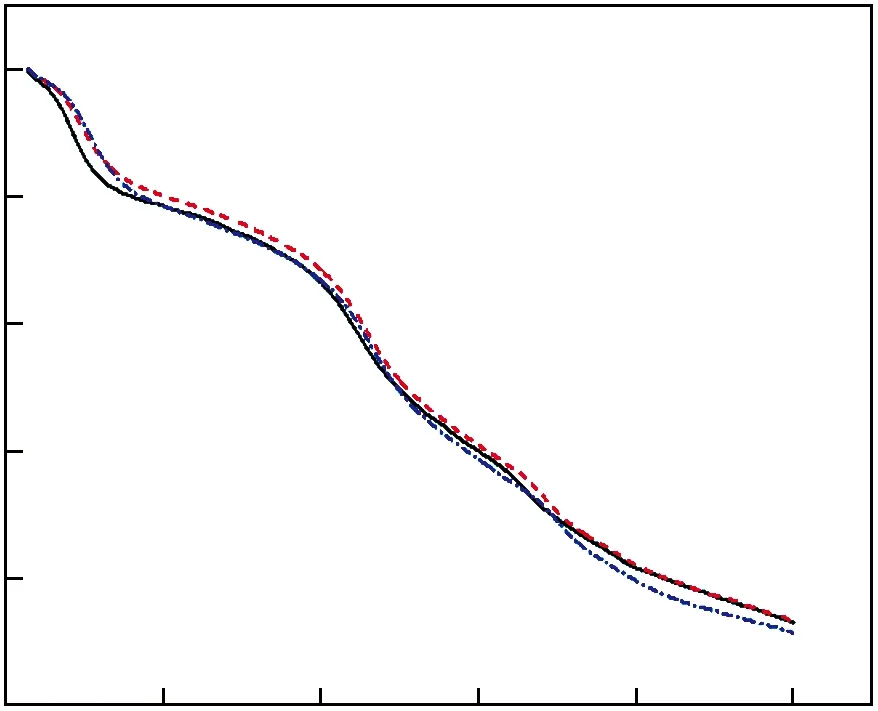
图4 不同升温速率下改质长焰煤单独热解时的 TG-DTG曲线Fig.4 TG-DTG curves of modified long flame coal pyrolysis at different heating rate
图4b中不同升温速率下改质长焰煤单独热解的DTG曲线也具有相同的趋势,不同的是它们的失重速率有着明显的差别,出现的三个峰中,失重率对应的峰值绝对值在升温速率从10 ℃/min到30 ℃/min条件下依次变大,这可能是由于升温速率高能够在短时间内提供更多的热量,使得反应速率更快,试样失重速率更大[15]。同时,这三条曲线随着升温速率变高略向温度升高方向移动,这可能是因为试样在加热时升温速率影响到外层试样与内部试样间的传热速率和温度梯度,升温速率的提高使温度梯度增量变大。升温速率越快,试样内部温度梯度所带来的滞后效应就越明显,表现为在DTG曲线上热解曲线右移。这也导致升温速率的不同将在一定程度上影响到改质长焰煤挥发分开始析出温度Ta、析出终止温度Tb和失重速率最大时的温度Tmax。
2.2.2 松木单独热解特性
图5所示为不同升温速率条件下松木单独热解时的TG-DTG曲线。
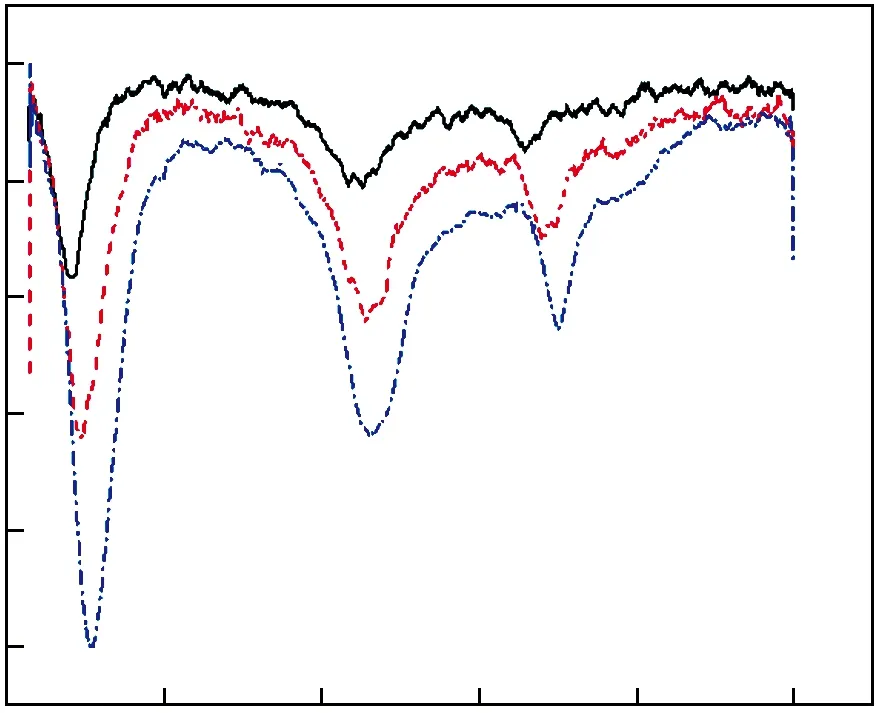
图5 不同升温速率下松木单独热解 时的TG-DTG曲线Fig.5 TG-DTG curves of pine pyrolysis at different heating rate
由图5a可以看出,在脱挥发分阶段,松木单独热解的TG曲线比改质长焰煤的TG曲线失重明显,且挥发分析出温度提前。第一阶段是干燥脱气阶段(室温~120 ℃),这一升温过程中,松木表面结合的水分和气体受热脱除从而导致试样质量略有下降。温度继续升至301.62 ℃时,开始第二阶段即脱挥发分阶段,松木在缺氧条件下开始剧烈分解,失重速率快速上升,出现一个较陡的肩状峰,并在400 ℃左右时完成热解。
由于松木含有不同组分且各组分热解温度不同,导致其DTG曲线出现两个失重峰以及两个侧峰。如图5b所示,第一个失重峰为干燥脱气阶段失重峰,松木在此阶段基本只发生物理结构变化。随着温度继续升高,松木中含有的纤维素、半纤维素和木质素逐步发生化学结构改变,根据生物质热解反应机理,第一个侧峰是半纤维素的失重峰,因为半纤维素结构中多为易断裂脱除的小分子支链结构,在较低的热解温度下便使得半纤维素结构受到破坏,热解释放出小分子气体;最高的峰为纤维素热解失重峰,纤维素结构中含有的羟基及吡喃糖环中的C—O键较半纤维素中的支链结构而言需要更多的热量才可断裂,但其脱除速度较快,在温度范围为350 ℃~380 ℃内分解速度最快[15];第二个侧峰为木质素热解失重峰,木质素热稳定性最高,因为其结构中含有的芳香类化合物键能较高。
与改质长焰煤热解过程相似,松木的DTG曲线同样出现了由于铝甑及试样内部存在温度梯度而引起的滞后现象,但松木较煤样而言滞后现象不太明显,这可能是由于松木有着较高的水分,使得导热效果较好,温度梯度增量较小。对比松木与改质长焰煤升温速率为10 ℃/min时的DTG曲线可以看到,改质长焰煤挥发分析出速率远小于松木,因为选用的煤样已经过低温干燥,所以其挥发分含量较低,远低于松木。
2.2.3 煤与松木共热解特性
改质长焰煤与松木按照不同比例掺混为C3S1,C1S1,C1S3,在升温速率为10 ℃/min下共热解热重实验所得TG-DTG曲线如图6所示,改质长焰煤、松木及其混合物(CS)具体热解特性参数见表2,其中,Ta为开始热解温度,Tb为终止热解温度,Tmax为出现最大失重速率时的温度,(dm)max为最大失重率,(dm/dt)max为最大失重速率。
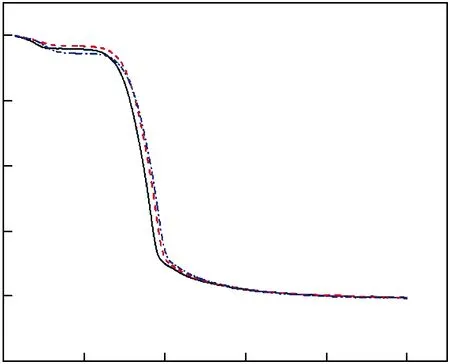
图6 改质长焰煤-松木共热解时的TG-DTG曲线Fig.6 TG-DTG curves of co-pyrolysis of modified long flame coal and pine
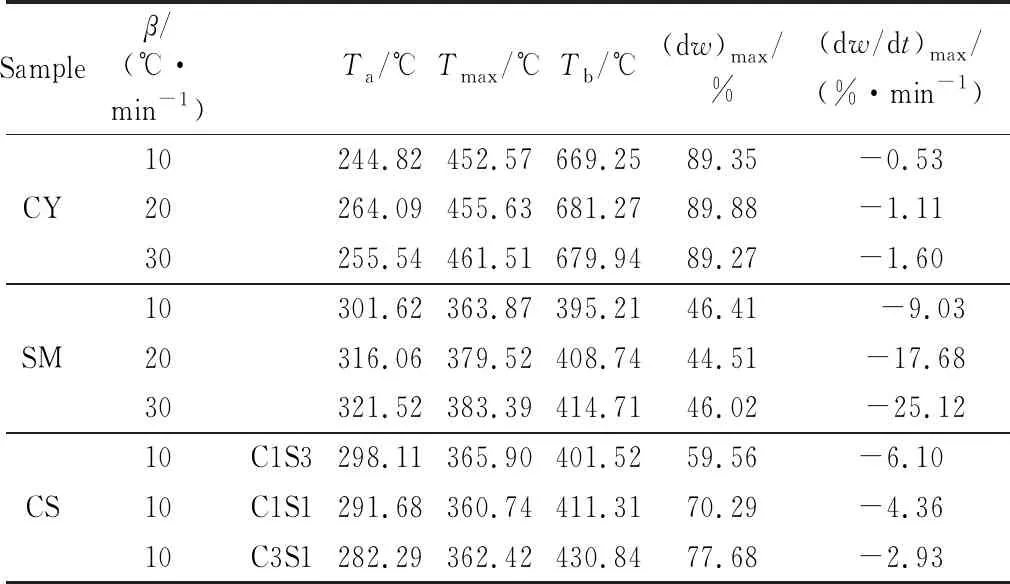
Sampleβ/(℃·min-1)Ta/℃Tmax/℃Tb/℃(dw)max/%(dw/dt)max/(%·min-1)CY10244.82452.57669.2589.35-0.5320264.09455.63681.2789.88-1.1130255.54461.51679.9489.27-1.60SM10301.62363.87395.2146.41-9.0320316.06379.52408.7444.51-17.6830321.52383.39414.7146.02-25.12CS10C1S3298.11365.90401.5259.56-6.1010C1S1291.68360.74411.3170.29-4.3610C3S1282.29362.42430.8477.68-2.93
TG曲线上可以看出热解温度达到200 ℃后失重速率受混合物掺混比的影响,松木含量越高,失重速率越大,因为松木中的挥发分含量远高于改质长焰煤,挥发分更易析出;热解结束后最终生成的产物量也与掺混比有关,随着松木含量的增多,产物量降低,因为较改质长焰煤而言,松木拥有非常低的灰分,而且松木热解后得到的生物质焦颗粒具有多孔结构,可以与氧气接触充分,有利于剩余还未反应的试样和氧气发生异相反应,使得反应更彻底[16]。
在DTG曲线中一次热解失重峰出现的温度与松木单独热解时挥发分析出温度接近(360 ℃左右),此峰右侧出现一侧峰,为改质长焰煤一次热解失重峰,对比改质长焰煤单独热解时的DTG曲线可以发现,松木的加入将改质长焰煤一次热解温度提前了30 ℃左右,原因可能是改质长焰煤中的高n(H)∶n(C)和碱金属含量对改质长焰煤的热解起到了催化作用。同时,改质长焰煤一次热解失重峰值绝对值却远小于松木一次热解失重峰值绝对值,这可能是因为改质长焰煤与松木掺混后附在松木颗粒表面的煤样颗粒导致松木的传热性能大大降低,使得此阶段混合物的失重速率低于松木单独热解时的失重速率。由此表明,松木的添加使得改质长焰煤的热解过程向低温区移动,降低了煤样的热解温度,这也和改质长焰煤与松木共热解时产物分布分析结果相吻合。
质量为1∶1的改质长焰煤与松木掺混后,在10 ℃/min的升温速率下进行热重实验的DTG曲线实验值与理论值的对比见图7。由图7可以看到,在300 ℃~430 ℃温度段改质长焰煤与松木存在协同效应。DTG曲线中380 ℃左右失重峰峰值绝对值的实验值大于理论值,造成这种情况的原因可能是:试样中混合在内改质长焰煤降低了松木的传热效果,使得松木的失重速率降低,实际剩余混合试样的质量略高于松木单独热解时此阶段的试样剩余质量;而在温度约为410 ℃时,DTG曲线显示出改质长焰煤与松木混合样失重速率绝对值的实验值比理论值大,此处出峰对应改质长焰煤单独热解时的一次热解失重峰,这说明松木与改质长焰煤共热解时存在协同作用,添加松木可以促进改质长焰煤的一次热解,使此阶段混合试样失重速率加快。此结果与图6的分析结果一致。
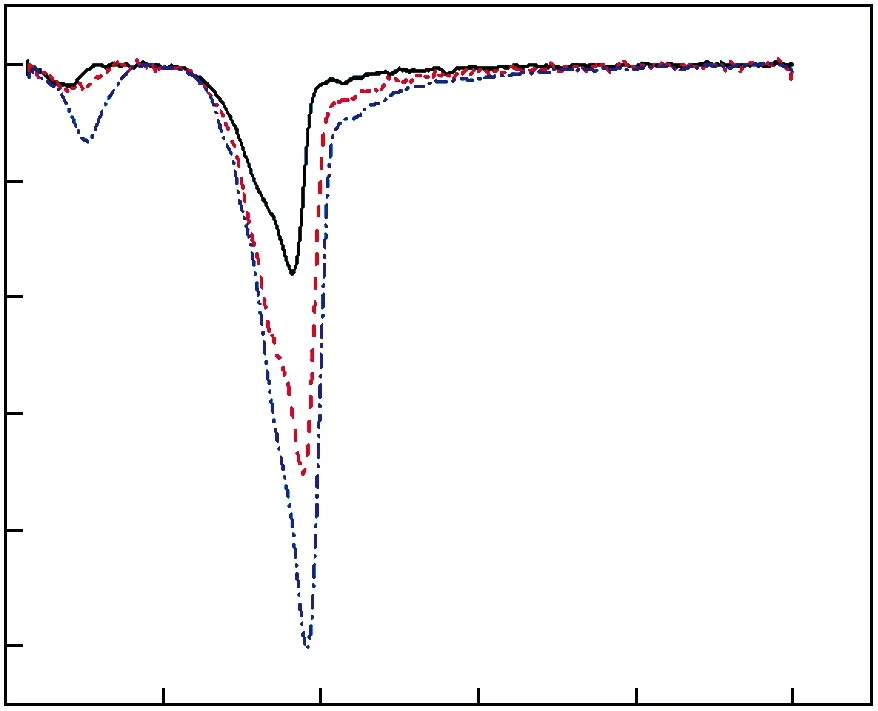
图7 改质长焰煤-松木共热解时DTG曲线的 实验值与理论值Fig.7 Experimental and theoretical value of DTG curve of modified long flame coal and pine co-pyrolysis
2.3 热解反应动力学分析
2.3.1 Coats-Redfern模型分析法
改质长焰煤和松木复杂的成分使其热解反应包括了许多连锁反应和平行反应,通过建立动力学数学模型描述煤样与松木的热解行为可以更好地反映其混合热解过程。
Coats-Redfern模型是将固体反应看作单一反应,根据Arrehenius 方程和质量守恒定律、Coats-Redfern方程及微商法,改质长焰煤与松木共热解反应速率方程可用式(3)表示[17]:
(3)
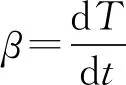
(4)
利用Coats-Redfern积分法对式(4)分离变量积分整理后可得到:
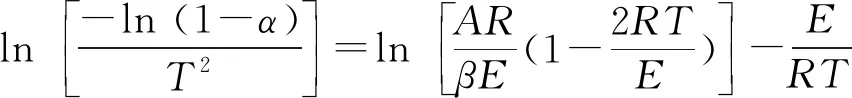
(5)
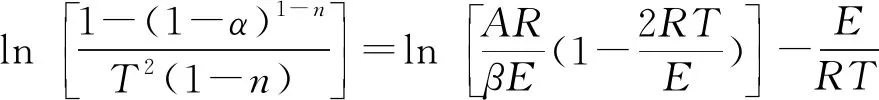
(6)
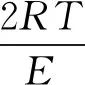
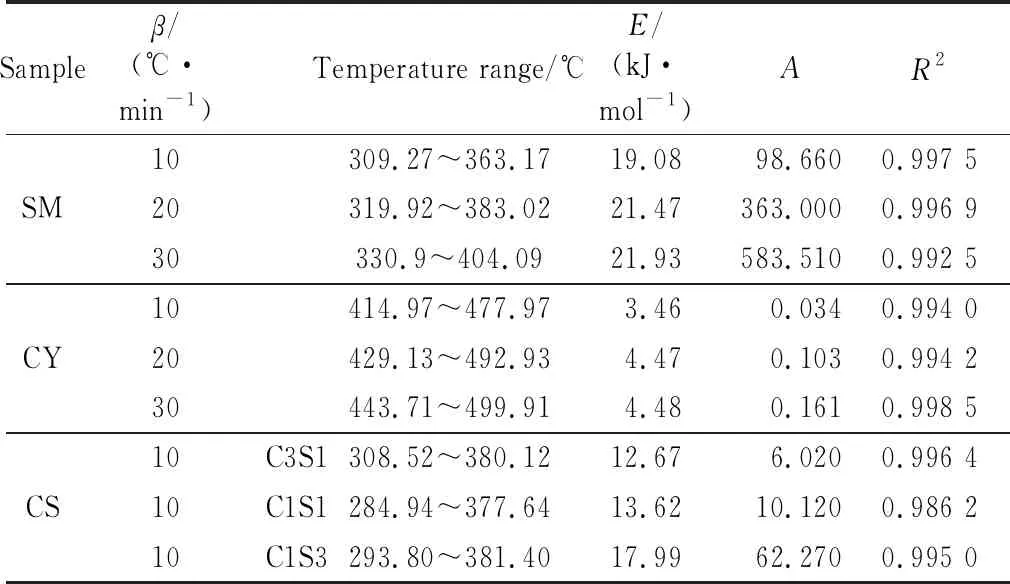
表3 Coats-Redfern模型法计算得到的试样 热解反应动力学参数Table 3 Kinetic parameters of sample pyrolysis reaction by Coats-Redfern model
由表3可以看出,改质长焰煤的活化能高于松木,活化能大意味着较低的反应活性;而松木的指前因子远高于改质长焰煤,指前因子越大,反应速率越快。这说明单独热解时改质长焰煤较松木而言更易析出挥发分,但松木的挥发分析出速率要远大于改质长焰煤,这与二者单独热解时TG曲线相一致。在10 ℃/min升温速率下,煤与生物质共热解时的指前因子比改质长焰煤单独热解时对应值大5.986 min-1,表明掺混松木可以大大提高改质长焰煤的热解速率。两者共热解时,随着松木掺混比的提高,活化能与指前因子都逐渐增大,活化能的增大会降低反应活性,而指前因子增大说明反应速率增大,即两者共热解时其反应活化能和指前因子之间存在补偿效应[18]。另外,升温速率增大时,煤样与松木都呈现出指前因子变大的趋势,说明挥发分的析出速率与升温速率正相关,这与图4a和图5a分析结果一致。
2.3.2 Satava-Sestak模型分析法
Satava-Sestak模型适用于求解热解曲线上任何一点处的动力学参数,以此模型与Coats-Redfern模型对比以选取最优拟合模型。
对式(4)左边等号两端积分后变形得到:
(7)
将上式改写后即为Satava-Sestak模型方程式[19]:
(8)
带入一级反应机理方程后得:
(9)
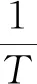
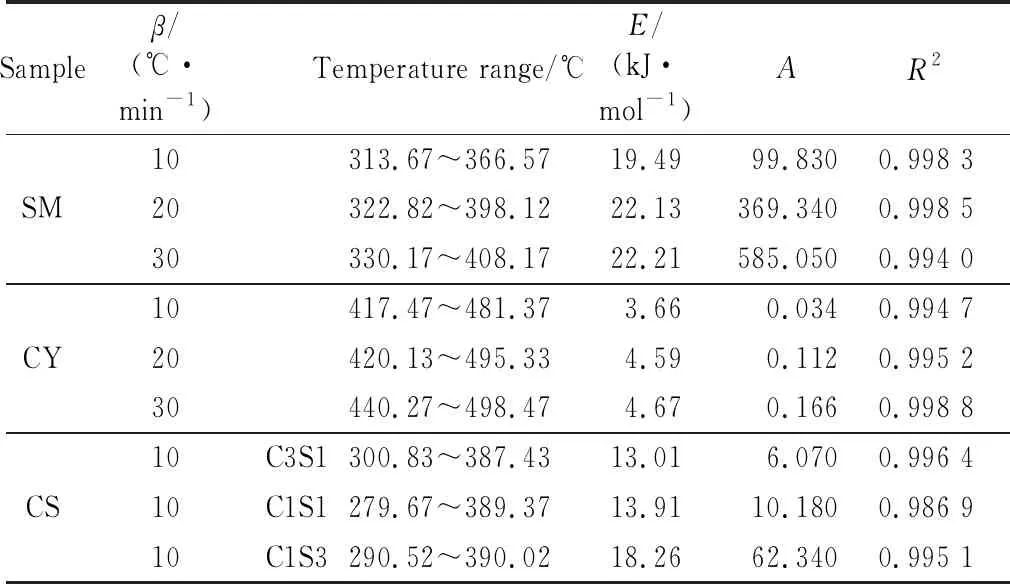
表4 Satava-Sestak模型法计算得到的试样 热解反应动力学参数Table 4 Kinetic parameters of sample pyrolysis reaction by Satava-Sestak model
Coats-Redfern模型法和Satava-Sestak模型法都为模型拟合分析法。这两种不同的模型分析法所得活化能与指前因子非常接近,分析结果相同。对比Coats-Redfern模型法,Satava-Sestak模型法所得参数略高,且拟合度更好。
2.3.3 Ozawa法
Ozawa法是一种非模型拟合分析法,此法将转化率α看作一个恒定的值,升温速率β仅与反应温度T相关,不涉及反应机理,避免了在选择反应机理函数时所带来的误差[9]。因此可利用此方法检验Coats-Redfern模型法和Satava-Sestak模型法所求的活化能的合理性。
对式(4)左边等号两端积分并整理得到方程
(7)

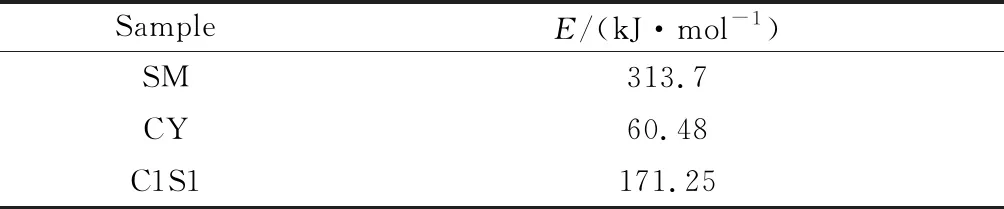
表5 Ozawa法计算得到的试样热解活化能Table 5 Activation energy of sample pyrolysis by Ozawa method
Ozawa模型所得活化能数值较高,但样品活化能大小规律与Coats-Redfern模型法和Satava-Sestak模型法所求的活化能一致,即E(SM)>E(CY),混合样C1S1的活化能介于二者之间,这证明了这两种模型法所得动力学参数是合理的。
3 结 论
1) 改质长焰煤与松木共热解时存在协同作用,随着松木掺混比的增大,焦油和热解气产率不断增大,半焦产率不断减小。松木掺混比为20%时,焦油产率实验值与理论值达到最大正偏差。
2) 热重分析表明,改质长焰煤与松木混合热解时在300 ℃~430 ℃区间存在协同效应。松木的掺入使得改质长焰煤热解过程向低温区移动,并使失重热解速率加快。
3) 通过对比Coats-Redfern模型和Satava-Sestak模型两种分析方法,得到的结果均表示改质长焰煤与松木共热解过程符合动力学一级反应模型,两者共热解时活化能与指前因子之间存在补偿效应,加入松木使反应活性降低,反应速率增大,协同作用主要表现在使共热解反应速率增大。同时,Satava-Sestak模型的拟合度更优。

