诺米林平衡溶解度和表观油水分配系数的测定*
郁林娜, 程盛勇, 付洋, 鲁文琴, 黄静, 罗喜荣*, 杨军
(1.贵州医科大学 药学院,贵州 贵阳 550025; 2.贵州医科大学附院 药剂科,贵州 贵阳 550004; 3.中国科学院 地球化学研究所,贵州 贵阳 550081)
诺米林(nomilin)是从桔核中提取分离得到的四环三萜类化合物,系桔核中含量仅次于柠檬苦素(limonin)的主要柠檬苦素类似物甙元[1]。诺米林具有抗肿瘤、抗病毒、抗血管生成、抗增殖活性、抗肥胖、调节糖代谢、抑制破骨细胞分化及免疫调节等作用,诺米林对正常细胞无毒副作用,但其口服吸收差、生物利用度低[2-10]。课题组前期研究发现诺米林水溶性差,其临床应用受限。药物的油水分配系数和溶解度与药物的吸收密切相关,对制剂设计具有重要的指导意义。目前国内外尚未见诺米林平衡溶解度和油水分配系数的研究报道,本文采用摇瓶法[11]和UPLC法[12]测定诺米林在不同介质中的平衡溶解度和表观油水分配系数,为改善其生物利用度的新剂型的设计提供依据。
1 材料与方法
1.1 仪器与试药
Agilent 1290 DAD超高效液相色谱仪(美国Agilent公司)、UC-10H加热超声波清洗器(上海泰坦科技股份有限公司)、pHS-3C酸度计(上海理达仪器厂)、SHZ-C水浴恒温振荡器(上海浦东物理光学仪器厂)、TGL-16G高速台式离心机(上海安亭科学仪器厂)、BSA224S电子天平(赛多利斯科学仪器有限公司)、诺米林(自制,纯度大于98%)、乙腈和甲醇(德国默克公司,色谱纯)、聚乙二醇400及吐温-80为化学纯,其余试剂均为分析纯。
1.2 方法
1.2.1溶液的配制 (1)对照品溶液的配制:精密称取诺米林11 mg置10 mL量瓶,加甲醇超声溶解、定容至刻度制得1.1 g/L储备液。精密量取储备液适量,采用逐级稀释法配制4.30、8.59、17.19、34.38、68.75、137.5及275 mg/L系列对照品溶液。(2)缓冲液的配制:取磷酸二氢钾0.68 g加水适量,以1 mol/L盐酸或氢氧化钠调制pH为1.2、2.0、3.0、4.0、5.0、6.0、6.8、7.4及8.0的系列磷酸盐缓冲液。(3)表面活性剂溶液的配制:分别取吐温80、聚乙二醇400(PEG400)、十二烷基硫酸钠(SDS)适量,配制成浓度为5、10、20、40、60及80 g/L的系列水溶液。
1.2.2色谱条件 色谱柱为Ultimate®AQ-C18 (2.1 mm×100 mm,1.8 μm),流动相为乙腈-水(45 ∶55),流速为0.3 mL/min,检测波长为210 nm,柱温为30 ℃,进样量为0.8 μL。在上述色谱条件下,诺米林的保留时间为5.2 min,色谱峰峰形及分离度良好,无杂质峰干扰,见图1。

图1 诺米林的UPLCFig.1 UPLC chromatogram of nomilin
1.2.3平衡溶解度的测定 取过量诺米林置西林瓶,分别用移液管移取加入2 mL有机溶剂、水、缓冲液、表面活性剂溶液,37 ℃超声(260 W,40 kHz)至药物过饱和,置于同温度水浴恒温振荡器中120 r/min振荡24 h,以15 000 r/min离心5 min,取上清液,稀释或浓缩至标准曲线浓度范围内,0.22 μm微孔滤膜过滤,按上述色谱条件进样检测,根据标准曲线计算诺米林在各介质中的平衡溶解度。
1.2.4表观油水分配系数的测定 取诺米林适量溶于水饱和的正辛醇中,使成饱和态,以15 000 r/min离心5 min。精密吸取上清液0.5 mL于10 mL离心管中,分别用移液管移取加入正辛醇饱和的水、缓冲液各5 mL,置于37 ℃恒温振荡器中120 r/min振荡24 h,以15 000 r/min离心5 min,取上层正辛醇相、下层水相,稀释至标准曲线浓度范围内,于0.22 μm微孔滤膜过滤,按上述色谱条件进样,根据标准曲线计算诺米林的正辛醇相即油相浓度C0和水相浓度CW,按lgP=C0/CW计算油水分配系数。
2 结果
2.1 方法学考察
2.1.1线性关系考察 分别取对照品溶液适量,于0.22 μm微孔滤膜过滤,按色谱条件进样检测,记录峰面积;以诺米林质量浓度X(mg/L)为横坐标对峰面积Y进行线性回归,得回归方程:Y=1.966 7X-2.264 9,R2=0.999 5,结果表明诺米林在4.30~275 mg/L范围内与峰面积呈良好的线性关系。
2.1.2精密度试验 分别取高、中及低浓度(275、34.38及4.30 mg/L)标准液,于0.22 μm微孔滤膜过滤,按色谱条件1 d内连续进样检测5次,记录峰面积,计算RSD;连续进样检测5 d, 1次/d,记录峰面积,计算RSD。结果其日内RSD分别为0.27%、0.69%及2.34%,日间RSD分别为0.61%、0.61%及2.23%,表明方法的精密度良好。
2.1.3重复性试验 分别配制高、中及低浓度(275、34.38及4.30 mg/L)标准液各5份,于0.22 μm微孔滤膜过滤,按色谱条件进样检测,记录峰面积,计算RSD。结果其重复性RSD分别为0.78%、1.38 %及1.82 %,表明方法的重复性良好。
2.1.4准确度试验 分别取高、中及低浓度(275、34.38及4.30 mg/L)标准液,于0.22 μm微孔滤膜过滤,按色谱条件进样检测,记录峰面积,根据标准曲线计算对应的浓度,按准确度为测定浓度值除以真实浓度值计算高、中及低浓度的准确度。结果其准确度分别为104%、96.24%及103.24%,表明方法的准确度良好。
2.2 平衡溶解度
按“1.2.3”项下方法测定诺米林的平衡溶解度,结果表明诺米林不溶于石油醚、正己烷、水及缓冲液,在二氯甲烷中的溶解度最大,SDS对其增溶作用最明显,见表1、图2。

表1 37 ℃条件下诺米林在不同介质中的平衡溶解度Tab.1 Equilibrium solubility of nomilin in different media at 37 ℃

图2 37 ℃条件下诺米林在不同介质中的平衡溶解度Fig.2 Equilibrium solubility of nomilin in different media at 37 ℃
2.3 表观油水分配系数
按“1.2.4”项下方法测定诺米林的表观油水分配系数,结果诺米林在正辛醇/水中的表观油水分配系数为131.05(lgP=2.12),在正辛醇/磷酸盐缓冲液中表观油水分配系数呈M形,在pH 3.0缓冲液中表观油水分配系数最大为783.07(lgP=2.89),见图3。
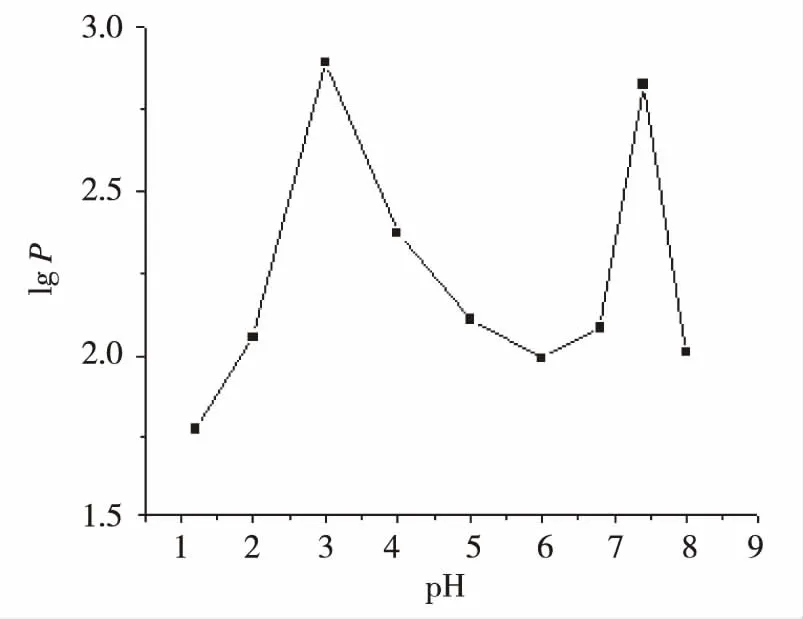
图3 诺米林在37 ℃条件下于正辛醇/磷酸缓冲液中的表观油水分配系数Fig.3 Apparent oil-water partition coefficient of nomilin in octanol/buffer at 37 ℃
3 讨论
目前,有关诺米林的报道主要集中在提取分离、药理作用的研究,鲜见其理化性质的研究报道。本文建立了诺米林含量的UPLC测定方法,测定了诺米林在不同介质中的平衡溶解度和表观油水分配系数。结果表明诺米林不溶于石油醚、正己烷、水及缓冲液,在二氯甲烷、丙酮、乙酸乙酯中溶解度较大,为中等极性化合物,属难溶性药物;诺米林在正辛醇-水/缓冲液中的lgP值为1.77~2.89,ACD/ChemSketch 12.0软件预测值为2.22±0.78,实测值与理论预测结果相近,提示其在整个胃肠道中均有较好的吸收,适于制成口服制剂。
诺米林水溶性差,其lgP提示膜渗透性好,属于生物药剂学分类系统的Ⅱ类药物。疏水性强不是限制诺米林口服吸收的主要原因(lgP>5的药物不易吸收),导致其生物利用度低的原因可能是药物溶解度小导致药物溶出速度太慢。因此在诺米林制剂设计时,可考虑采用增溶辅料或固体分散体、纳米粒、自微乳等制剂手段提高其溶解度和溶出速率,以提高其生物利用度。口服制剂溶出度的测定一般采用水、pH1.2盐酸溶液和pH6.8的磷酸盐缓冲液,诺米林在这3种介质中均达不到漏槽条件。
综上,本研究了3种表面活性剂对诺米林的增溶效果,其中SDS的增溶作用最大,提示诺米林水溶性差,但渗透性较好,适合制成口服制剂,可以将SDS作为诺米林制剂的溶出介质。

