抗栓治疗老年患者行结肠息肉内镜切除的安全性研究
傅亮,吴曦,唐永莲,王薇,罗庆锋,许乐,陈浩
(北京医院,a消化内科,b心内科;国家老年医学中心 北京 100730)
结肠息肉为凸起于结肠黏膜的隆起型病变,多为良性病变,但腺瘤性息肉癌变率高,内镜下切除治疗结肠息肉可降低结肠癌的发生率。老年人群中缺血性心血管疾病发病率及抗栓药物使用率正逐步上升,有资料显示老年人约1/3正服用抗栓药物[1-2]。在临床操作中围术期停用抗栓药物会增加血栓栓塞事件风险[3-4],不停用抗栓药物会增加出血事件的风险[5],这两者之间存在矛盾,如何在矛盾中降低不良事件风险困扰着消化内科及心血管内科医师。本研究针对抗栓治疗老年患者行内镜下结肠息肉切除不良事件、抗栓药物管理方案及相关危险因素进行研究探讨,旨在为临床提供参考。
1 资料与方法
1.1 一般资料 筛选2015年1月至2018年12月于我院行结肠息肉切除的抗栓治疗老年患者共2 299例,纳入标准:行结肠息肉切除的长期行抗栓治疗的患者;排除标准:病历资料不全、严重肝肾功能不全的患者。其中高血压病及冠心病患者1 555例(高血压冠心病组),冠心病支架置入术后患者435例(冠脉支架放置组),人工心脏瓣膜置换术后及心房颤动患者309例(人工心脏瓣膜+心房颤动组)。高血压冠心病组男性1 010例,女性545例;年龄(72.48±9.78)岁。冠脉支架放置组男性269例,女性166例;年龄(74.34±10.12)岁。人工心脏瓣膜+心房颤动组男性185例,女性124例;年龄(71.95±11.74)岁。三组患者年龄、性别、体质量指数(BMI)及息肉切除方式等差异均无统计学意义(P>0.05),具有可比性。
1.2 方法 通过电子病历系统记录术前服用抗栓药物种类及剂量,术后恢复抗栓药物种类及剂量,是否使用低分子肝素桥接抗凝治疗,记录息肉切除方式、息肉数目及大小,记录术前7 d至术后30 d发生的不良事件,出血事件包括大出血及小出血。记录血栓栓塞事件包括:急性冠脉综合征、缺血性脑卒中、肺栓塞及其他系统血栓形成。记录抗栓药物管理方案:术前停用抗栓药物时间:术前未停用抗栓药物、术前停用抗栓药物<3 d、术前停用抗栓药物3~5 d、术前停用抗栓药物>5 d,术后恢复抗栓药物时间:术后未恢复服用抗栓药物、术后<3 d恢复服药、术后3~5 d恢复服药、术后>5 d恢复服药。大出血:血红蛋白下降20 g/L或需要输注1 u红细胞或需要手术、住院治疗的出血事件。小出血:病历资料中记载患者出血,但未达到大出血标准的出血事件。
1.3 统计学处理 数据分析使用SPSS 17.0统计学软件进行。计数资料以百分比表示,组间比较采用χ2检验或精确概率检验。P<0.05为差异有统计学意义。
2 结果
2.1 服用抗栓药物及不良事件情况 高血压冠心病组1 555例中930例患者服用阿司匹林,497例患者服用氯吡格雷,128例患者服用阿司匹林+氯吡格雷;冠脉支架放置组435例中117例患者服用阿司匹林,79例患者服用氯吡格雷,239例患者服用阿司匹林+氯吡格雷;人工心脏瓣膜+心房颤动组309例患者均服用华法林抗凝治疗。围术期停用抗栓药物改用低分子肝素抗凝治疗患者476例。
共发生出血事件68例,其中消化道大出血9例,小出血59例,59例中大便潜血阳性55例,血尿2例,皮下出血1例,结膜出血1例。血栓栓塞85例,急性冠脉综合征60例,60例中不稳定性心绞痛56例、非ST段抬高心肌梗死3例、ST段抬高性心肌梗死1例,缺血性脑卒中20例,肺栓塞1例、其他系统血栓8例。研究中总体出血事件及血栓栓塞发生率分别为2.96%、3.70%,大出血及小出血发生率分别为0.39%、2.57%,缺血性脑卒中发生率为0.87%。
2.2 三组患者围术期不良事件情况对比 结肠息肉切除术前7 d至术后30 d,总体人群中出血事件68例,发生率为2.96%,血栓栓塞发生率为3.70%。冠脉支架放置组出血事件与血栓栓塞发生率高于高血压冠心病组及人工心脏瓣膜+心房颤动组,差异有统计学意义(P<0.05)。见表1。
2.3 总体人群抗栓药物管理与不良事件关系 术前停药情况与不良事件的关系:术前未停药、术前停药<3 d出血事件发生率高于术前停药3~5 d及术前停药>5 d,差异均有统计学意义(P<0.05)。术前停药>5 d出血事件发生率高于术前停药<3 d及术前停药3~5 d,差异均有统计学意义(P<0.05)。术前未停药出血事件与血栓栓塞发生率最低,分别为0.00%、0.00%,其次为术前停药3~5 d分别为2.00%、2.49%。
术后恢复服药情况与不良事件的关系:术后未恢复服药、术后<3 d恢复服药,术后3~5 d恢复服药,术后>5 d恢复服药四组出血事件发生率差异无统计学意义(P>0.05),四组血栓栓塞发生率差异有统计学意义(P<0.05),其中术后<3 d恢复服药栓塞发生率最低,为1.45%,分别与其他三组差异有统计学意义(P<0.05)。见表2。
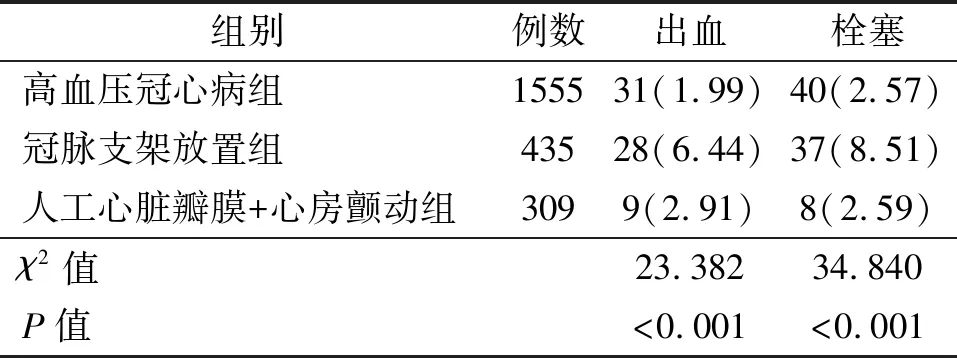
表1 抗栓治疗老年患者共2 299例不良事件情况分组对比[例(%)]

表2 抗栓治疗老年患者共2 299例中抗凝药物管理与不良事件情况[例(%)]
2.4 息肉大小及桥接抗凝治疗与出血事件关系 息肉≥1 cm患者内镜切除后出血事件发生率[11/168(6.55%)]高于息肉<1 cm[57/2131(2.67%)]患者,差异有统计学意义(χ2=6.844,P=0.009),低分子肝素桥接抗凝治疗患者出血事件发生率[14/476(2.67%)]对比未桥接抗凝患者[54/1 823(2.96%)],差异无统计学意义(χ2=0.001,P=0.981)。
3 讨论
目前共有四项关于消化道内镜围术期抗栓药物管理的指南,英国胃肠病学学会2008年发表的指南[6]认为内镜下切除息肉>1 cm出血风险高,而美国胃肠内镜协会2009年发表的指南[7]、欧洲胃肠内镜学会2011年发表的指南[8]及日本胃肠内镜学会2014年发布的指南[9]均认为内镜下息肉切除不论大小出血风险均较高。本研究中抗栓患者行内镜息肉切除围术期出血事件发生率为2.96%,有研究者进行大样本回顾性研究抗栓治疗患者行内镜息肉切除出血率为1.19%[10],本研究出血率较高,考虑与本研究中冠脉支架术后患者较多有关,冠脉支架放置组出血事件发生率显著高于高血压冠心病组及人工心脏瓣膜+心房颤动组(P<0.05),分析原因考虑与冠脉支架放置组高比例服用氯吡格雷有关,有研究者进行回顾性研究发现,患者术前长期服用氯吡格雷会增加息肉切除后的出血风险[11-12]。相对于出血事件发生血栓栓塞事件后果更加严重和致命,栓塞的发生与患者基础疾病密切相关,冠心病、高血压及心房颤动均是血栓栓塞的危险因素,本研究中冠脉支架放置组血栓栓塞发生率高于高血压冠心病组及人工心脏瓣膜+心房颤动组(P<0.05),BSG指南、ESGE指南及ASGE指南均指出冠状动脉药物洗脱支架置入<12个月,金属裸支架置入<6周停用抗血小板药物发生血栓栓塞风险较高,JGES指南认为冠状动脉药物洗脱支架置入<12个月,金属裸支架置入<2个月停用抗血小板药物发生血栓栓塞风险较高,因此支架置入术后也是血栓栓塞的危险因素。综上所述,建议放置冠脉支架的抗栓治疗患者除非特殊情况(如已经发生大出血、发现高级别瘤变)不行结肠镜检查和息肉切除。
针对抗栓治疗患者结肠息肉内镜下切除围术期抗栓药物管理,国内目前没有明确的指南,有研究证实患者停用抗血小板药物相较于未停药患者发生血栓栓塞的概率显著升高[13],而国际上的四项指南在停用抗栓药物的意见上并不一致,ESGE指南和JGES指南对于结肠息肉等出血高危操作推荐停用阿司匹林3~5 d,而ASGE指南则推荐停药5~7 d,四项指南均推荐术前停用5~7 d噻吩并吡啶类药物。关于术后抗栓药物恢复,有研究者报道术后3~5 d恢复服用阿司匹林可减低出血事件的发生,但同时血栓栓塞发生率仍会增加[14]。本研究中术前未停药、术前停药<3 d、术前停药3~5 d及术前停药>5 d四组出血事件及血栓栓塞发生率差异均有统计学意义(P<0.05),术前未停药出血事件与血栓栓塞发生率最低,分别为0.00%、0.00%,其次为术前停药3~5 d分别为2.00%、2.49%,由于术前未停药例数较少,未监测到不良事件的发生,本组倾向于术前停药3~5 d天更为合理。术后恢复服药情况:术后未恢复服药、术后<3 d恢复服药,术后3~5 d恢复服药,术后>5 d恢复服药四组出血事件发生率差异无统计学意义,四组血栓栓塞发生率中术后<3 d恢复服药栓塞发生率最低,因此本组认为结肠息肉切除术前3~5 d停用抗栓药物,术后<3 d恢复抗栓药物能降低出血事件及血栓栓塞发生概率,是合理的抗栓药物管理方案。
研究中观察到息肉≥1 cm患者内镜息肉切除后出血事件发生率高于息肉<1 cm患者,这也印证了有研究者认为息肉大小是术后出血发生的危险因素的结论[15]。同时本研究发现低分子肝素桥接抗凝治疗不会增加患者术后出血事件发生的概率,部分研究者认为在内镜围术期使用桥接治疗能降低栓塞风险同时不会增加出血风险[16],这与本研究结论相符。
综上所述,放置冠脉支架的抗栓治疗患者行结肠息肉切除风险较高,除非特殊情况(如已经发生大出血、发现高级别瘤变)不建议行结肠镜检查和息肉切除,患者结肠息肉≥1 cm会增加出血风险,结肠息肉切除术前3~5 d停用抗栓药物,术后<3 d恢复抗栓药物能降低出血事件及血栓栓塞发生概率,有助于提高老年患者结肠息肉内镜切除安全性,是合理的抗栓药物管理方案。

