枇杷黄酮醇合成酶FLS基因表达与黄酮醇积累的相关性分析
郑雪莲 李嘉仪 杨俊
摘 要:以解放钟枇杷为材料,分析果实发育过程中黄酮醇合成酶(Flavonol Synthase,FLS)基因表达与黄酮醇积累的相关性,进而探讨枇杷果实黄酮醇积累的分子机制。利用高效液相色谱法(HPLC)对不同时期枇杷果实黄酮醇含量进行测定,通过RT-qPCR技术检测了不同发育时期果实黄酮醇合成酶FLS基因的表达量。结果表明:枇杷果实中以黄酮醇含量最高,其次是二氢黄酮醇。黄酮醇含量在成熟过程中总体呈现下降趋势,特别在果实发育前期(花后55~65 d)其含量下降幅度较大;而二氢黄酮醇含量呈上升趋势,黄酮醇合成酶FLS基因的表达量变化与黄酮醇含量变化趋势相似。枇杷果实不同时期的黄酮醇合成酶FLS基因表达量与黄酮醇含量呈显著正相关,但与二氢黄酮醇含量呈显著负相关,表明黄酮醇合成酶FLS基因对枇杷果实黄酮醇的合成具有明显的正调控作用。
关键词:枇杷; 黄酮醇; 黄酮醇合成酶基因; 基因表达量
Abstract: With Jiefangzhong loquat as material, the correlation between flavonol synthetase (FLS) genetic expression and flavonol accumulation during fruit development was analyzed in this paper, and then the molecular mechanism of flavonol accumulation in loquat fruits was discussed. High Performance Liquid (HPLC) was used to determine the content of flavonol in loquat fruits at different stages, and the expression level of FLS gene in fruits at different development stages was detected by using RT-PCR. The results showed that the content of flavonol was the highest in loquat fruits, followed by that of flavanonol. And the content of flavonol has tended to decrease on the whole in the ripening process, which was reducing greatly especially in the early stage of fruit development (55-65 d after anthesis). However, the content of flavanonol was on the rise, and the change trend of the expression level of FLS gene was similar to that of flavanol. The expression level of FLS gene in loquat fruits at different stages had significant positive correlation with the content of flavonol, while it had significant negative correlation with the content of flavanonol, indicating that FLS gene had a significant positive regulating effect on the synthesis of flavonol in loquat fruits.
Key words: Loquat; Flavonol; Flavonol synthase gene; Expression level of gene
枇杷Eriobotrya japonica是薔薇科亚热带常绿果树,原产于我国东南部,被广泛种植在日本、意大利、巴基斯坦、西班牙等30多个国家。我国枇杷栽培历史悠久,种质资源丰富,年产量高达106 t,位居世界第1。我国枇杷主栽区域为东南沿海地区、华中地区、西南高原地区和华南沿海地区。特别在东南沿海地区(福建省),枇杷已成为当地重要的经济特色水果。枇杷果实色泽风味俱佳,且具有较高的药用价值,其果实中起主要药用作用的物质为类黄酮,类黄酮是自然界中一类重要的天然次生代谢产物,具有抗氧化与自由基消除活性作用,抗肿瘤及抗癌作用,抗心血管疾病的作用,对酒精中毒的解毒作用和治疗酒依赖作用[1]。类黄酮可分为黄酮醇类、黄酮类、查尔酮类、花青素类、黄烷酮类和异黄酮类等六大类,其中黄酮醇类含量占比最多,黄酮醇具有其他类黄酮化合物所具有的所有药用功能[2-3]。枇杷果肉富含黄酮醇,其果肉中起主要药用作用芦丁、槲皮素等都属于黄酮醇类。枇杷作为新的黄酮醇植物资源具有重要的研究价值和巨大的开发潜力。因此,研究黄酮醇合成酶FLS在枇杷果实黄酮醇积累中的作用,有利于揭示枇杷果实中大量积累黄酮醇的生化机理,为枇杷黄酮醇的开发利用提供指导。
前人通过对苦荞麦Fagopyrum tataricurn[4]、烟草Nicotiana tabacun[5]、茶树Camellia sinensis[6]、金银花Lonicera iaponica[7]等多种植物的研究,对黄酮醇生物合成途径及参与其中多种酶类的作用进行了初步研究,结果发现黄酮醇的合成需要多种酶的共同作用,其中起关键调控作用的为黄酮醇合成酶FLS[8]。生物合成黄酮醇大体可以分为3个阶段,第1阶段是苯丙烷代谢途径,苯丙氨酸转化为反式肉桂酸,这种氨消除反应是由生物体内的关键调节酶苯丙氨酸解氨酶(PAL)催化[9]。反式肉桂酸在肉桂酸4羟化酶(C4H) 的催化下形成反式4香豆酸。反式4
香豆酸在香豆酸辅酶A连接酶(4CL)的催化下,生成产物香豆酰辅酶A,香豆酰辅酶A被活化后在查尔酮合酶(CHS)的作用下轉化为查尔酮,开启了类黄酮物质的合成代谢。第2阶段,查尔酮异构酶(CHI)催化查尔酮转变成无色的黄烷酮,进而衍生出该途径中所有的类黄酮化合物[10]。黄烷酮经过黄烷酮羟基化酶(F3H)催化生成二氢黄酮醇,二氢黄酮醇是花青苷与黄酮醇共用的底物。第3阶段,二氢黄酮醇在黄酮醇合成酶FLS的催化下合成黄酮醇[11-15]。目前对枇杷类黄酮的研究大部分是针对叶[16]和花[17],未见枇杷果实中与类黄酮物质相关的研究报道。目前,枇杷果实黄酮醇合成积累的模式和机理尚不明确,其中黄酮醇合成酶FLS作为黄酮醇合成途径的重要酶类之一,对枇杷果实中黄酮醇的积累起到不可缺少的作用。本研究以福建省主栽枇杷品种解放钟为试验材料,分析黄酮醇合成酶FLS基因对黄酮醇合成积累的机制进行研究,为探讨枇杷果实发育过程中黄酮醇积累的分子机制提供理论依据。
1 材料与方法
1.1 试验材料
1.1.1 供试样品 所取试材为福建省莆田市常太镇果园提供的解放钟枇杷,于花后55、65、95、125 d 4个时期各采1次果,选择管理水平和生长势大致相同的3株枇杷树,从每株树上采6个果实,取样后果实立即用双蒸水洗净,去除果皮,切取果实中部果肉10.00 g,称取后的样品用液氮迅速冷冻,置-80℃超低温冰箱保存待测定。
1.1.2 引物序列设计及合成 从枇杷果实转录组数据库(未公布)中挑选所需基因的CDS序列,利用NCBI数据库(http://www.ncbi.nlm.nih.gov/pubmed/)进行Blast分析,选择相似度较高的序列,初步筛选所需基因序列,使用primer 5.0软件进行引物设计,并由铂尚生物公司合成。
1.2 试验方法
1.2.1 类黄酮物质含量测定 类黄酮含量测定参照吴宏伟等[18]的方法,略有改动。取0.3 g鲜样于液氮中研磨,并加入2 mL DMSO甲醇(1∶1),超声15 min,取上清液10000 r·min-1,4℃离心10 min后分出上清液,取上清液,重复提取3次。合并上清转入10 mL容量瓶中。取1 mL提取液过0.22 uL的有机滤膜,所得滤液用无水乙醇稀释至10 mL,摇匀,备用。每个样品设3次生物重复和3次技术重复。精密称取类黄酮标准品分别置于10 mL量瓶中,加无水乙醇超声溶解,并稀释至刻度,摇匀;再分别精密吸取类黄酮标准品1 mL置于10 mL量瓶中,用无水乙醇定容至刻度,摇匀,备用。色谱柱:Kromasil C18(4.6 mm×250 mm,5 um);流动相∶乙腈∶水∶冰醋酸为500∶500∶1;流速1 mL·min-1;柱温25℃;检测波长347 nm。依照上述色谱条件分别精密吸取对照品和供试品各10 uL,分别进样。
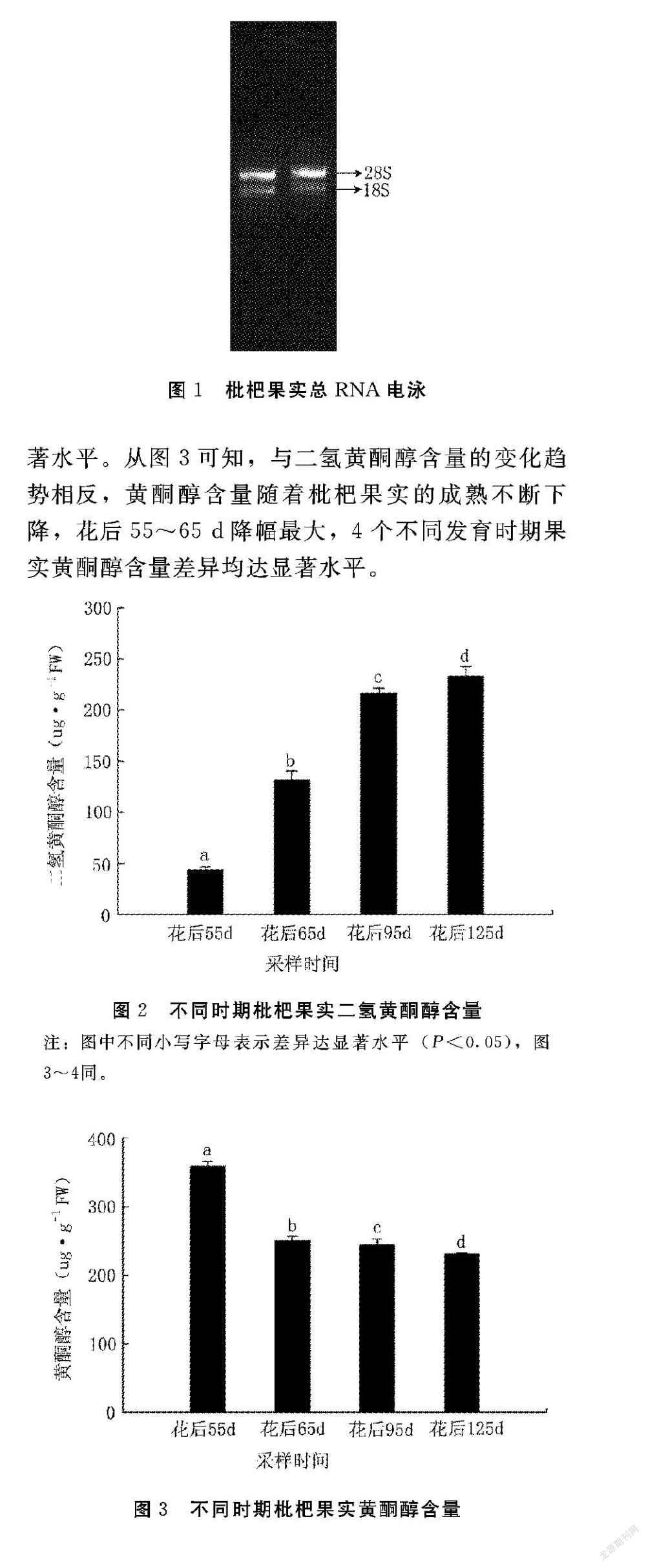
1.2.2 枇杷果实总RNA的提取 由于枇杷果肉中多糖多酚及水分含量较高,因此在提取过程中参照Biospin多糖多酚植物总RNA提取试剂盒的说明书稍有改动。RNA的完整性、纯度和浓度是衡量RNA质量的指标。用超微量分光光度计对所提RNA浓度和纯度进行测定,并用1.0%琼脂凝胶电泳对枇杷果实总RNA的质量进行检测。
1.2.3 逆转录的操作方法 严格参照PrimeScript RT reagent Kit With gDNA Eraser试剂盒说明书进行操作。
1.2.4 实时荧光定量PCR 从枇杷果实的转录组测序结果中挑选出黄酮醇合成酶FLS基因序列,采用Beacon Designer 7引物设计软件进行引物设计。使用耶拿qTOWER2.2荧光定量仪完成定量分析。反应参数为95℃ 30 s,1个循环;95℃ 5 s,60℃ 20 s,45个循环,每个样品设3次生物重复和3次技术重复,利用2ΔΔCT对定量数据进行分析。
1.3 数据统计
试验数据采用SPSS17.0 数据统计软件进行相关性和线性回归等统计分析。
2 结果与分析
2.1 枇杷果实总RNA的提取
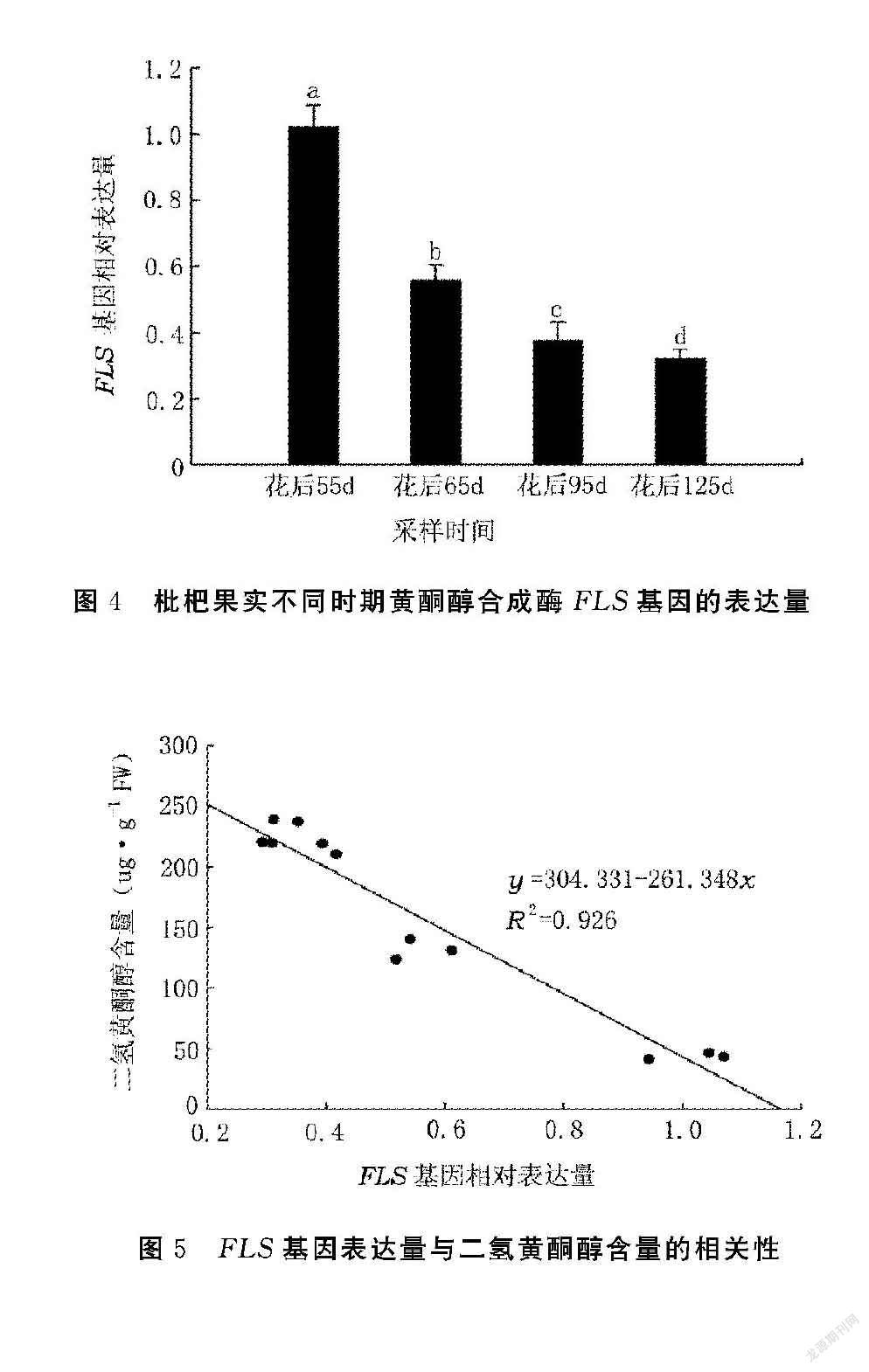
2.2 枇杷果实发育过程中黄酮类物质含量的动态变化
以花后55、65、95、125 d 4个采样时期的枇杷果实为试材,利用HPLC对枇杷果实二氢黄酮醇含量(以柚皮苷和芸香柚皮苷总量计)、黄酮醇含量(以芦丁和槲皮素总量计)进行测定。从图2可知,二氢黄酮醇含量在花后55、65、95、125 d 4个时期均呈上升趋势,花后65~95 d增幅最大,4个不同发育时期的果实二氢黄酮醇含量差异均达显著水平。从图3可知,与二氢黄酮醇含量的变化趋势相反,黄酮醇含量随着枇杷果实的成熟不断下降,花后55~65 d降幅最大,4个不同发育时期果实黄酮醇含量差异均达显著水平。
2.3 枇杷果实发育过程中黄酮醇合成酶FLS基因的表达
由图4可知,黄酮醇合成酶FLS基因表达量随着枇杷果实的成熟而不断降低,在花后55~65 d下降幅度最大,与黄酮醇含量变化趋势基本一致。黄酮醇合成酶FLS基因表达量在果实发育的4个时期之间差异均达显著水平。
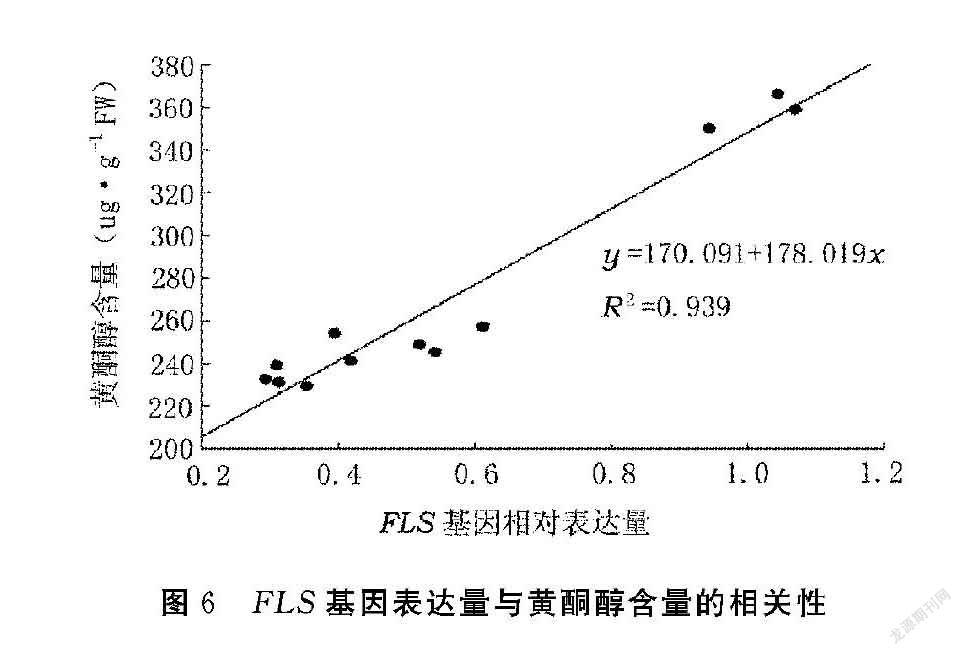
2.4 黄酮醇含量、二氢黄酮醇含量与黄酮醇合成酶FLS基因表达量的相关性
利用SPSS 17.0软件对二氢黄酮醇含量、黄酮醇含量与黄酮醇合成酶FLS基因表达量进行相关性分析。 在枇杷果实成熟过程中,二氢黄酮醇含量与黄酮醇合成酶FLS基因表达量之间呈显著负相关(图5),黄酮醇含量与黄酮醇合成酶FLS基因表达量呈显著正相关(图6),表明黄酮醇合成酶FLS基因对枇杷果实黄酮醇合成具有明显的调控作用。
3 讨论与结论
本研究结果表明,随着枇杷果实的成熟,枇杷果实中黄酮醇含量呈下降趋势,且各个时期果实中的黄酮醇含量间均存在显著差异,与Jaakola等[19]在越橘果实中的研究结果相似。黄酮醇的合成是一个复杂的过程,黄酮醇合成酶FLS是参与此过程的重要酶类之一。Ben-Meir等[20]从受辐射的欧芹细胞中第1次观察到二氢黄酮醇转变为黄酮醇,随后研究人员在紫罗兰[21]、康乃馨[22]花蕾提取物中也检测到黄酮醇合成酶FLS的活性。在拟南芥与温州蜜柑中,黄酮醇合成酶FLS基因被归为早期基因,在花朵和嫩叶片中的表达量较高,而在成熟叶片组织中的表达量较低,主要在植物发育的早期阶段起作用[23]。柑橘果实幼嫩汁胞的黄酮醇含量高于成熟汁胞黄酮醇含量[24]。说明黄酮醇合成酶FLS基因在枇杷果实中可能也是一个早期基因,促使黄酮醇在幼果中积累。
本研究结果还表明,随着黄酮醇合成酶FLS基因表达量的降低,黄酮醇含量亦逐渐下降,二者呈现相同的变化趋势,特别是在果实发育早期(花后55~65 d),枇杷果实黄酮醇含量的降幅较大,同时黄酮醇合成酶FLS基因表达量的趋势与之相似,黄酮醇合成酶FLS基因转录水平与黄酮醇含量相关性分析表明该基因对黄酮醇的积累起到正调控的作用。目前有许多研究报道关于黄酮醇合成酶FLS基因的表达与黄酮醇含量之间的关系,黄酮醇合成酶FLS基因关系到黄酮醇合成支路对代谢流的竞争能力,影响着黄酮醇合成支路代谢流的强弱,控制黄酮醇积累[25]。类黄酮合成相关基因表达模式的比较表明,黄酮醇合成酶FLS和二氢黄酮醇4还原酶DFR基因的不平衡表达决定了玫瑰、野蔷薇、桃、香石竹、杜鹃、山茶以及矮牵牛7种植物红花和白花花瓣中黄酮醇类化合物的积累,黄酮醇合成酶FLS基因表达量越高,花瓣中黄酮醇含量越高;过表达黄酮醇合成酶FLS基因能够增强烟草叶片黄酮醇的合成;紫花洋桔梗中抑制黄酮醇合成酶FLS基因表达,导致花瓣中黄酮醇含量低于检测限[26]。拟南芥种子萌发过程中,白光照射能引起拟南芥黄酮醇合成酶FLS1基因在不同组织中的差异性表达,从而导致黄酮醇不同程度的积累[27]。玉米中黄酮醇合成酶FLS1基因的上调表达也会引起组织中黄酮醇含量的上升[28]。对苦荞麦进行NaCl胁迫处理,发现黄酮醇合成酶FLS基因的上调表达可以促进其根、茎、种子内黄酮醇的积累[29]。遮阴抑制了葡萄果实中黄酮醇合成酶FLS4基因的表达,从而抑制果实黄酮醇的积累
[30]。枇杷果实中黄酮醇合成酶FLS基因的表达与黄酮醇合成趋势相一致,这与前人的研究相符。枇杷果实中其他与黄酮醇合成相关酶基因表达以及酶活性的调控机理还有待于进一步研究。
参考文献:
[1]王云梅.橄榄叶黄酮合成相关基因cDNA的克隆[D].福州:福建农林大学,2009.
[2]延玺,刘会青,邹永青,等.黄酮类化合物生理活性及合成研究进展[J].有机化学,2008, 28(9):1534-1544.
[3]黄琼林,蔡春.不同植物黄酮醇合成酶FLS的生物信息学分析[J].广东农业科学,2014,41(13):140-143.
[4]祝婷.苦荞麦黄酮醇合成酶基因FLS的克隆及其花期表达分析[D].雅安:四川农业大学,2011.
[5]黄伟伟.烟草黄酮醇合成酶基因的分离及其序列分析[D].武汉:华中科技大学,2007.
[6]马春雷.茶树查尔酮异构酶、黄酮醇合成酶和无色花色素还原酶等基因的克隆与表达分析[D].北京:中国农业科学院,2007.
[7]乔中全.金银花chs、fls、c11i基因全长克隆及序列分析[D].长沙:中南林业科技大学,2012.
[8]廖靖军,安成才,吴思,等.查尔酮合酶基因在植物防御反应中的调控作用[J].北京大学学报(自然科学版),2000,36(4):566-575.
[9]CHENG G W,BREEN P J.Activity of Phenylalanine Ammonia-Lyase (PAL) and Concentrations of Anthocyanins and Phenolics in Developing Strawberry Fruit[J].Journal of the American Society for Horticultural Science,1991,116(5):117-124.
[10]LI S J,DENG X M,MAO H Z,et al.Enhanced anthocyanin synthesis in foliage plantCaladium bicolor[J].Plant Cell Reports,2005, 23(10-11):716-720.
[11]FORKMANN G,MARTENS S.Metabolic engineering and applications of flavonoids[J].Current opinion biotechnology,2001,12(2):155-160.
[12]乔小燕, 马春雷, 陈亮.植物类黄酮生物合成途径及重要基因的调控[J].天然产物研究与开发,2009,21(2):354-360.
[13]WINKEL-SHIRLEY B.Biosynthesis of Flavonoids and Effects of Stress[J].Current Opinion in Plant Biology,2002,5(3):218-223.
[14]MARA L FALCONE FERREYRA,SEBASTIN P RIUS,CASATI P.Flavonoids:Biosynthesis,Biological functions and Biotechnological applications[J].Frontiers in Plant Science,2012,3(222):222.
[15]VIANELLO A,PATUI S,BERTOLINI A,et al.Plant Flavonoids-Biosynthesis,Transport and Involvement in Stress Responses[J].International Journal of Molecular Sciences,2013,14(7):14950-14973.
[16]毛延妮.植物枇杷葉黄酮类化合物提取与抑菌性研究[D].福州:福建农林大学,2010.
[17]李琪,廖颖.枇杷花中黄酮的分离鉴别研究[J].食品与发酵科技, 2011,47(1):86-88.
[18]吴宏伟,雷海民,李强, 等.高效液相色谱法测定陈皮多甲氧基黄酮部位中三种黄酮的含量[C]//中华中医药学会中药化学分会2006年度学术研讨会论文集,2006:181-184.
[19]JAAKOLA L,MTTK,PIRTTIL A M,et al.Expression of genes involved in anthocyanin biosynthesis in relation to anthocyanin,proanthocyanidin,and flavonol levels during bilberry fruit development[J].Plant Physiology,2002,130(2):729-739.
[20]BEN-MEIR H,ZUKER A,WEISS D,et al.Molecular Control of Floral Pigmentation:Anthocyanins[C]//Breeding for Ornamentals:Classical and Molecular Approaches. Kluwer: Dordrcht, 2002:253-272.
[21]FROEMEL S, VLAMING P D,SPRIBILLE R,et al.Genetic and biochemical studies on the conversion of flavanones to dihydroflavonols in flowers of Petunia hybrida[J]. Z Naturforsch,1985,41(C):179-186.
[22]FORKMANN G.Flavonoids as Flower Pigments:The Formation of the Natural Spectrum and its Extension by Genetic Engineering[J].Plant Breeding,1991,106(1):1-26.
[23]CHEN X Q,ITANI T,WU X J,et al.Physiological factors affecting transcription of genes involved in the flavonoid biosynthetic pathway in different rice varieties[J].Plant Signaling & Behavior,2013,8(12):e27555.
[24]MORIGUCHI T,KITA M,OGAWA K,et al.Flavonol synthase gene expression during citrus fruit development[J].Physiologia plantarum,2002,114(2):251-258.
[25]HOLTON T A,BRUGLIERA F,TANAKA Y.Cloning and expression of flavonol synthase from Petunia hybrida[J].The Plant Journal,1994, 4(6):1003-1010.
[26]NIELSEN K,DEROLES S C,MARKHAM K R,et al.Antisense flavonol synthase alters copigmentation and flower color in lisianthus[J].Molecular Breeding,2002,9(4):217-229.
[27]STRACKE,R,ISHIHARA,H,HUEP G,et a1.Differential regulation of closely related R2R3-MYB transcription factors controls flavonol accumulation in different parts of the Arabidopsis thaliana seedling[J].The Plant Journal,2007,50(4):660-677.
[28]FERREYRA M L F,RIUS S,EMILIANI J,et a1.Cloning and characterization of a UV-B-inducible maize flavonol synthase[J].The Plant Journal,2010,62(1):77-91.
[29]LI X H,KIM Y B,KIM Y,et al.Differential stress-response expression of two flavonol synthase genes and accumulation of flavonols in tartary buckwheat[J].Journal of Plant Physiology,2013,170(18):1630-1636.
[30] FUJITA A,GOTO-YAMAMOTO N,ARAMAKI I.Organ-specific transcription of putative flavonol synthase genes of grapevine and effects of plant hormones and shading on flavonol biosynthesis in grape berry skins.[J].Bioscience,biotechnology,and biochemistry,2006,70(3):632-638.
(責任编辑:林玲娜)

