高效液相色谱法同时测定吴茱萸醇提物中4种生物碱*
张敏,董嘉皓,李斐,肖素芸,袁金斌
(1.南昌市食品药品检验所南昌市中药质控与安全性评价重点实验室,南昌 330015;2.江西中医药大学现代中药制剂教育部重点实验室,南昌 330004;3.江西中医药大学药学院中药学科研实践班,南昌 330004)
吴茱萸为芸香科植物吴茱萸[Euodiarutaecarpa(Juss.)Benth.]、石虎[Euodiarutaecarpa(Juss.)Benth.var.officinalis(Dode)Huang]或疏毛吴茱萸[Euodiarutaecarpa(Juss.)Benth.var.bodinieri(Dode)Huang]的干燥近成熟果实[1]。吴茱萸性味辛、苦、热,有小毒;具有散寒止痛、降逆止呕、助阳止泻等功效。现代研究表明,吴茱萸中含有多种化学成分,主要为生物碱类、柠檬苦素类、挥发油类、木脂素、黄酮、多糖等[2],其中生物碱类为其主要有效成分,具有镇痛、抗炎等药理作用[3-4]。
吴茱萸生物碱类成分众多,主要包括吲哚喹啉类和喹诺酮类生物碱。目前关于吴茱萸质量控制方面的研究多集中于吲哚喹啉类生物碱(如吴茱萸碱和吴茱萸次碱)的含量测定[1,5-10],较少涉及其他生物碱。文献表明去氢吴茱萸碱和吴茱萸新碱是吴茱萸所特有的生物活性成分[2,10],笔者前期研究发现二者的含量相对较高[11-13],在讨论吴茱萸质量标准与质量控制方法时,有必要将二者列入考虑范围。
本实验拟以去氢吴茱萸碱、吴茱萸碱、吴茱萸次碱和吴茱萸新碱为含测指标,通过优化高效液相色谱(HPLC)条件,建立一种同时测定吴茱萸生物碱的方法,并对其进行系统验证,以期为研究吴茱萸质量标准的提升提供前期研究基础,为吴茱萸药材及其饮片的质量控制提供可靠的分析方法。
1 仪器与试药
1.1仪器 Agilent 1260 series高效液相色谱仪(包括四元泵、自动进样器、柱温箱、DAD检测器);Mettler AE 240电子天平(瑞士Mettler公司,感量:0.000 1 g);PS-80A超声波清洗机(东莞市洁康超声波设备有限公司);GZX-9140MBE电热鼓风干燥箱(上海博迅实业有限公司医疗设备厂);116B摇摆式高速中药粉碎机(瑞安市永历制药机械有限公司)。
1.2试药 吴茱萸药材采自江西省新干市,经江西中医药大学曹岚副教授鉴定为芸香科植物石虎[Euodiarutaecarpa(Juss.)Benth.var.officinalis(Dode)Huang]的干燥近成熟果实。去氢吴茱萸碱对照品购自上海源叶生物科技有限公司(批号:B21028),吴茱萸新碱对照品购自上海胤珂生物科技有限公司(批号:15266-38-3),吴茱萸碱对照品(批号:110802-200504)、吴茱萸次碱对照品(批号:0801-9702)购自中国食品药品检定研究院。所有对照品标示含量均大于98.5%(HPLC分析)。乙腈为色谱纯,水为双蒸水,其他试剂均为分析纯。
2 方法与结果
2.1对照品溶液的制备 精密称取各对照品适量,以甲醇溶解并定容,得单一成分对照品溶液。再分别取上述4个对照品溶液各1 mL加入10 mL量瓶中,以甲醇定容,摇匀,得混合对照品储备溶液。混标溶液中,各对照品的浓度分别为:去氢吴茱萸碱503 μg·mL-1、吴茱萸碱501 μg·mL-1、吴茱萸次碱503 μg·mL-1和吴茱萸新碱511 μg·mL-1。
2.2供试品溶液的制备 吴茱萸药材净制,放入60 ℃烘箱,烘2 h,粉碎,称取约0.3 g(过孔径355 μm筛),置于具塞锥形瓶中,精密加入70%乙醇25mL,称定质量,浸泡1 h后超声处理(功率100 W,频率40 kHz)40 min,放冷,再称定质量,用70%乙醇补足减失的质量,摇匀,滤过,取续滤液,过孔径0.22 μm滤膜,备用。
2.3色谱条件 Agilent Zorbax Eclipse Plus-C18色谱柱(4.6 mm×100 mm,3.5 μm);流动相:乙腈(A)-0.1%磷酸溶液(B);梯度洗脱:0~10 min,17%→21%A;10~12 min,21%→40%A;12~15 min,40%→44%A;15~17 min,44%A;17~18 min,44%→60%A;18~28 min,60%→75%A;28~30 min,75%→100%A;30~35 min,100%A。流速:1.0 mL·min-1;检测波长:326 nm;柱温:30 ℃;进样量5 μL。
2.4系统适用性实验及专属性考察 将混合对照品溶液、供试品溶液和空白溶剂分别按照“2.3”项下色谱条件分别进样检测,色谱图见图1。可知,空白溶剂在去氢吴茱萸碱峰、吴茱萸碱峰、吴茱萸次碱峰和吴茱萸新碱峰位置处均无吸收峰,即溶剂对测定无干扰;供试品溶液中,4种组分峰均与其他组分峰达到基线分离,分离度>1.5,且与混合对照品溶液中4种组分峰的保留时间一致。
2.5线性关系考察 逐级稀释“2.1”项混合对照品溶液,得6个浓度系列的混合对照品溶液,分别进样分析。以浓度为横坐标(X),峰面积为纵坐标(Y)进行线性回归分析。得回归方程分别为:去氢吴茱萸Y=9808.2X-23.844(R2=0.999 5),吴茱萸碱碱Y=1691.6X-3.8455 (R2=0.999 5),吴茱萸次碱Y=29413X+6.062 7(R2=0.999 7),吴茱萸新碱Y=8259.8X-4.184 7(R2=0.999 7)。去氢吴茱萸碱、吴茱萸碱、吴茱萸次碱、吴茱萸新碱的线性范围分别为2.52~503,2.50~501,2.52~503和2.56~511 μg·mL-1。
2.6精密度实验 精密吸取供试品溶液5 μL,按“2.3”项下色谱条件连续进样6针,以峰面积计算RSD值,得去氢吴茱萸碱、吴茱萸碱、吴茱萸次碱、吴茱萸新碱的RSD值分别为0.7%,0.6%,0.5%,0.8%。
2.7重复性实验 取同一批吴茱萸药材6份,按“2.1”项下供试品溶液制备方法和“2.3”项下色谱条件分别进样测定,记录峰面积,计算含量,以 6次含量的RSD评价方法的重复性。去氢吴茱萸碱、吴茱萸碱、吴茱萸次碱和吴茱萸新碱RSD值分别为1.0%,1.1%,1.6%,1.3%。
2.8稳定性实验 取吴茱萸粉末,制备,分别室温下静置0,2,4,6,12,24,48 h后再按照“2.3”项下色谱条件进样测定,记录峰面积,以峰面积计算RSD值,去氢吴茱萸碱、吴茱萸碱、吴茱萸次碱、吴茱萸新碱RSD值分别为1.1%,0.8%,1.0%,1.1%。
2.9加样回收率实验 精密称取己知含量的同一吴茱萸粉末6份,分别精密加入相当于样品100%含量的去氢吴茱萸碱(0.313 mg·mL-1)、吴茱萸碱(0.456 mg·mL-1)、吴茱萸次碱(0.235 mg·mL-1)和吴茱萸新碱(0.146 mg·mL-1)的对照品1 mL,制备,按上述的色谱条件进样,计算加样回收率。其平均回收率(RSD)分别为:去氢吴茱萸碱,98.4%(2.4%);吴茱萸碱98.7%(2.4%);吴茱萸次碱,100.9%(2.4%)和吴茱萸新碱,101.1%(2.4%)。
2.10不同产地样品的含量测定 取不同产地的吴茱萸药材10批,分别按“2.3”项下供试品溶液制备方法和“2.2”项下色谱条件制备和进样测定,记录色谱图,见图2。10批不同产地吴茱萸中4种成分的含量结果见表1。
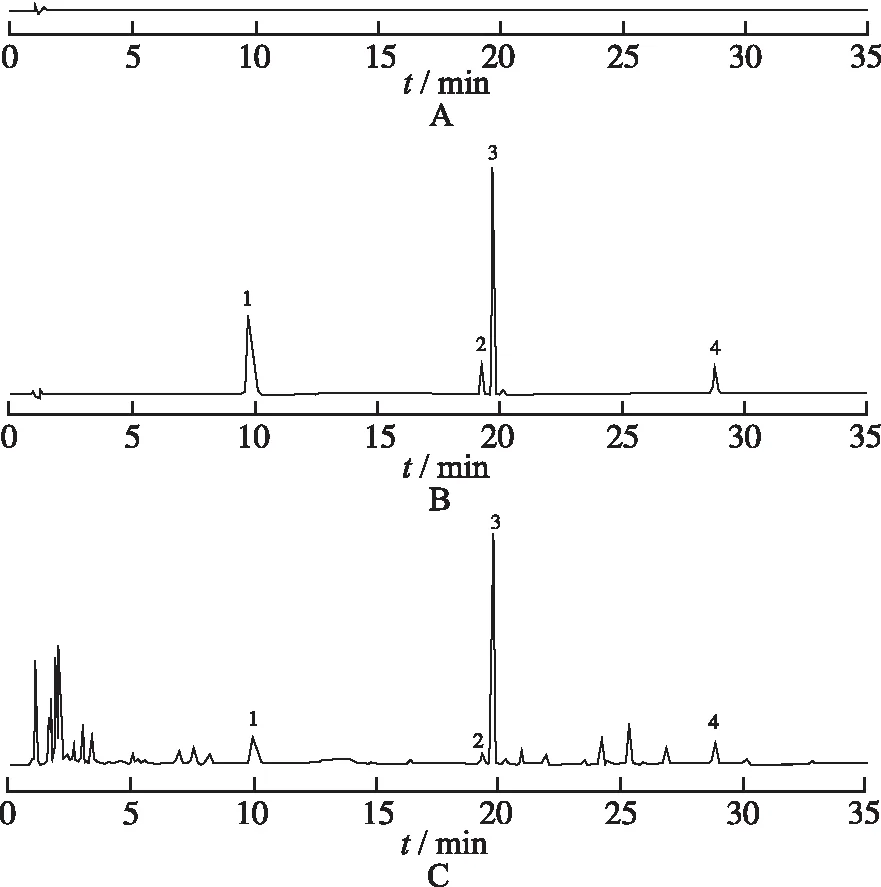
A.空白溶剂;B.对照品;C.供试品;1.去氢吴茱萸碱;2.吴茱萸碱;3.吴茱萸次碱;4.吴茱萸新碱。图1 3种溶液的HPLC色谱图A.blank solution;B.reference;C.samples;1.dehydroevodiamine;2.evodiamine;3.rutaecarpin;4.evocarpine.Fig.1 HPLC chromatogram of three kinds of solution

S1.江西樟树1;S2.江西樟树2;S3.江西丰溪1;S4.江西丰溪2;S5.江西新干;S6.湖南新晃;S7.湖南沅江;S8.云南昭通;S9.云南曲靖;S10,贵州凯里;1.去氢吴茱萸碱;2.吴茱萸碱;3.吴茱萸次碱;4.吴茱萸新碱。图2 不同产地的吴茱萸色谱图S1.Zhangshu 1,Jiangxi;S2.Zhangshu 2,Jiangxi;S3.Fengxi 1,Jiangxi;S4.Fengxi 2,Jiangxi;S5.Xingan,Jiangxi;S6.Xinhuang,Hunan;S7.Yuanjiang,Hunan;S8.Zhaotong,Yunnan;S9.Qujing,Yunnan;S10.Kaili,Guizhou;1.dehydroevodiamine;2.evodiamine;3.rutaecarpin;4.evocarpine.Fig.2 Chromatograms of Euodia rutaecarpa from different origins

表1 10批不同产地吴茱萸4种生物碱含量测定结果Tab.1 Results of content determination on ten batches of four alkaloids in Euodia Rutaecarpa from different origins %,n=6
3 讨论
3.1流动相的选择 本实验考察乙腈-0.2%甲酸溶液、乙腈-0.2%醋酸溶液和乙腈-0.1%磷酸溶液,发现在乙腈-0.1%磷酸溶液下4种成分的色谱峰分离效果较好,可达到完全分离,且出峰时间适中。因此选用了乙腈-0.1%磷酸溶液为本实验的流动相。
3.2提取溶剂的选择 吴茱萸生物碱是脂溶性化合物,易溶于有机溶剂,如乙醇、甲醇、乙酸乙酯溶液等。从环境友好和经济适用的角度看,乙醇是最佳的提取溶剂。前期实验[10]表明吴茱萸生物碱进行提取用浓度为70%的乙醇,生物碱得率最高。因此,本实验使用的提取溶剂为70%乙醇。
3.3检测波长的选择 文献中有关吴茱萸碱和吴茱萸次碱的检测波长多设置为215和225 nm[8-10],本实验发现波长设置为215和225 nm时,吴茱萸碱和吴茱萸次碱中有个小峰,使二者的分离度均小于1.5,且基线漂移较大。当以DAD检测器在190~400 nm波长下进行全波长扫描时发现该杂质峰在326 nm处无吸收,而4个目标化合物均有合适的响应,且色谱图的基线平稳,各色谱峰峰的分离度都大于1.5,故检测波长选择为326 nm。
3.4不同产地样品的含量分析 从图2和表1可知,不同产地吴茱萸中化学成分含量的差异较大。其中吴茱萸碱和次碱在各个样品中的含量差异最大,去氢吴茱萸碱含量差异相对较小。按《中华人民共和国药典》2015年版标准,樟树1#和丰溪的3个样品竟为不合格产品,具体原因尚需进一步调查取样。
吲哚喹啉类、喹诺酮类生物碱是吴茱萸中的两类主要生物碱,去氢吴茱萸碱、吴茱萸碱、吴茱萸次碱和吴茱萸新碱是这两类生物碱的典型代表,特征性强,含量相对比较丰富。笔者首次将代表喹诺酮类生物碱的吴茱萸新碱纳入到吴茱萸的含测指标,更能反映吴茱萸药材的质量属性。
在充分优化分析条件的基础上,本文建立了吴茱萸中4种生物碱的HPLC同时测定方法,并对其进行严格的方法学验证。该方法简单、稳定、可靠,可用于吴茱萸药材及其饮片的质量评价。

