天麻破壁粉与冻干粉对小鼠急性肝肾毒性研究
刘春艳,卢礼平,田兴中,柴艺汇,谢 宇,周 雯,牛建均,张丽艳*
(1.贵州中医药大学,贵州贵阳 550025;2.贵州威门药业股份有限公司,贵州贵阳 550018;3.张家口市第五医院,河北张家口 075000;4.贵州广济堂药业有限公司,贵州贵阳 550014)
天麻具有悠久的历史,最早记载于《神农本草经》,并将其列为上品,具有熄风止痉、平抑肝阳、祛风通络之功效,治疗癫痫抽搐、肢体麻木、风湿痹痛等病症[1],主产于贵州、云南、四川及华北地区[2]。现代药理学研究发现,天麻具有神经保护、抗惊厥、降血压、增强免疫力等多种作用[3]。天麻化学成分复杂,其主要成分为天麻素、天麻苷元,此外还含有多种氨基酸及微量元素等[4]。历代本草均认为天麻无毒,现代临床应用天麻饮片亦未见毒性报道。另外,天麻还被视为“药食两用”的名贵中药保健产品被广泛食用。中药破壁粉和冻干粉是为改善传统中药饮片使用方式,采用先进工艺制成的新型中药剂型。中药破壁粉是通过现代粉碎技术将传统中药饮片加工至D90<45 μm的粉体[5],天麻冻干粉是通过低温条件下水的升华性能,使传统饮片在真空环境低温脱水形成的干燥粉剂。二者在不改变传统中药饮片的物质基础上,实现中药品质的均匀性及确保中药的安全性,也提高了中药材的利用率[6]。有研究发现,天麻破壁饮片工艺有助于提高其溶出效率[7]。其冷冻干燥技术可更好地保持药材品质,同时使天麻有效成分避免因受热干燥造成的分解和散失[8-10]。目前,尚未出现专门针对天麻破壁饮片、冻干粉毒副作用、毒性物质基础和产生毒副作用的剂量范围的相关研究。本实验以小鼠为研究对象,观察24 h内多次给予小鼠不同剂量天麻破壁饮片或冻干粉,观察其对小鼠日常行为及肝、肾功能的影响,并与抗癫痫治疗中的一线药物丙戊酸钠毒性反应进行比较[11],为天麻破壁粉和冻干粉在医药、保健方面的应用提供实验依据。
1 材料与仪器
1.1 动物
SPF级昆明种健康小鼠100只,体重18~22 g,雌雄各半,动物许可证号:SCXK(军)2012-0011,购于庆腾鑫比尔实验动物销售有限公司。
1.2 试剂
丙戊酸钠(赛诺菲安万特(杭州)制药有限公司,批号:6HG0478);生理盐水;多聚甲醛(国药集团化学试剂有限公司,批号:20180112);PBS磷酸盐缓冲液(北京中杉金桥生物技术有限公司,批号:ZLI-9062);无水乙醇(江苏海兴化工有限公司,批号:GB678-90),二甲苯(天津致远化学试剂有限公司,批号:20180110);苏木素染液(珠海贝索生物技术有限公司,批号:BA-4097);伊红染液(珠海贝索生物技术有限公司,批号BA-4099),中性树胶(国药集团化学试剂有限公司,批号:20171009)。
1.3 仪器
TSJ-Ⅱ型全自动封闭式组织脱水机(常州市中威电子仪器有限公司);BMJ-Ⅲ型包埋机(常州郊区中威电子仪器厂);PHY-Ⅲ型病理组织漂烘仪(常州市中威电子仪器有限公司);BA400Digital数码三目摄像显微镜(麦克奥迪实业集团有限公司);图像分析软件Image-Pro Plus 6.0(美国Media Cybernetics公司)。
1.4 药物
本品来源于贵州大方,药材经贵州中医药大学植物栽培教研室魏升华教授鉴定为兰科植物天麻GastrodiaelataBl.的干燥块茎。破壁粉:60 ℃烘干,经破壁粉碎加工、干压制粒而成;冻干粉:新鲜天麻切制,灭菌,再用真空干燥机冻干,过药典小钢磨粉碎后过6号筛。
2 方法
2.1 动物分组及给药
将100只昆明小鼠随机分为10组,雌雄各半,分别为正常组给予等量生理盐水,丙戊酸钠低、中、高剂量组(0.3 g/kg、0.6 g/kg、0.9 g/kg),天麻(破壁饮片、冻干粉)低、中、高剂量组(15 g/kg、30 g/kg、45 g/kg)。给药组天麻破壁饮片、天麻冻干粉,加适量蒸馏水研磨均匀,分别配制成刚好通过16号灌胃针的混悬液最大浓度,再根据各剂量组所需给药剂量稀释成所需浓度,各组1日之内灌胃给药3次,灌胃溶积为0.2 mL/10 g动物体重(小鼠灌胃最大容积),间隔时间为6 h。给药后即刻开始观察药物的毒理反应情况,给供试品当天连续观察18 h,记录3次。以后每天观察记录2次,连续观察14天。
2.2 观察动物一般体征
观察动物的活动、毛发、分泌物、大小便等一般体征,观察急性毒性试验动物反应性指标。若有动物死亡,记录死亡数目和死亡时间,详细记录每只动物出现毒性反应的症状及症状开始、消失的时间。
2.3 血清生化指标检测
断头采集小鼠血液,以2 500 rpm/min,4 ℃离心15 min后吸取血清,全自动生化仪检测小鼠血清谷丙转氨酶(ALT)、谷草转氨酶(AST)、碱性磷酸酶(AKP)、单核细胞趋化蛋白-1(MCP-1)、尿酸(UA)、尿素氮(BUN)、肌酐(Cr)含量。
2.4 小鼠肝脏及肾脏病理检测
取小鼠新鲜肝肾组织适当大小迅速放入4%多聚甲醛中固定,石蜡包埋、切片,HE染色,采用麦克奥迪实业集团有限公司生产的BA200Digital数码三目摄像显微摄像系统对切片进行图像采集,每张切片先于40倍下观察全部肝脏组织,观察大体病变,选择要观察的区域采集400倍图片,观察具体病变。
2.5 统计学处理

3 结果
3.1 小鼠体重变化及一般情况
与正常组比较,天麻破壁粉与冻干粉各剂量组小鼠体重在第1天、第7天、第14天比较,差异均无统计学意义(P>0.05)。小鼠一般体征变化以丙戊酸钠各剂量组较为多发,以神经系统方面反应为主。第1、2、3次给药后丙戊酸钠、天麻破壁粉及冻干粉各剂量组小鼠均以安静为主要表现,考虑为丙戊酸钠和天麻正常药理反应,非毒性反应。丙戊酸钠0.3 g/kg组第2次给药后个别小鼠出现兴奋现象,丙戊酸钠0.6 g/kg组第2次给药后个别小鼠出现震颤,丙戊酸钠0.9 g/kg组第2次给药后多只小鼠出现不安、异常叫声,持续时间均较短;天麻破壁粉及冻干粉高剂量组个别小鼠在给药过程中出现异常叫声、震颤、运动失调现象,持续时间均较短。各给药组在给药后第2~14天均未出现异常体征。
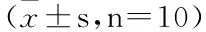

组别剂量(g·kg-1)第1天第7天第14天Control-26.23±3.3832.56±3.5636.66±3.75VPA-0.30.326.45±3.1531.69±3.8334.16±3.16VPA-0.60.628.06±3.1631.95±3.4936.22±3.50VPA-0.90.927.76±4.3632.53±4.2234.95±5.01PB-151526.30±4.1133.63±3.9834.44±3.85PB-303026.00±3.1632.72±3.2035.75±2.83PB-454527.19±3.8233.04±3.9138.25±5.40DG-151526.81±4.0532.50±4.1234.59±2.54DG-303027.32±4.4031.89±3.9134.83±3.61DG-454527.17±4.5532.67±2.9836.41±3.80
注:Control:正常组;VPA-0.3:丙戊酸钠低剂量组;VPA-0.6:丙戊酸钠中剂量组;VPA-0.9:丙戊酸钠高剂量组;PB-15:天麻破壁粉低剂量组;PB-30:天麻破壁粉中剂量组;PB-45:天麻破壁粉高剂量组;DG-15:天麻冻干粉低剂量组;DG-30:天麻冻干粉中剂量组;DG-45:天麻冻干粉高剂量组。
3.2 小鼠血清ALT、AST、AKP含量检测结果
与正常组比较,丙戊酸钠0.6、0.9 g·kg-1组小鼠血清ALT含量显著升高(P<0.05),天麻破壁粉与冻干粉各剂量组及丙戊酸钠0.3 g·kg-1组小鼠血清ALT含量与正常组比较差异无统计学意义(P>0.05),均显著低于丙戊酸钠0.9 g·kg-1组;与正常组及丙戊酸钠各剂量组比较,天麻破壁粉与冻干粉各剂量组小鼠肝功能检测指标AKP、AST血清含量比较差异无统计学意义(P>0.05)。
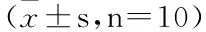
注:与Control比较,1)P<0.05;与VPA-0.3组比较,2)P<0.05;与VPA-0.6组比较,3)P<0.05;与VPA-0.9组比较,4)P<0.05。
3.3 小鼠血清MCP-1、BUN、Cr、UA含量检测结果
与正常组比较,丙戊酸钠0.6 g·kg-1、0.9 g·kg-1组小鼠血清MCP-1、Cr含量显著升高(P<0.05),天麻破壁粉与冻干粉各剂量组及丙戊酸钠0.3 g·kg-1组小鼠血清ALT含量与正常组比较无显著差异,均显著低于丙戊酸钠0.6、0.9 g·kg-1组;与正常组及丙戊酸钠各剂量组比较,天麻破壁粉与冻干粉各剂量组小鼠肾功能检测指标BUN、UA血清含量比较差异无统计学意义(P>0.05)。见表3。
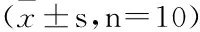
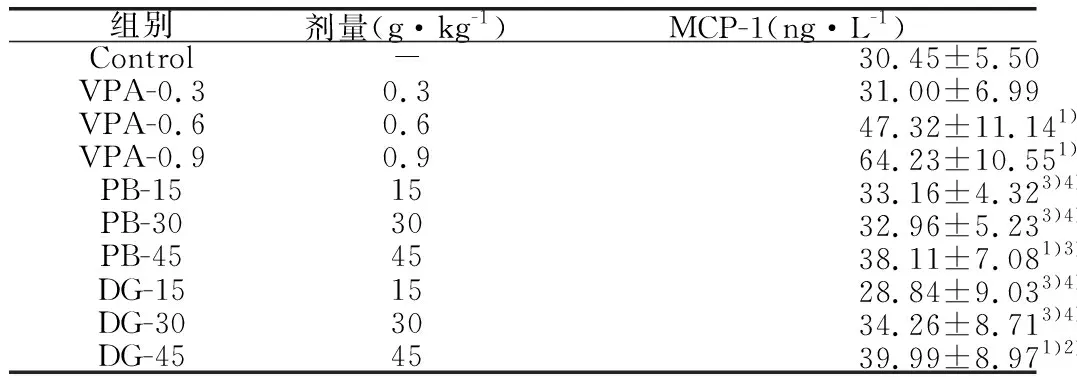
组别剂量(g·kg-1)MCP-1(ng·L-1)Control-30.45±5.50VPA-0.30.331.00±6.99VPA-0.60.647.32±11.141)2)VPA-0.90.964.23±10.551)2)3)PB-151533.16±4.323)4)PB-303032.96±5.233)4)PB-454538.11±7.081)3)4)DG-151528.84±9.033)4)DG-303034.26±8.713)4)DG-454539.99±8.971)2)3)4)
注:与Control比较,1)P<0.05;与VPA-0.3组比较,2)P<0.05;与VPA-0.6组比较,3)P<0.05;与VPA-0.9组比较,4)P<0.05。
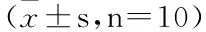

组别剂量(g·kg-1)Ccr(μmol·L-1)BUN(mmol·L-1)UA(μmol·L-1)Control-11.34±5.956.29±1.4993.50±22.95VPA-0.30.315.41±2.431)6.09±1.4994.50±30.93VPA-0.60.626.36±6.381)2)5.89±1.25106.50±29.98VPA-0.90.927.50±4.501)2)6.88±1.02111.50±32.90PB-151512.93±2.623)4)6.49±0.81115.50±38.38PB-30308.62±2.372)3)4)6.80±1.61101.50±34.71PB-454512.64±2.323)4)6.76±0.93103.50±32.21DG-151512.30±3.153)4)6.80±1.13105.50±34.58DG-303011.51±2.633)4)6.81±1.03108.50±36.04DG-454512.30±4.213)4)6.03±1.07101.50±37.99
注:与Control比较,1)P<0.05;与VPA-0.3组比较,2)P<0.05;与VPA-0.6组比较,3)P<0.05;与VPA-0.9组比较,4)P<0.05。
3.4 小鼠肝组织病理检测结果
HE染色结果显示,正常组肝脏组织结构正常,肝细胞分叶不明显,肝细胞形态正常,未见纤维组织增生及炎细胞浸润等病理变化。丙戊酸钠低剂量组部分样本可见肝细胞少量点状坏死,丙戊酸钠中剂量组部分样本可见肝细胞点状或灶状坏死,肝细胞坏死及炎细胞浸润较丙戊酸钠中剂量组重;天麻破壁中剂量组部分样本出现肝细胞脂肪变性,可见肝细胞呈轻微的点状或小灶状肝细胞坏死;天麻破壁粉及冻干粉高剂量组肝细胞出现点状或小灶状肝细胞坏死并伴有轻微炎细胞浸润,以天麻破壁粉高剂量组相对较重。天麻破壁低剂量组及冻干粉低、中剂量组与正常组比较无显著差异。在光镜观察下,本实验部分动物肝脏组织可见少量肝细胞空泡变性,可能与动物解剖前禁食不完全致使肝细胞内肝糖原过多所致,也可能与缺氧等环境因素有关,多考虑为自发性病变,与受试药物无关。见图1。
3.5 小鼠肾组织病理检测结果
HE染色结果显示,正常组肾脏被膜完整,皮质和髓质分界清晰,皮质内肾小球结构完整,肾皮质、肾髓质、肾曲小管、髓袢及集合小管内均未见明显病理变化。丙戊酸钠低剂量组部分样本可见轻度肾小球变性及肾小管上皮细胞变性或脱落,丙戊酸钠中剂量组部分样本可见轻度肾小球肿大,可见肾小管上皮细胞不同程度肿胀变性,呈“气球”样,部分组织可见肾小管管腔扩张,其内可见均质红染的透明管型;丙戊酸钠高剂量组部分样本可见皮质内肾小球萎缩,中央血管球体积缩小,肾小囊腔增大,部分组织可见肾小球不同程度的肿大,肾小囊腔几乎不可见,均可见肾小管上皮细胞不同程度肿胀变性,部分变性细胞脱落于管腔中,偶见细胞核浓缩变小;天麻破壁粉中、高剂量组及天麻冻干粉高剂量组部分样本均可见肾小管上皮细胞变性或脱落,肾小管上皮细胞不同程度肿胀变性,部分变性细胞脱落于管腔中,偶见细胞坏死,细胞核固缩;天麻破壁粉高剂量组还可见部分样本肾小球肿大。天麻破壁低剂量组及冻干低、中剂量组与正常组比较未见显著差异。在光镜观察下,本试验部分动物肾脏组织均可偶见少量肾小管上皮细胞空泡变性,可能是由于组织固定及制片过程中造成的人工假象,或是由环境中缺氧等因素引起,多考虑与受试药物无关。见图2。
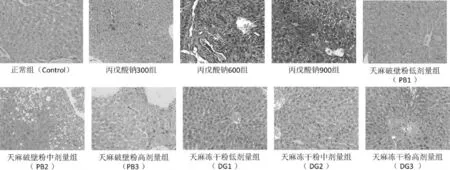
图1 天麻破壁粉、冻干粉、丙戊酸钠各剂量组小鼠肝组织病理检测(HE染色)结果(×400)

图2 天麻破壁粉、冻干粉、丙戊酸钠各剂量组小鼠肾组织病理检测(HE染色)结果(×400)
4 讨论
《本草纲目》云:“天麻,为治风之神药。”天麻乃肝经气分之药,贵州天麻素有“北参黔麻”的美誉,现代药理研究认为天麻具有抗惊厥、保护神经细胞等药理作用,且在治疗惊厥方面疗效显著[12]。中药药效不只由药物特有的化学成分所决定,还可能与药物的物理化学状态等因素密切相关,中药中天麻尚未见中毒或致死报道。
根据2014年《药物单次给药毒性研究技术指导原则》,急性毒性是指“药物在单次或24 h内多次给予后一定时间内所产生的毒性反应”[13],本实验依据小鼠最大单次给药容积和浓度进行计算,24 h内给予天麻破壁粉、冻干粉3次,天麻破壁粉(PB)和冻干粉(DG)低、中、高剂量组最终给药剂量分别为15 g/kg、30 g/kg、45 g/kg,分别为天麻临床等效用量的10倍、20倍、30倍;丙戊酸钠用量为天麻用量的1/50,分别为0.3 g/kg、0.6 g/kg、0.9 g/kg,分别为丙戊酸钠临床等效用量的1倍、2倍、3倍。观察时间为14天,就肝肾功能血清指标谷丙转氨酶(ALT)、谷草转氨酶(AST)、碱性磷酸酶(AKP)、单核细胞趋化蛋白-1(MCP-1)、尿酸(UA)、尿素氮(BUN)、肌酐(Cr)含量,一般情况及肝肾HE染色组织病理改变,探讨其对小鼠肝、肾组织的急性毒性反应。结果显示,10倍天麻临床等效剂量的破壁粉与20倍天麻临床等效剂量的冻干粉低剂量组小鼠血清ALT、AST、AKP、MCP-1、BUN、Cr、UA水平,体重及肝肾组织病理改变与正常组比较差异无统计学意义(P>0.05),20及30倍天麻临床等效剂量的破壁粉中、高剂量组及30倍天麻临床等效剂量的冻干粉高剂量组小鼠肝肾组织病理改变与正常组比较有显著性差异,且天麻破壁粉与冻干粉高剂量组小鼠血清MCP-1水平显著高于正常组(P<0.05),表明天麻破壁粉与冻干粉出现毒副反应的剂量远高于临床正常应用量。本研究部分填补了天麻破壁粉与冻干粉药理毒理研究,为其在临床及保健方面的推广运用提供了一定的实验依据。

