杨梅素溶解度测定与关联
于 帅,程 燕,薛富民,李赛钰,李 剑,郝郁文,刘玉智,孙芸芸
(1.齐鲁工业大学(山东省科学院) 山东省分析测试中心,山东 济南 250014;2.山东蓝城分析测试有限公司,山东 济南 250102)
杨梅素(CAS号:529-44-2,分子式C15H10O8),又名杨梅黄酮,属于黄酮类药物,其结构式如图1所示。杨梅素为黄色针状晶体,多存在于蔬菜、水果、草药中。由于杨梅素具有抗氧化性,其常被应用于食品和药物中,此外,研究表明杨梅素还具有抗病毒、抗菌作用和抗癌功效[1-2]。

图1 杨梅素分子结构式Fig.1 Molecular formula of myricetin
结晶过程工艺条件的选取对于产物的性质具有重要的影响,溶解度数据则是寻找结晶操作空间的重要前提。由于杨梅素溶解性较差,目前对于杨梅素溶解度的报道非常少。本文对杨梅素在纯溶剂中的溶解度进行了测定和关联,为后期杨梅素结晶过程的优化提供了数据基础。
1 实验部分
1.1 实验试剂与仪器
实验试剂包括杨梅素(纯度大于99.5%)、正丙醇(AR)、正丁醇(AR)、异丁醇(AR)、仲丁醇(AR)、丙酮(AR)、甲醇(HPLC级)和超纯水(实验室超纯水机制备)。
实验仪器包括超级恒温水浴(宁波新芝生物科技股份有限公司,DC-2020,精确度为0.1 K)、磁力搅拌器(DLAB,MS-H-S)、夹套反应器、分析天平(梅特勒,ME104)、高效液相色谱仪(HPLC,岛津,LC-20AT,C18柱)、X射线粉末衍射仪(XRD,日本理学,D/max-rB)、热分析仪(NETZSCH,SAT499F3-QMS403C)、真空干燥箱(上海一恒科学仪器有限公司,DZF-6050)等。
1.2 实验方法
杨梅素的溶解度测定采用HPLC法:将过量被测物放置于100 mL夹套反应器中,向反应器中加入80 mL初始溶剂,夹套中接通恒温水浴(冷却介质为50% vol的乙二醇水溶液),开启磁力搅拌,在某指定温度下恒温6 h(预实验已确定平衡时间)。之后停止搅拌使体系静置1 h,用一次性医用注射器吸取一定量的上清液,过0.22 μm有机相针式过滤器,之后迅速用移液枪移取一定量过滤后的溶液并用甲醇定容,通过液相色谱进行溶解度测定。
用一次性胶头滴管吸取每个温度点的残留固体,经过滤、真空干燥后进行XRD分析表征。本实验液相色谱条件为进样体积5~25 μL,检测波长为360 nm,流动相甲醇∶水=85∶15,流速0.5 mL/min,柱温为35℃。实验过程中要保证每次测量的HPLC积分面积落在建模时面积范围内,本实验所建立的HPLC外标模型的R2为0.9998,符合预测标准。
1.3 系统适用性验证
以槲皮素在水中的溶解度数据[3]作为对比,验证了本实验系统的适用性,实验数据与文献数据的相对偏差均小于3.40%(公式5),说明本实验的方法符合溶解度测定的标准。
2 溶解度模型与计算方法
2.1 溶解度模型
2.1.1 van't Hoff 模型
van't Hoff 模型[4]是通过对数方程将溶解度与温度关联起来的
(1)
其中,x1为溶质的摩尔分率溶解度,A和B为模型的参数,T是溶液的平衡温度。
2.1.2 Apelblat模型
Apelblat模型[5]是根据固液平衡理论提出的,该半经验方程可以表示为
(2)
其中x1为溶质的摩尔分率溶解度,a,b和c为模型的参数,T是溶液的平衡温度。由于修正项clnT的引入使得Apelblat模型具有了更广泛的适用性。
2.1.3λh模型
λh模型是由Buchowski等人[6]提出的一个两参数模型,其形式为

其中,x1为溶质的摩尔分率溶解度,λ和h为模型的参数,T是溶液的平衡温度,Tm为溶质的熔点温度。
2.2 计算方法
杨梅素的溶解度采用摩尔分率表示(x1):

其中m1和m2分别为溶质和溶剂的质量,M1和M2分别为溶质和溶剂的相对分子质量。
采用平均相对偏差 (Average Relative Deviation,ARD)对溶解度模型的拟合效果评估。

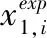
3 结果与讨论
3.1 物质表征
杨梅素在不同溶剂体系和温度下残余固体的XRD图谱均与图2(a)相同,说明在测定的溶剂体系中溶质未发生晶型转化。杨梅素的差式扫描热分析如图2(b)所示,熔点在620 K左右。

图2 (a) 杨梅素X射线粉末衍射图,(b) 杨梅素差式扫描热图Fig.2 (a) XRD pattern of myricetin,(b) DSC curve of myricetin
3.2 溶解度

表1 杨梅素在五种纯溶剂中溶解度数据 (0.1 MPa)aTable 1 The solubility data of myricetin in five pure solvents (0.1 MPa)a
注:a温度的不确定度u(T)=0.5 K,压力的不确定度u(P)=5 kPa,溶解度测量的不确定度ur(xA)=0.01。
预实验中采用了水、甲醇、乙醇、正丙醇、异丙醇、正丁醇、异丁醇、仲丁醇、丙酮、乙腈、甲苯、DMF、DMSO作为溶剂。发现在乙醇中杨梅素溶解度很大,在测定过程中会形成胶体状物质;在水、异丙醇、甲苯中溶解度极小,所测得的数据无规律;在甲醇、乙腈中杨梅素发生了晶型转化;在DMF和DMSO中溶质变质且与溶剂形成了胶状物质。所以,最终确定的实验溶剂为正丙醇、正丁醇、异丁醇、仲丁醇和丙酮。杨梅素在以上五种溶剂中的溶解度如表1所示,在实验选取的纯溶剂中,杨梅素溶解度均随着温度的上升而增大。在温度小于298.15 K时,不同溶剂中溶解度顺序为仲丁醇>正丙醇>异丁醇>丙酮>正丁醇;在温度大于等于298.15 K时,不同溶剂中溶解度顺序为仲丁醇>正丙醇>异丁醇>正丁醇>丙酮;而溶剂的极性顺序为正丙醇(61.7)>正丁醇(60.2)>异丁醇(55.2)>仲丁醇(50.6)>丙酮(35.5)[7],说明极性并不是影响杨梅素溶解度的唯一因素,杨梅素中含有多个羟基并且含有双键和苯环结构,其与溶剂分子间的相互作用力以及氢键都会影响溶质的溶解度。
3.3 模型拟合
杨梅素的溶解度较低,采用传统的重量法或动态法测量溶解度是不合适的,本研究中采用的HPLC法可以更为精确地测定溶解度较小的物系的溶解度。分别用van't Hoff方程、Apelblat方程和λh方程对溶解度数据进行了拟合,拟合曲线与数据点如图3所示。拟合结果如表2所示,三种模型对杨梅素溶解度的拟合相关性较好,就ARD值而言,Apelblat方程的平均相对偏差均小于0.37%,拟合效果要优于van't Hoff方程和λh方程。原因是相比于van't Hoff方程,Apelblat方程存在一个clnT的修正项。


(a)van't Hoff 方程,(b) Apelblat方程,(c) λh方程 图3 不同热力学模型拟合的杨梅素溶解度图 Fig.3 Solubility of myricetin fitted by different thermodynamic models 表2 在五种纯溶剂中van't Hoff方程,Apelblat方程,与λh方程对杨梅素溶解度拟合的模型参数Table 2 Parameters for the van't Hoff,Apelblat and CNIBS/R-K models for the solubility of myricetin in five pure solvents

表2(续)
4 结论
采用HPLC法测定了杨梅素在正丙醇、正丁醇、异丁醇、仲丁醇和丙酮五种纯溶剂中的溶解度,测定的温度范围为283.15~308.15 K。发现在实验选取的纯溶剂中,杨梅素溶解度均随着温度的上升而增大。采用van't Hoff方程、Apelblat方程和λh方程对溶解度数据进行关联,Apelblat方程拟合效果最佳,其平均相对偏差均小于0.37%。该溶解度数据为杨梅素的结晶制备过程提供了数据基础。

