环磷酰胺对以KLH为特异性抗原BALB/c小鼠TDAR实验定量分析①
杨照新 田树红 黄绵庆 刘 莹 林春华 肖 敏 黄 凌
(海南医学院,海口 571199)
目前T细胞依赖性抗体反应(T cell-dependent antibody response,TDAR)实验被认为是能够较好地检测药物免疫毒性反应的功能性实验,它通过引入异体抗原,反映机体免疫功能,以预测药物的免疫毒性,并在免疫毒理学研究中得到广泛重视[1,2]。本研究通过制备BALB/c小鼠免疫功能低下的模型动物,以血蓝蛋白(Keyhole limpet hemocyanin,KLH)作为T细胞依赖性抗原,分析和考察环磷酰胺对小鼠TDAR的影响,并对外周血淋巴细胞亚群及免疫器官形态学等指标进行综合分析和评价,探讨以KLH为特异性抗原的TDAR实验定量分析的应用价值,现报道如下。
1 材料与方法
1.1材料
1.1.1动物 SPF级BALB/c小鼠36只,雌雄各半,体重16~20 g,由湖南斯莱克景达实验动物有限公司提供,实验动物生产许可证:SCXK(湘)2016-0002;所有动物饲养均在海南省药物安全性评价研究中心屏障设施内,实验动物使用许可证:SYXK(琼)2016-0013,所用实验动物均经海南省药物安评中心动物伦理委员会批准,并按实验动物使用的3R原则给予人道关怀。
1.1.2试剂 酶标板购自Jet Biofil公司;Goat Anti-Mouse IgG/HRP酶标二抗购自北京博奥森生物技术有限公司;吐温20(Tween20)购自Aladdin公司;PBS购自博士德生物工程公司;KLH购自Sigma公司;CD3-Percp、CD4-APC、CD8-PE、CD19-FITC抗体均购自美国BD公司;环磷酰胺购自德国Baxter Oncology Gmbh;HE染液购自珠海贝索生物技术有限公司。
1.1.3仪器 Multiskan FC型全波段酶标仪(Ther-mo Scientific赛默飞世尔科技);BD Accuri C6 Flow Cytometer型流式细胞仪(BD biosciences公司)。
1.2方法
1.2.1实验分组及动物模型的建立 分组:BALB/c小鼠按体重随机平均分为阴性对照组、平行对照组和环磷酰胺组;造模方法:平行对照组和环磷酰胺组腹腔注射环磷酰胺,给药剂量40 mg/kg,阴性对照组腹腔注射等体积0.9%氯化钠注射液,间隔 24 h追加给药一次,常规饲养。
1.2.2KLH免疫方法[1]造模给药后5 d(即第6天),阴性对照和环磷酰胺组经腹腔进行KLH免疫,免疫剂量为5 mg/kg,首次免疫后第7天加强免疫1次,平行对照组不予免疫;末次免疫后第8天,所有实验动物采集EDTA-2K抗凝血和血清。
1.2.3小鼠TDAR实验定量检测方法 KLH包被浓度为80 μg/ml;待检样品血清的稀释度为1∶400;Goat Anti-Mouse IgG/HRP酶标抗体的稀释度为1∶16 000;每个待检样品均设复孔,实验结果以OD值表示。
1.2.4小鼠TDAR实验定性检测方法 KLH包被浓度为20 μg/ml;待检样品血清的稀释度为1∶5;Goat Anti-Mouse IgG/HRP酶标抗体的稀释度为1∶16 000;每个待检样品均设复孔,定性结果的判定标准为当(样品血清OD值-空白OD值) / (阴性血清OD值-空白OD值)>2.1,即认为是阳性。
1.2.5免疫细胞检测方法 应用流式分析技术检测外周血CD3+CD4+、CD3+CD8+T淋巴细胞及CD3-CD19+B淋巴细胞百分比;分离脾脏,4%中性甲醛固定,常规HE染色。
1.3统计学分析 使用微软Office Excel 2007和SPSS24.0软件进行统计学分析,计量资料组间比较采用单因素方差分析,定性结果分析采用χ2检验,P<0.05表示差异具有统计学意义。
2 结果
2.1各组淋巴细胞亚群变化 流式细胞术检测结果发现与阴性对照相比环磷酰胺对淋巴细胞具有明显免疫抑制作用,能够明显降低外周血CD3+CD4+、CD3+CD8+T细胞数量和CD3-CD19+B细胞数量(P<0.05);同时平行对照组和环磷酰胺组之间CD3-CD19+B细胞数量具有明显差异(P<0.05),说明KLH能够刺激外周血B淋巴细胞的增殖,见表1。
2.2各组实验动物外周血清KLH IgG抗体产生情况 血清KLH IgG抗体定量分析结果显示,与阴性对照相比,环磷酰胺能够降低外周血KLH IgG抗体产生数量(P<0.05),而定性分析结果(χ2检验)却无统计学意义(P>0.05),见表2、3。

GroupsLymphocyte subsets(%)CD3+CD4+T cellCD3+CD8+T cellCD3-CD19+B cellControl46.55±3.9713.67±1.7333.86±5.28Parallel control 28.00±4.971)7.60±1.481)15.16±3.211)Cyclophosphamide31.97±7.731)9.56±1.671)19.40±1.411)2)
Note:Compared with the control group,1)P<0.05;compared with the parallel control group,2)P<0.05.


GroupsKLH IgG(OD)Control1.39±0.18Parallel control group 0.17±0.02Cyclophosphamide group 0.65±0.111)2)
Note:Compared with the control group,1)P<0.05;compared with the parallel control group,2)P<0.05.
表3 各组实验动物外周血清KLH IgG抗体定性分析结果(n=12)
Tab.3 Results of KLH IgG in various groups(n=12)

GroupsKLH IgG+-Control120Parallel control group 012Cyclophosphamide group 111Total2313
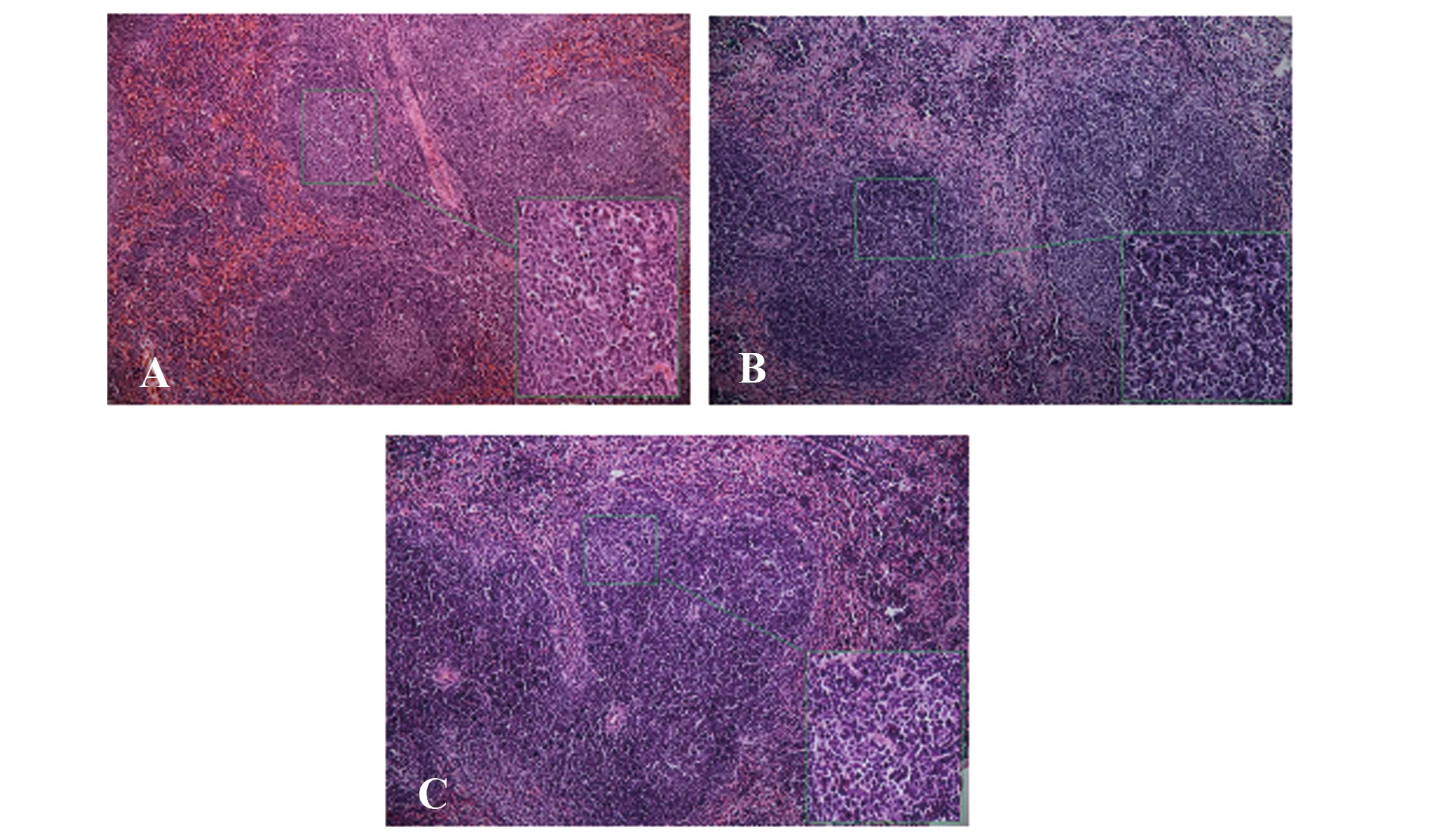
图1 各组脾脏病理组织学结果示例图(×200)Fig.1 Histopathological results of spleen in each group(×200)Note: A.The lymphoid follicles and germinal centers in splenic corpuscles were formed,a small amount of B lymphocyte apoptosis was observed,and the cells in marginal zone increased;B.The cells were loosely arranged and there were a large number of necrotic cells in the splenic sinus;C.The cells were loosely arranged,and the lymphoid follicles and germinal centers in splenic corpuscles were slightly formed and marginal cells were slightly increased,and there were a large number of necrotic cells in the splenic sinus.
2.3各组脾脏病理组织学结果 脾脏组织病理组织学检查结果显示环磷酰胺对脾脏有明显毒性反应,可以使脾脏内淋巴细胞数量减少,坏死细胞增多,边缘区细胞数量减少;同时KLH能够刺激脾小体内生发中心的形成,见图1。
3 讨论
TDAR实验是机体接触特异性抗原后产生特异性抗体的过程,它涉及一系列免疫反应,包括B细胞、T细胞等多种免疫细胞的参与。该途径出现任何问题均能导致特异性抗体生成障碍,因此该方法在药物免疫毒理学研究中逐渐得到广泛应用[2,3]。但受抗原标准化和检测方法的限制,目前该方法在实际应用中也存在诸多问题。首要问题就是抗原的标准化,KLH是具有高度免疫原性的蛋白,比绵羊红细胞(Sheep red blood cell,SRBC)更易获得,性质更稳定,更适合作为标准化的T细胞依赖性抗原[4]。Lebrec和Peachee等[5,6]研究发现KLH作为抗原,比SRBC法变异性更小,结果更稳定。其次在于特异性抗体的检测手段,目前大多抗体检测手段均为定性或半定量检测,难以客观准确地反映药物对机体的免疫抑制作用,因此TDAR实验如能进行定量分析,将能极大提高该方法的实用性。
本文通过KLH IgG抗体定性和定量两种分析方法研究发现,环磷酰胺能够降低外周血清KLH 特异抗体产生量,与阴性对照组进行定量分析比较,差异具有统计学意义(P<0.05),但是定性分析差异无统计学意义(P>0.05),说明TDAR实验定量分析方法能够很好地反映环磷酰胺对机体的免疫抑制作用。同时如能结合淋巴细胞亚群和免疫组织器官组织学检查,能够更全面地评价药物对免疫系统的抑制作用。例如本文研究中发现环磷酰胺除了能够明显降低外周血清KLH IgG抗体产生量外,还能够降低外周血CD3+CD4+、CD3+CD8+T淋巴细胞及CD3-CD19+B淋巴细胞数量,同时对脾脏等组织器官也有明显毒性反应,具有明显免疫抑制作用。有文献报道环磷酰胺能够抑制免疫细胞增殖,尤其对B淋巴细胞,能够通过减少B淋巴细胞而降低相应抗体的生成[7]。
通过上述研究发现以KLH为特异性抗原的TDAR定量分析方法能够很好地预测药物的免疫抑制作用,应用这种定量分析检测方法,能够提高TDAR实验的灵敏性及实用性,特别是在评价一些肿瘤化疗药的免疫抑制程度、提高检测药物潜在免疫毒性的灵敏性上,具有重要应用价值。

