马凡综合征合并胸腹主动脉瘤的手术治疗及早中期结果
马明星,常 谦,于存涛,舒 畅,钱向阳,孙晓刚,魏 波,胡晓鹏
中国医学科学院 北京协和医学院 国家心血管病中心 阜外医院心血管外科,北京 100037
马凡综合征(Marfan syndrome,MFS)是常染色体显性遗传性结缔组织疾病,由编码原纤维蛋白原-1基因突变引起,病理改变是主动脉中层囊性变性与弹力纤维断裂造成主动脉壁薄弱,是胸腹主动脉瘤(thoracoabdominal aortic aneurysm,TAAA)的重要病因之一。TAAA自然预后差,5年内破裂率约20%[1]。胸腹主动脉替换术是治疗TAAA的标准方式[2]。然而,对比MFS和非MFS患者TAAA手术治疗效果的研究较少。本研究回顾性分析2009年1月至2017年12月MFS患者在中国医学科学院阜外医院接受胸腹主动脉替换术的早中期结果,以期评价MFS对TAAA外科治疗结果的影响。
对象和方法
对象和定义 选取2009年1月至2017年12月在阜外医院接受胸腹主动脉替换术的156 例TAAA患者纳入本研究,其中MFS患者58 例为研究组(M组),非MFS患者98 例为对照组(N组)。MFS诊断依据改良Ghent标准,需综合评价包括家族史、主动脉根部Z评分、晶状体脱位 、致病性原纤维蛋白-1基因突变和全身系统评分(基于腕指征、鸡胸、漏斗胸或胸部不对称、足跟畸形、平足、气胸、硬脊膜膨出、髋关节内陷、上部量/下部量、臂长/身高、脊柱侧凸或后凸、面征、皮纹征、近视大于300 度、二尖瓣脱垂)[3]。解剖分型依据Crawford分型标准[4]。术后30 d死亡包括术中死亡、院内死亡或转院后死亡。术后肾功能衰竭依据改善全球肾脏病组织指南[5],定义为血肌酐水平超过基础值3倍,或≥353.6 μmol/L,或需要透析者。肺部并发症包括气管切开、再次气管插管、呼吸机辅助>72 h和肺部感染。脊髓损伤:即时为术后清醒时即已出现;延迟为术后清醒时无损伤表现;截瘫为双下肢肌力0级;轻瘫为双下肢肌力1~4级。脑卒中为有神经系统症状,头部CT有影像学证据。
手术指征 (1)MFS患者:胸腹主动脉瘤体直径≥5.0 cm,或者扩张速度≥0.5 cm/年;非MFS患者:胸腹主动脉瘤体直径≥5.5 cm,或者扩张速度≥1.0 cm/年。(2)出现胸背痛、腹痛症状,用其他病因不能解释的;(3)主动脉瘤已经破裂或有破裂倾向者。
手术方法 所有胸腹主动脉替换手术均采用四分支人工血管(Hemashield;MAQUET,Wayne,NJ),依具体病情在不同循环管理方式(直接阻断、深低温停循环、股-股转流和主动脉-髂动脉转流)下完成手术。所有患者均采用双腔气管插管,左后外侧胸部切口,断肋弓,弧形切开膈肌显露胸主动脉,腹膜外显露腹主动脉,顺序分段阻断下完成手术。依具体病变解剖,在适宜水平端端吻合人工血管主干完成近端主动脉重建,阻断钳置于腹腔干上方,切开胸降主动脉,清理血栓和/或剥离的夹层内膜片,“肋间动脉卷”法重建T8-L2间通畅的肋间动脉[6],通常腹腔干、肠系膜上动脉和右肾动脉开口周围主动脉壁修剪成血管片端端吻合于人工血管主干远端,或者对于MFS及内脏动脉开口相距较远者采用分支重建,左肾动脉、双侧髂动脉分别与分支血管吻合重建完成手术。
随访 全部患者通过门诊和电话完成随访,心脏彩超和主动脉CT血管成像在出院前,出院后3、6个月分别完成,以后每年复查1次。
统计学处理 使用SPSS 24.0统计软件(IBM Corp,Armonk,NY)进行数据处理。连续变量用均数±标准差(范围)或中位数(四分位数)描述,组间比较采用t检验或Mann-WhitneyU检验。分类变量用例数(百分比)描述,组间比较采用卡方检验或Fisher精确检验。对于生存分析和免于再干预分析采用Kaplan-Meier方法分析,Log-rank检验比较两组生存率和免于再干预率的差异。P< 0.05 为差异有统计学意义。比较两组术后早期死亡率、并发症发生率、中期随访的生存和再干预情况。
结 果
术前一般情况 MFS组患者较非MFS组更年轻(t=9.603,P=0.000),有家族史者更多(χ2=19.996,P=0.000),男性和吸烟者比例更低(χ2=11.489,P=0.001;χ2=17.686,P=0.001),其余方面差异均无统计学意义(P均>0.05)(表1)。

表1 两组患者术前一般情况比较Table 1 Comparison of preoperative characteristics between two groups
MFS:马凡综合征;—:Fisher精确检验,无统计值
MFS:Marfan syndrome;—:Fisher exact test without statistic
手术情况及术后早期情况 两组在急诊手术比例、预防性脑脊液引流、手术时间、术中循环管理方式、术中用血量方面差异均无统计学意义(P均>0.05)(表2)。


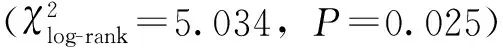
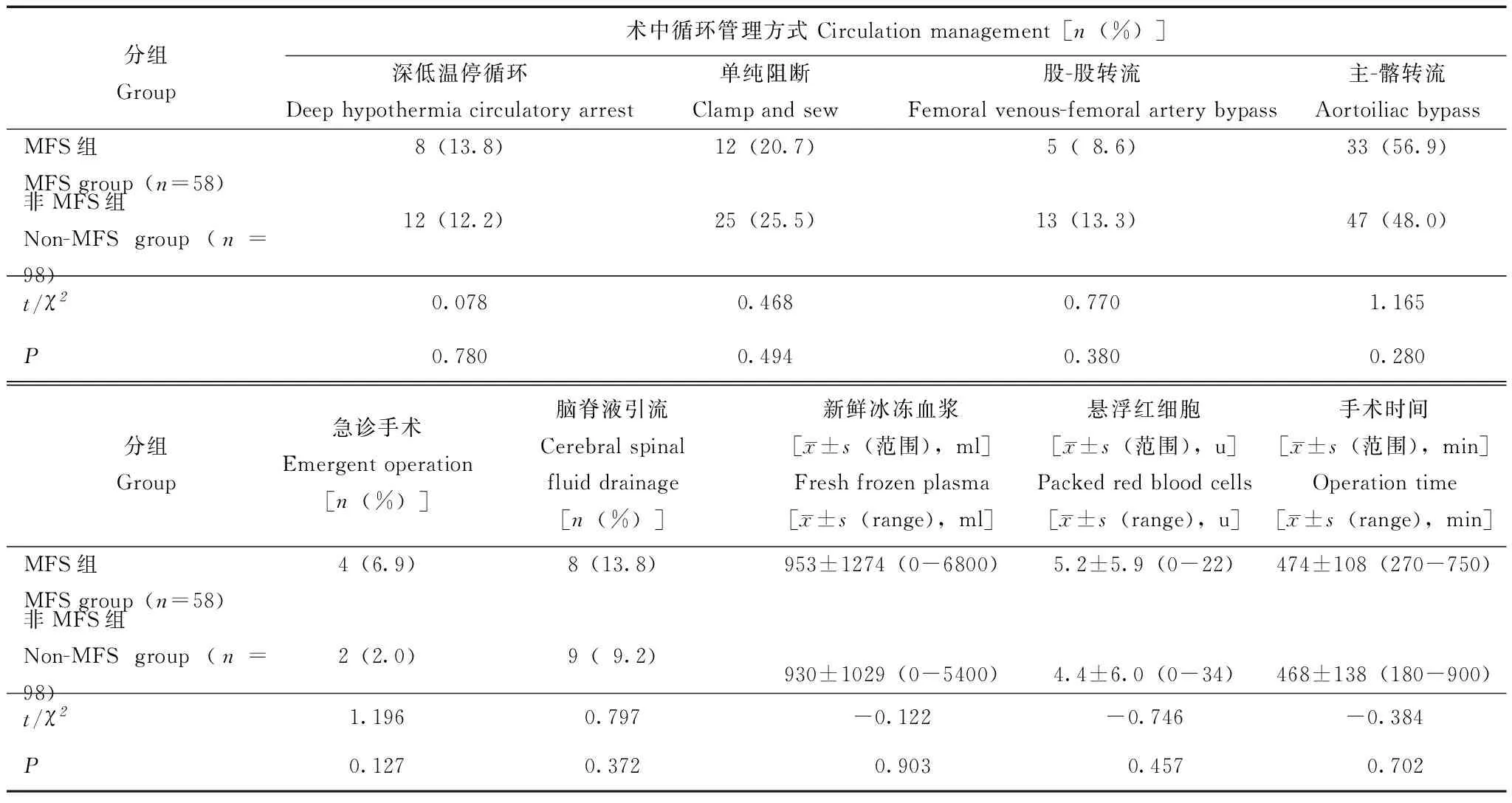
表2 两组术中情况比较Table 2 Comparison of intraoperative details between two groups
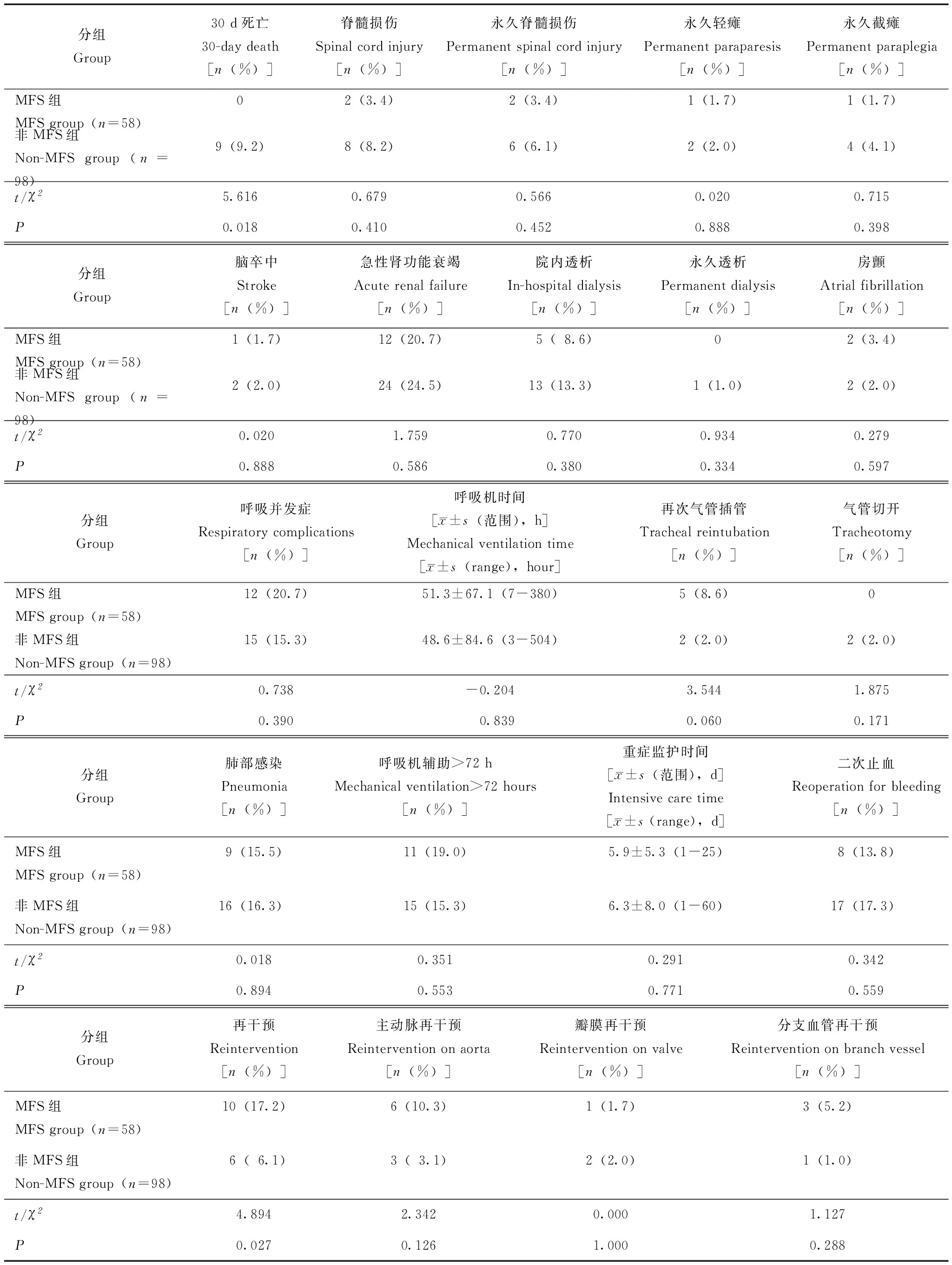
表3 两组术后早期情况和再干预情况比较Table 3 Comparison of early postoperative outcomes and reinterventions between two groups
讨 论
TAAA累及多个重要脏器,又因MFS的病理特点,主动脉组织脆弱,部分患者合并夹层病变,使手术难度大、创伤大、出血和脏器损伤风险高,远期可能形成吻合口假性动脉瘤,且保留的自体主动脉组织可能继续瘤样扩张[7-8]。因此MFS患者TAAA术后结果值得关注。
目前世界最大单中心TAAA研究报道了30年3309例手术结果显示,手术死亡7.9%,脊髓损伤9.6%,肾功能衰竭12.3%,透析7.6%,其结果显示,主动脉替换范围最广的Crawford-Ⅱ型和年龄增加仍是增加手术死亡及并发症风险的重要危险因素[9]。因此,手术策略需要在尽可能多切除自体主动脉组织和尽可能降低围手术期风险间寻求平衡。
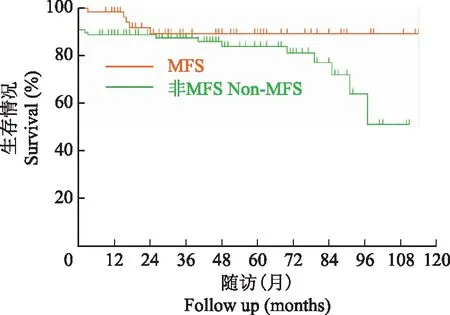
图1 MFS和非MFS患者在胸腹主动脉替换术后的中期生存曲线
Fig 1 Midterm survival curves after open repair of thoracoabdominal aortic aneurysm in patients with and without MFS

图2 MFS和MFS患者在胸腹主动脉替换术后的中期免于再干预情况
Fig 2 Curves of free from reintervention in patients with and without MFS after open repair of thoracoabdominal aortic aneurysm
由于MFS患者的全程主动脉都具有自发扩张及破裂的趋势,外科医生倾向于对此类患者采取更为广泛的胸腹主动脉替换方式,但是其术后早期死亡率较退行性病变者低。本研究MFS组和非MFS组中Crawford Ⅱ型TAAA的比例相近,分别为89.7%和77.6%(P=0.057),而两组的术后30 d死亡率差异有统计学意义,分别为0和9.2%(P=0.018),其原因与MFS组患者较非MFS组患者更加年轻有关(t=9.603,P=0.000)。多因素Logistic分析显示,年龄增加是术后早期死亡的独立危险因素(OR=1.153,P=0.010)。美国国家手术质量改进计划数据库中2005至2016年1048例TAAA患者资料显示,平均年龄为67岁,以退行性动脉瘤为主,其中MFS者仅占0.9%,围手术期死亡率为14%[10]。而几项关于MFS患者TAAA手术结果的研究显示,平均年龄为38.5~45.0岁,50%~79%为Crawford Ⅱ型TAAA,手术死亡0~4%[11-13]。与本研究结果相似,Mommertz等[14]在研究中比较了MFS患者和非MFS患者的TAAA术后结果,MFS患者较非MFS患者更为年轻(中位年龄分别为40和66岁),手术死亡率也更低(分别为0和12.4%)。
截瘫是TAAA术后的灾难性并发症,其核心机制是围手术期脊髓的缺血和再灌注损伤。胸主动脉近端阻断后,来自锁骨下动脉和内脏动脉的侧支循环网对于维持脊髓血供非常重要。本组共8例患者发生永久脊髓损伤,可能与术中侧支循环建立不良有关。其中,3例为Ⅰ型夹层行全主动脉弓替换时重建的左侧锁骨下动脉失败、闭塞,1例为Ⅲ型夹层行覆膜支架腔内介入治疗时部分覆盖左锁骨下动脉开口致其严重狭窄,均影响来自上段的侧支循环。内脏动脉开口段主动脉真腔狭小、假腔大量血栓形成(1例)和主动脉破裂后内脏动脉附近大范围血肿压迫(1例)均导致内脏动脉灌注差,可能影响远端侧支循环的有效建立。1例MFS合并急性Ⅲ型主动脉夹层患者,胸主动脉近端吻合时远端平均灌注压只能维持在60 mmHg(1 mmHg=0.133 kPa)左右,术后出现急性肾功能衰竭和下肢轻瘫,另1例为覆膜支架腔内介入治疗术后合并内漏的慢性Ⅲ型夹层患者,术后早期出现短期的低血压,麻醉清醒后即发现双下肢轻瘫,2周后恢复为肌力4级。 这2例的围手术期低灌注状态可能是脊髓损伤的重要原因。因此,术前注意识别可能影响脊髓侧支循环建立的危险因素,术中及术后维持适当的灌注压,减少脊髓缺血时间,必要时进行腹腔干和肠系膜上动脉选择性灌注可能有利于建立脊髓侧支循环,减少脊髓损伤。
脑脊液引流是降低脊髓损伤风险的有效措施[15]。由于担心蛛网膜下腔穿刺可能导致出血并发症,且术中全量肝素化可加重这一情况,本院没有常规预防性应用脑脊液引流技术。尽管没能得出关于脑脊液引流的有统计学意义的结果,但是17例应用预防性脑脊液引流者未出现任何程度的脊髓损伤,8例患者出现脊髓损伤后立即采用治疗性脑脊液引流,其中1例轻瘫患者完全恢复,1例肌力恢复为4级,其余无变化。因此,今后应更加重视预防性脑脊液引流的应用。
对比MFS和非MFS患者TAAA手术后随访结果的研究较少。早年日本报道的MFS患者平均年龄为39.3岁,1年和5年生存率为88.5%和81.7%[16]。近期美国报道的此类患者平均年龄为43.4岁,2年和8年生存率为87%和75%,2年和8年免于再干预率为94%和86%,合并结缔组织疾病患者的TAAA术后5年免于再干预率为85%[17]。另外一项研究中,Coselli等[9]报道的3309例TAAA患者手术结果(其中MFS患者比例仅为8.7%)中,平均年龄67岁,1、5和10年生存率分别为83.5%、63.6%和36.8%,5和10年免于再干预率分别为97.9%和95.3%。由此可见,MFS患者在TAAA手术时较非MFS者明显年轻,术后1年生存率与之基本相当,5或8年以后的生存率明显优于非MFS患者,但是5或8年以后的免于再干预率差于非MFS患者。
由于手术降低了主动脉破裂风险,患者的中期生存情况较好,两组5年生存情况无差异,但是MFS组1和5年生存率略优于非MFS组,可能与全组患者整体比较年轻有关。而MFS组再干预情况明显多于非MFS组,与文献报道相似。
未处理的近端主动脉为常见的再干预区域。MFS组中6例为主动脉近端及弓部再干预,其中2例为原有病变,4例为病变进展,均顺利接受开放手术。
重建肋间动脉和内脏动脉时应尽量少地保留自体主动脉组织,以减少扩张瘤变可能。2018年Coselli等[8]在再次胸腹主动脉手术研究中发现,内脏动脉血管片动脉瘤多见于年轻、有结缔组织疾病者和夹层病变者。Kulik等[18]报道11例肋间动脉片动脉瘤中5例为MFS患者。本研究MFS组随访中观察到1例在术后11个月出现“肋间动脉卷”动脉瘤,成功实施介入封堵治疗,未出现截瘫症状。目前尚未出现吻合口假性动脉瘤和内脏动脉血管片动脉瘤。
鲜有文献报道胸腹主动脉替换术后分支血管动脉瘤再干预。本研究随访中发现3例此类病例,均为MFS患者。1例为锁骨下动脉瘤,经开放手术切除动脉瘤,人工血管完成重建。胸廓内动脉瘤很罕见,仅为个例报道[19-20]。本研究随访中发现2例胸廓内动脉瘤,均采用弹簧栓成功封堵,远期效果仍待密切随访。
对于MFS患者,介入治疗后内漏、继发夹层、破裂等并发症较多[21]。除特殊情况,如主动脉破裂、急性主动脉夹层合并脏器灌注不良等需要紧急过渡治疗外,目前指南不推荐介入治疗应用于MFS患者[2]。
本研究为单中心、回顾性研究,样本量小,随访时间短,而且胸腹主动脉瘤病变范围、既往病史差别大,影响样本均一性,可能使结果产生偏倚,有待于多中心、大样本和前瞻性队列研究及长期的随访结果。
综上,本研究显示MFS患者TAAA术后早期死亡率低于非MFS患者,中期生存情况与非MFS患者相似,但再干预率明显高于非MFS患者,术后密切随访非常重要,以便及时完成再干预。

