微波辅助提取-分散固相萃取净化-超高效液相色谱-串联质谱法测定畜禽肉中的7种非选择性环氧化酶抑制药物残留
励 炯,林伟杰,曹青文,金朦娜,邱红钰
(杭州市食品药品检验研究院,浙江杭州310017)
非选择性环氧化酶(COX)抑制药物是属于非甾体类抗炎药物(Nonsteroidal Anti-Inflammatory Drugs,NSAIDs)中的一大类药物,具有抗炎、止痛和解热功能,临床上主要应用于缓解肌肉、关节及炎症免疫性疾病的局部疼痛、肿胀等治疗[1-3]。由于非选择性COX抑制药物价格低廉、疗效好,被广泛应用于养殖业中,用于食源性动物的感染性炎症的预防和治疗[4]。近年来,非选择性COX抑制药物在禽畜类养殖业中有滥用的趋势,而食用含有非选择性COX抑制药物残留的肉类产品会对机体产生极大的副作用。欧盟已经规定了部分非选择性COX抑制药物的最大残留量[5-7]。
水体中非选择性COX抑制药物的检测研究已经有很多文献报道[8-10],但由于畜禽肉基质的复杂性,没有检测畜禽肉中较低含量非选择性COX抑制药物残留的相关报道。复杂基质的样品,比如土壤中非选择性COX抑制药物的检测方法已有研究[11-14],其前处理方法主要通过溶剂萃取[15]、微波辅助提取[16]、超声提取[17]、加压溶剂萃取[18]、QuEChERS法[19]等来提取非选择性COX抑制药物残留。样品经提取后,用一定填料的固相萃取(SPE)进行净化处理。而检测方法有气-质(GC-MS)联用法[20-21]、高效液相色谱法(HPLC)[22-23]以及液-质(HPLC-MS/MS)联用法[24-26]。本文通过用微波辅助萃取,结合分散固相萃取(MAE-DSPE),对畜禽肉中非选择性COX抑制药物残留进行提取及净化,采用兼顾灵敏度高及抗干扰性强的超高效液相色谱-串联质谱法(UPLC-MS/MS),对畜禽肉中的7种非选择性COX抑制药物残留进行定性定量分析。本法简便、灵敏、高效,可满足畜禽肉的质量监测需求。
1 实验部分
1.1 仪器与试剂
Agilent 1290高效液相色谱仪、Agilent 6425串联四极杆质谱仪(美国,Agilent公司);Mars 5高压微波消解仪(美国,CEM公司);MultiReax萃取仪(德国,Heidolph公司);Mili-Q去离子水发生器(美国,Millipore公司);MS3旋涡混合器(德国,IKA公司)。
标准品:水杨酸、布洛芬、双氯芬酸钠、吲哚美辛、吡罗昔康、萘普生和保泰松,均购自中国食品药品检定研究院;甲酸铵、NaCl、无水MgSO4、无水Na2SO4、无水柠檬酸钠、柠檬酸氢二钠(分析纯,购自国药集团化学试剂有限公司);乙腈、甲酸、乙酸乙酯、丙酮(色谱纯,德国Merck公司);十八烷基键合硅胶吸附剂(C18)和NH2-丙基乙二胺吸附剂(NH2-PSA)购自上海岛津技术公司。
1.2 样品前处理
1.2.1 提取 精密称取5.0g猪肉,置于高压微波消解罐中,加入85%乙腈水溶液(pH=2)10mL,微波提取功率为400W,经8min温度由室温升至90℃,然后90℃保持15min进行提取,冷却后置于50mL聚氟乙烯离心管中,加入6g无水 MgSO4,1.5g NaCl,1.5g无水柠檬酸钠和0.75g柠檬酸氢二钠,漩涡振荡1min。将有机相层移入一新的50mL聚氟乙烯离心管中,待净化。
1.2.2 净化 在待净化样液中加入净化剂(内含2 000mg无水 Na2SO4、500mg C18及300mg NH2-PSA),旋涡混匀1min,以4 000r/min的速度离心5min后,全部转移至试管中,于40℃水浴下氮吹至近干。加入1mL含0.1%甲酸的水溶液-含0.1%甲酸的乙腈溶液(90∶10,V/V),旋涡混匀1min溶解残渣,用0.22μm微孔有机滤膜过滤。
1.3 仪器条件
1.3.1 色谱条件 Waters CORTECS C18色谱柱(100×2.1mm,1.7μm);流动相:A 相为含0.1%甲酸的水溶液,B相为含0.1%甲酸的乙腈溶液;梯度洗脱程序:0~8min,90%~45%A;8~9min,45%A;9.1~12min,90%A。柱温:40℃;流速:0.4mL/min,进样量1μL;运行时间:12min。
1.3.2 质谱条件 电喷雾离子源(ESI+和ESI-);多反应监测(MRM)模式;干燥气温度:200℃;干燥气流速:14L/min;毛细管电压:3.5kV;毛细管出口电压(Fragmentor):380V;校准方法:质量轴自动调谐校正;MRM 进行分段扫描:0~4.5min,水杨酸;4.5~6.0min,吡罗昔康;6.0~7.5min,萘普生;7.5~8.85min,吲哚美辛、双氯芬酸钠和布洛芬;8.85~12.0min,保泰松。其他质谱分析参数详见表1。
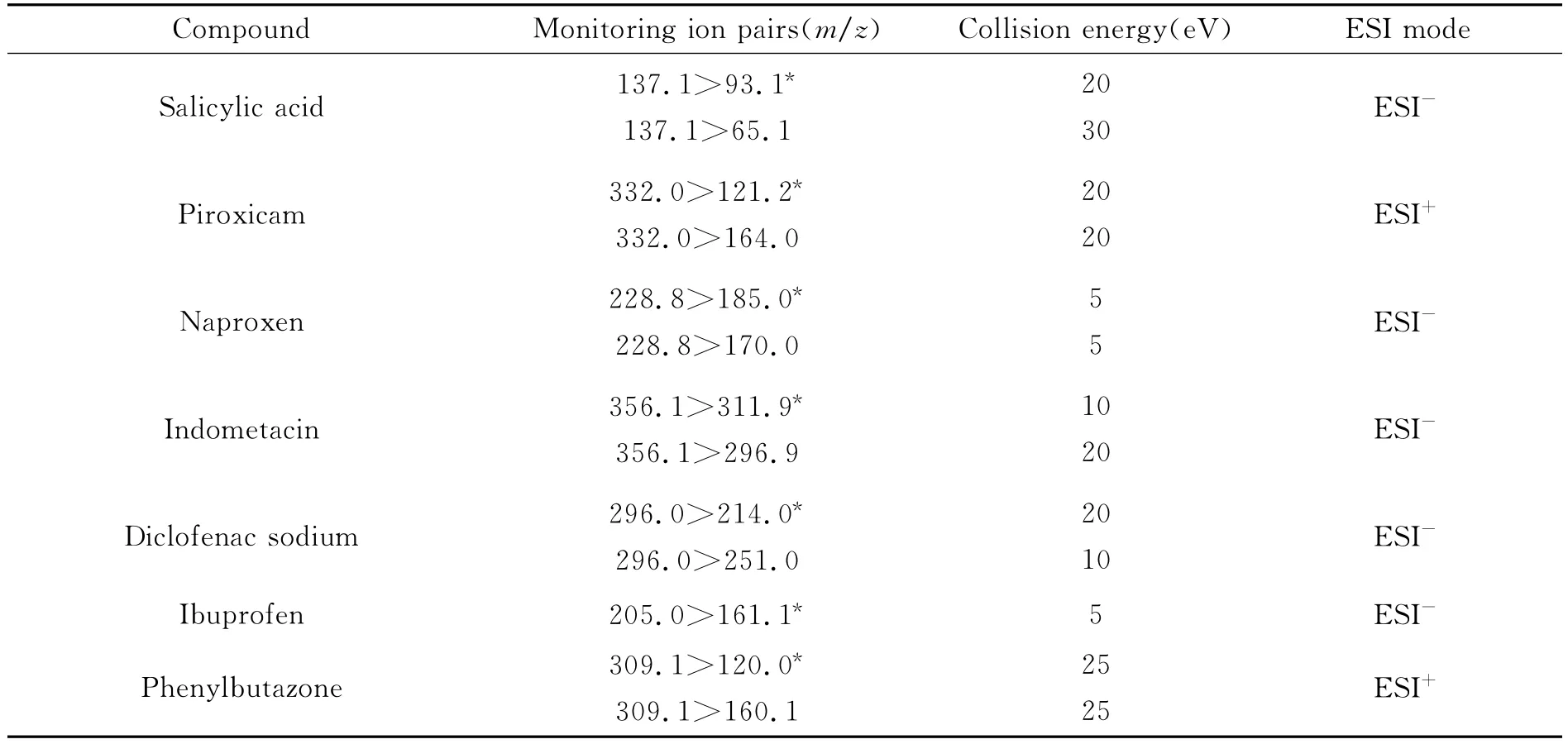
表1 7种非选择性COX抑制成分的质谱分析参数Table 1 MS parameters of 7non-selective cyclooxygenase inhibitors
2 结果与讨论
2.1 质谱和色谱条件优化
除了吡罗昔康和保泰松两种成分在ESI+模式下的灵敏度较ESI-模式高,其余5种非选择性COX抑制剂在ESI-模式下灵敏度较高,在各自的模式下以m/z100~400扫描范围下对7种目标物进行一级质谱扫描,得到精确的母离子质荷比,优化毛细管电压后,进一步对7种目标物的二级质谱参数进行优化,详细参数参见表1。其中布洛芬的碎片离子只有一个,所以本文采用一个离子通道对畜禽肉中的布洛芬进行检测。
流动相中加入一定量的挥发性酸或者挥发性盐,能够增强目标化合物的离子化程度,而在ESI-模式下,流动相中加入一定量的甲酸可以提高分析物的灵敏度[25]。据此本文考察了以下三组流动相下的色谱行为:(1)A为含0.1%甲酸的水溶液,B为含0.1%甲酸的甲醇;(2)A为含0.1%甲酸的水溶液,B为0.1%甲酸的乙腈溶液;(3)A 为含0.1%甲酸的5mmol/L甲酸铵溶液,B为0.1%甲酸的乙腈溶液。结果发现将流动相(2)作为分析7种非选择性COX抑制剂的流动相时,7种目标物峰形较好,灵敏度满足要求。7种非选择性COX抑制剂的MRM色谱图见图1。
2.2 提取方式的优化
本文首先对提取溶剂进行考察,选用了三种常用的提取剂,包括乙腈、乙酸乙酯、丙酮进行回收率实验,结果发现采用乙腈作为提取溶剂时7种目标化合物的回收率均达到80%以上,而采用乙酸乙酯和丙酮提取时,布洛芬和萘普生的回收率均低于20%。已有文献报道采用微波辅助提取时,加入一定比例的水,有助于目标化合物的提取效率[11]。所以本文采用80%、85%、90%、95%、100%5组比例的乙腈水溶液进行回收率考察,结果发现当乙腈比例为85%时,7种目标化合物的回收率均高于80%,其余4组比例提取的布洛芬和萘普生的回收率普遍低于75%。除了有机溶剂类型和水的比例能影响目标化合物的提取效率,还有文献报道提取溶剂中水的pH值也会影响回收率[12],所以本文用1mol/L HCl调成4组不同的pH值(分别为2、3、4、5)的去离子水,配制成85%乙腈水溶液,结果当水的pH值为2时,7种目标化合物的回收率均最高,达到80%。所以本文采用85%乙腈水溶液(pH=2)作为畜禽肉类中的7种非选择性COX抑制药物的残留的提取溶剂。
同时我们对加入的提取盐组分进行考察,采用4组比例:(1)6g无水 MgSO4+1.5g NaAc;(2)4g无水 MgSO4+1g NaCl;(3)6g无水 MgSO4+1.5g NaCl+1.5g无水柠檬酸钠+0.75g柠檬酸氢二钠;(4)4g无水MgSO4+1g NaCl+1g无水柠檬酸钠+0.5g柠檬酸氢二钠。结果发现加入第3组比例的7种目标物回收率最高,均高于80%,其余3组的双氯芬酸钠的回收率均低于70%。所以本文采用6g无水 MgSO4,1.5g NaCl,1.5g无水柠檬酸钠和0.75g柠檬酸氢二钠组成的4种盐进行提取。

图1 7种非选择性COX抑制成分(20μg/L)的 MRM色谱图Fig.1 MRM chromatograms of 7non-selective cyclooxygenase inhibitors(20μg/L)Peak identifications:1.salicylic acid;2.ibuprofen;3.naproxen;4.diclofenac sodium;5.phenylbutazone;6.piroxicam;7.indometacin.
2.3 净化方式的优化
本文同时考察了两种常见的净化方式,包括分散固相萃取(DSPE)和固相萃取(SPE)净化。分散固相萃取净化见1.2节,SPE采用Oasis HLB固相萃取柱进行回收率考察。结果发现当用Oasis HLB固相萃取柱进行净化后,布洛芬和双氯芬酸钠的回收率均低于10%,所以本文采用DSPE净化法,提取液中加入内含2 000mg无水Na2SO4、500mg C18及300mg NH2-PSA组成的净化剂进行净化,7种目标化合物回收率均高于80%。
2.4 线性关系与检出限
采用猪肉空白基质配制10、20、50、80、100、200μg/L的基质标准系列溶液,以定量监测离子对的离子流中谱峰峰面积(Y)为纵坐标,标准溶液浓度(X,μg/L)为横坐标进行线性关系考察,结果见表2。7种非选择性COX抑制剂在各自线性范围内线性关系较好(r2均大于0.9965)。
取空白样品(检测结果为阴性的猪肉),加入适当稀释的混合标准品溶液,按样品制备方法制备供试品溶液,得信噪比为3和10时分别为7种非选择性COX抑制剂的检测限(LOD)与定量限(LOQ),结果见表2。

表2 7种非选择性环氧化酶抑制剂的线性关系、检测限和定量限Table 2 Regression equation,limits of detection and(LOD)and limits of quntifacation(LOQ)of 7non-selective cyclooxygenase inhibitors
2.5 方法回收率与精密度
取空白样品(检测结果为阴性的猪肉),分别在5、10、20μg/kg 3个添加水平下进行加标回收率实验,平行6份,结果见表3。7种非选择性COX抑制剂的三个浓度水平的平均回收率为81.3%~93.8%,相对偏差(RSD)为2.5%~7.6%。

表3 猪肉中7种非选择性COX抑制剂的回收率与精密度试验(n=6)Table 3 The recoveries and precision of 7non-selective cyclooxygenase inhibitiors in pork(n=6)
2.6 实际样品检测
利用本文建立的方法完成了50批次的畜禽肉产品(包括10批次猪肉,10批次牛肉,10批次羊肉,10批次鸡肉,10批次鸭肉)中7种非选择性COX抑制药物残留情况的检测,其中一批次的猪肉中检出布洛芬16μg/kg,一批次的牛肉检出双氯芬酸钠12μg/kg,检出样品的MRM色谱图详见图2。

图2 阳性样品的MRM色谱图(A为猪肉,B为牛肉)Fig.2 MRM chromatograms of positive samples(A:pork;B:beef)
3 结论
本研究建立了微波辅助提取-分散固相萃取净化-超高效液相色谱-串联质谱法测定畜禽肉类产品中7种非选择性COX抑制剂残留的分析方法,优化了仪器条件和样品前处理条件。以85%乙腈水溶液(pH=2)作为提取剂,经微波辅助提取,再加入6g无水 MgSO4,1.5g NaCl,1.5g无水柠檬酸钠和0.75g柠檬酸氢二钠组成的4种盐进行提取,再使用2 000mg无水 Na2SO4、500mg C18以及300mg NH2-PSA组成的净化剂进行净化处理。本方法简单、高效,有效地降低了基质效应,提高了分析方法的选择性和灵敏度,为畜禽肉中7种非选择性COX抑制药物残留的检测提供了一种较好的方法

