过氧化氢催化分解制备氧气的实验改进研究
王丽丽 吴暾艳 张艳华 谭宗俊
摘要: 在梳理二氧化锰催化过氧化氢分解实验中粉末状二氧化锰转化成颗粒状的研究成果的基础上,对二氧化锰颗粒化进行了系列研究和设计。通过实验验证,效果良好,便于一线教师操作和使用。对初中教材三种制备氧气方法进行了综合比较,认为过氧化氢催化分解法最优。
关键词: 二氧化锰; 过氧化氢; 催化分解; 实验改进 文章编号: 10056629(2019)6007303 中图分类号: G6338 文献标识码: B
1 该实验的不足和改进方法的文献综述
用二氧化锰催化过氧化氢分解生成氧气这个实验已经成为现行初中化学教材中的经典实验,尽管不同版本的初中教材对该实验的叙述和要求有所不同,但是教材中使用的二氧化锰都为粉末状是相同的。粉末状的二氧化锰与过氧化氢接触面积较大,反应速率较快,但是粉末状的二氧化锰存在以下问题: 过氧化氢与粉末状二氧化锰形成黑色的悬浊液在反应中不停翻滚,影响了实验现象的观察;由于反应速率较快,收集氧气时教师一个人操作有点困难,时常手忙脚乱、顾此失彼;另外,二氧化锰粉末颗粒非常小,不方便回收,所以大多数教师放弃回收而造成资源浪费和环境污染。
为了解决上述问题,很多研究者均考虑将粉末状的二氧化锰加工成块状(或颗粒状,或用胶水粘附,或用滤纸包裹等),达到使二氧化锰方便回收并可以重复使用之目的[1~9]。
基于上述已有研究成果,我们也试图寻找能够使二氧化锰粉末形成块状或颗粒状的简便易行的方法。
2 粉末状二氧化锰形成块状、颗粒状途径
用堵漏剂和乳白胶调和使二氧化锰粉末块状化
生活中下水道漏水时需要用堵漏剂修补时,在漏水处敷上调和好的堵漏剂会很快固化防止漏水,受此启示,用堵漏剂使二氧化锰粉末块状化。
实验药品: 二氧化锰粉末、堵漏剂、乳白胶
实验步骤:
(1) 用二氧化锰粉末和堵漏剂分别按照1∶1、 1∶2的质量比,加入适量水和乳白胶调和,乳白胶的主要成分是聚乙烯醇,无毒,可以和水以任意比例互溶。
(2) 将调和好的糊状混合物装入方形塑料袋中,压成约05cm厚的片状。
(3) 用切口整齐光滑的刀将步骤(2)中的物质切压成1cm左右的方格。(注意不要切破塑料袋,糊状混合物硬化的时间有10分钟左右,完全可以有时间从容做完这一步)
(4) 待两、三天完全硬化后,扳开即成為规则的小方块。
用熔化的石蜡使二氧化锰粉末颗粒化
蜡烛点燃时,固态蜡会受热液化,冷却又会转变为固体,用此性质使二氧化锰粉末颗粒化。
实验药品: 二氧化锰粉末、蜡烛
实验步骤:
(1) 点燃蜡烛,使熔化后的蜡滴入二氧化锰粉末中并不断搅拌,粉末粘附在蜡滴颗粒上。
(2) 冷却后用洗涤剂清洗颗粒外面附着不稳的粉末。
(3) 使用5%的过氧化氢溶液置于烧杯中,将固化的二氧化锰投入其中。进一步除去表面附着力不够的粉末,即可得到颗粒状的催化剂。
用补鞋胶水使二氧化锰粉末颗粒化
实验药品: 二氧化锰粉末、补鞋胶水
实验步骤:
(1) 将补鞋胶水滴入二氧化锰粉末中(补鞋胶水为成都因尔达胶业有限公司生产),边滴边来回摇动粉末,当滴入6~7滴后,胶水将粉末聚合成小圆球状。
(2) 固化后的颗粒用洗涤剂反复洗掉外层没有粘牢固的粉末后晾干备用。
用补鞋胶水固化二氧化锰粉末,补鞋胶水的主要成分为树脂,承受温度在80℃左右,比502胶水承受温度高,502胶水的主要成分为α氰基丙烯酸乙酯,使用时在空气中微量水的催化作用下发生加聚反应生成高分子化合物而粘合物体,承受温度60~70℃。因补鞋胶水固化速度比502胶水略慢,因此比502胶水固化二氧化锰后的颗粒更接近圆球状,美观度更好。
3 用块状二氧化锰催化剂做过氧化氢催化分解实验
常规实验
实验药品和仪器: 双氧水、块状或颗粒状二氧化锰催化剂(上述三种)、试管等
实验操作和现象:
(1) 取三支试管,分别放入适量的质量分数为5%的过氧化氢溶液和使用适量的三种不同材料制作的块状或颗粒状二氧化锰催化剂。三支试管中的催化剂表面都产生了大量的气泡,溶液澄清,将带有火星的木条伸入试管内,木条复燃。实验现象明显。
(2) 将颗粒状或块状的二氧化锰洗净、晾干、重复上述操作,现象依然明显。
制备氧气的实验
实验药品和仪器: 药品同31;仪器为锥形瓶、长颈漏斗、止气夹、玻璃导管,纱布
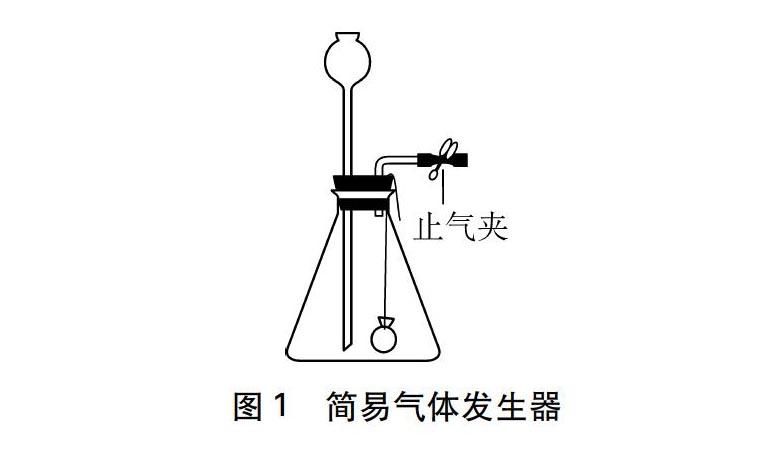
组成如图1所示的简易气体发生装置:
检查好气密性,将上面制成的块状固体用纱布包裹,用细线扎好吊于锥形瓶口,将5%的过氧化氢溶液30mL从长颈漏斗倒入,可以像实验室制备二氧化碳一样制备氧气。收集好一瓶氧气后,关闭止气夹,过氧化氢溶液被压入长颈漏斗,反应停止,打开止气夹反应继续进行。
意外的发现
在实验中,我们用15%左右的过氧化氢溶液与上述三种块状、颗粒状催化剂进行反应,发现使用补鞋胶和堵漏剂制作的催化剂都可正常使用,而使用蜡烛制作的催化剂出现了石蜡熔化,粉末状二氧化锰分散在过氧化氢溶液中的情况。究其原因,是因为过氧化氢浓度较大,反应速率较快,产生大量的热,而石蜡根据成份不同,在47~64℃之间可发生熔化。因此,某些气温较高的地区不适合使用。
4 结论
本文提供了三种简便易行的制作块状、颗粒状二氧化锰催化剂的方法。具有材料易得、操作简单、绿色环保、节约资源等益处。
材料易得
无论是堵漏剂、白乳胶、蜡烛还是补鞋胶都是生活中常见的物质,获取途径方便。
操作简单
无论选择何种材料来固化粉末狀二氧化锰,都只需要简单的几步操作即可。
三种制备氧气方法比较与建议
三种制备氧气方法比较
当前的初中化学教材中,只有沪教版介绍氧气制取时,教师的演示实验是用二氧化锰催化过氧化氢分解法。其他版本,或用KMnO4加热分解法,或用KClO3加热分解法,学生实验活动中,人教版安排的也是高锰酸钾加热分解法[10]。有研究者对三种方法作过比较[11],无论是从消耗资源、能源还是装置的简便性或者试剂的安全性以及对环境的绿色友好等,均是二氧化锰催化H2O2的方法更好[12]。
现行初中教材介绍的3种制备氧气的方法实验成本研究结果表明,按照2015年的试剂价格,制备32g氧气时3种方法不计算前二者酒精加热的费用,成本依次为: KMnO4 316元>KClO3 84元>H2O2 66元(其中二氧化锰成本4元[13],如果二氧化锰能够制备成规则的颗粒状便于回收从而反复使用,则成本仅26元),可以看出还是过氧化氢分解法成本最低。
建议
(1) 实验仪器试剂供应商可以在了解一线学校和学科教师需求的基础上,与试剂生产厂家联系,统一生产颗粒状或者方块状的二氧化锰,这样便于回收和重复使用,以解决学科教学的需求。
(2) 建议在初中化学教材再次改编时,无论是教师演示还是学生必做实验,实验室制备氧气时应选择采用二氧化锰催化过氧化氢分解法,此法不仅材料易得、操作简单、成本低,而且更能体现和落实绿色化学的理念。
参考文献:
[1] 白福秦, 何静. 氧气的实验室制法[J]. 化学教育, 1988, 9(1): 46.
[2] 王发应, 李太锐, 熊伦. 来自石膏像制作方法的启示[J]. 化学教学, 2015, (9): 61~62.
[3] 高改玲, 钱博. 用过氧化氢分解制取氧气[J]. 中学化学教学参考. 2002, (Z1): 77.
[4] 卢香宇. 过氧化氢制取氧气的新方法[J]. 化学教学, 2008, (3): 9~10.
[5] 顾鸣英, 丁伟. 实验室用过氧化氢制取氧气方法的改进[J]. 化学教学, 2009, (10): 18~19.
[6] 李焱. 二氧化锰催化分解过氧化氢的探究性实验设计[J]. 化学教与学, 2013, (9): 88.
[7] 王胤琪. 对二氧化锰催化过氧化氢制取氧气实验的改进[J]. 中小学实验与装备, 2013, 23(3): 38.
[8] 崔迎春. “分解过氧化氢制氧气反应中二氧化锰作用”的实验改进[J]. 中学化学, 2014, (1): 24.
[9] 中国教育装备行业协会.第三届全国中小学实验教学说课活动[R].广州:2015.
[10] 王晶, 郑长龙. 义务教育课程标准实验教科书·化学(九年级上册)[M], 北京: 人民教育出版社, 2012: 45~46.
[11][12][13] 潘国荣, 白显圣, 陈正美, 实验室制取氧气方法的对比及建议[J]. 化学教学, 2015, (9): 45~48.

