一种全新结构PDE-5抑制剂的成药性研究
黄艳妮,房绍英,刘 纯,郑晓霞,何小华,张洪坤,程艳玲*
(1.山东省药学科学院 山东省化学药物重点实验室,山东 济南 250101;2.山东商业职业技术学院,山东 济南 250101)
勃起功能障碍(erectile dysfunction,ED)是指在过去的3个月中,阴茎持续不能达到或维持足够的勃起以进行满意的性交[1],是男科常见的一种疾病。有研究表明,全球约有1.5亿的男性患有不同程度的ED,其中40岁以上男性发病率约为40 %,且随着年龄的增加ED发病率逐年升高,在超过70岁的男性中,ED的发生率为75 %[2]。ED的发生不仅与年龄有关,还与心理因素、手术创伤、生活习惯及心血管疾病等直接相关[3]。ED的产生会严重影响患者及伴侣的身体及心理健康,给家庭和社会带来沉重负担。
目前治疗ED的药物包括以下几类:5型磷酸二酯酶抑制剂(PDE-5)、平滑肌松弛药物、α-肾上腺素能受体抑制剂、5-羟色胺受体抑制剂、激素类药物、中药等[4]。在这些药物中,PDE-5抑制剂是治疗ED的一线药物,可用于各种原因导致的ED,其安全性和有效性在临床上得到广泛认可,已上市的PDE-5抑制剂类药物包括西地那非、他达拉非、伐地那非、阿伐那非、优地那非和米罗那非等7个药物[5-6]。
PDE-5抑制剂临床应用过程中,仍存在一些有效性及安全性问题,有研究发现[7],有约20 %的患者对PDE-5抑制剂无应答,且西地那非及伐地那非对PDE-6的选择性较差,临床使用过程中患者会出现视觉障碍的不良反应;他达拉非解决了对PDE-6的选择性问题,但对PDE-11有一定的抑制作用,临床使用过程中可能出现背痛症状,因此研发全新结构的新型PDE-5抑制剂用于治疗ED,具有重要的临床意义及社会意义。
1 仪器与材料
1.1 仪器
数显游标卡尺(桂林广陆数字测控公司);Scout SE型电子天平(奥豪斯公司);Thermo Fisher Ultimate 3000高效液相色谱仪(美国赛默飞世尔科技公司);API4500三重四级杆质谱仪(ABSCIEX中国公司);Eppendorf移液器(德国艾本德公司);AUW-120D型电子分析天平(日本岛津公司);MS3型漩涡混悬器(IKA公司);Z216MK高速冷冻离心机(德国哈默股份公司);Milli-Q Advantage A10超纯水仪[默克化学技术(上海)公司];EZ Reader Ⅱ酶标仪(Caliper公司)。
1.2 材料与试剂
化合物1(山东康迈祺,批号:PU-170617,纯度:99.67 %);枸橼酸西地那非(Maya-R提供,批号:MAYA-CR-1138,纯度:99.5 %);羧甲基纤维素钠(上海沪试实验室器材公司,批号:F20110211);PDE5A1(BPS,批号:60050);PDE6C(BPS,批号:60062);PDE11A4(BPS,批号:60110);384孔板(Perkin Elmer,批号:6007279);格列吡嗪(中国食品药品检定研究院,批号:100281-201203,含量:99.5 %);甲醇[赛默飞世尔科技(中国)公司,色谱纯,批号:140400];甲酸[赛默飞世尔科技(中国)公司,批号:163701];乙腈[赛默飞世尔科技(中国)公司,色谱纯,批号:151296];肝素钠注射液(山东鲁抗辰欣药业,批号:1609286421)。
1.3 实验动物
KM小鼠,80只,雄性,体重18.1~25.2 g。SD大鼠,27只,雄性,体重220~270 g,大、小鼠均由济南朋悦实验动物繁育有限公司提供,生产许可证号:SCXK(鲁)20140007。大、小鼠均饲养于万级屏障环境中,按GB/16886.2动物的福利要求规范进行管理,室温控制为20~25 ℃,相对湿度控制为40 %~70 %,昼夜明暗交替时间12 h/12 h。动物使用许可证号:SCXK(鲁)20140008。
新西兰兔,24只,雄性,体重为2.0~2.5 kg,由济南西岭角养殖繁育中心提供,生产许可证号:SCXK(鲁)20150001。普通环境中饲养,每笼1只,室温19~26 ℃,温差≤4 ℃,换气次数8~10次/h,昼夜明暗交替时间12 h/12 h。动物使用许可证号:SCXK(鲁)20140008。
2 方法
2.1 化合物1对PDE-5A1,PDE-6C及PDE-11A4的体外抑制作用
准确称取化合物1,加入DMSO充分溶解,配置成10 mmol/L母液保存。试验时稀释为所需浓度,最高浓度为10 μmol/L,然后依次4倍稀释。体外酶活性检测方法如下:在96孔板中加入20 μl底物[10 μmol/L荧光素标记的环-磷鸟苷(FL-cGMP) ],化合物1溶液1 μl,1.38 ng/μl酶缓冲液[缓冲液由100 mmol/L羟乙基哌嗪乙硫磺酸(pH 7.5),5 mmol/L MgCl2和0.002 %月桂醇聚氧乙烯醚组成]29 μl。30 ℃孵育1 h,加入 70 μmol/L EDTA 20 μl终止反应,每孔转移反应液26 μl至384孔板,EZ Reader II酶标仪检测读数,计算抑制率,Prism 5.0软件计算半数抑制浓度(IC50)。抑制率=(转化率ZEP-转化率样品)/(转化率ZEP-转化率HEP)×100 %,式中转化率ZEP为不加化合物1的空白对照组的荧光值,转化率样品为加化合物1样本的荧光值,转化率HEP为不加酶的空白对照的荧光值。
2.2 化合物1对正常家兔阴茎勃起功能的影响[8-9]
取雄性新西兰兔24只,适应1周后开始试验,试验时按体重随机分为4组,分别为西地那非组(剂量2.3 mg/kg)、化合物1高、中、低剂量(2.3,1.15,0.06 mg/kg)组,每组6只。开始试验前每天捉拿家兔,让家兔习惯反复的捉拿操作后开始给药刺激。各给药组灌胃给予相应的药物溶液5 ml/kg,灌胃给药前及给药后5,15,30,60,120,240,300 min分别用数显游标卡尺测兔阴茎长度,每次测量过程中避免卡尺触碰阴茎。根据各时间点阴茎长度及时间,绘制长度-时间曲线,并计算曲线下面积(AUC)。
2.3 化合物1 SD大鼠体内药动学研究
取雄性SD大鼠22只,适应1周后开始试验,试验时按体重随机分为4组,分别为化合物1静注组(剂量4.5 mg/kg)、化合物1口服高、中、低剂量(9,4.5,2.25 mg/kg)组,每组5~6只。禁食不禁水约12 h后,各组灌胃或静脉注射给予相应的药物溶液10 ml/kg。各组大鼠给药前眼眦采血,静注组于药后0.25,0.5,1,1.5,2,4,6,8,10,12,24 h 眼眦采血,口服组于药后0.5,1,2,4,6,7,8,10,12,14,24,30 h眼眦采血。采血约0.5 ml,置入肝素钠抗凝的离心管,4 ℃ 10 000 r/min离心5 min,制备血浆。血浆样品采用高效液相质谱-串联色谱(LC/MS/MS) 分析,梯度洗脱,MS检测离子对:化合物1(m/z470.9/371.1),格列吡嗪(内标,m/z446.2/321.0)。利用DAS3.2.6软件计算药动学参数,以AUC0-∞计算化合物1的生物利用度。
2.4 化合物1大鼠血浆蛋白结合率研究
2.4.1 样本采集方法 取雄性SD大鼠5只,适应1周后开始试验,大鼠禁食不禁水12 h后,尾静脉注射给予4.5 mg/kg化合物溶液。于药后0.25,0.5,1 h眼眦采血,采血约0.5 ml,置入肝素钠抗凝的离心管,4 ℃ 10 000 r/min 离心5 min,制备血浆。取血浆100 μl于超滤离心管中,8 ℃、13 000 r/min离心30 min,收集滤液,其余血浆用于测定总药物浓度。
2.4.2 吸附率测定 配制浓度为30,150,300 ng/ml的化合物的20 %乙腈溶液,取100 μl,置入超滤离心管,8 ℃、13 000 r/min离心30 min,收集滤液。测定超滤前(ρpre)及超滤后(ρpost)化合物1浓度,根据以下公式计算药物非特异性结合吸附率(NSB)。
NSB=(ρpre-ρpost)/ρpre×100 %。
2.4.3 血浆蛋白结合率计算 分别取20 μl未经超滤血浆、超滤后血浆样本置入1.5 ml离心管,加入内标乙腈溶液(格列吡嗪浓度200 ng/ml)180 μl,涡旋2 min,12 000 r/min(15 ℃)离心5 min,取上清,进样2 μl检测。根据公式F=(A-B)/A计算大鼠体内血浆蛋白结合率,其中A为总药物浓度,B为游离药物浓度。
2.5 化合物1小鼠急性毒性初步研究[10]
取雄性KM小鼠80只,适应3 d后开始试验,试验时按体重随机分为8组,分别为西地那非不同剂量(758.4,568.8,426.7,320 mg/kg)组、化合物1不同剂量(21.8,19.3,14.5,10.9 g/kg)组,每组10只,禁食不禁水12 h后,各组小鼠灌胃给药1次,给药体积为40 ml/kg,给药后观察4 h,之后每天上、下午观察并记录小鼠的一般活动、行为、体重及死亡情况,共观察14 d,计算半数致死量(LD50)。
2.6 统计分析
3 结果
3.1 化合物1对PDE-5A1,PDE-6C及PDE-11A4的体外抑制作用
化合物1对PDE-5A1的IC50为0.17 nmol/L,而西地那非对PDE-5A1的IC50为5.38 nmol/L,提示化合物1对PDE5A1的抑制活性优于西地那非。化合物1对PDE-6和PDE-11的抑制活性与西地那非相近。见表1。

表1 化合物1对PDE-5A1、PDE-6C及PDE-11A4的IC50值/nmol·L-1
3.2 化合物1对正常家兔阴茎勃起功能的作用
化合物1对正常家兔阴茎勃起功能的作用见图1。由图1可见,化合物1剂量为0.6 mg/kg时对家兔阴茎勃起没有促进作用,剂量为1.15,2.3 mg/kg时可明显促进家兔阴茎勃起。此外,化合物1在给药后15 min起效,在该模型中的最低起效剂量为1.15 mg/kg,维持时间为2 h左右,与西地那非相近。经计算,化合物1与西地那非在剂量为2.3 mg/kg时AUC分别为379.8,183.8 mm·min,两者差异无统计学意义(P>0.05),进一步的比较需放大样本进行。

图1 化合物1在不同剂量下对正常家兔阴茎勃起功能的作用
3.3 化合物1 SD大鼠体内药动学研究
化合物1 SD大鼠中体内药动学参数见表2,血药浓度-时间曲线(C-T曲线)见图2、图3。由表2可见,化合物1口服给药剂量为2.25~9 mg/kg时Cmax、AUC0-t、AUC0-∞随剂量增加呈线性递增趋势,说明化合物1在SD大鼠中呈线性药动学特征。
相同剂量下,相比于静注给药组,化合物1口服给药组暴露量低(Cmax、AUC0-t、AUC0-∞均低于静注组,P<0.05)。同时,口服组表观分布容积(Vd)和清除率(CL)均高于静注组(P<0.05),说明口服途径化合物1分布广,清除速率高。经计算,化合物1的生物利用度(F)值为13.63 %。

表2 化合物1在SD大鼠中的药动学参数
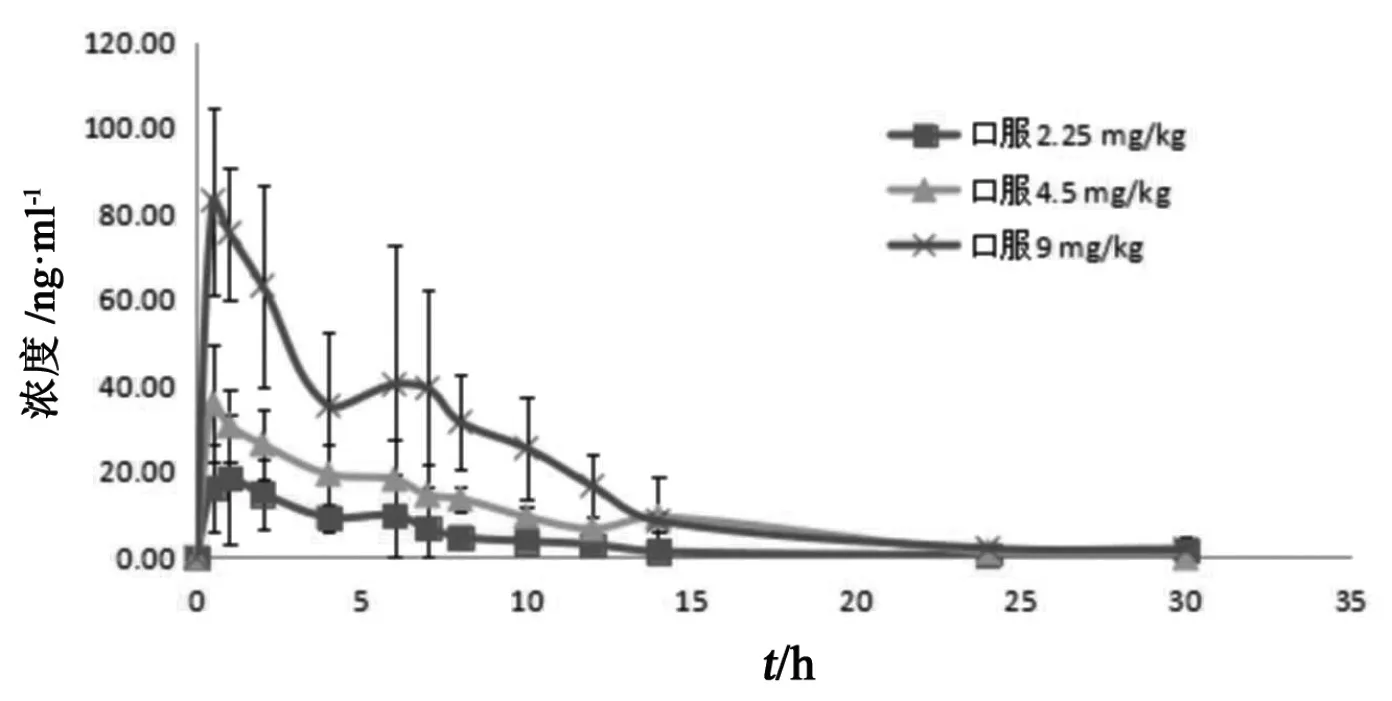
图2 SD大鼠分别灌胃给予低、中、高剂量化合物1后,平均血药浓度-时间曲线(n=6,5,5)

图3 SD大鼠静脉给予化合物1后,平均血药浓度-时间曲线(n=6)
3.4 化合物1大鼠血浆蛋白结合率研究
根据超滤膜非特异性结合(NSB)公式:NSB/%=(ρpre-ρpost)/ρpre×100 % 计算得药物吸附率为-9.41 %~2.99 %,表明超滤膜对药物不存在非特异性结合,可采用超滤法测定血浆蛋白结合率。经过进一步测试,化合物1的血浆蛋白结合率为99.97 %,见表3。

表3 化合物1血浆蛋白结合率
3.5 化合物1小鼠急性毒性初步研究
化合物1小鼠急性毒性初步研究结果表明:化合物1与西地那非出现的毒性反应相似,表现为消瘦、活动减少、体重增长缓慢等症状;死亡时间集中于给药后第6~9天,死亡动物主要脏器(脑、心、肝、脾、肺、肾)未见其他明显异常。化合物1灌胃给药的 LD50为14.8 g/kg,西地那非的LD50为580.6mg/kg。
4 讨论
ED是成年男子常见的一种疾病,随着我国老龄化的加剧,ED的发生呈明显的上升趋势。在40~70岁的男性中,ED的发生率高达50 %以上,虽然患病率居高,但去正规医院诊治的患者低于10 %[11]。正常的阴茎勃起是血管、神经、激素、海绵体多种因素共同参与,其中任何一个环节出现问题均可导致ED的发生。
在阴茎勃起的生理过程中,NO发挥着重要作用,当阴茎海绵体中的NO浓度增加时,直接激活鸟苷酸环化酶,从而促使第二信使环磷酸鸟苷(cGMP)的浓度增加,继而引起细胞内Ca2+浓度下降,平滑肌舒张,阴茎海绵体膨胀,体积增大,从而导致海绵体的白膜拉伸延长,白膜下静脉压迫变窄,静脉回流受阻,阴茎勃起,而当cGMP被PDE5降解时,cGMP浓度降低,从而不能引起阴茎勃起[12-13]。因此特异性阻断PDE5的药物可提高阴经海绵体内cGMP的浓度,用于治疗勃起功能障碍。
PDE家族有PDE-1~PDE-11 11个成员,在人体脑、心、肺、血管等部位分布广泛。PDE具有不同的底物专一性,其中,PDE-5,6,9特异性地选择作用于cGMP,PDE4,7,8选择性作用于环磷酸腺苷(cAMP),其他的PDE则对cAMP和cGMP均起作用[14]。参考已上市的PDE-5抑制剂药物文献[15],在药物筛选阶段,我们重点考察药物对3个酶的抑制性,即PDE-5,PDE-6和PDE-11。其中PDE-5与药物的作用机制直接相关,而对PDE-6,PDE-11的抑制可能与药物的不良反应有关,PDE-6可能与视物模糊有关,PDE-11则可能与背痛和肌肉酸痛有关。在上市的PDE-5抑制剂类药物中,西地那非、伐地那非、优地那非、米罗那非和罗地那非对PDE-6的选择性较差;他达拉非对PDE-6的选择性较好,但其对PDE-11的选择性较差,但半衰期较长;而新一代的阿伐那非对PDE-6,11的选择性均好,但半衰期较短。
化合物1是山东康迈祺公司自主研发的1.1类创新药。化合物1对PDE-5A1的体外抑制作用优于西地那非,IC50为西地那非的1/31;化合物1在1.15~2.3 mg/kg剂量下可剂量依赖性地促进正常家兔阴茎勃起,同时在2.3 mg/mg剂量下,即西地那非的临床等效剂量,化合物1促进家兔勃起的作用略强于西地那非;化合物1具有较好的药动学性质,清除率较低,半衰期较长,可达3.9~12.42 h;化合物1的大鼠血浆蛋白结合率为99.97 %,属于高血浆蛋白结合率药物;小鼠急性毒性试验中,化合物1毒性明显低于西地那非。总之,化合物1具有较好的体内、外活性,对PDE-6及PDE-11具有较好的选择性,安全性较高,具有良好的成药性,值得进一步研究。

