抗生素不同给药途径联合牙周基础治疗在广泛型侵袭性牙周炎中的临床疗效分析
杨善麟,杨 番
(上海沪东医院口腔科,上海 200129)
侵袭性牙周炎(aggressive periodontitis,AgP)是一种慢性非特异性的牙周炎症,根据患牙的分布可分为局限型侵袭性牙周炎和广泛型侵袭性牙周炎(generalized aggressive periodontitis,GAgP)[1],后者在我国的发病率更高,危害更大[2],能在短期内破坏牙槽骨,丧失牙周附着,严重影响患者的生存质量[3]。目前GAgP的治疗原则与慢性牙周炎基本相同,患者需进行龈上洁治、龈下刮治与根面平整等牙周基础治疗,通过机械治疗帮助牙周组织的再附着[4],但单纯机械治疗有局限性,临床上常应用抗生素来抑制或清除牙周致病菌,以提高临床疗效。在牙周炎患者的基础机械治疗中通过辅助应用相关的抗菌药物,可使药物的作用深达牙周袋底,并能有效消除侵入患者牙周袋壁上颌口腔黏膜中的致病菌,对于单纯机械治疗的方案效果更加显著。本研究旨在比较抗生素不同给药途径联合牙周基础治疗GAgP的应用效果,为临床提供参考依据,现报道如下。
1 资料与方法
1.1一般资料 选取2016年1月至2018年12月上海沪东医院口腔科收治的126例GAgP患者为研究对象。入选标准:①符合1999年Armitage[5]国际研讨会提出的牙周疾病和状况分类系统中GAgP的诊断标准;②近半年内未服用任何抗生素;③既往未接受正畸治疗,且近1年内未接受牙周治疗;④临床资料完整可靠。排除标准:①全口牙不足25颗;②对四环素类药物等抗生素过敏;③合并心、肝、肾等脏器的严重疾病或全身系统性疾病史;④吸烟者;⑤妊娠期妇女。上述患者根据治疗方法不同分为局部组、全身组、对照组,各42例,患牙数分别为526颗,498颗,515颗。各组患者的性别、年龄、体质指数、患牙的位置分布比较差异无统计学意义(P>0.05)。见表1。本研究方案及方法经上海沪东医院医学伦理委员会批准,标本的采集过程以及研究方法均符合赫尔辛基宣言,患者本人或家属均签署了书面《知情同意书》。
1.2方法 患者确诊后均给予牙周基础治疗,首先对患者进行口腔的卫生指导,如正确刷牙、使用牙线等,然后在Primacaine(碧兰麻)局部麻醉下完成彻底的龈上洁治、龈下刮治和根面平整术,并用3%过氧化氢冲洗牙周袋。在此基础上,局部组选择牙周探诊深度(probing depth,PD)>5 mm的位点,将2%盐酸米诺环素软膏(Sunstar INC Japan生产,批号:H20100244)通过注射器注入牙周袋的底部,注意注射速度不能过快,直到龈缘处可见软膏,给药后1 h内禁食、禁止漱口,每周注射1次,连续给药4周;全身组患者口服阿奇霉素,每次0.5 g,每日1次,饭后2 h服用,连用3 d。
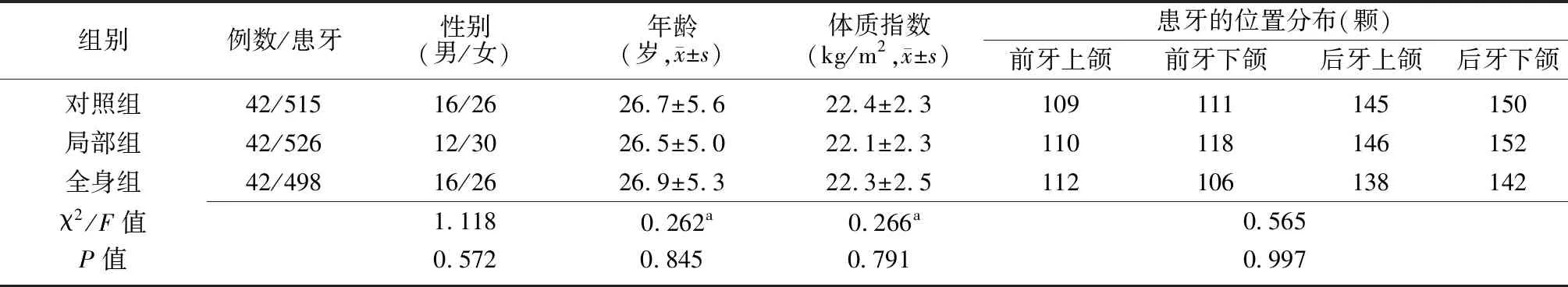
表1 各组GAgP患者基线资料比较
GAgP:广泛型侵袭性牙周炎;对照组:给予牙周基础治疗;局部组:给予牙周基础治疗联合米诺环素局部注射;全身组:给予牙周基础治疗联合口服阿奇霉素;a为F值,余为χ2值
1.3观察指标
1.3.1牙周疗效 全部患者在治疗前、治疗后6周进行牙周疗效评估,选择PD≥5 mm位点进行观察,每颗牙记录近中颊、颊正中、远中颊和舌正中4个位点,评估牙周相关指标:出血指数(bleeding index,BI)、菌斑指数(plaque index,PLI)、临床附着丧失(clinical attachment loss,CAL)、PD。BI是用牙周探针轻探入牙周袋底,取出探针30 s后观察有无出血,总分0~5分,分数越高表明出血情况越严重。PLI是通过肉眼直接观察与探针探查来确定龈缘附近牙面的菌斑量,总分0~3分,分数越高表明菌斑量越多。CAL、PD分别是指袋底至釉牙骨质界的距离、龈缘至袋底或龈沟底的距离。
1.3.2血清炎症指标与生化指标 在治疗前、治疗后6周,采集全部患者的清晨空腹静脉血5 mL,采用双抗体夹心聚合酶链反应法检测肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、血清降钙素原(procalcitonin,PCT)、高敏C 反应蛋白(high-sensiti-vity C-reaction protein,hs-CRP)、白细胞介素-6(interleukin-6,IL-6)水平。

2 结 果
2.1各组患者治疗前后牙周相关指标比较 三组间BI、PLI、CAL、PD比较差异均有统计学意义(P<0.01),各组治疗后BI、PLI、CAL、PD均明显低于治疗前(P<0.01),局部组降低更显著(P<0.01),各时间点间BI、PLI、CAL、PD差异均有统计学意义(P<0.01),各指标组间和时点间交互作用比较差异无统计学意义(P>0.05)。见表2。
2.2各组患者治疗前后血清炎症因子水平比较 各组间TNF-α、PCT、hs-CRP、IL-6比较差异均有统计学意义(P<0.01),各组治疗后TNF-α、PCT、hs-CRP、IL-6均低于治疗前(P<0.01),局部组降低更显著(P<0.01),各时点间TNF-α、PCT、hs-CRP、IL-6比较差异均有统计学意义(P<0.01),组间和时点间交互作用比较差异无统计学意义(P>0.05)。见表3。
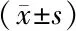
组别例数BI (分)治疗前治疗后PLI (分)治疗前治疗后CAL (mm)治疗前治疗后PD (mm)治疗前治疗后对照组423.41±0.452.05±0.322.75±0.661.90±0.346.73±1.985.32±1.126.40±1.324.86±1.27局部组423.23±0.531.63±0.692.66±0.511.19±0.396.69±1.883.82±0.526.39±1.533.06±0.83全身组423.33±0.501.86±0.232.53±0.561.39±0.436.83±1.964.13±0.646.59±1.663.39±1.02 组间F=15.231 P<0.001F=16.012 P<0.001F=18.023 P<0.001F=20.124 P<0.001 时点间F=20.031 P<0.001F=22.331 P<0.001F=16.331 P<0.001F=15.336 P<0.001 组间·时点间F=2.332 P=0.152F=1.053 P=0.166F=1.077 P=0.157F=1.665 P=0.167
GAgP:广泛型侵袭性牙周炎;BI:出血指数;PLI:菌斑指数;CAL:临床附着丧失;PD:牙周探诊深度;对照组:给予牙周基础治疗;局部组:给予牙周基础治疗联合米诺环素局部注射;全身组:给予牙周基础治疗联合口服阿奇霉素
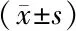
组别例数TNF-α(ng/L)治疗前治疗后PCT (μg/L)治疗前治疗后hs-CRP (mg/L)治疗前治疗后IL-6 (mg/L)治疗前治疗后对照组4250.65±8.0335.46±4.0620.01±4.2012.21±2.3225.36±4.8115.33±2.3630.41±5.5615.32±2.45局部组4250.33±5.3919.69±3.9620.09±3.098.69±1.9325.33±2.819.93±1.8130.39±2.5613.93±2.01全身组4255.69±8.3623.39±8.8918.59±3.6910.23±5.0823.98±4.0312.33±5.1928.13±4.0511.69±4.33 组间F=16.235 P<0.001F=17.332 P<0.001F=19.022 P<0.001F=16.339 P<0.001 时点间F=19.556 P<0.001F=20.036 P<0.001F=17.432 P<0.001F=18.475 P<0.001 组间·时点间F=2.065 P=0.165F=1.374 P=0.184F=1.366 P=0.173F=1.399 P=0.109
GAgP:广泛型侵袭性牙周炎;TNF-α:肿瘤坏死因子-α;PCT:降钙素原;hs-CRP:高敏C 反应蛋白;IL-6:白细胞介素-6;对照组:给予牙周基础治疗;局部组:给予牙周基础治疗联合米诺环素局部注射;全身组:给予牙周基础治疗联合口服阿奇霉素
3 讨 论
GAgP是一种临床上较少见的严重牙周炎,好发于年轻女性,其主要特征是在短时间内快速、严重地破坏牙周组织,表现为牙周附着的快速丧失与牙槽骨的快速吸收,引起牙齿松动、移位与脱落,牙周组织的破坏速度是慢性牙周炎的3~4倍,常累及全口的多数牙齿,病变广泛,不仅影响患者的咀嚼功能,还严重影响患者的心理健康和生存质量,近年来越来越受到牙周科医师的关注。目前认为,牙龈卟啉单胞菌、福赛坦菌、放线放线杆菌等特定的微生物感染是GAgP的关键致病因素,这些微生物及其毒素能引起局部的免疫反应,释放一系列炎症因子[6-10],故早期抑制或彻底清除病原微生物,长期保持牙周组织的环境健康是GAgP的治疗目的。与慢性牙周炎类似,GAgP患者同样需要牙周基础治疗,主要指龈上洁治、龈下刮治和根面平整术,干扰致病菌的生态环境,清除可疑的致病菌,实现牙周组织的再附着,是GAgP的基础治疗手段,临床应用广泛。但由于龈下牙根面的解剖结构较为复杂,单纯实施牙周的机械治疗效果有限,致病菌的清除率不高,且容易复发,尤其是已侵入牙周结缔组织者。对此,临床上常联合应用抗生素治疗,包括局部注射和口服两种给药途径,各有优缺点。
在全身用药方面,口服阿莫西林和甲硝唑是AgP的常用治疗方案,阿莫西林是一种半合成青霉素类广谱β-内酰胺类抗生素,对溶血链球菌、肺炎链球菌、葡萄球菌、流感嗜血杆菌、大肠埃希菌、奇异变形杆菌、粪肠球菌等多个细菌敏感,而甲硝唑主要用于厌氧菌引起的系统或局部感染,两者联合后扩大了抗菌谱,抗菌效果显著。但两者的不良反应均较严重,甲硝唑能引起皮疹、胃肠道不适、头痛、粒细胞减少、潮红、肠痉挛、肝毒性等,且有致畸作用,不适合于妊娠期和哺乳期妇女;阿莫西林也较容易引起过敏、恶心呕吐、腹泻等不良反应,故两药联用后的应用范围较窄,容易出现患者不耐受,尤其是需要长期服药者,这也是近年来局部给药越来越受到临床重视的原因之一。阿奇霉素是一种半合成、广谱的大环内酯类抗生素,对厌氧菌、多数革兰阴性菌、产黑色素类杆菌、螺旋体和一些非典型致病菌等具有很强的抗菌活性,具有组织渗透性佳、半衰期长、抗菌作用强等优点,且不良反应较弱,基本无明显的过敏反应。而作为AgP患者龈下菌斑的常见可疑致病菌牙龈卟啉单胞菌与福赛坦菌均为专性厌氧的革兰阴性菌,对阿奇霉素的敏感性均较高[11],故阿奇霉素适合于AgP的抗菌治疗。阿奇霉素的组织渗透性较强,能有效渗透进口腔生物膜,抑制多糖的合成,从而阻止菌斑生物膜的生成,降低细菌的黏附能力,这也是甲硝唑+阿莫西林治疗方案的优势,且阿奇霉素能被吞噬细胞所摄取,能长时间在炎症组织中释放,故在局部牙周炎症组织中的药物浓度同样较高[12]。此外,阿奇霉素的全身毒性较弱,不良反应较少,故治疗依从性更好,应用范围较广。国内已有研究证实,AgP患者在牙周基础治疗后口服阿奇霉素与口服甲硝唑+阿莫西林的效果比较差异无统计学意义,两者治疗后的BI、PD、CAL比较差异无统计学意义[13]。
米诺环素又称为美满环素,是一种抗菌作用最强的四环素类抗生素,其抗菌谱广泛,具有较强的组织穿透力,对大多数牙周致病菌敏感[14],且能抑制胶原酶,促进牙周组织再生长,适合于牙周炎的治疗[15]。由于全身应用米诺环素的不良反应较多,临床上常采用局部注射的给药途径,米诺环素也成为当前AgP等牙周炎局部用药的首选药物,局部给药能明显升高牙周袋内的药物浓度,延长作用时间,且血药浓度较低,不良反应相对较小,临床应用广泛[16-18]。肖艳等[19]研究表明在常规治疗的基础上局部辅助米诺环素软膏对AgP的疗效显著,能改善血清CRP、TNF-α和IL-17等炎症因子水平。但局部应用米诺环素也有不足之处,如引起皮肤的局部色素沉着,出现黑舌等,这可能与其引起口腔菌群失调有关。
关于抗生素的局部用药与全身用药,仲琳等[20]研究比较了GAgP患者牙周基础治疗后局部应用米诺环素与口服甲硝唑+阿莫西林这两种方案的应用效果,结果表明与单纯牙周基础治疗相比,抗生素的两种给药方式均能明显提高GAgP的临床疗效,但短期内两者的应用效果无明显区别。目前国内比较GAgP患者局部应用米诺环素与口服阿奇霉素的研究较少。本研究结果显示,局部组和全身组治疗后的牙周相关指标BI、PLI、CAL、PD及血清TNF-α、PCT、hs-CRP、IL-6炎症因子水平均显著低于治疗前及对照组治疗后,且局部组的治疗效果更佳。提示两种治疗方案均有明显的临床疗效,但局部用药具有靶向作用,治疗效果更佳。
局部应用抗生素能明显减少注射部位的细菌量,减轻炎症反应,避免全身用药的不良反应,安全性较高,但其只能在牙周袋内进行注射给药,无法作用于定植在颊部、扁桃体、舌背等黏膜处的细菌,作用范围较窄,且治疗周期长,每周注射1次,需连续给药4周。而口服抗生素能让药物通过血液达到口腔多个部位的黏膜处,进一步抑制致病菌的入侵与在袋内的再定植,预防病变复发,还能减少疾病活跃的位点,有助于长期控制病情,且口服阿奇霉素只需连用3 d,用药依从性较高,但全身给药后牙周袋内的药物浓度相对较低,且更容易引起机体的菌群失调,不良反应也相对较多。局部用药可能更适合于全口受累牙数较少,或不能口服抗生素、有药物过敏史的患者,而全身用药可能更适合于牙感染位点较多、局部用药仍不能控制者,可在选择局部用药基础上联合全身用药,提高临床疗效,防止炎症复发。值得注意的是,抗生素的应用对于GAgP均是辅助治疗方法,单用任何抗生素都不能有效治疗GAgP,需在用药前实施彻底的龈上洁治、龈下刮治和根面平整术,通过机械治疗来清除菌斑牙石,破坏菌斑的生物膜结构,同时需进行口腔卫生的健康宣教与指导,加强对菌斑的控制。
综上所述,局部注射米诺环素、口服阿奇霉素这两个抗生素给药方案联合牙周基础治疗对GAgP均有显著的治疗效果,局部应用抗生素能明显改善牙周相关指标与炎症反应,治疗效果更加明显。

