火焰原子吸收光谱法测定U3O8产品中钾钠含量的不确定度评定
龚明明,曹淑琴,孙雪云,郭国龙,杨丹丹
(核工业北京化工冶金研究院,北京 101149)
U3O8中钾钠含量是重要控制指标,测量结果必须准确可靠。测量不确定度是与测量结果相关联的参数[1],用于表征合理赋予被测量之值的分散性,是对测量结果质量的定量表征。不确定度越小,测量结果质量越高;不确定度越大,测量结果质量越低。笔者以火焰原子吸收光谱法测定U3O8中钾、钠的含量为例,对测量过程中的样品称量、定容体积、标准溶液、测量结果重复性、树脂吸附、工作曲线等产生的不确定度进行分析评定。
1 试验部分
1.1 主要仪器与试剂
1)仪器:原子吸收光谱仪,日立 Z-2010;电子天平,BS210S,德国赛多利斯,精确度为0.000 1 g。
2)试剂:钾标准溶液,质量浓度为100 μg/mL(GBW(E)080184,核工业北京化工冶金研究院);钠标准溶液,质量浓度为100 μg/mL(GBW(E)080185,核工业北京化工冶金研究院);硝酸、氢氟酸,北京化学试剂厂,优级纯;实验室用水为超纯水。
1.2 标准溶液的配制
1)钾标准溶液的配制。用10~100 μL的可调移液器移取质量浓度为100 μg/mL的钾标准溶液0.00、0.05 mL,用100~100 0 μL的可调移液器移取质量浓度为100 μg/mL的钾标准溶液0.1、0.5、1.0、2.0 mL,均定容到100 mL容量瓶中,摇匀,得到质量浓度分别为0.00、0.05、0.10、0.50、1.00、2.00 μg/mL的钾标准溶液。
2)钠标准溶液的配制:用10~100 μL的可调移液器移取质量浓度为100 μg/mL的钠标准溶液0.00、0.05 mL,用100~1 000 μL的可调移液器移取质量浓度为100 μg/mL的钠标准溶液0.1、0.5、1.0、2.0 mL,均定容到100 mL容量瓶中,摇匀,得到质量浓度分别为0.00、0.05、0.10、0.50、1.00、2.00 μg/mL的钠标准溶液。
1.3 检测方法
准确称取U3O8样品0.500 0 g于50 mL聚四氟烧杯中,用水润湿;加入3 mL浓硝酸在电热板微热后,取下,不断摇动;待剧烈反应停止后,滴加3滴氢氟酸,加热使样品完全溶解后,蒸至近干;再加入2 mL浓硝酸,加热溶解蒸至近干;再加入2 mL浓度为3 mol/L HNO3溶解,经CL-TBP萃淋树脂柱分离铀基体,将淋洗液移入25 mL A级石英玻璃容量瓶中,稀释至刻度,摇匀待测。用空气-乙炔火焰原子吸收法,对钾、钠标准溶液、待测液、试剂空白液进行测定;以钾、钠标准溶液的含量和对应吸光度绘制标准曲线;以浓度为横坐标,吸光度为纵坐标,绘制工作曲线,通过工作曲线法求得样品中钾、钠的含量(μg/g)。
2 结果计算和不确定度分析
2.1 钾、钠含量的计算公式
钾、钠含量的计算公式为
(1)
式中:wB—试样中钾或钠的质量分数,μg/g;ρB—从工作曲线上查到的钾或钠质量浓度,μg/mL;V—待测液的体积,mL;m—试样的质量,g。
2.2 不确定度分析
影响U3O8中钾、钠含量分析结果不确定度的来源包括:样品称量产生的不确定度[2];样品溶液中钾、钠的浓度产生的不确定度[3];样品定容体积产生的不确定度和树脂吸附产生的不确定度。
1)样品称量产生的不确定度包括:天平的精密度和重复性产生的不确定度。
2)样品消解后待测溶液定容体积产生的不确定度包括:容量瓶容量允差、定容读数和温度变化产生的不确定度。
3)样品溶液中钾、钠的测量过程产生的不确定度包括:通过标准曲线拟合求得钾、钠浓度所产生的测量不确定度、标准贮备液配制时产生的不确定度和样品溶液重复测量产生的不确定度。
4)树脂吸附产生的不确定度包括:采用阳离子交换树脂分离富集钾、钠过程中,钾、钠回收率产生的不确定度。
3 各分量不确定度的评定
3.1 样品称量产生的不确定度u1
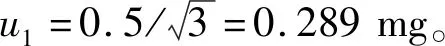
urel(1)(K)=urel(1)(Na)=
u1×10-3×100%/m=0.057 8%
(2)
3.2 样品消解后待测溶液定容体积产生的不确定度u2
3.2.1 100mL容量瓶产生的标准不确定度u2-1
容量瓶产生的不确定度分2个部分:1)容量瓶允许差产生的不确定度(u2-1-1);2)温度变化产生的不确定度(u2-1-2)。
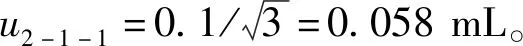
则100 mL容量瓶产生的标准不确定度为
(3)
则100 mL容量瓶产生的相对标准不确定度为
urel(2-1)(K)=urel(2-1)(Na)=
u2-1/100×100%=0.084%
(4)
3.2.2 25mL容量瓶产生的标准不确定度u2-2
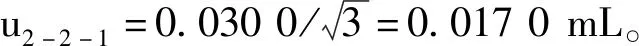
则25 mL容量瓶产生的标准不确定度为
(5)
则25 mL容量瓶产生的相对标准不确定度为
urel(2-2)(K)=urel(2-2)(Na)=
u2-2/100×100%=0.063%
(6)
样品消解后待测溶液定容体积产生的相对标准不确定度为
(7)
urel(2)(K)=urel(2)(Na)=0.105%
(8)
3.3 样品溶液中钾、钠测量过程中产生的不确定度
3.3.1测量重复性产生的不确定度u3-1
U3O8中钾钠测量结果的不确定度评定分A类和B类,测量的重复性产生的不确定度属于A类不确定度[4]。采用钾钠重复性测量结果的标准方差来计算u3-1,同一个U3O8样品重复性测量12次,测量结果见表1。
样品重复测定结果的标准偏差计算公式为
(9)
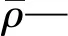
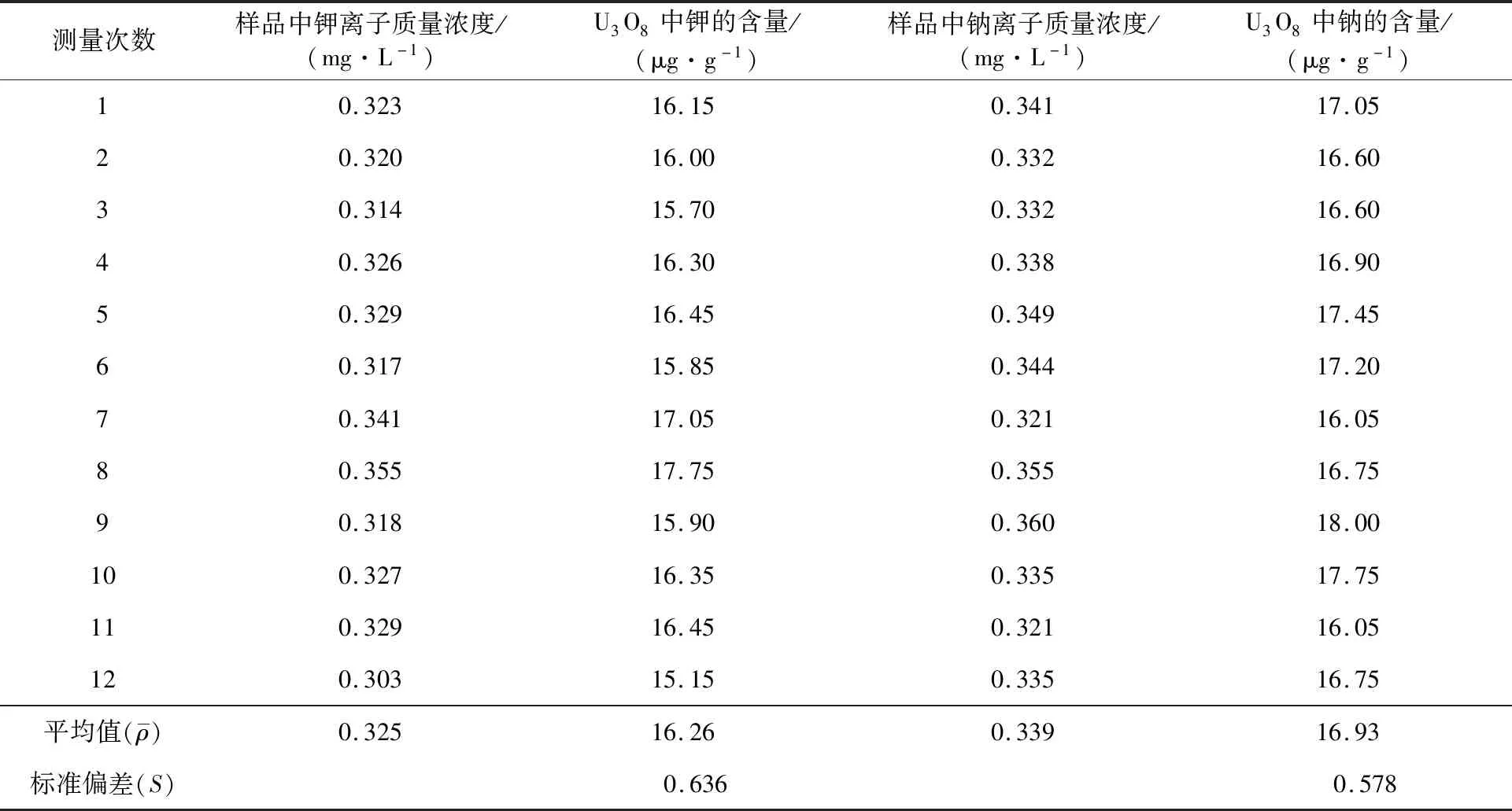
表1 U3O8中钾钠含量的重复性测定结果
测量的重复性产生的不确定度为
(10)
故测量的重复性产生的不确定度为
u3-1(K)=0.184 ;u3-1(Na)=0.167。
因此,得出相对标准不确定度为
(11)
(12)
3.3.2标准溶液产生的不确定度u3-2
此次采用的钾、钠标准溶液由核工业北京化工冶金研究院提供,质量浓度为100 μg/mL,标准证书出具钾、钠的相对标准不确定度均为1.4%,按均匀分布计算,则
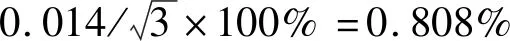
(13)
3.3.3标准溶液配制产生的标准不确定度u3-3
由标准溶液配制方法可知,不确定度来源包括100 mL容量瓶产生的标准不确定度和可调移液器产生的标准不确定度。10~100 μL的可调移液器允差为3%,100~100 0 μL的可调移液器允差为2%,取0.00、0.05、0.10、0.50、1.00、2.00 mL标准溶液,体积允许差分别为0.000 0、±0.001 5、±0.002 0、±0.010 0、±0.020 0、±0.040 0 mL,按均匀分布计算,则标准不确定度分别为0.000 0、0.000 9、0.001 2、0.005 8、0.012 0、0.023 0 mL。
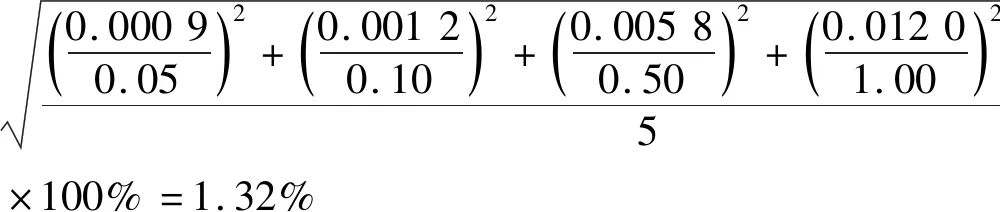
(14)
3.3.4标准曲线拟合求得钾、钠质量浓度所产生的测量不确定度u3-4
钾、钠标准系列溶液质量浓度和吸光度分别见表2和表3,每份标准溶液吸光度重复测3次,采用最小二乘法拟合得到钾、钠标准曲线线性回归方程分别为:A=0.094 2ρ-0.000 3,R=1.000;
A=0.035ρ+0.001 5,R=1.000。根据标准溶液浓度通过线性回归方程计算出吸光度理论值,计算实际吸光度值与理论值的残差[5]:Aij-(a+bc),由贝塞尔公式求得吸光度残差的标准偏差SA,进而求得标准曲线拟合产生的不确定度。
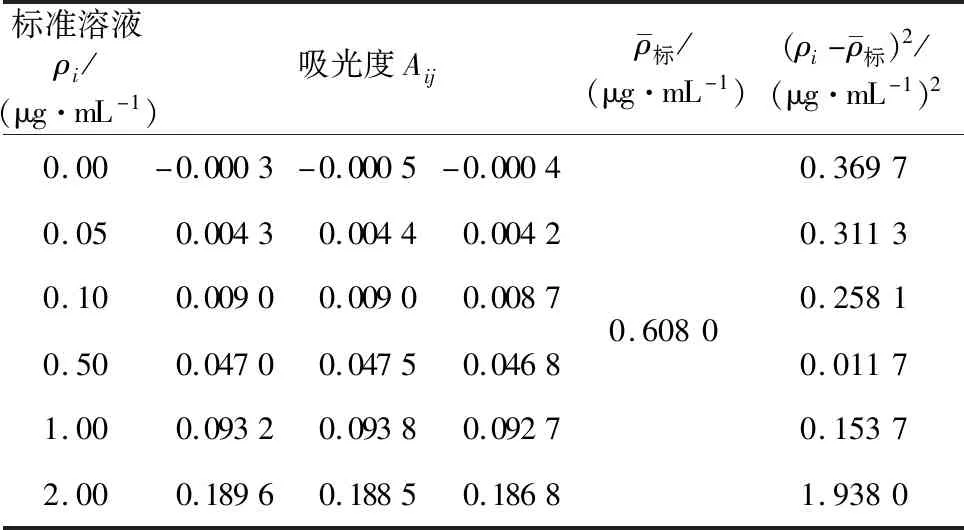
表2 钾标准溶液的浓度和吸光度
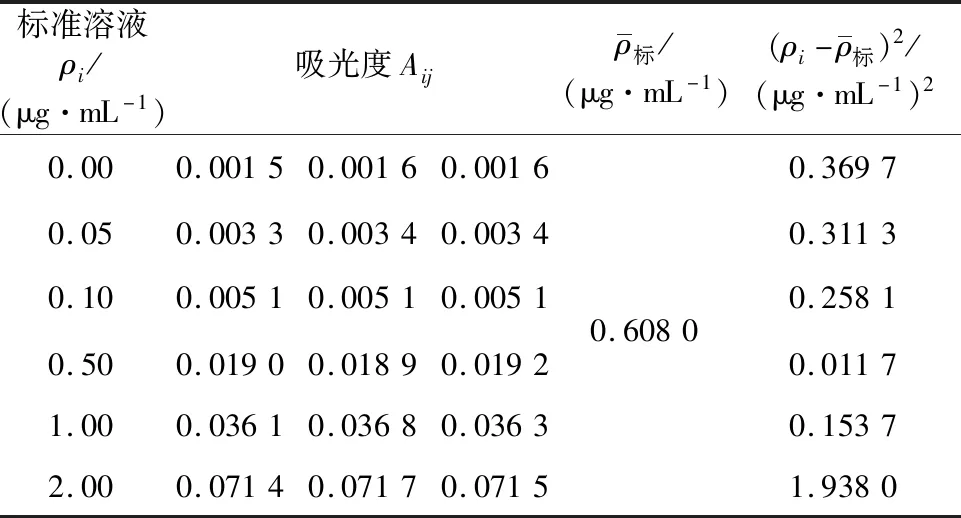
表3 钠标准溶液的浓度和吸光度
工作曲线标准差
(15)
式中:Aij—样品溶液测得吸光度;m—标准溶液重复测定次数,m=3;n—标准溶液个数,n=6;ρi—标准溶液质量浓度,μg/mL。
计算得出
SA(K)=6.558×10-4;SA(Na)=1.745×10-4;
工作曲线变动性引起的相对不确定度为
(16)
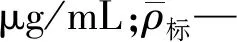
计算得出
urel(3-4)(K)=0.002 8 μg/mL;u3-4(Na)=0.002 0 μg/mL。
则钾、钠工作曲线变动性引起的相对标准不确定度分别为
urel(3-4)(K)=u3-4(K)/ρ0(K)×100%=0.862%
(17)
urel(3-4)(Na)=u3-4(Na)/ρ0(Na)×100%=0.590%
(18)
3.3.5测量过程中产生的合成标准不确定度u3
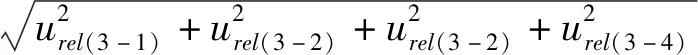
(19)
计算得出
urel(3)(K)=2.10%;u(3)(Na)=1.93%。
3.4 树脂分离铀基体产生的不确定度u4
样品溶液经CL-TBP萃淋树脂柱分离铀基体后,导致样品中钾、钠产生损失,其回收率见表4。
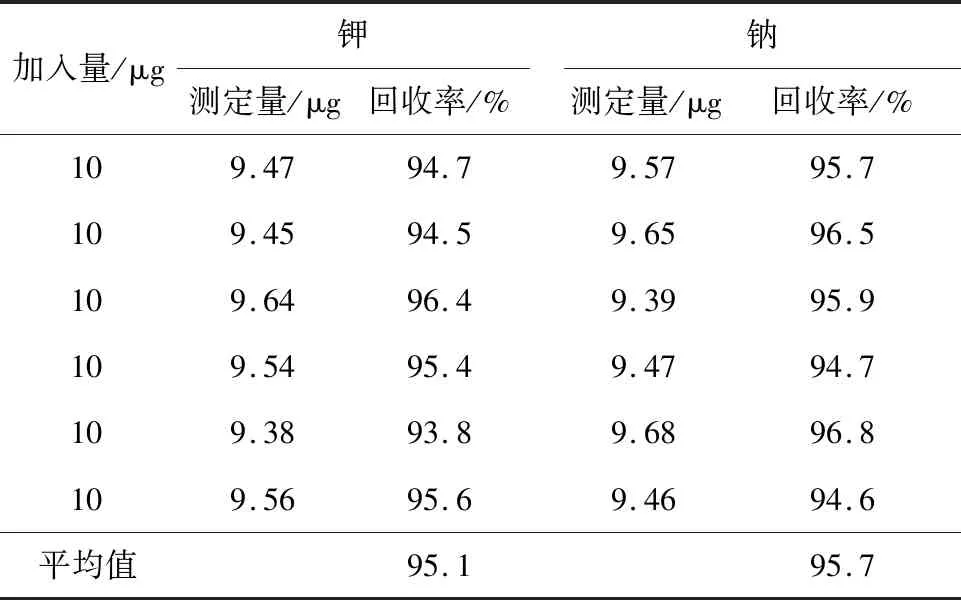
表4 树脂分离铀基体后,钾、钠回收率
由表4可知:树脂分离铀基体后,钾回收率为93.8%~96.4%;钠回收率为94.6%~96.8%。回收率分布区间(a-=xi-b-,a+=xi+b+)是不对称的,即相对于回收率最佳估计值xi(100%)并不对称。在缺乏用于准确判断分布状态的信息时,按均匀分布对树脂分离铀基体产生的不确定度进行评定,计算公式为
(20)
计算得出
u(4)(K)=1.41%;u(4)(Na)=1.32%。
则相对不确定度分别为
urel(4)(K)=1.48%;urel(4)(Na)=1.38%。
3.5 相对合成标准不确定度和扩展不确定度
因各不确定度分量相互独立,故相对合成标准不确定度计算公式为
(21)
计算得出
urel(K)=2.57%;urel(Na)=2.38%。
3.6 合成标准不确定度
uK=16.26×2.57%=0.42 μg/g
(22)
uNa=16.93×2.37%=0.40 μg/g
(23)
3.7 扩展不确定度
取扩展因子k=2,则扩展不确定度为
UK=0.42×2=0.84 μg/g
(24)
UNa=0.40×2=0.80 μg/g
(25)
3.8 结果与表示
U3O8中钾含量为(16.26±0.84) μg/g
(26)
U3O8中钠含量为(16.93±0.80) μg/g
(27)
4 结论
当采用火焰原子吸收光谱法(AAS)测定U3O8中钾、钠的含量时,钾、钠的含量结果的不确定度主要来源于样品溶液中钾、钠的测量过程中产生的不确定度(标准曲线拟合、标准溶液配制和重复性)和树脂分离铀基体产生的不确定度;而样品称量产生的不确定度和待测溶液定容体积产生的不确定度较小[6],可忽略不计。故在测定过程中应控制标准曲线线性和范围[7],使仪器保持在最佳状态[8],规范标准溶液配制和控制树脂分离条件,最大程度降低测量结果的不确定度。

