中国前列腺癌患者基因检测专家共识(2019年版)
中国抗癌协会泌尿男生殖系肿瘤专业委员会,中国临床肿瘤学会前列腺癌专家委员会
1 前言
随着第二代测序(n e x t-g e n e r a t i o n sequencing,NGS)技术在包括前列腺癌等肿瘤临床诊疗中得到愈发广泛的应用,对NGS在前列腺癌临床应用过程中的检测内容、检测技术、生物信息学分析、数据处理及解读等环节的质量管理提出了更高的要求。国外已出台了诸如《基因检测对遗传性前列腺癌风险评估作用:2017费城前列腺癌会议共识》[1](以下简称《费城共识》)等共识以规范该技术在前列腺癌患者诊疗及筛查中的应用;中国抗癌协会泌尿男生殖系肿瘤专业委员会也于2018年出版了《中国前列腺癌患者基因检测专家共识(2018版)》。《中国前列腺癌患者基因检测专家共识(2019年版)》(以下简称《本共识》)进一步综合国内外共识指南、最新发表的前列腺癌分子特征以及精准治疗相关研究数据,规范和指导前列腺癌基因检测的检测对象、检测内容、检测技术、数据处理及解读。推荐有意愿进行基因检测的受检者进行初步的肿瘤遗传咨询,在充分理解检测价值及必要性的情况后再进行相关检测。同时需要指出,虽然近年来已有部分数据发表,但中国前列腺癌患者基因突变特征及精准治疗的研究数据依然匮乏,未来需进一步结合中国前列腺癌患者的基因突变特征数据更新共识;同时呼吁建立医院、基因检测实验室(公司)等相关机构共同参与的协作数据共享平台或数据库,以明确中国前列腺癌患者的驱动基因突变分子特征及其与转移、复发、疗效评估、药物不良反应的相关性等信息。《本共识》专家委员会也倡导各单位组建生殖泌尿肿瘤精准医学专家团队(genitourinary molecular tumor board,GU-MTB),为肿瘤治疗提供更多选项,优化患者的个体化诊疗方案,并建立生物标志物引导的临床治疗路径。
2 适宜进行基因检测的对象
不同病情和治疗阶段的前列腺癌患者的基因突变特征各异[2],基于前列腺癌临床实践以及药物研发现状,推荐符合表1所列情形的前列腺癌患者考虑进行NGS基因突变检测。评估是否适宜进行基因检测需要结合前列腺癌患者的家族史、临床及病理学特征。其中家族史需要考虑:① 是否有兄弟、父亲或其他家族成员在60岁前诊断为前列腺癌或因前列腺癌死亡;② 是否在同系家属中具有多名包括胆管癌、乳腺癌、胰腺癌、前列腺癌、卵巢癌、结直肠癌、子宫内膜癌、胃癌、肾癌、黑色素瘤、小肠癌以及尿路上皮癌患者,特别是其确诊年龄≤50岁;③ 患者个人是否有男性乳腺癌或胰腺癌病史;④ 是否已知家族携带相关胚系致病基因突变。
对于初诊未进行风险评估、极低风险至中风险的前列腺癌患者,其家族史、临床特征的获得及遗传咨询是检测前的必要步骤:对于具有明确相关家族史、已知家族成员携带胚系致病基因突变的上述风险级别患者,推荐进行DNA损伤修复相关基因(特别是BRCA2、BRCA1、ATM、MSH2、MSH6、GEN1、FANCA、CHEK2)的胚系变异检测;对于家族史不详的上述风险级别患者,需要结合临床特征进行遗传咨询后综合判断是否有必要进行相关检测。而对于高风险、极高风险、局部进展及转移性前列腺癌患者,推荐进行DNA修复基因(特别是BRCA2、BRCA1、
AT M、M S H 2、M S H 6、G E N 1、FA N C A、CHEK2)的胚系变异检测。而对于所有转移性去势抵抗性前列腺癌(metastatic castration-resistant prostate cancer,mCRPC)患者,推荐进行至少包含DNA修复基因胚系及体细胞变异的检测。如肿瘤组织检测已发现与肿瘤发病风险相关基因突变而缺乏胚系变异验证的前列腺癌患者,建议遗传咨询后再考虑是否进行检测。
另外,前列腺导管内癌(i n t r a d u c t a l carcinoma of the prostate,IDC-P)和前列腺导管腺癌(ductal adenocarcinoma of the prostate,DAP)是前列腺癌中具有独特病理学特征的亚型。DAP发生率较低,仅占全部前列腺癌的1%;而IDC-P在不同的样本类型、风险及临床分期前列腺癌患者中所占比例不同:在低风险、中风险、高风险及转移复发前列腺癌中,IDC-P的比例分别为2.1%、23.1%、36.7%及56.0%[3]。与腺癌患者相比,IDC-P和DAP患者基因组不稳定性、错配修复基因及同源重组修复基因(特别是BRCA2基因突变)比例更高[4-6]。IDC-P和DAP患者预后较差,对具有该病理学特征的前列腺癌患者,不论是否存在明确的肿瘤家族史均推荐进行胚系基因检测。

表 1 适宜进行基因检测的前列腺癌患者
3 检测内容
虽然通过NGS技术发现多数mCRPC患者存在具有临床价值的基因突变[7],但是由于药物研发及相关药物在前列腺癌患者临床研究中的证据有限,针对前列腺癌患者的NGS基因检测应在增加受检者获益及避免过度检测中求得平衡。《二代测序技术在肿瘤精准医学诊疗中的应用专家共识》建议检测应包含国际、国内指南中明确指定、美国食品药品管理局(Food and Drug Administration,FDA)/中国国家药品监督管理局(National Medical Products Administration,NMPA)批准的适应证相关的临床分型基因突变,还应纳入正在开展的任何期别(Ⅰ~Ⅲ期)临床试验中的药物相关靶点、已完成或即将开展的临床试验的入组标准中药物相关靶点及其他癌种指南中推荐的药物相关靶点。有限基因数量的组合则可能导致治疗、遗传相关基因突变信息遗漏并增加受试者后续检测费用及样本损耗。因此《本共识》建议针对不同遗传背景及检测目的的受检者,应根据实际需要进行检测组合的筛选,检测组合和检测流程应在临床应用前进行充分的性能分析评估。其中,国际指南、共识及大型临床研究均发现DNA修复基因缺陷型前列腺癌患者可能对奥拉帕利(olaparib)等多聚腺苷二磷酸核糖聚合酶[poly(ADP-ribose)polymerase,PARP]抑制剂及铂类药物敏感;而DNA修复基因野生型前列腺癌患者对奥拉帕利的响应有限。再者,目前受到广泛关注的免疫检查点抑制剂如PD-1/PD-L1抗体在未经筛选前列腺癌患者中受益有限;《美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)指南》(以下简称《NCCN指南》)建议通过检测错配修复及微卫星不稳定性筛选出的错配修复缺陷(mismatch repair deficiency,dMMR)及高微卫星不稳定(microsatellite instability-high,MSI-H)型前列腺癌患者再考虑帕博利珠单抗(pembrolizumab)治疗(表2~3)。
同时根据检测目的需要区分胚系(germline)或肿瘤基因变异检测。其中胚系变异是指来源于父母生殖细胞的变异,可使用受试者的血液(优先考虑)、唾液、口腔拭子等样本进行检测;而肿瘤基因变异是指利用受试者肿瘤组织(如新鲜肿瘤组织、石蜡包埋组织切片等)或循环肿瘤DNA(circulating tumor DNA,ctDNA)进行变异检测,检测应包括胚系以及体细胞(机体细胞后天产生的基因变异),必要时需要进行胚系基因变异验证(或同时进行胚系基因变异检测)。
3.1 BRCA2、BRCA1及ATM
一项在2 019例受试者中进行的研究发现,携带胚系BRCA1/2基因突变与更具侵袭性、更高概率的淋巴结、远端转移发生及更短的生存时间相关[8]。TOPARP-A、TRITON2及TOPARP-B等多项大型临床研究均发现,具有DNA修复(特别是BRCA1/2)基因体细胞或胚系变异型mCRPC患者可能对PARP抑制剂敏感(表4)。目前PARP抑制剂尚未获得NMPA批准用于mCRPC患者的治疗,但有多项临床试验正在开展;同时有限的证据显示携带该分子特征的前列腺癌患者可能对铂类药物化疗敏感。国外数据显示,携带BRCA2基因突变的mCRPC患者比例为5%~9%,携带ATM基因突变的患者比例约为2%,携带BRCA1基因突变的患者比例约为1%[9];中国前列腺癌患者携带BRCA1/2及ATM基因突变比例的研究数据较为匮乏,近期发表的一项纳入316例中国前列腺癌患者的研究显示,6.33%的受试者携带BRCA2,0.63%的受试者携带BRCA1,0.63%的受试者携带ATM基因胚系致病变异[10]。

表 2 推荐前列腺癌患者进行的基因突变检测内容

表 3 前列腺癌基因检测的必要性等级说明
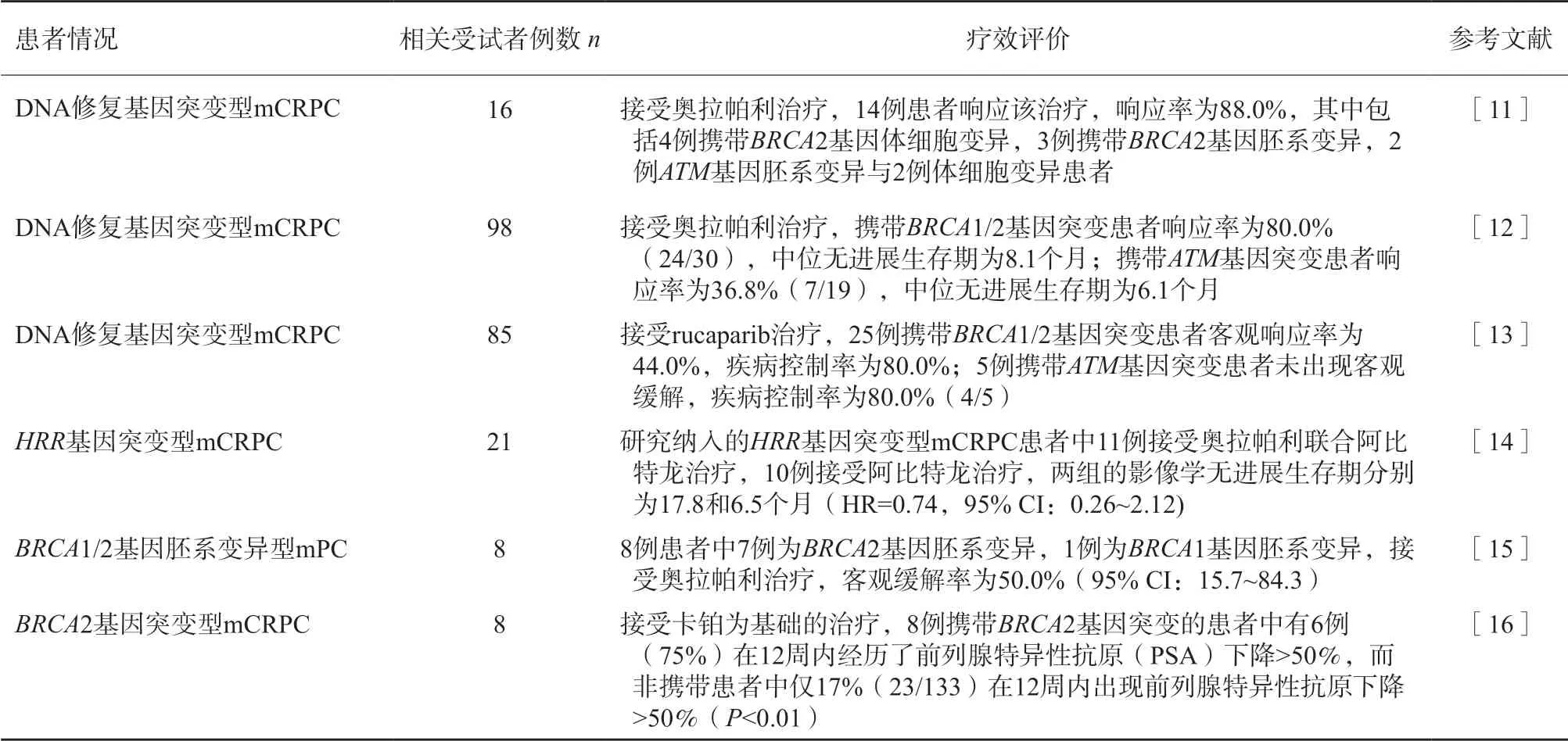
表 4 PARP抑制剂及铂类药物对前列腺癌患者的疗效评估
3.2 其他DNA修复相关基因
在转移性、高风险和中低风险前列腺癌患者中携带DNA修复基因突变的比例为11.8%、6.0%和2.0%[9];除上述的BRCA1/2及ATM基因外,在转移性前列腺癌患者中还检出CHEK2、RAD51D、ATR、NBN、GEN1、MRE11A、BRIP1及FAM175A等DNA修复基因胚系变异[9]。中国316例前列腺癌患者中除BRCA1/2、ATM外,还检出2例GEN1(0.63%)、1例CHEK2(0.31%)及1例FANCA(0.31%)基因胚系致病变异,提示中国转移性前列腺癌患者胚系基因突变谱与国外人群存在差异[10]。导致DNA修复缺陷的相关基因的胚系变异和体细胞变异,均是铂类药物和PARP抑制剂的增敏性潜在生物标志物,但由于携带该基因突变前列腺癌患者比例较低且临床入组人数有限,因此上述基因及具体变异与铂类药物和PARP抑制剂疗效的相关性有待进一步临床验证[11]。约5%的mCRPC患者可能携带CDK12基因突变/缺失,CDK12缺失与基因组不稳定性及免疫原性相关,有限的证据显示,携带该分子特征的患者可能对PARP抑制剂[12-13]及免疫检查点抑制剂敏感[17]。
3.3 错配修复基因
回顾性研究发现,错配修复基因突变型前列腺癌患者的临床和病理学特征更具侵袭性[18]。国外报道,前列腺癌患者中dMMR及MSI-H患者比例为2%~5%[7,19]。另有研究报道,约3%的前列腺癌患者携带MSH2(2%)、MLH1(1%)、MSH6(1%)及PMS2(<1%)基因体细胞变异,携带上述基因突变的患者往往具有最高的总体基因突变数量[2]。在中国316例前列腺癌患者中,携带MSH6、MSH2基因胚系致病变异的患者比例均为0.63%,未发现携带MLH1、PMS2基因胚系致病变异患者[10]。
既往研究认为,免疫检查点抑制剂在前列腺癌或CRPC患者中疗效不佳[20-21]。PD-1抗体帕博利珠单抗已于2017年5月获得美国FDA批准用于不可切除或转移性dMMR或MSI-H型实体瘤治疗。多项研究中纳入的有限数量的dMMR/MSI-H型前列腺癌患者均显示对帕博利珠单抗有较高的敏感性(表5)。《NCCN指南》推荐局部进展、转移性及mCRPC患者进行MSI-H及dMMR检测,如确诊为MSI-H或dMMR型,mCRPC患者可在特定治疗阶段考虑帕博利珠单抗治疗(2B类),同时需要进行遗传咨询及考虑林奇综合征(Lynch syndrome)的相关基因检测,进一步的MMR基因胚系变异检测可以明确其遗传性改变规律。考虑到先行免疫组织化学或MSI再根据结果决定行胚系变异检测的时间比较久,对于符合阿姆斯特丹标准或中国人林奇综合征家系标准(详见《遗传性结直肠癌临床诊治和家系管理中国专家共识》)、且有意愿将胚系变异的检测前置的前列腺癌患者可以考虑直接进行胚系变异检测[22]。

表 5 PD-1抗体对错配修复异常型前列腺癌患者的药效研究
3.4 其他基因
多项研究报道,在家族性前列腺癌患者中发现HOXB13基因突变(主要为G84E)[24];但是基于中国前列腺癌遗传学联合会前列腺癌的研究数据,在671例受检者中仅有3例携带HOXB13基因突变(P=0.027),且突变为G135E而非高加索人中的G84E热点[25]。HOXB13基因的检测并无明确的治疗指导作用,但对直系家属具有肿瘤风险评估价值。《费城共识》提出需要对与遗传性前列腺癌相关的HOXB13基因进行检测(共识率95%),但鉴于其在中国患者中的发生率及靶向治疗相关性,《本共识》建议综合受检者前列腺癌家族史考虑HOXB13基因突变的检测意义。
除同源重组修复基因及DNA错配修复通路相关基因外,研究发现前列腺癌患者中还会出现包括AR、TP53、PI3K/AKT信号转导通路(PTEN、PIK3CA、PIK3R1、AKT1、AKT3等)、WNT信号转导通路(APC、CTNNB1、RNF43等)、细胞周期通路(RB1、CCND1、CDKN2A/B、CDKN1B、CDK4等)、MAPK信号转导通路(BRAF、HRAS、KRAS等)以及染色体重塑(KMT2A、KMT2C、KMT2D、KDM6A等)等基因突变,但是由于药物研发及相关靶向药物在前列腺癌临床应用中的证据有限,对上述基因突变检测的意义仍有待进一步确认,同时鼓励具有相关基因突变的前列腺癌患者积极参与药物临床研究。
近期多项研究发现,RB1基因突变或缺失对mCRPC患者具有重要的预后预测价值。在mCRPC中,RB1基因突变/缺失与更差的生存期及阿比特龙或恩杂鲁胺更短的治疗时间有关[26-27]。另外,AR基因扩增/配体结构域变异及TP53基因突变也与前列腺癌阿比特龙及恩杂鲁胺敏感性降低相关[26]。
4 NGS检测流程的规范
NGS检测的全部流程包括从符合送检要求的样本中提取DNA、其后基于杂交捕获或扩增子建库方法进行文库构建,文库需测序至符合要求的测序深度;对于不同类型变异(包括碱基取代、插入缺失、拷贝数改变和基因重排)采用特定生物信息学分析方法进行分析和注释,最后对检测发现的基因突变信息进行分析并提出报告。送检样本及全部检测和分析报告流程应符合《临床分子病理学实验室二代基因检测专家共识》、《二代测序技术在肿瘤精准医学诊疗中的应用专家共识》和《基于下一代测序技术的BRCA基因检测流程中国专家共识》等共识基本要求,配备完善的标准操作流程及独立的质量控制程序。
5 GU-MTB
《本共识》专家委员会倡导各单位组建GUMTB,以进一步规范本中心的基因检测与精准治疗。GU-MTB成员至少应包括1名熟悉精准医学的肿瘤科医师(基于患者的临床病理学信息发起基因检测需求,熟悉检测信息用于患病风险、预后疗效、靶向治疗等临床场景,并对患者的检测及治疗结果进行跟踪随访)、1名病理科医师(评估患者的肿瘤标本特征并提供符合检测需求的送检样本)、1名经培训的肿瘤遗传咨询医师(对检测结果进行解读和咨询工作,并开展可能的家族患病风险评估和早期干预),以及充分认知相关领域精准医学进展的放射诊断科医师、外科医师、内科医师、核医学科医师和本中心临床试验管理医师(参与精准医学临床试验的设计和开展)。GU-MTB有助于为肿瘤治疗提供更多选项,优化患者的个体化诊疗方案,并建立生物标志物引导的临床治疗路径[28]。
参与本次共识讨论和审定的专家(按姓氏笔画排序):
丁德刚 河南省人民医院
马 琪 宁波市第一医院
王海涛 天津医科大学第二医院
王红霞 上海市第一人民医院
王小林 南通市肿瘤医院
王增军 江苏省人民医院
史本康 山东大学齐鲁医院
孙忠全 复旦大学附属华东医院
叶定伟 复旦大学附属肿瘤医院
何朝宏 郑州大学附属肿瘤医院
刘 承 北京大学第三医院
刘 南 重庆大学附属肿瘤医院/重庆市肿瘤研究所/重庆市肿瘤医院
齐 隽 上海交通大学医学院附属新华医院
邢金春 厦门大学附属第一医院
朱绍兴 中国科学院大学附属肿瘤医院(浙江省肿瘤医院)
朱伟智 宁波市鄞州第二医院
朱 耀 复旦大学附属肿瘤医院
陈惠庆 山西省肿瘤医院
苟 欣 重庆医科大学附属第一医院
肖 峻 中国科学技术大学附属第一医院
杨 勇 北京大学肿瘤医院
张爱莉 河北省肿瘤医院
张奇夫 吉林省肿瘤医院
邹 青 江苏省肿瘤医院
姚 欣 天津市肿瘤医院
胡 滨 辽宁省肿瘤医院
胡志全 华中科技大学同济医学院附属同济医院
袁建林 空军军医大学西京医院
涂新华 江西省肿瘤医院
翁志梁 温州医科大学附属第一医院
崔殿生 湖北省肿瘤医院
蒋军辉 宁波市第一医院
廖 洪 四川省肿瘤医院
魏 强 四川大学华西医院
薛波新 苏州大学附属第二医院
执笔专家:
朱 耀

