不同阶段慢性肾脏病患者血清成纤维细胞生长因子23与血管钙化的相关性
邢玥,贾俊亚,张雅濡,贺丹丹,林珊
(天津医科大学总医院 肾内科,天津 300052)
慢性肾脏病(chronic kidney disease, CKD)患者多存在钙、磷等矿物质代谢紊乱,骨骼结构及其组成的改变,血管和其他组织的异位钙化[1-3]。成纤维细胞生长因子23(fibroblast growth factor-23, FGF-23)可通过抑制机体对磷的吸收发挥降磷的作用,是磷代谢的重要调节因子,而磷代谢异常与肾脏功能异常密切相关,且磷代谢异常可诱发血管钙化[4-5]。本研究分析不同阶段CKD患者血清FGF-23的表达,并进一步研究其与钙磷代谢、肾功能指标及血管钙化的关系,现报道如下。
1 资料与方法
1.1 一般资料
选取2017年1月—2018年6月天津医科大学总医院肾内科收治的CKD患者128例。根据肾小球滤过率(glomerular filtration rate, GFR)将其分为CKD 1期组:GFR≥90[ml/(min·1.73m2)],CKD 2期组:GFR 60~89[ml/(min·1.73m2)],CKD 3期组:GFR 30~59[ml/(min·1.73m2)],CKD 4期组:GFR 15~29[ml/(min·1.73m2)],CKD 5期组:GFR<15[ml/(min·1.73m2)][6]。其中CKD 1~2期组患者41例,CKD 3~4期组患者共52例,CKD 5期组患者35例。 纳入标准:①符合《慢性肾脏病筛查诊断及防治指南》中关于CKD的诊断标准[6];②未接受透析治疗; ③临床资料完整,患者同意并配合完成本研究所有检测项目。排除标准:①合并有恶性肿瘤者;②合并有急性肾损伤、自身免疫性肾损伤;③原发性甲状旁腺功能亢进;④合并有严重感染、肝功能损害;⑤原发骨代谢疾病;⑥骨折;⑦妊娠期或哺乳期妇女。另选取同期在本院体检的健康群众50例作为对照组。各组研究对象的年龄、性别、体重指数(body mass index, BMI)比较,差异无统计学意义(P >0.05),CKD 1、2期组,CKD 3、4期组及CKD 5期组原发疾病比较,差异无统计学意义(P >0.05)。本研究获得本院伦理委员会的批准。见表1。
1.2 方法
CKD组患者于入院次日清晨、对照组于体检当日清晨抽取空腹静脉血5 ml,在室温下静置1 h,3 000 r/min离心10 min,分离血清,将其置于-70℃冰箱中待测。采用酶联免疫吸附法检测血清中FGF-23的水平,采用全自动生化分析仪(7600型,日本日立公司)检测血清中尿素氮(urea nitrogen, BUN)、血清肌酐(serum creatinine, Scr)、胱抑素C(Cystatin C, Cys C)、钙及磷的水平。通过简化肾病改良饮食公式来计算GFR。采用彩色多普勒超声仪(Sequoia 512型,德国西门子公司)检测颈动脉内中膜厚度(intimamedia thickness, IMT),测量双侧颈动脉分叉处的IMT,IMT>0.9 mm则定义为颈动脉粥样硬化,存在心血管钙化。采用彩色多普勒超声仪(Sonos 5500型,荷兰飞利浦公司)检查心脏超声结构,若主动脉瓣、二尖瓣瓣膜或瓣环出现1个或多个>1 mm的强回声即判为瓣膜钙化,若心肌探及>1 mm的强回声即判为心肌钙化。采用X射线检测所有患者的第11、12胸椎和第1~5腰椎,若发现条形或纵向线状高密度影即判为腹主动脉钙化。若患者存在心血管、瓣膜、心肌及腹主动脉钙化中的一种或者多种则纳入钙化组,否则纳入无钙化组,分别有43和85例。
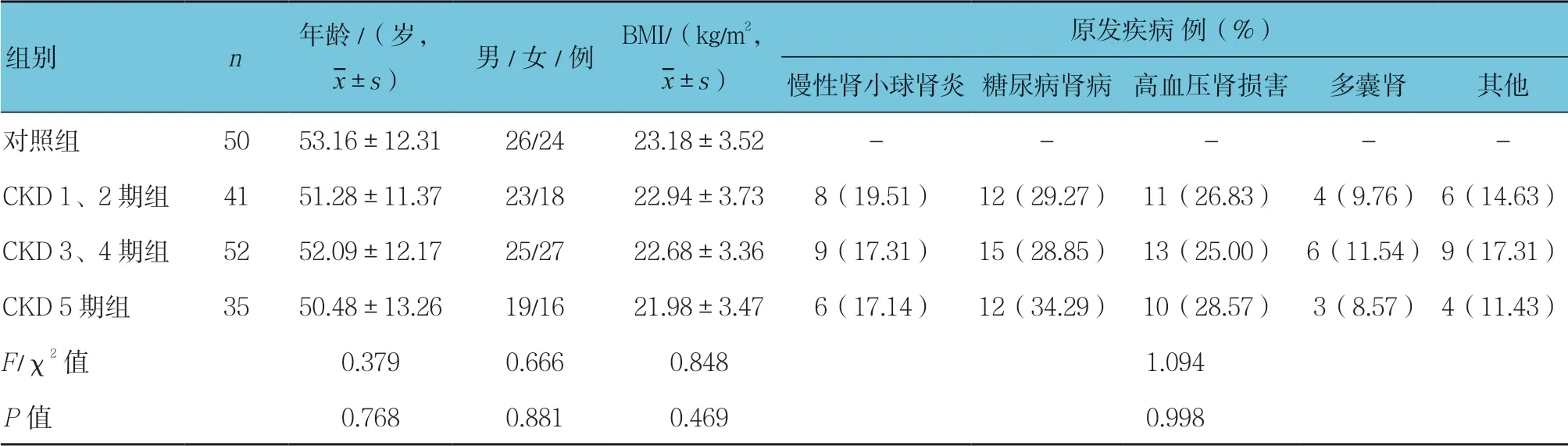
表1 各组一般资料比较
1.3 统计学方法
数据分析采用SPSS 20.0统计软件。计数资料以率(%)表示,比较用χ2检验,两两比较用χ2分割法;计量资料以均数±标准差(±s)表示,比较用方差分析,进一步的两两比较用LSD-t检验;相关分析用Pearson法;影响因素的分析采用非条件Logistic多元回归模型,P <0.05为差异有统计学意义。
2 结果
2.1 不同CKD分期组患者血清FGF-23及临床相关指标比较
不同CKD分期组和对照组患者血清FGF-23、BUN、Scr、Cys C、GFR、磷、钙及钙化率比较,差异有统计学意义(P <0.05),CKD 5期组的血清FGF-23、BUN、Scr、Cys C及磷均高于其他3组(P <0.05),GFR、钙均低于其他3组(P <0.05);CKD 3、4期组的血清FGF-23、BUN、Scr及Cys C均高于CKD 1~ 2期组和对照组(P <0.05),GFR低于CKD 1、2期 组和对照组(P <0.05);CKD 1、2期组的血清Scr、Cys C高于对照组(P <0.05),GFR低于对照组(P <0.05)。见表2。

表2 不同CKD分期组患者血清FGF-23及临床相关指标比较
2.2 有无血管钙化患者血清FGF-23及临床相关指标比较
有无血管钙化组和对照组患者血清FGF-23、BUN、Scr、Cys C、GFR及磷比较,经方差分析,差异有统计学意义(P <0.05),钙化组的血清FGF-23、BUN、Scr、Cys C及磷均高于无钙化组和对照组(P <0.05),GFR低于无钙化组和对照组(P <0.05)。见表3。
表3 有无血管钙化患者血清FGF-23及临床相关指标比较 (±s)

表3 有无血管钙化患者血清FGF-23及临床相关指标比较 (±s)
组别nFGF-23/ (pg/ml)BUN/(mmol/L)Scr/(μmmol/L)Cys C/(mg/L)GFR/[ml/(min·1.73m2)]磷/(mmol/L)钙/(mmol/L)对照组5021.68±6.234.73±1.2650.36±14.520.82±0.18112.31±12.651.21±0.182.17±0.14无钙化组8552.63±15.4210.81±4.93196.31±42.512.28±0.3746.91±9.651.35±0.252.08±0.24钙化组4395.13±21.2419.47±6.18464.73±63.623.51±0.9623.03±10.171.72±0.312.11±0.25 F值263.917121.730995.836278.047912.88853.0522.612 P值0.0000.0000.0000.0000.0000.0000.075
2.3 CKD患者血清FGF-23与临床相关指标的相关性
经Pearson分析显示,CKD患者血清FGF-23与BUN、Scr、Cys C及磷呈正相关(r =0.532、0.653、0.548和0.384,P =0.000、0.000、0.000和0.012),与GFR呈负相关(r =-0.637,P =0.000),与钙无相关性(r =-0.152,P =0.152)。
2.4 CKD患者血清FGF-23的Logistic回归分析
以FGF-23为应变量,其余差异有统计学意义指标为自变量,建立非条件Logistic多元回归模型。为使回归结果的OR意义准确清晰,各变量均进行两分类转化:取CKD患者血清FGF-23及其他指标的均值为界,高于均值为高表达,低于则为低表达,其中高表达赋值为1,低表达赋值为0,存在血管钙化赋值为1,无血管钙化赋值为0。回归过程采取后退法,α退出=0.05。经Logistic回归分析得知,GFR和磷是血清FGF-23的影响因素(P <0.05),GFR(升高)为负向(保护)影响因素,磷(升高)为正向(危险)影响因素。见表4。

表4 CKD患者血清FGF-23的Logistic回归分析参数
3 讨论
全世界CKD患病率已达到14.3%[7]。我国流行病学调查显示,我国成年人的CKD患病率为10.8%~13.4%,可见CKD已成为重要的公共卫生问题[8]。在CKD患者的肾功能进行性损害过程中机体会出现明显的钙、磷代谢紊乱,肾功能受损后导致肾脏排磷能力减弱,出现磷潴留,而血磷水平过高可加速钙的磷酸化,降低血钙水平[9]。此外,有大量研究发现,CKD患者进展至终末期后发生心血管事件的概率会大幅度增加,这主要是因为CKD患者在疾病进展过程中易出现血管钙化[10-12]。
本研究结果显示,随着临床分期的不断增加,CKD患者的肾功能受损越来越严重,且钙化率越来越高,FGF-23的水平在CKD 3、4期开始上升,钙、磷水平在CKD5期出现波动。虽然在CKD早期即会出现钙、磷代谢紊乱,但机体可通过代偿机制分泌FGF-23和甲状旁腺激素来进行调节[13-14]。同时FGF-23可通过抑制Ⅱ型钠磷协同转运子的表达减少肾脏对磷的重吸收和肠道磷的吸收,进而维持钙磷稳 态[15-16]。然而在CKD晚期,患者的GFR下降明显,FGF-23通过尿磷的排泄调节血磷的作用越来越微弱,而另一方面机体的Klotho蛋白会随着肾功能的下降而减少,这会影响FGF-23与其受体结合,导致尿磷排泄减少,此外,血磷的升高会刺激FGF-23分泌,导致FGF-23水平持续升高[17]。在CKD早期,由于血磷水平过高,机体通过代偿机制分泌FGF-23来调节磷代谢,增加FGF-23的表达,而在CKD终末期,血磷与FGF-23的正反馈调节机制会刺激FGF-23水平持续上升,因此FGF-23水平在CKD进展的过程中保持上升的趋势。本研究结果还显示,存在血管钙化的患者血清FGF-23、磷水平均高于无血管钙化的患者和对照组,血磷过高是引起血管钙化的重要危险因素。高磷环境可促使血管平滑肌细胞向成骨样细胞表型转换,并且可促进血管平滑肌细胞释放基质囊泡,进而导致细胞外基质重塑[18]。廖琳等[19]研究证明,钙磷乘积为血液透析患者颈动脉钙化独立危险因素。而YAO等[20]通过动物实验证明,高磷可通过激活Wnt/β-catenin通路活化β-catenin,进而调控III型钠磷转运体,促进血管平滑肌细胞的表型转换,进而加速血管钙化进程。由此可以推测,血清FGF-23可能是通过调节磷代谢来参与血管钙化的进展。此外本研究还显示,CKD患者血清FGF-23与BUN、Scr、Cys C及磷呈正相关,与GFR呈负相关,这进一步说明血清FGF-23可以衡量CKD患者的肾损伤程度。非条件Logistic多元回归分析结果显示,GFR和磷是血清FGF-23的显著影响因素,这进一步说明血清FGF-23会受到GFR和磷的影响。
综上所述,CKD患者的血清FGF-23水平在 CKD 3、4期明显上升,且在CKD5期呈异常高表达,并且在存在血管钙化的CKD患者血清中也呈异常高表达。

