七水氯化镧结晶介稳区的测定和初级成核分析
张文豪,杨立斌,沙作良,王彦飞,朱 亮,赵晓昱
(天津科技大学化工与材料学院,天津市海洋资源与化学重点实验室,天津市海洋化工技术工程中心,天津300457)
氯化镧是非常重要的一类稀土化合物,广泛应用于陶瓷、荧光、电子等领域[1],在化学工业生产中发挥着重要作用。目前,氯化镧的制备方法主要有干法和湿法两种。其中湿法主要是盐酸法,这种方法是用盐酸与含有丰富稀土镧元素的氧化物、氢氧化物或碳酸盐进行反应,制得氯化镧水溶液,再经过蒸发浓缩,冷却结晶得到含有一定数目结晶水的氯化镧晶体。根据之前文献的报道可知七水氯化镧平衡固相的温度区间在 264.15~367.15 K[2],最重要的结晶过程也是在这一区间进行,所以取这一温度区间中最为代表性的部分273.15~353.15 K作为研究对象。 J.E.Powell等[3]测定了 273.15~353.15 K 部分温度下氯化镧在纯水中的溶解度,但是测定的结果存在一定的偏差。另外,氯化镧结晶生产工艺虽然比较成熟,但在生产中仍然存在产品纯度不高、晶体粒度小或分布较宽等问题。有些研究者对氯化镧的结晶纯化过程和制备方法进行了初步论述[1,4],但与结晶纯化工艺和制备方法有关的其他基础数据,诸如结晶介稳区、晶体成核等,还未见系统研究的报道。根据以往研究中存在的不足,分别测定了七水氯化镧在水中的溶解度和超溶解度数据,并对所得数据点进行了拟合,得到了氯化镧水溶液冷却结晶介稳区宽度的数据;同时,分别考察了在不同的温度下介稳区宽度受降温速率与搅拌速率变化的影响,并通过模型分析得到过程参数如搅拌速率和降温速率与成核级数的关系,为氯化镧结晶工艺优化和工业设计生产提供基础数据和理论指导。
1 实验试剂及仪器
1.1 材料与试剂
七水氯化镧(纯度≥99.9%);硝酸银(AR);铬酸钾(AR);蒸馏水(自制)。
1.2 设备与分析仪器
85-2A型数显恒温测速磁力搅拌器;PL3002型电子精密天平;K6型控温装置;JDW-3型激光电源;JHS-2/90型恒速数显搅拌器。
2 实验方法
2.1 七水氯化镧在水中溶解度的测定
在圆柱形玻璃加套结晶器中加入一定量的蒸馏水,采用恒温循环水浴装置恒定在设定温度。加入过量的七水氯化镧固体,恒温搅拌一段时间直至溶解平衡,停止搅拌,静置。采用预热过的带滤膜的10 mL注射器取上层清液备用,采用化学滴定方法分析氯离子含量;采用药匙从底部取少量固体,抽滤,得到固体后在303 K下真空干燥至恒重。实验装置见图1。
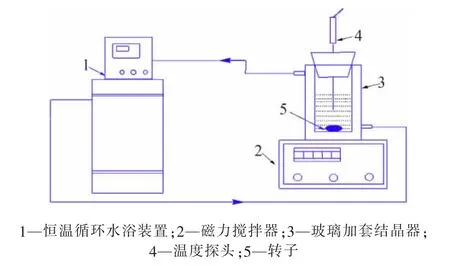
图1 氯化镧水溶液溶解度测定实验装置
2.2 氯化镧水溶液冷却结晶介稳区的测定
氯化镧水溶液冷却结晶介稳区宽度采用激光接收系统测定,即在玻璃夹套结晶器中配制一定浓度的氯化镧水溶液,开启恒温循环水浴装置控制溶液达到设置温度 (高于此时达到饱和溶液所需的温度),开启搅拌。同时开启激光接收系统,恒温搅拌至激光记录仪的示数基本不变,开始按设定降温速率降温冷却,密切关注激光记录仪的示数变化,当数值发生突变时,记录溶液的温度。实验装置见图2。
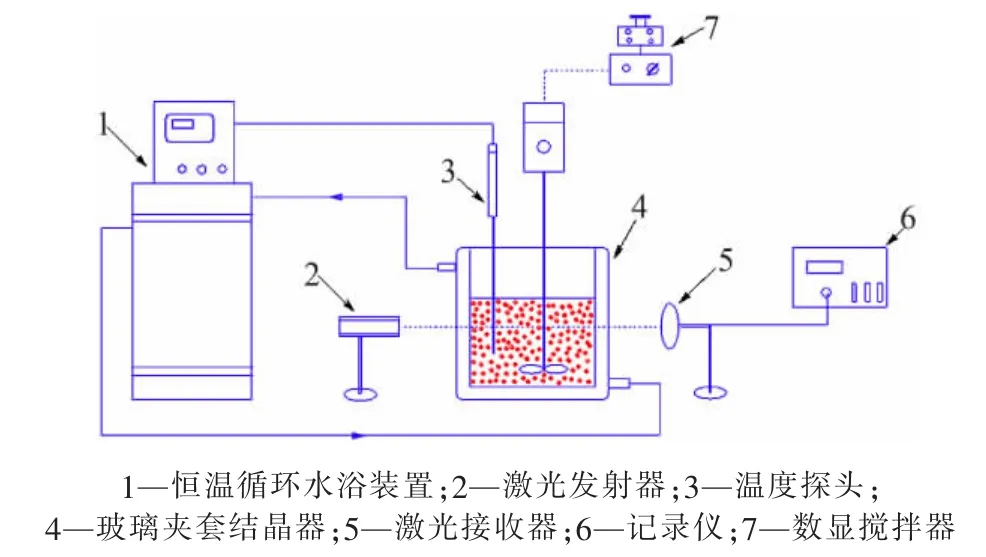
图2 氯化镧介稳区测定实验装置
3 实验结果与讨论
3.1 七水氯化镧在水中的溶解度
七水氯化镧在水中的浓度用物质的量分数x表示,见式(1):

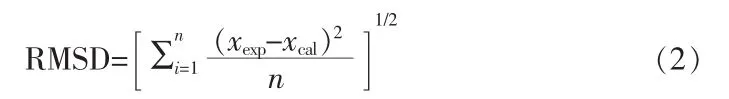
式中,n为实验点数,xexp为溶解度的实验值,xcal为溶解度的模型计算值。
无机盐类水溶液体系可以选用Apelblat方程和λh方程来描述和预测其溶解平衡。
3.1.1 Apelblat方程拟合的结果
基于固液平衡理论,得到了描述固-液平衡一致性的溶解度方程即 Apelblat方程[5]:
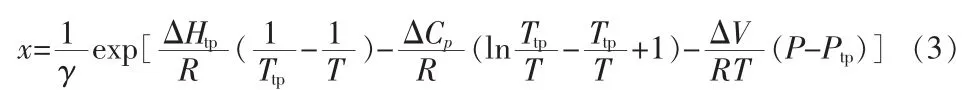
式中,m1和m2分别为七水氯化镧、水的质量,g;M1和M2分别为七水氯化镧、水的摩尔质量,g/mol。
用均方根偏差(RMSD)评估七水氯化镧在水中的溶解度的模型值与实验值的一致性,见式(2):
式中,x为溶质在溶剂中的物质的量分数,%;γ为溶质的活度系数;ΔHtp为固液转化时三相点处的摩尔熔融焓,J/(mol·K);R为气体常数,8.314 J/(mol·K);Ttp为三相点处的溶解温度,一定条件下可用熔点(Tm)代替,K;T为溶液温度,K;ΔCp为在熔点处固液两相的恒压热容差,J/(mol·K);ΔV为体积变化的差值,m3/mol;Ptp为在三相点处的压力,Pa。
当满足一定条件时,将式(3)进一步简化可以写成修正的 Apelblat方程[6],如式(4)所示:

式中,x为七水氯化镧的物质的量分数,%;T为溶液的热力学温度,K;A,B,C分别为用溶解度的实验数据拟合得到的回归参数。
3.1.2 λh方程拟合的结果
H.Buchowski等[7-8]推导出了溶质在溶剂中的溶解度,溶质的活度系数和温度之间的关系,并根据固-液溶解相平衡理论推导得到了缔合溶液的溶解度模型,被称之为λh方程,其具体形式见式(5):
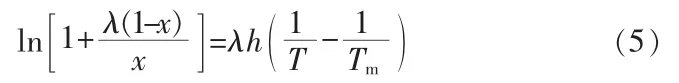
式中,x为七水氯化镧的物质的量分数,%;T为溶液的热力学温度,K;Tm为七水氯化镧的熔点,K;λ是非理想性溶液体系中的无因次参数;另一个参数h的定义如下:
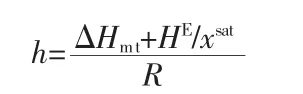
式中,ΔHmt为固液转化过程的熔融焓变,J/(mol·K);HE为混合过程的过量焓,J/(mol·K);xsat为溶质在饱和溶液中的物质的量分数,%。由于缺少基本的热力学数据,所以方程中的模型参数λ和h通常由实验数据进行拟合得到[9]。
将实验所测量得到的溶解度数据分别采用Apelblat模型方程(4)和 λh模型方程(5)进行非线性拟合,并用均方根偏差(RMSD)评估,结果见图3。分析表明两种模型方程均适用七水氯化镧在水中的溶解度,两个模型方程拟合结果如公式(6)和公式(7)所示,相关系数R2分别为0.995 2和0.987 5,均方根偏差分别为2.842×10-3和 4.998×10-3。 如图 3所示,Apelblat模型方程拟合曲线和λh模型方程拟合曲线均能有效地描述七水氯化镧在水中的溶解度变化规律,即七水氯化镧在水中的溶解度随温度的升高而增大且呈指数型变化。
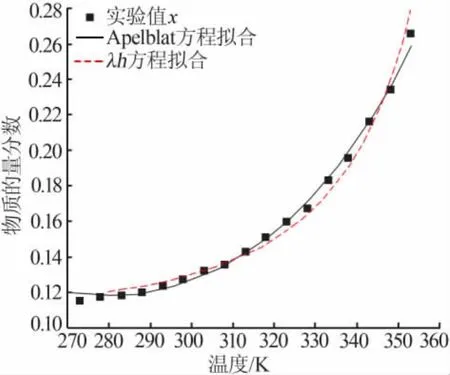
图3 Apelblat方程和λh方程对实验值的拟合结果
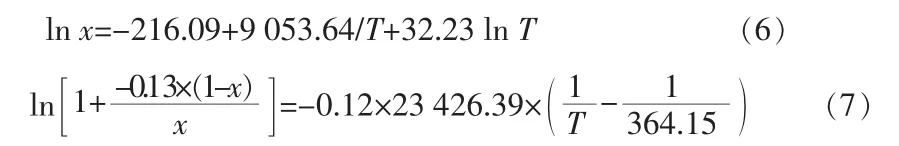
3.2 氯化镧冷却结晶介稳区宽度
为了描述氯化镧冷却结晶过程中控制参数与过饱和度变化及晶体成核的关系,除溶解度数据外,超溶解度与溶解度间的介稳区域也是关键数据之一。如图4所示,超溶解度曲线与溶解度曲线间的区域是氯化镧的介稳区,其介稳区的宽度在49.4~69.8 K,一般的无机盐如氯化钾和氯化钠等[10-11]的介稳区宽度在4~16 K,氯化镧的介稳区比一般无机盐的介稳区要宽很多,这主要是因为氯化镧本身的溶解度特别大,而且结晶产物含有7个结晶水,这就造成了氯化镧成核所需要的过饱和度要很大,在结晶过程中水占到晶格上需要克服能垒,成核难度增加,使得氯化镧的结晶介稳区变宽。由于氯化镧的结晶介稳区宽度大,所以氯化镧的结晶受温度的影响很大,因此,对后面成核级数的实验测定有很大的必要性。
氯化镧的介稳区具体变化趋势见图5,随着溶液浓度的升高,所对应的氯化镧介稳区宽度呈现先减小再增大的趋势。这是因为当溶液的浓度相对较低时,如果增大溶液浓度,则溶质离子的数目增多,相互碰撞的机率变大,离子更容易克服成核能垒,而相互聚集在一起形成晶坯,晶坯会继续长大形成晶核和一定尺寸的晶体;随着温度升高,溶液饱和浓度变大,溶质离子的扩散系数减小,离子之间的热运动会降低,使氯化镧离子克服成核能垒的难度增大,不易成核,从而介稳区又变宽。
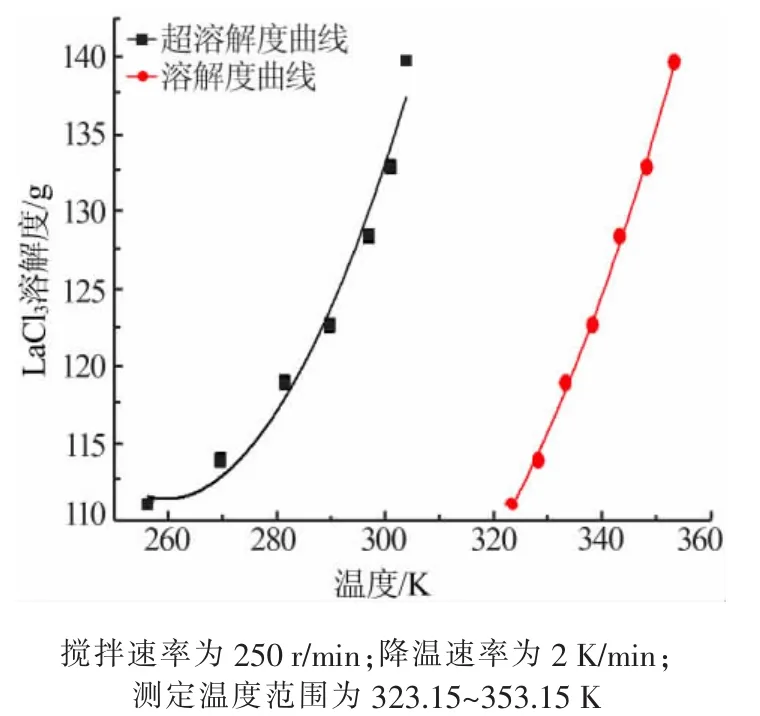
图4 氯化镧水溶液中的超溶解度曲线和介稳区
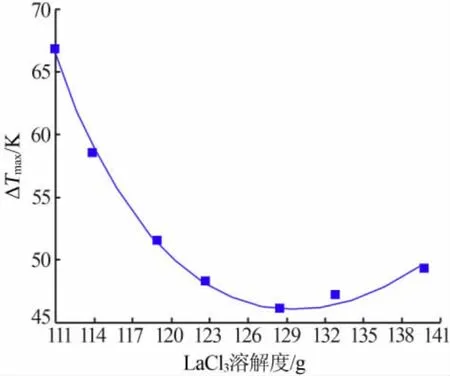
图5 不同饱和浓度下氯化镧结晶介稳区宽度的变化曲线
3.3 氯化镧冷却结晶初级成核分析
通过蒸发或者冷却可以使氯化镧溶液达到过饱和状态,当系统过饱和度增大到一定程度即超过临界过饱和度时,溶液会发生晶体的初级成核。根据经典成核理论,成核速率可表示为:

式中,B0为成核速率,kg/(m3·min);K0为成核速率常数;N为搅拌速率,r/min;m为与过饱和度大小相关的成核级数;n为与搅拌速率大小相关的成核级数。
根据 J.Nyvlt[12]得到的冷却结晶的分析理论,初级成核速率能够用由冷却产生的过饱和度速率来表示,即:

式中,q为每单位质量的溶液冷却1 K时结晶析出溶质晶体的量,kg/(m3·K);b为溶液的降温速率,K/min。
q为结晶固体质量和溶液浓度变化的函数:

式中,ε为物系常数;溶液的最大过饱和度与最大介稳区宽度的关系为:
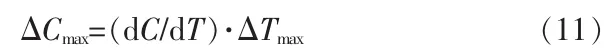
式中,ΔCmax为溶液最大过饱和浓度,kg/m3;C是溶液的饱和浓度,kg/m3;ΔTmax是溶液最大介稳区宽度的值即最大过冷度,K。
将式(9)、(10)、(11)代入式(8)可得:
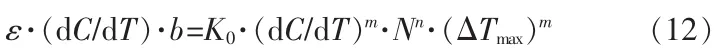
将式(12)两边取对数可得:
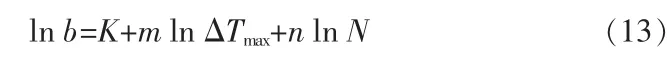
其中
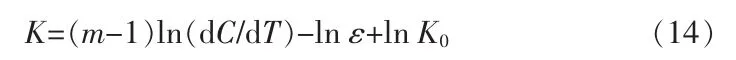
当搅拌速率一定时,式(13)可以简化为:

同理,当降温速率一定时,式(13)可以简化为:
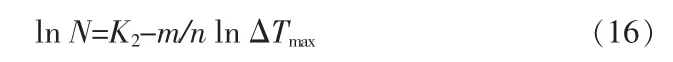
lnb、lnN与ln ΔTmax作图均可得到直线,直线的斜率即为成核级数。
3.3.1 降温速率对初级成核的影响
在该实验中,实验条件是搅拌速率恒定为250 r/min,通过观察在不同的降温速率条件下晶体成核的过程变化,来得到所需的氯化镧冷却结晶介稳区数据。
不同降温速率与介稳区宽度关系见图6。从图6可以看到,在一定的初始温度下,保持恒定的搅拌速率,介稳区宽度会随降温速率b的不断增大而变宽,这是由于随着降温速率b的增大,形成过饱和溶液的时间变短,容易形成较大的过饱和度,才有可能爆发成核,即介稳区变宽。
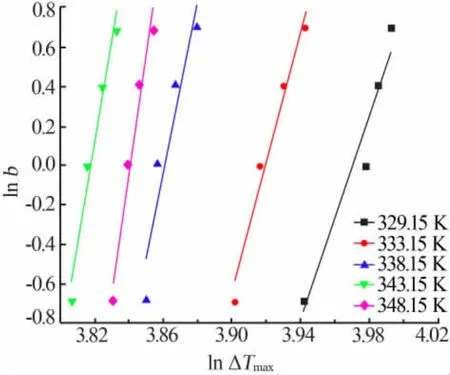
图6 不同降温速率与介稳区宽度关系
根据公式(15),可推导出降温速率与介稳区宽度的关系,分别拟合不同初始温度下降温速率与介稳区宽度的关系式如表1所示。从表1可以得知,氯化镧溶液冷却结晶成核过程中,受降温速率影响的成核级数m与温度有关,随温度升高而增大。成核级数越大,冷却结晶时越易爆发成核。这是因为氯化镧的溶解度随温度的升高而变大,当以一定的初始浓度恒定降温速率进行冷却结晶时,初始浓度越高,因冷却产生的过饱和度就会越大,晶核形成后数量会急剧增多,容易发生爆发成核,表现出的成核级数就会越大。

表1 不同降温速率下成核级数方程与成核级数
氯化镧溶液受降温速率影响的成核级数m,比一般无机盐的成核级数大得多,如氯化钾和无水硫酸钠[10,13]的成核级数均在 2~6 之间,说明氯化镧结晶受温度的影响更大,爆发成核的程度会更加剧烈,不易控制。
3.3.2 搅拌速率对初级成核的影响
实验中降温速率b恒定为2 K/min,改变搅拌速率观察晶核出现的温度变化,得到氯化镧介稳区宽度数据。搅拌速率与介稳区宽度关系见图7。如图7所示,随着搅拌速率的增大,氯化镧溶液冷却结晶过程中的介稳区宽度会变窄。因为搅拌速率增大,加快了溶液中的传质、传热速率,使溶质离子的碰撞机率增加,同时,加快了溶液的热量扩散,降低了溶液的过饱和度,因此,溶液中形成晶核的机率增大,介稳区宽度变窄[13]。
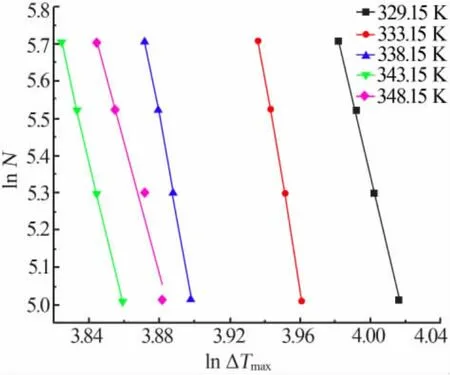
图7 搅拌速率与介稳区宽度关系
结合公式(16)可推导出搅拌速率与介稳区宽度的关系,分别拟合不同温度下搅拌速率与介稳区宽度的关系式如表2所示。从表2可以得知,在冷却结晶过程中,lnN与ln ΔTmax之间均呈线性关系,且直线斜率不相等,表明成核级数与温度相关。受搅拌速率影响的成核级数n随温度的升高而增大,成核级数越大,溶质离子越容易聚集成核。

表2 不同搅拌速率下成核级数方程与成核级数
由以上拟合得到的不同温度下降温速率、搅拌速率与介稳区宽度的关系式,得到了受降温速率和搅拌速率影响的初级成核级数m和n,根据表1和表2中初级成核级数的分析,可以看出受降温速率影响的初级成核级数m的值远远大于受搅拌速率影响的初级成核级数n的值,这说明在氯化镧的冷却结晶过程中降温速率对成核的影响程度更为关键。因此,在氯化镧结晶过程中,应根据具体的情况选择最适宜的降温速率,维持结晶体系所需过饱和度的稳定,使溶液中的溶质能及时附着在晶核上,避免因爆发成核影响晶体的生长。受降温速率和搅拌速率影响的初级成核级数m和n与介稳区宽度的关系确定,为氯化镧的结晶工艺和动力学的研究提供了必要的理论基础。
4 结论
1)七水氯化镧的溶解度随温度的升高而增大,Apelblat经验方程和λh方程均可高度拟合溶解度数据。2)氯化镧相比一般无机盐的结晶介稳区宽度要大得多,说明氯化镧的结晶过程受温度的影响更为显著。随着溶液浓度的增大,氯化镧水溶液冷却结晶介稳区宽度呈现先减小再增大的趋势;随着降温速率b的增大和搅拌速率N的减小,氯化镧冷却结晶介稳区的宽度变宽。3)受降温速率b和搅拌速率N影响的成核级数m和n,均与冷却结晶的温度有关,即随温度的升高而增大,且温度越高成核越容易,越易爆发成核,且与一般无机盐相比,成核级数大得多,成核受温度的影响更大,爆发成核的程度会更加剧烈。

