伊马替尼、尼洛替尼和达沙替尼对慢性粒细胞白血病慢性期的临床分析
陈锋文 何宏梅

【摘要】 目的:探討伊马替尼、尼洛替尼和达沙替尼对慢性粒细胞白血病慢性期的临床效果情况。方法:分析广东省化州市人民医院2013年2月-2016年2月收治的慢性粒细胞白血病患者78例临床资料,依据治疗药物不同进行分组,治疗Ⅰ组(伊马替尼治疗)22例,治疗Ⅱ组(尼洛替尼治疗)30例,治疗Ⅲ组(达沙替尼治疗)26例。观察三组慢性粒细胞白血病患者不同时间点完全细胞遗传缓解率(CCyR)、完全血液学缓解率(CHR)、分子生物学缓解率(MMR)、不良反应情况。结果:三组患者CHR比较,差异均无统计学意义(P>0.05)。治疗18个月时,治疗Ⅱ组、治疗Ⅲ组患者MMR均高于治疗Ⅰ组,差异均有统计学意义(P<0.05);治疗6、18个月时,治疗Ⅱ组、治疗Ⅲ组患者CCyR均高于治疗Ⅰ组,差异均有统计学意义(P<0.05);治疗Ⅱ组、治疗Ⅲ组患者头痛、呕吐、水肿发生率均低于治疗Ⅰ组,差异均有统计学意义(P<0.05);三组患者血小板减少症、嗜中性粒细胞减少发生率比较,差异无统计学意义(P>0.05)。结论:尼洛替尼和达沙替尼治疗慢性粒细胞白血病患者,CCyR和MMR改善效果更加明显,值得临床推广应用。
【关键词】 伊马替尼; 尼洛替尼; 达沙替尼; 慢性粒细胞白血病慢性期
doi:10.14033/j.cnki.cfmr.2019.10.007 文献标识码 A 文章编号 1674-6805(2019)10-00-03
The Clinical Analyzing of Chronic Myeloid Leukemia in Chronic Phase by Imatinib,Nilotinib and Dasatinib/CHEN Fengwen,HE Hongmei.//Chinese and Foreign Medical Research,2019,17(10):-17
【Abstract】 Objective:To approach clinical result of chronic myeloid leukemia in chronic phase by Imatinib,Nilotinib and Dasatinib.Method:The 78 cases clinical data of chronic myeloid leukemia in the people hospital Guangdong province Huazhou city from February 2013 to February 2016 were analyzed,the patients were divided into three groups by different treatment drug,treatment group Ⅰ(22 cases,Imatinib treatment),treatment group Ⅱ(30 cases,Nilotinib treatment) and treatment group Ⅲ(26 cases,Dasatinib treatment).The CCyR,CHR,MMR,adverse reactions of three group chronic myeloid leukemia in different time were detected.Result:The CHR of three group were compared,the differences were no statistical significance(P>0.05);at treatment of 18 months,the MMR of treatment group Ⅱ,treatment group Ⅲ were higher than treatment group Ⅰ,the differences were statistically significant(P<0.05).At 6 and 18 months of treatment,CCyR of treatment group Ⅱ and treatment group Ⅲ were higher than those of treatment group Ⅰ,with statistical significance(P<0.05).The headache,vomit,edema rate of treatment group Ⅱ,treatment group Ⅲ patients were lower than those of treatment group Ⅰ,the differences were statistical significant(P<0.05).The thrombocytopenia,neutrophils rate of three group patients were compared,the differences were no statistical significance(P>0.05).Conclusion:The chronic myeloid leukemia patients by Nilotinib and Dasatinib,improving result of CCyR and MMR is obviously,it is worth to be used.
【Key words】 Imatinib; Nilotinib; Dasatinib; Chronic myeloid leukemia in chronic phase
First-authors address:The Peoples Hospital in Huazhou City,Huazhou 525100,China
慢性粒细胞白血病起源于造血干细胞,其不断激活断点簇集区-艾贝尔逊白血病毒酪氨酸激酶,形成恶性骨髓增殖[1-2]。其典型特征是费城染色体、断点簇集区-艾贝尔逊白血病毒蛋白,可以活化下游多个信号转导通路,促进白血病细胞增殖、凋亡[3-4]。伊马替尼作为一线治疗慢性粒细胞白血病药物,其属于酪氨酸激酶抑制剂[5]。随着医药技术不断进步,酪氨酸激酶抑制剂不断发展,慢性粒细胞白血病临床效果也在不断提高。笔者通过分析广东省化州市人民医院2013年2月-2016年2月收治的慢性粒细胞白血病慢性期患者78例临床资料,拟探讨伊马替尼、尼洛替尼和达沙替尼对慢性粒细胞白血病慢性期的临床效果,现将结果汇报如下。
1 资料与方法
1.1 一般资料
选取广东省化州市人民医院2013年2月-2016年2月收治的慢性粒细胞白血病慢性期患者78例临床资料进行分析,入选标准:慢性粒细胞白血病慢性期诊断标准参照《中国慢性髓性白血病诊断与治疗指南(2016年版)》标准,即外周血嗜碱粒细胞比例小于20%,原始细胞比例<15%,骨髓增生现象明显[6];通过酪氨酸激酶抑制剂进行治疗,对其随访时间>18个月,呈现Ph阴性。排除标准:既往有酪氨酸激酶抑制剂治疗史患者,非慢性期患者。依据治疗药物不同进行分组,治疗Ⅰ组22例,男13例,女9例;年龄20~69岁,平均(38.4±10.6)岁;Sokal评分:低危10例,中危10例,高危2例。治疗Ⅱ组30例,男17例,女13例;年龄21~68岁,平均(37.5±11.8)岁,Sokal评分:低危12例,中危13例,高危5例。治疗Ⅲ组26例,男14例,女12例;年龄24~67岁,平均(37.1±11.2)岁;Sokal评分:低危11例,中危11例,高危4例。三组患者一般资料比较,差异无统计学意义(P>0.05)。
1.2 方法
治疗Ⅰ组给予伊马替尼(瑞士诺华制药有限公司,批号:S0167)初始剂量400 mg/d,1次/d,当发生耐药症状,增加剂量达到600~800 mg/d,1次/d,如果达到800 mg/d仍然耐药,给予尼洛替尼或者达沙替尼(用药量参照Ⅱ组、Ⅲ组)进行治疗,1次/d,治疗后Ⅰ组患者最终均无换药治疗。
治疗Ⅱ组给予尼洛替尼(瑞士诺华制药有限公司,批号:AMN108)治疗,300 mg/d,1次/d,服药前禁食2 h,服药之后禁食1 h,当发生耐药时,增加剂量达到600 mg/d,1次/d。
治疗Ⅲ组给予达沙替尼(江苏正大天晴药业有限公司,批号:130205)治疗,100 mg/d,1次/d。
上述三组如果发生不良反应,停止用药。三组患者连续治疗18个月。
1.3 观察指标
观察三组慢性粒细胞白血病慢性期患者不同时间点完全细胞遗传缓解率(CCyR)、完全血液学缓解率(CHR)和分子生物学缓解率(MMR)情况,完全细胞遗传缓解是指通过临床治疗后骨髓中未发现Ph(+)细胞[7-8];完全血液学缓解是指患者外周血白细胞(WBC)<10×109/L,血小板(PLT)<450×109/L,WBC分类中无幼稚细胞,无白血病的临床症状和体征[9-10];分子生物学缓解是指骨髓RT-PCR,bcr-abl/abl<5[11-12]。不同时间点为治疗后3、6、18个月。
观察三组慢性粒细胞白血病慢性期患者不良反应情况。主要观察头痛、呕吐、水肿、血小板减少症、嗜中性粒细胞减少。
1.4 统计学处理
本研究数据采用SPSS 22.0统计学软件进行分析和处理,计量资料以(x±s)表示,采用t检验,计数资料以率(%)表示,采用字2检验,P<0.05为差异有统计学意义。
2 结果
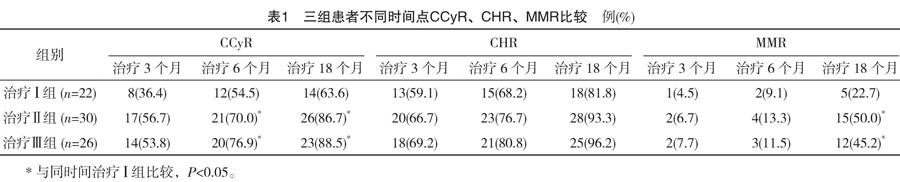
2.1 三组患者不同时间点CcyR、CHR、MMR比较
治疗3、6、18个月,治疗Ⅱ组和治疗Ⅲ组与治疗Ⅰ组的CHR比较,差异均无统计学意义(字2=1.835、1.907,P>0.05;字2=0.953、0.967,P>0.05;字2=2.063、2.057,P>0.05)。治疗18个月时,治疗Ⅱ组、治疗Ⅲ组MMR均高于治疗Ⅰ组(字2=6.847、20.682,P<0.05);治疗6、18个月时,治疗Ⅱ组和治疗Ⅲ组CcyR均高于治疗Ⅰ组(字2=16.735、10.196,P<0.05;字2=17.428、18.163,P<0.05),差异均有统计学意义(P<0.05),见表1。
2.2 三组患者不良反应情况比较
治疗Ⅱ组、治疗Ⅲ组患者头痛、呕吐、水肿发生率均低于治疗Ⅰ组,差异均有统计学意义(字2=18.746、19.018、18.746,P<0.05;字2=18.746、19.018、18.746,P<0.05)。治疗Ⅱ组和治疗Ⅲ组与治疗Ⅰ组的血小板减少症、嗜中性粒细胞减少发生率比较,差异无统计学意义(字2=2.675、3.187,P>0.05;字2=3.196、3.028,P>0.05),见表2。
3 讨论
慢性粒细胞白血病属于粒系细胞增殖为特征的血液系统恶性疾病,起源于骨髓造血干细胞[13-14]。其按照病情的进展,可以分为慢性期、急性期和加速期,起初患者多处于慢性期,但是如果进展到急性期和加速期,患者病情会剧烈的变化,严重的影响预后水平,同时随着病情不断发展,也会出现低热、乏力、腹胀、肝脏、脾脏肿大等一系列的临床表现[15-16]。
笔者通过分析广东省化州市人民医院2013年2月-2016年2月收治的慢性粒细胞白血病患者78例临床资料,依据治疗药物不同进行分组,治疗Ⅰ组22例,治疗Ⅱ组30例,治疗Ⅲ组26例。治疗Ⅰ组中伊马替尼可以对酪氨酸激酶进行特异性的抑制,属于第一代酪氨酸激酶抑制剂,主要是对断点簇集区-艾贝尔逊白血病毒酪氨酸激酶信号传统通路进行抑制,竞争性的抑制ATP和酪氨酸蛋白结合,阻止酪氨酸激酶磷酸化,抑制融合基因增殖,完成整个靶向治疗过程。伊马替尼不会对正常的细胞增殖造成影响,其抑制作用具有特异性[17-18]。治疗Ⅱ组中尼洛替尼属于第二代酪氨酸激酶抑制剂,可以和酪氨酸激酶结合,结合的亲和力高于伊马替尼近30倍,抑制各个细胞系中的BCR-ABL发生磷酸化,并且对于一些耐药的病例有很好的效果[19]。治疗Ⅲ组中达沙替尼属于强效BCR-ABL酪氨酸激酶抑制剂,在分子结构上有别于伊马替尼,和ABL激酶结构域中的非活化构象和活化构象均可以结合。达沙替尼常被用在初次发作的CML-CP中,提高了治疗效率。在慢性粒细胞性白血病中,早期细胞遗传学和分子生物学反应对于患者远期疗效具有重要的意义和价值。通过比较结果表明,三组患者CHR比较,差异无统计学意义,治疗18个月时,治疗Ⅱ组、治疗Ⅲ组患者MMR均高于治疗Ⅰ组,治疗6、18个月时,治疗Ⅱ组、治疗Ⅲ组患者均高于治疗Ⅰ组,治疗Ⅱ组、治疗Ⅲ组患者头痛、呕吐、水肿发生率均低于治疗Ⅰ组,提示尼洛替尼和达沙替尼在控制CCyR和MMR效果均優于伊马替尼,同时头痛、呕吐、水肿发生率也低于伊马替尼治疗的患者,安全性较高。
综上所述,尼洛替尼和达沙替尼治疗慢性粒细胞白血病患者,CCyR和MMR改善效果更加明显,值得临床推广应用。
参考文献
[1]庞迎旭.伊马替尼治疗慢性粒细胞白血病近期疗效观察及安全性分析[J].慢性病学杂志,2018,19(6):719-720.
[2] Jorge E,Giuseppe S,Hagop M,et al.Final 5-year study results of DASISION:the dasatinib versus imatinib study in treatment-naive cronic myeloid leukemia patients trial[J].J Clin Oncol,2016,34(20):2334-2340.
[3]丁卓玲,邓明凤.初发慢性粒细胞白血病采用甲磺酸伊马替尼治疗临床检验观察[J].湖北中医药大学学报,2016,18(4):109-111.
[4] Hughes T P,Saglio,Quintascardama A,et al.BCR-ABL1 mutation development during first-line treatment with dasatinib or imatinib for chronic myeloid leukemia in chronic phase[J].Leukemia,2015,29(9):1832-1838.
[5]马永华,张开金,刘桂圆,等.使用伊马替尼治疗的慢性粒细胞白血病患者的生命质量影响因素分析[J].上海交通大学学报,2016,36(7):1059-1062.
[6]中华医学会血液学分会.中国慢性髓性白血病诊断与治疗指南(2016年版)[J].中华血液学杂志,2016,37(8):633-639.
[7]王慧睿,郭淑利,李波,等.伊马替尼和达沙替尼治疗初发慢性粒细胞白血病慢性期患者疗效观察[J].新乡醫学院学报,2018,35(6):495-497,501.
[8] Zhuang Q,MAO W,XU P,et al.Identification of differential genes expression profiles and pathways of bone marrow mesenchymal stem cells of adolescent idiopathic scoliosis patients by microarray and Integrated gene network analysis[J].Spine,2016,41(10):840-855.
[9]汪玉芳,柯善栋,柯金勇,等.慢性粒细胞白血病患者使用伊马替尼早期治疗前后CFLI-1表达水平变化及其临床意义[J].贵州医药,2018,42(5):560-562.
[10] Ju H Q,Zhan G,Huang A,et al.ITD mutation in FLT3 tyrosine kinase promotes warburg effect and renders therapeutic sensitivity to glycolytic inhibition[J].Leukemia,2017,31(10):2143-2150.
[11] Hanfstein B,Müller M C,Hehlmann R,et al.Early molecular and cytogenetic response is predictive for long-term progression-free and overall survival in chronic myeloidleu kemia(CML)[J].Leukemia,2012,26(9):2096-2102.
[12] Xia H G,Najafov A,Geng J,et al.Degradation of HK2 by chaperone-mediated autophagy promotes metabolic catastrophe and cell death[J].
J Cell Biol,2015,210(5):705-716.
[13]蒋明,陈文聪,郑多.BCR-ABL融合基因在慢性粒细胞白血病临床诊治中的研究进展[J].中南医学科学杂志,2016,44(3):356-360.
[14] Zhang H N,Yang L,Ling J Y,et al.Systematic identification of arsenic-binding proteins reveals that hexokinase-2 is inhibited by arsenic[J].Proc Natl Acad Sci USA,2015,112(49):15084-15089.
[15]吴薇,韩瑞玲,张力,等.RQ-PCR在慢性粒细胞白血病细胞BCR-ABL融合基因检测中的应用[J].检验医学与临床,2016,13(22):3133-3134.
[16]胡敏,袁凯锋,李晓明,等.伊马替尼、尼洛替尼和达沙替尼对慢性粒细胞白血病慢性期患者的临床疗效[J].中国临床药理学杂志,2016,32(6):511-513.
[17]白晓川,刘芳芳.甲磺酸伊马替尼治疗慢性髓细胞白血病的临床疗效[J].宁夏医科大学学报,2017,39(3):313-315.
[18]薛磊,杨会志,王兴兵,等.尼洛替尼与伊马替尼治疗慢性粒细胞白血病早期临床疗效比较[J].安徽医学,2018,39(8):944-947.
[19]荆凌华,刘松年,马利敏,等.尼洛替尼和伊马替尼对慢性粒细胞白血病表达谱的影响[J].中国现代医学杂志,2018,28(19):28-33.

